
Наследственная оптическая нейропатия Лебера: массовая гибель аксонов зрительного нерва
Наследственная оптическая нейропатия Лебера (НОНЛ) – тяжелая инвалидизирующая нейроофтальмологическая патология, поражающая преимущественно молодых людей и представляющая большие проблемы для врачей при диагностике и лечении.
Автор: Павел Калинчев
Визитная карточка заболевания

Впервые НОНЛ была описана в 1871 году немецким офтальмологом Теодором Карлом Густафом фон Лебером.2
Основной клинический симптом НОНЛ – наследственная атрофия зрительных нервов, к которой приводит дегенерация ганглиозных клеток сетчатки (ГКС). При развитии НОНЛ в первую очередь поражается подгруппа макулярных ГКС, обеспечивающих аксонами папиллярно-макулярный пучок и отвечающих за центральное зрение. Это приводит к потере остроты зрения, дисхроматопсии, большим центральным скотомам и временной бледности диска зрительного нерва.3,4

Факторы риска, увеличивающие вероятность манифестации НОНЛ:9



1. Диагностика атрофии зрительного нерва Лебера (патогенные варианты c.152A>G (p.Tyr51Cys) в гене DNAJC30 , m.11778G>A, m.14484T>C, m.3243A>G, m.3460G>A, m.8344A>G, m.8993T>G). https://helix.ru/kb/item/42-138 (Дата обращения: 16.04.2025.).
2. Leber T. Uber hereditare und congenital-angelegte Sehnervenleiden. Arch Ophthalmol. 1871, 17, p. 249ー291.
3. Carelli V., Ross-Cisneros F.N., Sadun A.A. Mitochondrial dysfunction as a cause of optic neuropathies. Prog Retin Eye Res. 200, 23, p. 53ー89.
4. Yu-Wai-Man P., Griffiths P., Chinnery P. Mitochondrial optic neuropathies — disease mechanisms and therapeutic strategies. Prog. Retin Eye Res. 2011 (Mar.), 30 (2), p. 81ー114. https://doi.org/10.1016/j.preteyeres.2010.11.002
5. Neringa J., Patrick Y. Leber hereditary optic neuropathy: bridging the translational gap. Current Opinion in Ophthalmology. 2017, 28 (5), p. 403ー409.
6. Полехина Н.В., Федотова Е.Ю., Байдина Е.В., Ершова М.В., Клюшников С.А. Наследственная оптическая невропатия Лебера: обзор литературы и клиническое наблюдение // Нервные болезни. № 3, 2018, с. 63ー68.
7. Shemesh A., Margolin E. Leber optic atrophy. StatPearls. Treasure Island (FL): Stat Pearls Publishing; 2018.
8. Казаков В.М., Скоромец А.А., Руденко Д.И., Стучевская Т.Р., Колынин В.О. Митохондриальные болезни: миопатии, энцефаломиопатии и энцефаломиелополиневропатии // Неврологический журнал. Т. 23, № 6, 2018, с. 272ー281.
9. Руина Е.А., Чадаева О.И., Паршина Е.В., Смирнов А.А. Оптическая невропатия Лебера // Медицинский альманах. № 5 (50), 2017, с. 120ー126.
Молекулярная генетика болезни
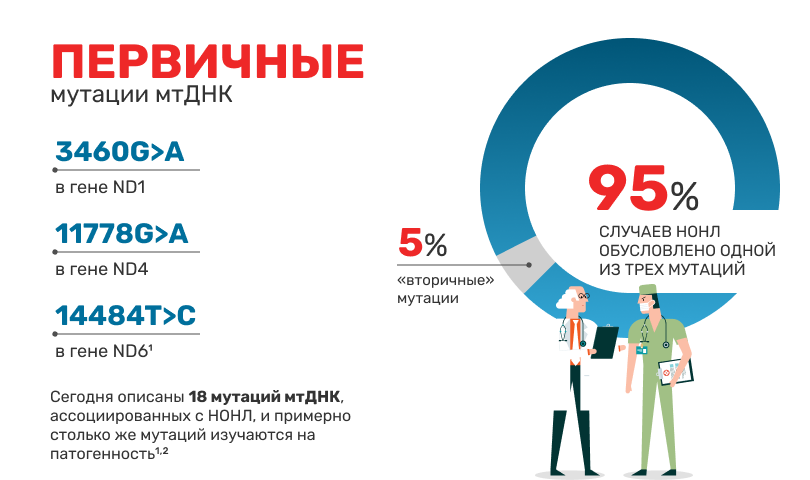
Причина возникновения наследственной оптической нейропатии Лебера (НОНЛ) связана с мутациями только митохондриальной ДНК (мтДНК). Мутацию наследуют все дети женщины-носительницы (митохондриальное наследование).1
В результате патогенной мутации мтДНК нарушается работа белка HAДH-дегидрогеназы. Это приводит к дисфункции I комплекса дыхательной цепи; нарастанию энергодефицита (снижение количества АТФ, ухудшение энергетически зависимого транспорта митохондрий на периферию аксона), увеличению количества свободных радикалов. Эти процессы ведут к дегенерации ганглионарных клеток сетчатки и вторичной атрофии зрительного нерва.3
Изучение этиопатогенеза НОНЛ продолжается. Ученым предстоит ответить еще на многие вопросы. Например, какова природа межклеточных взаимодействий, позволяющих вовлечь в процесс гибели одновременно огромное количество клеток. Каким образом после 2ー3 десятилетий нормального функционирования большинство из 1,2 млн аксонов зрительного нерва погибает одновременно1.
1. Мазунин И.О., Володько Н.В. Наследственная оптическая нейропатия Лебера // Вестник офтальмологии. 2018, 134 (2), с. 92ー97. https://doi.org/10.17116/oftalma2018134292-96
2. Koilkonda R., Guy J. Leber’s Hereditary Optic Neuropathy-Gene Therapy: From Benchtop to Bedside. J Ophthalmol. 2011:179412. https://doi.org/10.1155/2011/179412
3. Полехина Н.В., Федотова Е.Ю., Байдина Е.В., Ершова М.В., Клюшников С.А. Наследственная оптическая невропатия Лебера: обзор литературы и клиническое наблюдение // Нервные болезни. № 3, 2018, с. 63ー68.
Клиническая картина


Клинические проявления НОНЛ у пациентов могут широко варьировать. Среди атипичных случаев – увеличение остроты зрения, уменьшение размеров центральных скотом и переход скотомы из абсолютной в относительную при сохранении на глазном дне картины частичной атрофии зрительных нервов.6
Снижение остроты зрения при НОНЛ может сопровождаться неврологическими симптомами – тремором, атаксией, спастическими парезами.7 Вместе с этим могут наблюдаться некоторые костно-суставные изменения, кардиальные нарушения.
В некоторых случаях может наблюдаться частичное спонтанное восстановление зрения – в зависимости от типа мутации и возраста на момент начала заболевания: у 5% пациентов с мутацией m.11778G>A, у 22% – с мутацией m.3460G>A, у 37ー65% – с мутацией m.14484T>C.8,9
1. Мазунин И.О., Володько Н.В. Наследственная оптическая нейропатия Лебера // Вестник офтальмологии. 2018, 134 (2), с. 92ー97. https://doi.org/10.17116/oftalma2018134292-96
2. Полехина Н.В., Федотова Е.Ю., Байдина Е.В., Ершова М.В., Клюшников С.А. Наследственная оптическая невропатия Лебера: обзор литературы и клиническое наблюдение // Нервные болезни. № 3, 2018, с. 63ー68.
3. Карушин О.И., Гафаров И.З. Оптическая невропатия Лебера. Клинический случай // Российский офтальмологический журнал, Т. 9, № 2, 2016, с. 84ー89. doi: 10.21516/2072-0076-2016-9-2-84-89 7
4. Руина Е.А., Чадаева О.И., Паршина Е.В., Смирнов А.А. Оптическая невропатия Лебера // Медицинский альманах. № 5 (50), 2017, с. 120ー126.
5. Полукарова Е.А., Волкова А.К., Байдалина Е.В., Берг А.К., Соколов С.В. Клинический случай пациента с наследственной оптической нейропатией Лебера // Медицина в Кузбассе. 2023. № 2. С. 140ー144.
6. Abu-Amero K. Leber’s Hereditary Optic Neuropathy: The Mitochondrial Connection Revisited. Middle East Afr. J. Ophthalmol. 2011, 18 (1), p. 17ー23. https://doi.org/10.4103/0974-9233.75880].
7. DiMauro S., Schon E., Carelli V., Hirano M. The clinical maze of mitochondrial neurology. Nat. Rev. Neurol. 2013, 9 (8), p. 429ー444. https://doi.org/10.1038/nrneurol.2013.126
8. Stone E.M., Newman N.J., Miller N.R., Johns D.R., Lott M.T., Wallace D.C. Visual recovery in patients with Leber's hereditary optic neuropathy and the 11778 mutation. J. Clin. Neuroophthalmol. 1992, 12, p. 10ー14.
9. Yu-Wai-Man P., Griffiths P.G., Hudson G., Chinnery P.F. Inherited mitochondrial optic neuropathies. J. Med. Genet. 2009, 46, p. 145ー158.
Сложные задачи диагностики

Диагностика НОНЛ включает полный комплекс нейроофтальмологических обследований:1-3
- исследование глазного дна;
- исследование полей зрения на белый и цветные стимулы;
- регистрацию вызванных зрительных потенциалов (ЗВП);
- электроретинографию (ЭРГ);
- оптическую когерентную томографию (ОКТ);
- нейровизуализацию структур орбиты и головного мозга;
- ДНК-диагностику и генетическое консультирование.
Серьезные трудности возникают и при дифференциальной диагностике – с рассеянным склерозом (РС), заболеваниями спектра нейрооптикомиелита (ЗСНОМ).3-4

Для заболеваний спектра нейрооптикомиелита (ЗСНОМ) более характерно снижение зрения, сопровождающееся болевым синдромом в глазных яблоках, выпадение зрения по типу нецентральных скотом либо квадрантных гемианопсий, отеком зрительного нерва, выявляемым при офтальмоскопии, отсутствием ЗВП (из-за повреждения аксонов). При проведении дифференциальной диагностики требуется выполнение прицельной МРТ структур орбиты и зрительных нервов, шейного отдела позвоночника, а также выявление антител к аквапорину-4.4,5
Дополнительные трудности в диагностику вносят комбинированные формы НОНЛ и рассеянного склероза, носящие название Harding-синдром.5,6
1. Полукарова Е.А., Волкова А.К., Байдалина Е.В., Берг А.К., Соколов С.В. Клинический случай пациента с наследственной оптической нейропатией Лебера // Медицина в Кузбассе. № 2, 2023, с. 140ー144.
2. Копишинская С.В., Светозарский С.Н., Густов А.В. Наследственная оптическая невропатия Лебера //. Современные технологии в медицине. Т. 6, № 2, 2014, с. 148ー152.
3. Маслова Н.Н., Андреева Е.А., Ерохина Е.В. Болезнь Лебера. Клиническое наблюдение // Бюллетень сибирской медицины. Т. 12, № 5, 2013, с. 126ー132.
4. Шмидт Т.Е. Дифференциальный диагноз оптического неврита (обзор литературы) // Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски. Т. 112, № 9ー2, 2012, с. 5ー9.
5. Галиуллин Т.Р., Рахматуллин А.Р., Галиуллина И.В., Бахтиярова К.З. Сложности дифференциальной диагностики болезни Лебера и рассеянного склероза (клиническое наблюдение) // Практическая медицина. Т. 16, № 9, 2018, с. 155ー160.
6. Полехина Н.В., Федотова Е.Ю., Байдина Е.В., Ершова М.В., Клюшников С.А. Наследственная оптическая невропатия Лебера: обзор литературы и клиническое наблюдение // Нервные болезни. № 3, 2018, с. 63ー68.
Перспективы лечения
При современном уровне понимания природы молекулярного патогенеза НОНЛ терапия этой патологии остается спорной. Сегодня многие предполагаемые методы лечения проходят стадии испытания. Основные подходы к лечению – медикаментозная терапия и экспериментальные методы генной терапии.1-3
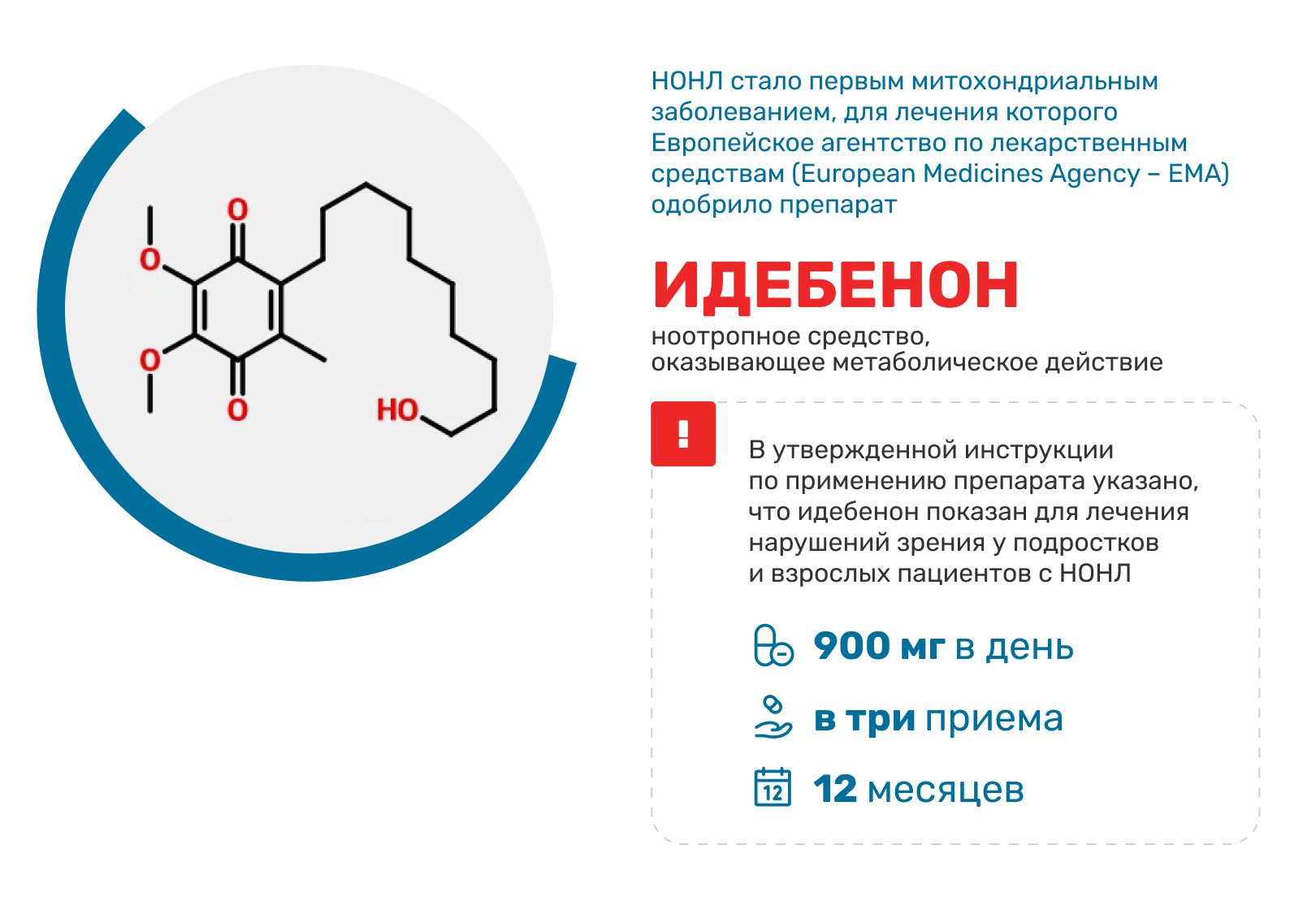
Однако из-за отсутствия общепринятых определений, критериев и рекомендаций по клиническому ведению пациентов с НОНЛ его появление вызвало у практикующих врачей множество вопросов.
Ответы на многие из них дал Международный консенсус о клиническом и терапевтическом лечении наследственной оптической нейропатии Лебера.4 Так, по поводу применения идебенона при НОНЛ эксперты пришли к единому мнению: препарат показан при подостром и динамическом течении заболевания в дозировке 900 мг/день (не менее 12 месяцев).5

Также эксперты достигли единогласия по поводу продолжения лечения у пациентов, ответивших на терапию (на основании установленных показателей BCVA и полей зрения), и критериев определения клинически значимого ответа.6 Однако с применением препарата в качестве поддерживающей терапии у пациентов, не ответивших на лечение в течение одного года, специалисты не согласилась. Не подтвердили они и применение идебенона у пациентов на хронической стадии с продолжительностью заболевания 1ー5 лет – нет достаточных доказательств.
Последние годы ведется большая работа по разработке методов, направленных на этиологическую терапию – генную. И хотя большинство из них находятся на стадиях лабораторных исследований (на клеточных линиях или животных моделях), специалисты отмечают значительный прогресс.1

