Что оказывает влияние на респираторный иммунитет?
Влияние нормальной микрофлоры кишечника на иммунорегуляцию вне желудочно-кишечного тракта (ЖКТ) — в легких — активно изучается в настоящее время. Сигналы от микроорганизмов и продуктов их метаболизма взаимодействуют с TLR, индуцируют эффекторные функции, связанные с экспрессией ядерного фактора транскрипции каппа-В (NF-κB), дендритными клетками, Тr-лимфоцитами, хемокинами и цитокинами. Метаболиты бактерий, в частности короткоцепочечные жирные кислоты (SCFAs), действуют непосредственно на эпителиальные и иммунные клетки, способствуя мощному иммунному ответу. Установлено, что короткоцепочечные жирные кислоты оказывают влияние путем активации деятельности NF-κB и продукции TNF-α, а также уменьшают стимуляцию рецепторов распознавания антигенных структур (pattern recognition receptors — PRR)2.
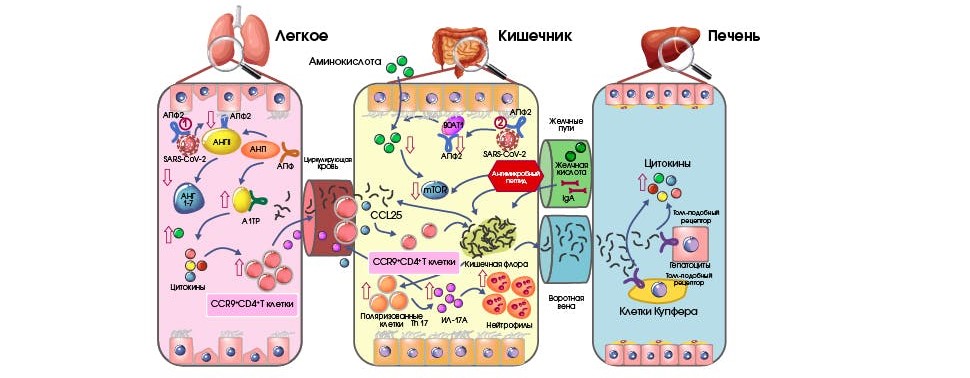
На экспериментальных животных моделях было показано: микробиота участвует в поддержании респираторного иммунитета3,4. Стимулирующие противоинфекционную защиту сигналы, полученные в нижних отделах ЖКТ, распространяются на слизистые оболочки других биотопов, включая респираторный тракт. Это дает основание для изучения возможностей использования пробиотических препаратов, с точки зрения таксономии содержащих в своем составе пробиотические виды Lactobacillus и Bifidobacterium, в комплексном лечении и профилактике острых респираторных инфекций (ОРИ)2.
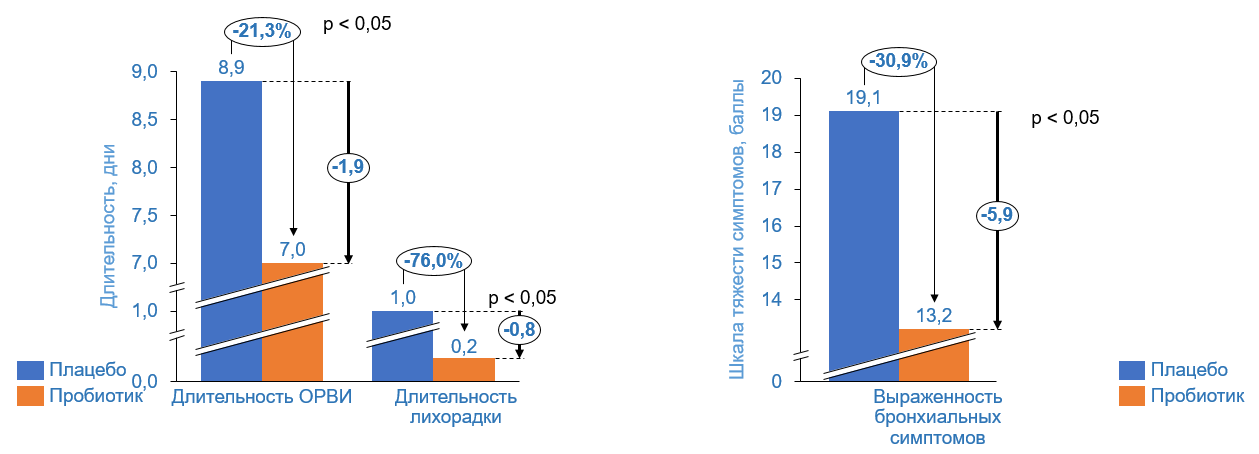
Пробиотические эффекты и степень влияния на иммунитет обусловлены штаммоспецифичностью. Для примера: в двойном слепом рандомизированном плацебоконтролируемом клиническом исследовании рассматривалось влияние Bifidobacterium longum в течение как минимум 3 месяцев на тяжесть симптомов, частоту и продолжительность простуды. По окончании исследования были опубликованы выводы, что прием пробиотика снижал длительность ОРВИ и лихорадки при уменьшении тяжести бронхиальных симптомов10.
Пробиотики — это живые микроорганизмы, которые вызывают улучшение здоровья организма-хозяина при применении в адекватных количествах5.
В 2017 году Всемирная гастроэнтерологическая организация сформулировала ряд требований к производителям коммерческих препаратов-пробиотиков, согласно которым они должны6:
- быть определены по виду и штамму;
- быть живыми и кислотоустойчивыми или иметь специальный способ доставки к местам прикрепления;
- обеспечивать достаточное количество бактерий на конец срока годности — 10⁶–10⁹, доходить к местам прикрепления в необходимых количествах;
- продемонстрировать высокие показатели действия в плацебоконтролируемых клинических исследованиях.
Только штаммы, доказавшие свое действие в рандомизированных плацебоконтролируемых исследованиях, могут быть использованы для производства лекарственных препаратов-пробиотиков. Пробиотические препараты могут содержать один микроорганизм или смесь из нескольких видов. Наличие бактериального синергизма оправдывает применение препаратов, содержащих симбионтные штаммы пробиотиков, так как способность к адгезии увеличивается при сочетании штаммов. Пробиотический лекарственный препарат «Бифиформ» имеет сбалансированный состав, содержит два штамма бактерий — Enterococcus faecium ENCfa-68 и Bifidobacterium longum ВВ-46. Двухслойная капсула защищает бактерии, входящие в состав препарата, от кислой среды желудка и доставляет их в кишечник без потерь. «Бифиформ» действует в тонкой и толстой кишке7.
Интересными представляются данные, полученные исследователями в Германии. В исследовании deVrese и соавт. (2005 г.) оценивали влияние приема Bifidobacterium longum 5×106 КОЕ, Lactobacillus gasseri 4×107 КОЕ, Bifidobacterium bifidum 5×106 КОЕ 1 раз в сутки на протяжении 3 (n = 121) или 5,5 (n = 117) месяцев у здоровых добровольцев (средний возраст 38 ± 13 лет) на тяжесть, частоту развития и длительность симптомов ОРВИ. Кроме того, у отдельной группы пациентов (122 человека), получавших пробиотик, через 14 дней приема оценивали показатели клеточного иммунитета, а также количество лакто- и бифидобактерий в кале. Прием пробиотика сопровождался снижением длительности ОРВИ (почти на 2 дня) и лихорадки при уменьшении тяжести бронхиальных симптомов. При оценке показателей клеточного иммунитета через 14 дней отмечалось усиление Т-супрессоров (CD8+) и Т-хелперов (CD4+) в группе пробиотика в сравнении с плацебо. Содержание лакто- и бифидобактерий в кале добровольцев значительно увеличилось после приема пробиотика8.
В исследовании, проведенном в Малайзии (2018 г.), прием Bifidobacterium longum (5×109 КОЕ в сутки, 5 раз в неделю в течение 10 месяцев) приводил к снижению риска развития ОРВИ и уменьшению длительности ее основных симптомов у детей в возрасте 2–6 лет. Кроме того, прием Bifidobacterium longum приводил к изменению микробиоты кишечника в сторону увеличения Faecalibacterium, которые обладают иммуномодулирующим эффектом9.
С началом применения в практике гастроэнтеролога таких препаратов, как «Бифиформ», наступает «эпоха Возрождения» микробиома человека.
Список литературы:
1. Корниенко Е.А. Микробиота кишечника как ключевой фактор формирования иммунитета и толерантности. Возможности пробиотиков // Медицинский совет. 2020. № 10. С. 92–100. DOI: 10.21518/2079-701X-2020-10-92-100.
2. Ивашкин В.Т., Зольникова О.Ю., Поцхверашвили Н.Д., Кокина Н.И., Буеверова Е.Л., Седова А.В., Трухманов А.С. Перспективы применения пробиотических препаратов при острых инфекциях респираторного тракта // Пульмонология. 2019. № 29 (5). С. 612–619. DOI: 10.18093/0869-0189-2019-29-5-612-619.
3. Gauguet S., D'Ortona S., Ahnger-Pier K. et al. Intestinal microbiota of mice influences resistance to Staphylococcus aureus pneumonia. Infect. Immun. 2015; 83 (10): 4003–4014. DOI: 10.1128/IAI.00037-15.
4. Ichiohe T., Pang I.K., Kumamoto Y. et al. Microbiota regulates immune defense against respiratory tract influenza A virus infection. Proc. Natl. Acad. Sci. USA. 2011; 108 (13): 5354–5359. DOI: 10.1073/pnas.1019378108.
5. FAO/WHO. Working group on drafting guidelines for the evaluation of probiotics in food. Guidelines for the evaluation of probiotics in food. 2002. URL: ftp://ftp. fao.org/es/esn/food/wgreport2.pdf.
6. WGO. Global guideline. Probiotics and prebiotics. URL: www.worldgastroenterology.org/UserFiles/file/guidelines/probiotics-and-prebiotics-russian-2017.pdf.
7. Корниенко Е.А., Мазанкова Л.Н., Горелов А.В. и др. Применение пробиотиков в педиатрии: анализ лечебного и профилактического действия с позиций доказательной медицины // Лечащий врач. 2015. № 9.
8. de Vrese M., Winkler P., Rautenberg P. et al. Effect of Lactobacillus gasseri PA 16/8, Bifidobacterium longum SP 07/3, B. bifidum MF 20/5 on common cold episodes: a double blind, randomized, controlled trial. Clinical nutrition. 2005, Aug 1; 24 (4): 481–491.
9. Lau A.S., Yanagisawa N., Hor Y.Y. et al. Bifidobacterium longum BB536 alleviated upper respiratory illnesses and modulated gut microbiota profiles in Malaysian pre-school children. Benef Microbes. 2018; 9 (1): 61–70. DOI: 10.3920/BM2017.0063. Epub 2017 Oct 25. PMID: 29065707.
10. Michael de Vrese 1, Petra Winkler, Peter Rautenberg, Timm Harder, Christian Noah, Christiane Laue, Stephan Ott, Jochen Hampe, Stefan Schreiber, Knut Heller, Jürgen Schrezenmeir. Effect of Lactobacillus gasseri PA 16/8, Bifidobacterium longum SP 07/3, B. bifidum MF 20/5 on common cold episodes: a double blind, randomized, controlled trial. 2005 Aug;24(4):481-91. doi: 10.1016/j.clnu.2005.02.006. Epub 2005 Apr 21.
Материал предназначен для сотрудников системы здравоохранения АО «ГлаксоСмитКляйн Хелскер» РФ, 123112, г. Москва, Пресненская наб., д. 10, помещение III, комната 9, эт 6. Тел. +7 (495) 777-98-50
Товарный знак принадлежит или используется Группой Компаний ГлаксоСмитКляйн
PM-RU-BIF-22-00012
Материал партнера: GSK















