ПроспектиВное исслЕдование по оценКе влияния нового фармаконуТрицевтика ревОкка (неомыляемые соединения авокадо и соевых бобов в соотношении 1:2, экстракт плодов шиповника, ресвератрол, цитрат цинка) на клинические проявления остеоаРтрита (ВЕКТОР)
|
Лила А.М.1,2, Таскина Е.А.1, Вукайлович Е.М.2, Кашеварова Н.Г.1, Стребкова Е.А.1, Савушкина Н.М.1, Шарапова Е.П.1, Короткова Т.А.1, Хальметова А.Р.1, Алексеева Л.И.1,2 1ФГБНУ «Научно-исследовательский институт ревматологии им. В.А. Насоновой», Москва.2ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава России, Москва. 1Россия, 115522, Москва, Каширское шоссе, 34А; 2Россия, 125993, Москва, ул. Баррикадная, 2/1, стр. 1. |
Lila A.M.1,2, Taskina E.A.1, Vukailovich E.M.1, Kashevarova N.G.1, Strebkova E.A.1, Savushkina N.M.1, Sharapova E.P.1, Korotkova T.A.1, Khalmetova A.R.1, Alekseeva L.I.1,2 1V.A. Nasonova Research Institute of Rheumatology, Moscow. 2Russian Medical Academy of Continuing Professional Education, Ministry of Health of Russia, Moscow. 134A, Kashirskoe Shosse, Moscow 115522, Russia; 22/1, Barrikadnaya Street, Build. 1, Moscow 125993, Russia. |
|
Цель исследования — оценка влияния нового фармаконутрицевтика Ревокка на клинические проявления остеоартрита (ОА). Материал и методы. В 3-месячное проспективное исследование было включено 50 женщин 40-75 лет (средний возраст — 58,3±10,1 года) с достоверным диагнозом ОА (ACR) коленных суставов (КС) II-III стадии по Kellgren-Lawrence, с болью при ходьбе ≥40 мм по визуальной аналоговой шкале (ВАШ), подписавших информированное согласие. Медиана длительности ОА составила 5 [3; 8] лет. У 22% больных имелся метаболический фенотип ОА, у 10% — воспалительный, у 12% — остеопоротический, у 26% — смешанный, у 30% фенотип не определен. Пациентки принимали по 2 капсулы фармаконутрицевтика 1 раз в день на протяжении всего периода наблюдения. Все они «по требованию» могли использовать нестероидные противовоспалительные препараты (НПВП). На протяжении исследования было предусмотрено три визита (В) к врачу. Эффективность лечения определялась по динамике интенсивности боли в целевом КС при ходьбе по ВАШ, индекса WOMAC, шкалы KOOS, показателей опросника EQ-5D. Учитывались также оценка общего состояния здоровья пациентом по ВАШ и оценка эффективности лечения врачом и пациентом, потребность в НПВП. Результаты и обсуждение. Через 1 мес терапии наблюдалась статистически значимая положительная динамика по всем оцениваемым параметрам (p<0,05), кроме скованности по WOMAC. Однако уже к 3-му месяцу было отмечено существенное снижение данного показателя, при этом другие изучаемые параметры продолжали демонстрировать дальнейшее улучшение. В частности, к В3 хороший ответ на терапию (уменьшение боли на ≥50% от исходного значения) был получен у 60% пациенток, а снижение интенсивности боли в анализируемом суставе до ≤40 мм по ВАШ выявлено у 88%. Отмечено уменьшение потребности в приеме НПВП: общее число случаев снижения дозы или отмены НПВП составило 40% к В2 и 48% к В3. Заключение. Результаты исследования свидетельствуют о быстром и выраженном клиническом эффекте Ревокка у больных с различными фенотипами ОА. Ключевые слова: остеоартрит коленных суставов; терапия; фармаконутрицевтик. Контакты: Елена Александровна Таскина; braell@mail.ru Для цитирования: Лила АМ, Таскина ЕА, Вукайлович ЕМ, Кашеварова НГ, Стребкова ЕА, Савушкина НМ, Шарапова ЕП, Короткова ТА, Хальметова АР, Алексеева ЛИ. ПроспектиВное исслЕдование по оценКе влияния нового фармаконуТрицевтика ревОкка (неомыляемые соединения авокадо и соевых бобов в соотношении 1:2, экстракт плодов шиповника, ресвератрол, цитрат цинка) на клинические проявления остеоаРтрита (ВЕКТОР). Современная ревматология. 2025;19(6):72-79. https://doi.org/10.14412/1996-7012-2025-6-72-79. |
Objective: to evaluate the effects of the novel pharmaconutraceutical Revocca on the clinical manifestations of osteoarthritis (OA). Material and methods. A 3-month prospective study included 50 women aged 40-75 years (mean age 58.3±10.1 years) with a confirmed diagnosis of knee OA according to ACR criteria, Kellgren-Lawrence grade II-III, with pain on walking ≥40 mm on a visual analogue scale (VAS), who provided written informed consent. The median OA duration was 5 [3; 8] years. A metabolic phenotype of OA was present in 22% of patients, an inflammatory phenotype in 10%, an osteoporotic phenotype in 12%, a mixed phenotype in 26%, while in 30% the phenotype could not be determined. Patients took 2 capsules of the pharmaconutraceutical once daily throughout the observation period. All patients were allowed to use nonsteroidal anti-inflammatory drugs (NSAIDs) «as needed.» Three physician visits (V) were scheduled during the study. Treatment efficacy was assessed by the dynamics of pain intensity in the target knee joint on walking (VAS), WOMAC index, KOOS scale, and EQ-5D questionnaire scores. Additional assessments included the patient’s VAS global health assessment, physician’s and patient’s assessments of treatment efficacy, and the need for NSAIDs. Results and discussion. After 1 month of therapy, a statistically significant positive change was observed in all evaluated parameters (p<0.05), except for stiffness on the WOMAC scale. However, by month 3 a substantial reduction in stiffness was recorded, while all other parameters continued to improve. By V-3, a good treatment response (≥50% pain reduction from baseline) was achieved in 60% of patients, and pain intensity ≤40 mm on VAS in the affected joint was documented in 88%. A reduced need for NSAIDs was noted: the total number of cases of dose reduction or NSAID discontinuation reached 40% by V-2 and 48% by V-3. Conclusion. The study results indicate a rapid and pronounced clinical effect of Revocca in patients with various OA phenotypes. Keywords: knee osteoarthritis; therapy; pharmaconutraceutical. Contact: Elena Aleksandrovna Taskina; braell@mail.ru For citation: Lila AM, Taskina EA, Vukailovich EM, Kashevarova NG, Strebkova EA, Savushkina NM, Sharapova EP, Korotkova TA, Khalmetova AR, Alekseeva LI. Prospective study assessing the effects of the novel pharmaconutraceutical Revocca (unsaponifiable compounds of avocado and soybeans in a 1:2 ratio, rosehip fruit extract, resveratrol, zinc citrate) on the clinical manifestations of osteoarthritis (VECTOR). Sovremennaya Revmatologiya=Modern Rheumatology Journal. 2025;19(6):72-79 (In Russ.). https://doi.org/10.14412/1996-7012-2025-6-72-79. |
Остеоартрит (ОА) остается одним из самых распространенных хронических заболеваний в мире, занимая лидирующие позиции среди причин как временной нетрудоспособности, так и стойкой ее утраты. Отчасти это обусловлено старением популяции, отчасти — малоподвижным образом жизни и изменением характера питания, что ведет к росту числа пациентов с ожирением и метаболическим синдромом.
За последние десятилетия взгляды на ОА эволюционировали: если раньше его рассматривали как процесс естественного старения организма и механического «износа» суставного хряща, то сегодня — как заболевание, характеризующееся системным поражением всех структур сустава и вовлечением организма в целом [1]. Многофакторный патогенез ОА включает сложную совокупность генетической предрасположенности и эпигенетических изменений, активации сигнальных путей, инициирующих каскад метаболических нарушений и воспалительных реакций в хондроцитах, синовиоцитах и клетках субхондральной кости, внешних воздействий и сопутствующих заболеваний. Все это обусловливает необходимость комплексного подхода к терапии ОА, а именно воздействия на различные патогенетические звенья заболевания, при этом важным условием является отсутствие отрицательного влияния на коморбидные состояния, которые так характерны для таких пациентов.
Недавно на отечественном рынке появился новый фармаконутрицевтик Ревокка, оказывающий многогранное позитивное воздействие на ОА за счет входящих в его состав пяти активных компонентов: неомыляемые соединения авокадо и сои (НСАС) 300 мг в соотношении 1:2, ресвератрол 70 мг, экстракт плодов шиповника 300 мг и цитрат цинка 12 мг, эффект каждого из которых является доказанным. Компоненты данного фармаконутрицевтика включены в клинические рекомендации терапии ОА коленных (КC) и тазобедренных (ТБС) суставов, генерализованного ОА, а также хронической боли у пациентов пожилого и старческого возраста [2-4].
Основная составляющаяей фармаконутрицевтика Ревокка — НСАС. Среди важнейших эффектов этих веществ — уменьшение интенсивности боли и воспаления, а также структурно-модифицирующее действие. Эти эффекты обусловлены рядом механизмов. В частности, НСАС ингибируют интерлейкин (ИЛ) 1 и снижают продукцию других провоспалительных цитокинов (ИЛ6, ИЛ8, фактора некроза опухоли a — ФНОa). Они также подавляют высвобождение матриксных металлопротеиназ (ММП), простагландина E2 (ПГE2) [5] и коллагеназы [6]. Одновременно НСАС стимулируют выработку аггрекана, коллагена II типа и синтез протеогликанов [7, 8]. Важным аспектом их действия является способность усиливать активность трансформирующего фактора роста b (TGFb), который, в свою очередь, стимулирует синтез компонентов внеклеточного матрикса и способен нивелировать негативное влияние ИЛ1 на хондроциты и синовиоциты [9, 10]. Кроме того, НСАС ингибируют образование медиаторов, участвующих в продукции активных форм кислорода (например, оксида азота). В экспериментальных работах показано, что НСАС подавляют активацию ядерного фактора каппа B (NF-kB), что приводит к снижению выработки не только цитокинов, хемокинов, но и макрофагального воспалительного белка 1b (MIP1b) [11]. Доказано влияние НСАС и на костную ткань в виде снижения синтеза щелочной фосфатазы и остеокальцина остеобластами субхондральной кости [12].
Следующий компонент — ресвератрол, который является природным фенольным соединением, обладающим широкой биологической активностью. Включение его в состав Ревокка оправдано с учетом усиления противовоспалительного эффекта, а также благоприятного влияния на коморбидные состояния.
Противовоспалительный эффект ресвератрола осуществляется путем частичного ингибирования пути NF-kB, индуцированного ИЛ1b, и снижения секреции ИЛ6 и других цитокинов. Кроме того, он уменьшает выраженность «низкоинтенсивного воспаления» при ОА, связанного с ожирением, посредством модулирования путей толл-подобного рецептора 4 (TLR4) и Янус-киназы 2 (JAK2)/STAT3. Также ресвератрол уменьшает дегенерацию хрящевой ткани и апоптоз хондроцитов [13-15], ингибирует резорбцию субхондральной кости, что особенно важно на ранних стадиях ОА, предотвращает деградацию внеклеточного матрикса хряща, замедляет потерю протеогликанов, лубрицина и аггрекана, а также развитие патологической васкуляризации [16-18]. Другой потенциальный механизм «хондропротективного» эффекта ресвератрола связан с уменьшением катаболического воздействия ИЛ1b на хондроциты за счет ингибирования экспрессии циклооксигеназы (ЦОГ) 2 [19].
Среди других биологических эффектов ресвератрола следует отметить иммуномодулирующее действие, снижение уровня глюкозы и инсулинорезистентности, протективное влияние на сердечно-сосудистую систему и снижение риска развития атеросклероза за счет улучшения липидного профиля и выраженного антиоксидантного эффекта, а также подавление пролиферации гладкомышечных клеток сосудов и агрегации тромбоцитов [20-24].
Цинк, входящий в состав Ревокка, также обладает рядом незаменимых биологических свойств. Противовоспалительная активность цинка связана не только с его способностью ингибировать сигнальный путь NF-kB и, как следствие, экспрессию провоспалительных цитокинов [25], но и с модулированием противовоспалительных путей цитокинов — TGFb, ИЛ2, ИЛ4 и ИЛ10 [26]. Важный эффект применения низких доз цинка — увеличение пролиферации культивируемых хондроцитов [27]. Также цинк содействует дифференцировке мезенхимальных стволовых клеток в хондроциты при остеохондральных дефектах [28]. Кроме того, он обеспечивает пролиферацию и созревание Ти В-лимфоцитов, поддерживает фагоцитарную активность нейтрофилов; является кофактором большой группы ферментов, участвующих в белковом обмене (в частности, в синтезе коллагена); входит в состав инсулина; повышает активность витамина D. Цинк обладает антиоксидантными свойствами (он содержится в ферменте супероксиддисмутаза, регулирующем перекисное окисление липидов, стабилизирует клеточные мембраны) [29-34].
Включенный в состав препарата шиповник обладает противовоспалительными свойствами, ингибируя высвобождение провоспалительных цитокинов, в том числе через сигнальный путь NF-kB, ЦОГ1, ЦОГ2 и 5-липооксигеназы. Это подтверждено снижением уровня мРНК ММП1, ММП3 и ММП13, ИЛ1 и ИЛ6, что ведет к уменьшению воспаления и деградации хряща при ОА [35]. В макрофагах и мононуклеарных клетках периферической крови препараты на основе шиповника подавляли продукцию оксида азота и ПГE2. Благодаря наличию в составе препарата витаминов С, Е и фенольных соединений он обладает антиоксидантным действием [36, 37].
В экспериментальных моделях шиповник предотвращал набор массы тела и снижал уровень глюкозы, инсулина и холестерина в крови. Методом непрямой калориметрии было установлено, что он обеспечивает более высокий уровень энергетического обмена. Эти данные позволяют предположить, что шиповник может оказывать профилактическое действие в отношении развития ожирения, являющегося одним из факторов риска прогрессирования ОА [38].
Предполагается, что синергический эффект хорошо изученных активных компонентов данного фармаконутрицевтика может способствовать выраженному уменьшению клинической симптоматики при ОА.
Цель исследования — оценка влияния нового фармаконутрицевтика Ревокка на клинические проявления ОА.
Материал и методы. В проспективное исследование включено 50 женщин в возрасте 40-75 лет (средний возраст — 58,3±10,1 года), медиана длительности ОА — 5 [3; 8] лет (от 3 до 8 лет), ИМТ — 27,9 [25; 32,5] кг/м2. У большинства пациенток (86%) определялась II рентгенологическая стадия ОА КС по Kellgren-Lawrence и у 14% — III стадия.
Критерии включения в исследование: пациенты мужского и женского пола 40-75 лет; первичный ОА КС по критериям ACR (American College of Rheumatology); рентгенологически подтвержденный ОА КС II-III стадии по Kellgren-Lawrence; боль при ходьбе в КС ≥40 мм по визуальной аналоговой шкале (ВАШ); соблюдение пациентом указаний врача; наличие подписанного и датированного информированного согласия на участие в исследовании.
Критерии невключения: наличие в анамнезе гиперчувствительности к любому из компонентов исследуемого препарата; боль при ходьбе в анализируемом суставе <40 и >90 мм по ВАШ; рентгенологическое поражение КС I или IV стадии по Kellgren-Lawrence; ИМТ ≥40 кг/м2; сопутствующий ОА ТБС и/или голеностопного суставов в тяжелой стадии, который может затруднить оценку интенсивности боли в КС или эффективности лечения; прием пероральных и парентеральных «хондропротекторов», в том числе БАД, для лечения ОА (хондроитина сульфат, глюкозамин, диацереин, НСАС, экстракт плодов шиповника, соединения цинка и др.) в течение 6 мес до скрининга; внутрисуставное введение любых препаратов в течение 6 мес до скрининга или пяти периодов полураспада (в зависимости от того, что было дольше); внутривенное/внутримышечное введение глюкокортикоидов в течение 3 мес или пероральный прием системных глюкокортикоидов в течение 1 мес до скрининга; вторичный ОА (инфекционный артрит, воспалительные заболевания суставов, подагра, болезнь депонирования кристаллов пирофосфата кальция, болезнь Педжета, внутрисуставные переломы, охроноз, акромегалия, гемохроматоз, болезнь Вильсона-Коновалова, первичный хондроматоз и др.). Воспалительные заболевания суставов (ревматоидный артрит, псориатический артрит, анкилозирующий спондилит и др.); хирургическое лечение указанного сустава в анамнезе; неконтролируемая артериальная гипертензия (АГ) и/или ишемическая болезнь сердца, хроническая сердечная недостаточность IIa-IIb, III стадии (III-IV функциональный класс по NYHA); декомпенсированный сахарный диабет (СД) 2-го типа или СД 1-го типа; тяжелые, декомпенсированные или нестабильные соматические заболевания (любые заболевания или состояния, которые угрожают жизни больного или ухудшают прогноз основного заболевания, а также делают невозможным его участие в клиническом исследовании); язва желудка или двенадцатиперстной кишки в анамнезе и/или эрозивный гастрит, выявленный менее чем за 6 мес до исследования; тяжелая почечная недостаточность (клиренс креатинина <30 мл/мин), прогрессирующие заболевания почек; наличие в анамнезе злокачественных новообразований, за исключением пациентов, у которых рецидив заболевания не наблюдался в течение последних 5 лет; полное или неполное сочетание бронхиальной астмы, рецидивирующего полипоза носа или околоносовых пазух и непереносимости ацетилсалициловой кислоты и других нестероидных противовоспалительных препаратов — НПВП (в том числе в анамнезе); злоупотребление наркотиками или алкоголем на момент скрининга или в прошлом, которое, по мнению исследователя, делает пациента непригодным для участия в исследовании; неспособность читать или писать, нежелание понять и следовать процедурам протокола исследования, а также любые другие сопутствующие медицинские или серьезные психические состояния, которые делают невозможным участие пациента в исследовании, ограничивают правомерность получения информированного согласия или могут повлиять на способность пациента участвовать в исследовании; одновременное участие в клиническом испытании других лекарственных средств; беременные или кормящие женщины либо пациентки, планирующие беременность во время клинического исследования; отсутствие письменного согласия на участие пациента в исследовании.
Исследование проводилось в течение 3 мес, за это время пациентки посетили врача 3 раза: визит (В) 0 — скрининг; В1 — начало терапии (совпадает с В0); В2 — через 1 мес после начала терапии; В3 (заключительный) — через 3 мес после начала терапии. Пациентки принимали по 2 капсулы фармаконутрицевтика 1 раз в день на протяжении всего периода наблюдения. Все они «по требованию» могли использовать НПВП.
Эффективность лечения определялась по динамике интенсивности боли в целевом КС при ходьбе по ВАШ; индекса WOMAC (Western Ontario and McMaster Universities Osteoarthritis Index) суммарного и его составляющих; шкалы KOOS (Knee Injury & Osteoarthritis Outcome Score — шкала оценки функции коленного сустава и активности пациента в повседневной и активной спортивной жизни); показателей опросника качества жизни EQ-5D (EuroQol-5 Dimensions). Дополнительно учитывались оценка общего состояния здоровья пациентом (ОСЗП) по ВАШ и оценка эффективности лечения врачом и пациентом (значительное улучшение, улучшение, отсутствие эффекта и ухудшение), потребность в НПВП.
У больных были представлены следующие фенотипы ОА: метаболический — у 22%, воспалительный — у 10%, остеопоротический — у 12%, смешанный — у 26%, в 30% случаев фенотип не определен. Помимо поражения КС, у 44% больных диагностирован ОА суставов кистей, у 38% — ОА ТБС, у 42% — боль в нижней части спины. Генерализованный ОА выявлен в 48% случаев.
Большинство пациенток (n=42, 84%) имели клинически значимые сопутствующие заболевания, среди которых чаще всего диагностировались патология сердечно-сосудистой системы (АГ — у 52%, дислипидемия — у 46%), ожирение (у 54%), метаболический синдром (у 32%) и СД 2-го типа (у 12%). В преобладающем большинстве случаев выявлено ≥2 коморбидных патологии: только у 10 пациенток имелось 1 сопутствующее заболевание, у 8 их было 2, у 19 — 3, у 5 — 4.
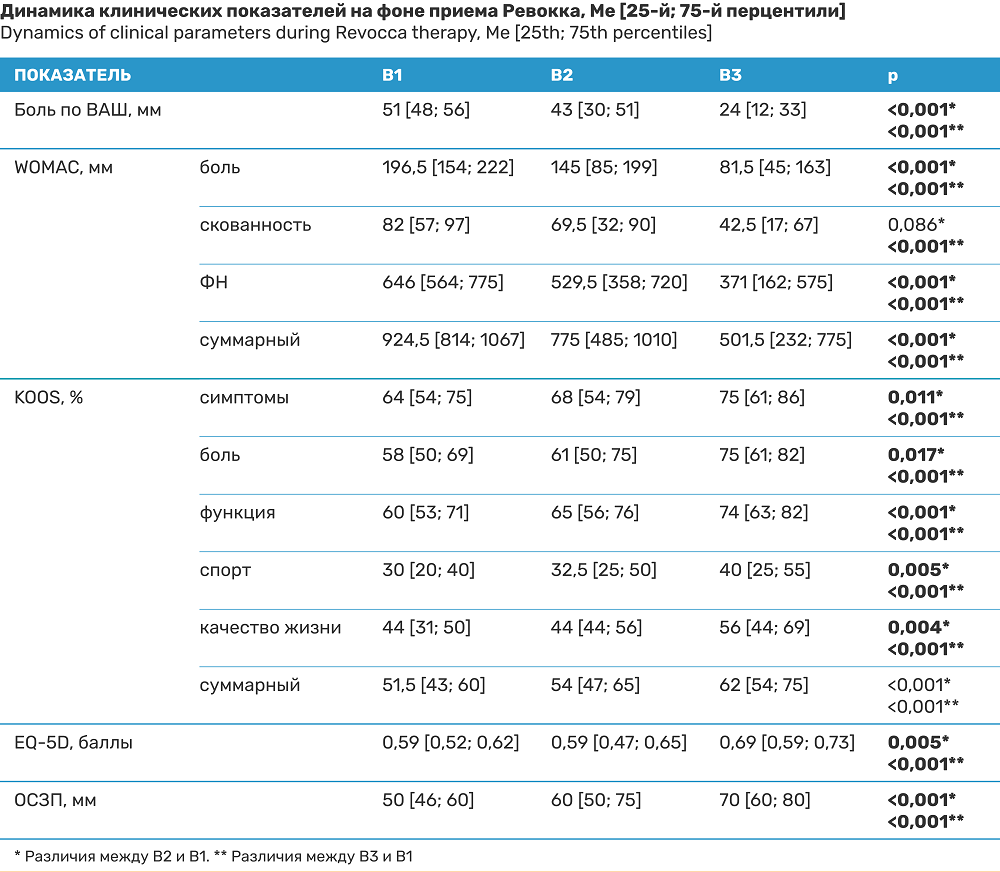
Статистическую обработку результатов осуществляли с помощью программного обеспечения Statistica 12.0 (StatSoft Inc., США). Проведены анализ на нормальность распределения переменных с использованием тестов Колмогорова- Смирнова, Шапиро-Уилка и частотный анализ. Применялись методы описательной статистики с вычислением минимальных, максимальных и средних значений переменных, стандартных отклонений, медианы и интерквартильного интервала (Ме [25-й; 75-й перцентили]), а также непараметрические (тест Вилкоксона, c2) критерии. Для сравнения показателя в динамике проводился дисперсионный анализ повторных измерений по Фридману. Различия считали статистически значимыми при р<0,05.
Результаты. Все больные (n=50) успешно завершили исследование и считались комплаентными (у них не зафиксировано каких-либо серьезных нарушений протокола исследования).
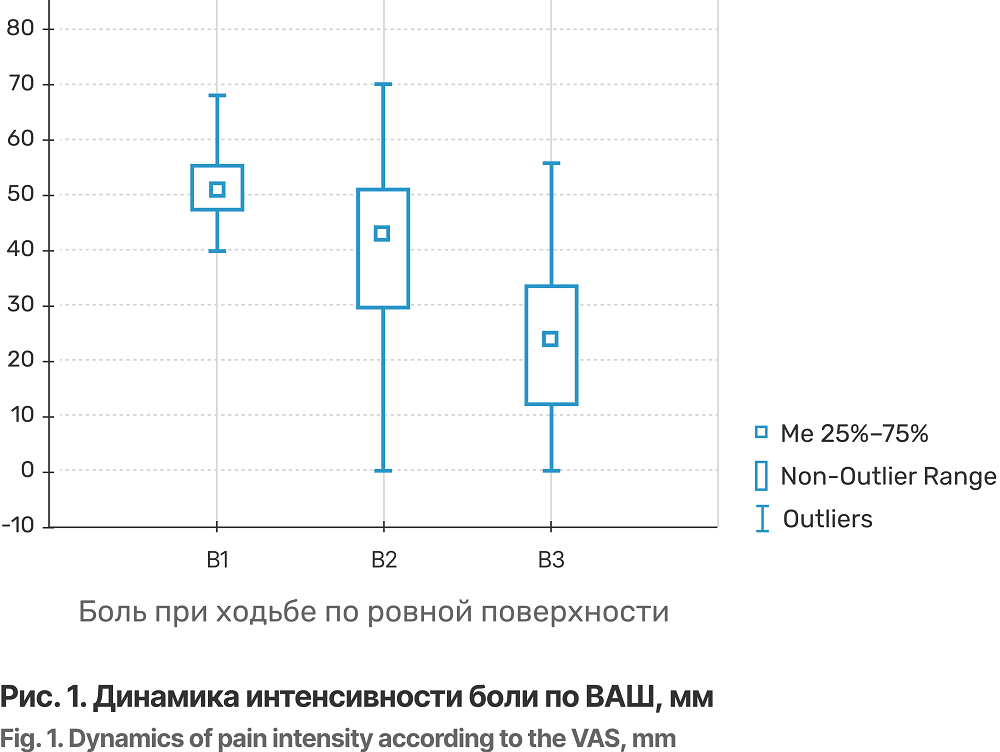
Результаты работы свидетельствуют о клиническом улучшении течения ОА на фоне приема изучаемого БАД. Значимое снижение боли в КС при ходьбе по ВАШ (p<0,001) отмечено уже через 30 дней после начала приема фармаконутрицевтика (см. таблицу). Дальнейшее уменьшение боли регистрировалось на протяжении всего периода исследования (рис. 1). Идентичная картина продемонстрирована при оценке как суммарного индекса WOMAC, так и его составляющих: боль и функциональная недостаточность — ФН (см. таблицу). При этом статистически значимое уменьшение показателей скованности по WOMAC было отмечено только к 3-му месяцу наблюдения.
Успешное применение Ревокка подтверждается улучшением шкалы KOOS и всех ее составляющих; EQ-5D и ОСЗП в течение всего периода лечения (см. таблицу).
Хороший ответ на терапию (уменьшение боли на ≥50% по сравнению с первоначальным значением) продемонстрирован у 60% больных; снижение боли в анализируемом КС ≤40 мм по ВАШ выявлено у 44% пациенток к В2 и у 88% к В3.
Об улучшении состояния больных на фоне приема фармаконутрицевтика также свидетельствует уменьшение потребности в приеме НПВП. В начале исследования для купирования боли различные НПВП принимали 37 (74%) пациенток: мелоксикам — 13 (26%), нимесулид — 7 (14%), целекоксиб — 5 (10%), напроксен — 4 (8%), ибупрофен — 3 (6%), ацеклофенак — 2 (4%), теноксикам — 2 (4%) и эторикоксиб — 1 (2%). На момент В2 снижение дозы НПВП зафиксировано у 16% участниц, 24% полностью прекратили их прием. К В3 число пациенток, снизивших дозу НПВП, возросло до 18%, а отменивших их прием — до 30%. Таким образом, общее число случаев снижения дозы или отмены НПВП составило 40% к В2 и 48% к В3.
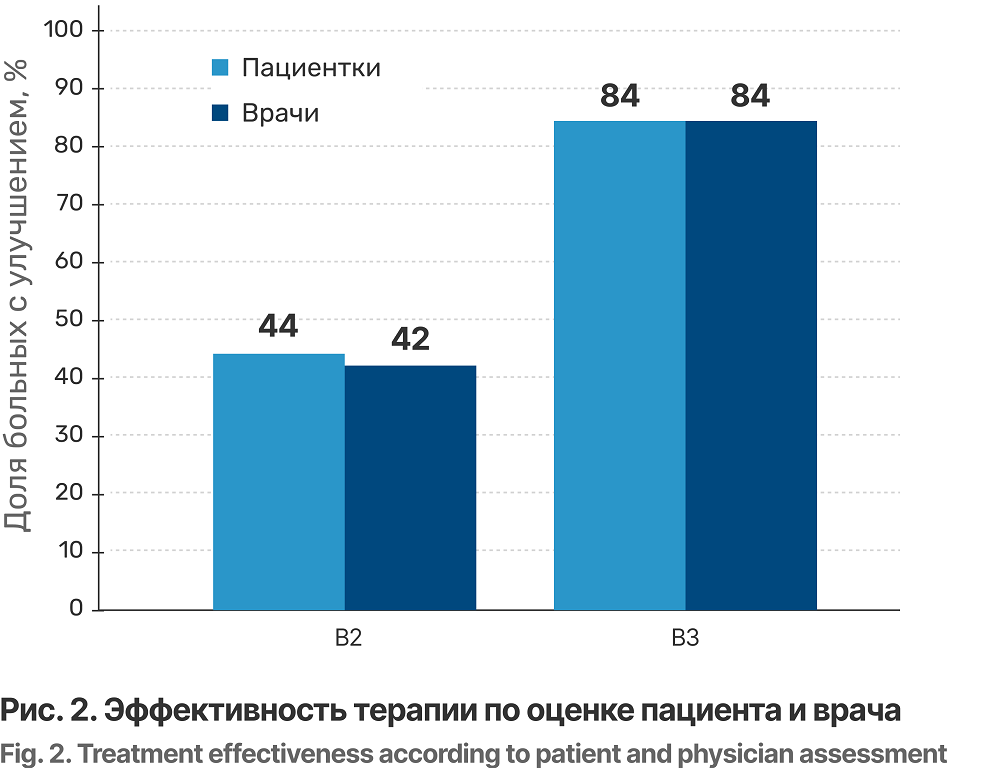
При оценке эффективности терапии через 1 мес после ее начала улучшение, по мнению пациента, отмечено в 22 (44%) случаях, по мнению врача — в 21 (42%). К концу наблюдения (В3) число участниц, указавших на положительную динамику, существенно увеличилось: 8 (16%) сообщили о значительном улучшении, 34 (68%) — об улучшении, и только у 8 (16%) состояние оставалось без изменений. Идентичные результаты получены и при оценке состояния больных врачами. Таким образом, доля женщин с положительным эффектом терапии (значительное улучшение или улучшение) увеличилась с 42-44% на момент В2 до 84% к В3 (рис. 2). Совпадение оценок больных и врачей указывает на высокую согласованность восприятия эффективности лечения.
В ходе исследования зарегистрировано 1 неблагоприятное явление (НЯ) у 1 пациентки, у которой на фоне приема фармаконутрицевтика появилась кожная сыпь без зуда. Реакция была легкой, не потребовала проведения дополнительной терапии и полностью самостоятельно купировалась в течение недели после завершения исследования. Отрицательного влияния на течение коморбидной патологии на протяжении исследования отмечено не было.
Таким образом, результаты исследования свидетельствуют о быстром и выраженном клиническом эффекте при использовании Ревокка у больных с различными фенотипами ОА: хороший ответ на терапию (снижение боли на ≥50% по сравнению с исходным значением) отмечен в 60% случаев, а в 88% боль в анализируемом КС составила ≤40 мм по ВАШ. Эффект терапии был оценен как положительный в 84% наблюдений как пациентками, так и врачами. Важным результатом стало снижение дозы или полная отмена НПВП у 48% больных к моменту завершения исследования.
Обсуждение. Большинство работ, в которых изучалась эффективность НСАС при ОА, продемонстрировали хороший симптоматический эффект препарата. Так, по данным Maheu и соавт. [39], применение НСАС привело к значимому уменьшению интенсивности боли по ВАШ, а также к заметному улучшению индекса Лекена при поражении КС и ТБС, эффект сохранялся на протяжении 6 мес. Схожие результаты приводятся в метаанализе, включавшем четыре рандомизированных двойных слепых плацебо-контролируемых исследования: выявлено значимое уменьшение боли и улучшение индекса Лекена у пациентов с ОА КС и ТБС, принимавших НСАС, при этом эффект отмечался с первых месяцев терапии [40]. Благодаря хорошему симптоматическому действию прием НСАС позволил снизить потребность в НПВП у большинства больных, различия с группой плацебо были статистически значимыми [41].
В отечественном открытом исследовании сравнительной эффективности НСАС и НПВП у 92 пациентов с ОА КС и ТБС получены доказательства более выраженного симптоматического эффекта НСАС (по сравнению с НПВП) после 3 мес терапии. Различия были выявлены в интенсивности боли и сохранялись до 6 мес [42].
Помимо симптоматического действия, в ряде исследований изучался структурно-модифицирующий эффект НСАС. Так, в рандомизированном контролируемом исследовании (РКИ), в котором участвовали 399 пациентов с ОА ТБС, было установлено, что применение НСАС в течение 3 лет приводило к замедлению рентгенологического прогрессирования заболевания. Пациентов с признаками рентгенологического прогрессирования (сужение ширины суставной щели) было значимо меньше в группе НСАС (40,4%), чем в группе плацебо (50,3%) [43]. В то же время в более раннем исследовании M. Lequesne и соавт. [44], включавшем 163 пациента с ОА ТБС, скорость рентгенологического прогрессирования в группе НСАС не отличалась от таковой в группе плацебо. Тем не менее при проведении post hoc анализа НСАС значимо замедляли скорость прогрессирования ОА (по сравнению с плацебо) в подгруппе с выраженным сужением ширины суставной щели (≤2 мм). Уменьшение ширины суставной щели за год составило 0,24 мм в группе НСАС и 0,47 мм в группе плацебо.
Многочисленные доказательства эффективности ресвератрола при ОА получены как в работах in vitro, так и в клинических исследованиях. В недавнем обзоре доклинических и клинических исследований приведены данные о позитивном действии ресвератрола при ОА КС и подробно описаны молекулярные механизмы его эффекта. В целом подтверждена его антивоспалительная активность, способность препятствовать апоптозу хондроцитов и стимулировать клеточную аутофагию, что обеспечивает возможность поддержания гомеостаза хрящевой ткани [21]. Появляется все больше доказательств того, что ресвератрол обладает многими позитивными плейотропными свойствами. В частности, исследования in vivo показали, что длительная терапия ресвератролом снижает гипергликемию, улучшает липидный профиль, ослабляет диабетическую кардиомиопатию и защищает b-клетки поджелудочной железы. По данным метаанализа, проведенного X. Zhu и соавт. [45], ресвератрол значимо улучшал показатели глюкозы в плазме крови натощак и инсулина. Также препарат снижал оценку индекса инсулинорезистентности и систолическое и диастолическое артериальное давление у пациентов с СД 2-го типа [45, 46].
Цинк считается одним из наиболее важных микроэлементов в организме человека. Показано, что его дефицит значительно замедляет пролиферацию хондроцитов [27, 47]. В недавнем исследовании, в котором сравнивалось содержание микроэлементов в сыворотке крови более чем у 300 женщин, обнаружено, что у больных ОА уровень цинка был примерно на 7-9 % ниже, чем у здоровых участниц [48]. In vitro добавление цинка приводило к повышению скорости пролиферации. На основании многочисленных исследований определены его терапевтические дозы при ОА. Так, Т.С. Huang и соавт. [49] отмечают, что для предотвращения прогрессирования ОА достаточно принимать цинк в дозе 1,6 мг/кг/сут, в то время как доза 8,0 мг/кг/сут не дает никаких преимуществ.
Однако избыток цинка способен повреждать суставной хрящ. В большинстве случаев при ОА наблюдается повышенный уровень ионов цинка. Считается, что это обусловлено дисбалансом его внутрии внеклеточной концентрации, которая регулируется семейством белков-переносчиков ZIP. В хондроцитах человека при ОА отмечается повышение внутриклеточного уровня цинка и экспрессии ZIP8, что приводит к увеличению продукции множества провоспалительных ферментов (особенно семейства цинк-зависимых MMP), усиливающих деградацию хряща [31, 34, 50]. Важность регуляции этих процессов подтверждается в работе W.S. Choi и J.S.Chun [51]. В хондроцитах мышей с индуцированным ОА ингибирование активности ММП13 путем воздействия на регуляцию ZIP8 с помощью miR-488 (микроРНК, обнаруженной в хондроцитах) восстанавливало дифференцировку хондроцитов.
Помимо влияния на воспаление, изменения в гомеостазе цинка, регулируемом транспортерами ZIP, могут вызывать ряд физиологических нарушений и способствовать возникновению и прогрессированию различных заболеваний (онкологических, неврологических и сердечно-сосудистых) [30, 34].
Получены данные об эффективности препаратов цинка при ОА. В плацебо-контролируемом исследовании у пациентов с ОА КС или ТБС продемонстрировано значительное улучшение показателей индекса WOMAC, а также снижение потребности в НПВП [52].
В последние годы сохраняется интерес к биологическим эффектам шиповника, в том числе возможности его использования при ОА. В 2019 г. опубликован систематический обзор РКИ, посвященных эффектам шиповника у пациентов с ОА. По данным обзора, прием шиповника способствовал уменьшению симптомов ОА, в частности боли по WOMAC, а также снижению общей оценки тяжести заболевания [37].
Эффективность порошка из плодов шиповника при ОА в отношении снижения интенсивности боли по сравнению с плацебо подтверждена результатами метаанализа трех исследований с участием 287 пациентов. Однако все эти исследования были краткосрочными (3-4 мес) [53]. По данным Кокрейновского обзора, включившего результаты 15 РКИ, в которых эффективность шиповника изучалась у большой когорты пациентов с ОА (n=1504), получены доказательства его симптоматического действия — уменьшение интенсивности боли и скованности.
В ряде исследований также установлено, что шиповник регулирует уровень липидов в крови и препятствует развитию ожирения, оказывая косвенное положительное влияние на течение ОА [54].
Результаты нашего исследования согласуются с приведенными выше данными. Мы также подтвердили значимый симптоматический эффект фармаконутрицевтика Ревокка у пациентов с ОА КС, развившийся в короткие сроки после начала терапии (1 мес). Небольшая длительность исследования не позволяет оценить структурно-модифицирующий эффект препарата. В то же время это первое клиническое испытание, в котором изученные ранее по отдельности компоненты объединены в одном препарате. В данном фармаконутрицевтике использованы те же дозы цинка и ресвератрола, эффективность и безопасность которых были исследованы в предыдущих работах. Положительные результаты терапии независимо от фенотипа ОА и коморбидных заболеваний позволяют предположить, что комбинация соединений, входящих в состав Ревокка, оказывает синергическое действие на выраженность симптомов ОА и воспаления (о чем, в частности, свидетельствует снижение потребности в приеме НПВП). Компоненты данного фармаконутрицевтика (помимо НСАС) могут стать дополнительным терапевтическим средством для лечения ОА. А отсутствие отрицательного влияния на коморбидную патологию и значимых взаимодействий с другими лекарственными средствами позволяет применять его при различных локализациях и фенотипах ОА.
Первичная публикация размещена на портале «Современная ревматология»
Литература














