Самые важные новости сферы здравоохранения теперь и в нашем Telegram-канале @medpharm.
FDA одобрило нейростимулятор для лечения болезни Паркинсона в режиме реального времени
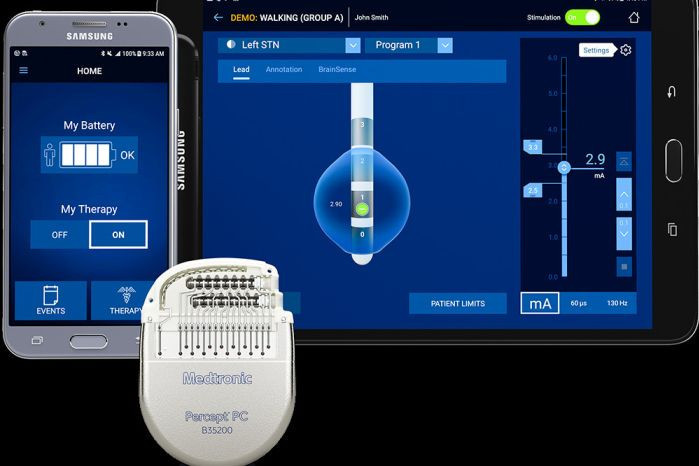
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) одобрило нейростимулятор для лечения двигательных симптомов болезни Паркинсона. Об этом сообщила пресс-служба компании Medtronic, создавшей устройство.
На разработку BrainSense ушло около десяти лет. Это набор электродов, которые вживляются в определенные участки головного мозга. Аналогично работе кардиостимуляторов, система посылает электрические сигналы, в режиме реального времени считывая изменения мозговой активности пациента и соответствующим образом корректируя терапевтическое воздействие.
Устройство анализирует работу областей мозга, связанных с болезнью Паркинсона, – бледного шара и субталамического ядра, и определяет т.н. фазы «включения» и «выключения», т.е. когда то или иное лекарство (как правило леводопа) активно подавляет симптомы, а когда его эффект ослабевает.
Когда наступает «выключение», моторные и немоторные проявления заболевания усиливаются. Как показали исследования, нейростимуляция помогает уменьшить потребность в лекарствах, одновременно минимизируя побочные эффекты, которые могут возникнуть при наложении электрических импульсов на высокую концентрацию препарата в крови.
Компания сообщила, что медучреждения в США активируют первые имплантированные нейроинтерфейсы в течение нескольких недель. Как утверждается, это существенно улучшит качество жизни пациентов, страдающих от неврологической патологии.
В начале февраля FDA одобрило систему введения апоморфина гидрохлорида для профилактики моторных нарушений у пациентов с поздней стадией болезни Паркинсона от компании Supernus Pharmaceuticals, писал «МВ». Устройство обеспечивает постоянную концентрацию лекарства в кровотоке и снижает частоту обострений симптомов.



Нет комментариев
Комментариев: 0