Эозинофильный эзофагит – хроническое, медленно-прогрессирующее иммуноопосредованное (Т2 типа) заболевание пищевода, характеризующееся выраженной эозинофильной инфильтрацией слизистой оболочки пищевода (15 и более эозинофильных лейкоцитов в поле зрения микроскопа высокого разрешения при увеличении х 400 или более 60 в 1 мм2), развитием субэпителиального и подслизистого фиброза, клинически проявляющееся дисфункцией пищевода (дисфагия, обтурация пищевода пищевым комком, рвота проглоченной пищей и др.) [1-10].
Диагноз «эозинофильный эзофагит» следует дифференцировать с другими заболеваниями, сопровождающимися эозинофилией пищевода (например, паразитарные и грибковые инфекции, болезнь Крона, гиперэозинофильный синдром, ахалазия, системные заболевания соединительной ткани и др.). Наряду с эозинофилами в процесс воспаления при ЭоЭ вовлечены различные субпопуляции лейкоцитов (лимфоциты, тучные клетки), эпителиальные клетки, фибробласты, гладкомышечные клетки и другие. Указание же в названии заболевания на эозинофильный характер воспаления призвано подчеркнуть появление и преобладание в составе инфильтрата в слизистой оболочке пищевода нехарактерных для данного отдела пищеварительной трубки клеток лейкоцитарного ряда – эозинофилов [21].
Важно, что из определения ЭоЭ исключен термин «антиген-опосредованное» заболевание, использовавшийся ранее [21]. Согласно накопленным на сегодняшний день данным, не существует однозначного представления о том, что служит триггером развития эозинофильного воспаления в слизистой оболочке пищевода: воздействие пищевых и респираторных антигенов на иммунокомпрометированный организм или же нарушение барьерной функции слизистой оболочки пищевода, способствующее более глубокому проникновению экзогенных антигенов в толщу слизистой оболочки и инициации иммунного воспаления.
Более того, было показано, что терапия ингибиторами протонного насоса, восстанавливая целостность эпителиального барьера, во многих случаях приводит не только к клинической, но и к гистологической ремиссии ЭоЭ. По этой же причине эзофагеальную эозинофилию, разрешающуюся при терапии ИПН, решено более не относить к отдельной нозологической форме, поскольку клинически, эндоскопически, гистологически и даже генетически она неотличима от ЭоЭ и, по всей видимости, является фенотипическим подтипом ЭоЭ [21].
Заболевание имеет относительно невысокую распространенность, которая по усредненным оценкам составляет 10-40 на 100000 человек [10]. Однако его развитие существенно нарушает качество жизни пациентов за счет характерных симптомов – дисфагии, острых эпизодов вклинения пищи в пищевод [1,2,3].
В настоящее время ЭоЭ рассматривается как Т2-ассоциированное воспалительное заболевание, характеризующееся эозинофильной инфильтрацией, рубцеванием и сужением просвета пищевода, а также его дисфункцией. Патогенез ЭоЭ обусловлен Т2-воспалением на всех стадиях заболевания от отека и экссудации слизистой оболочки пищевода до формирования стриктур. К факторам, играющим роль в формировании ЭоЭ, относятся [5,110,111,138]:
генетическая предрасположенность к развитию иммунного ответа по пути активации Т-хелперов 2 типа;
нарушение барьерной функции слизистой оболочки пищевода (воспаление, расширение межклеточных пространств, нарушение синтеза белков плотных контактов), способствующее более глубокой пенетрации антигенов в толщу слизистой оболочки;
сенсибилизация к респираторным и пищевым антигенам.
У детей определенную роль могут играть перинатальные факторы риска: лихорадочные состояния матери во время беременности, недоношенность, рождение путем кесарева сече-ния; после родов – антибиотикотерапия [185]. ЭоЭ достоверно чаще наблюдается у детей с врожденной атрезией пищевода в анамнезе (9,5%-17%) [186].
Роль T2 воспаления является центральной в понимании патогенеза ЭоЭ.
Этиопатогенез ЭоЭ связан с вовлечением звеньев адаптивного и врожденного иммунитета. При воздействии респираторных и пищевых аллергенов на слизистую оболочку пищевода у лиц с имеющейся генетической предрасположенностью к атопии и/или нарушением эпителиального барьера происходит высвобождение эпителиальных цитокинов (аларминов) TSLP, ИЛ-25, ИЛ-33, которые приводят к усилению функций антигенпрезентирующих клеток. Антигенпрезентирующие клетки поглощают антиген, процессируют его и в последующем представляют Т0-лимфоцитам, что приводит к их активации и дифференцировке в Т2-лимфоциты, синтезирующие ИЛ-4, ИЛ-5, ИЛ-13, ИЛ-9. ИЛ-4 вызывает пролиферацию В-лимфоцитов, играет роль в переключении синтеза антител на изотип IgE. IgE, синтезированные плазматическими клетками, фиксируются на высокоаффинных рецепторах FcέRI на мембране тучных клеток. При повторном контакте происходит перекрестное связывание антител с аллергеном, что приводит к дегрануляции тучных клеток и высвобождению преформированных медиаторов, в первую очередь, гистамина, и возникновению гистамин-опосредованных реакций. Воспаление в дальнейшем усиливается при образовании вновь синтезируемых медиаторов (производных арахидоновой кислоты). В то же время, согласно современным представлениям, IgE-зависимый механизм не играет ведущую роль в патогенезе ЭоЭ. Кроме того, ИЛ-4 участвует в дифференцировке T0-лимфоцитов в Т2-лимфоциты.
Наряду с этим в процесс вовлекаются звенья врожденного иммунитета – врожденные лимфоидные клетки 2 типа (ILC2). Данные клетки продуцируют аналогичный спектр цитокинов, за исключением ИЛ-4.
Перечисленные выше цитокины играют ключевую роль в развитии Т2- воспаления при ЭоЭ: их уровень коррелирует со степенью эозинофилии слизистой пищевода. ИЛ-5 является важным фактором, обуславливающим выживаемость и увеличение продолжительности жизни эозинофилов, а также, как и ИЛ-4 и ИЛ-13, способствует миграции эозинофилов в ткани. Известно, что ИЛ-13, оказывая влияние на эпителиальные клетки, приводит к увеличению синтеза эотаксина 3, который является эозинофил-активирующим хемокином, и периостина. Кроме того, ИЛ-13 приводит к гиперплазии базальных клеток, отложению коллагена, ремоделированию ткани, повреждению эпителиального барьера за счет снижения экспрессии десмосомального протеина десмоглеина [138,139]. У пациентов с ЭоЭ отмечается повышенная экспрессия ИЛ-13.
Таким образом формируется эозинофильная инфильтрация стенки, и в первую очередь – слизистой оболочки пищевода. Происходит дегрануляция эозинофилов, высвобождение белков с ферментативной активностью, в том числе главного основного белка, обладающего свойствами гистаминазы, катионного белка, эозинофильной пероксидазы, эозинофильного нейротоксина. Протеолитические ферменты эозинофилов оказывают выраженное деструктивное действие на эпителий, собственную пластинку слизистой оболочки пищевода и подслизистый слой (рисунок 1).
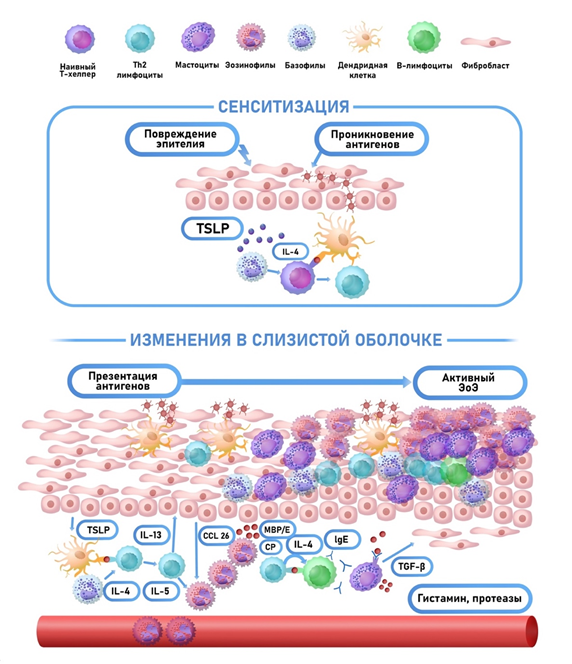
Рисунок 1. Патогенез эозинофильного эзофагита (адаптировано с O'Shea KM, Aceves SS, Dellon ES, Gupta SK, Spergel JM, Furuta GT, Rothenberg ME. Pathophysiology of Eosinophilic Esophagitis. Gastroenterology. 2018): факторы внешней среды (пищевые, воздушные антигены, микроорганизмы), контактируя с антигенпрезентирующими клетками в слизистой оболочке пищевода, стимулируют продукцию цитокинов (ИЛ-4, тимический стромальный лимфопоэтин (TSLP)). Данные цитокины детерминируют дифференцировку наивных Т-лимфоцитов по пути образования Т-хелперов 2 типа. Секреция Т-хелперами 2 типа цитокинов (ИЛ-13, ИЛ-5 и др.) запускает каскад иммунологических реакций с участием эозинофилов, мастоцитов, В-лимфоцитов и др.
Повреждение слизистой оболочки и подслизистого слоя пищевода иммунокомпетентными клетками постепенно приводит к вовлечению в процесс фибробластов, миоцитов и эндотелиоцитов, развитию гиперплазии базального слоя эпителия и гладкомышечных клеток, активации фиброзогенеза и ангионеогенеза в подслизистом слое, что обуславливает потерю эластичности соединительной и мышечной ткани, ремоделированию стенки пищевода, развитию стриктур [2,3,4,5,106].
Существует много фактов, свидетельствующих, что среди внешне-средовых триггеров развития ЭоЭ ведущую роль играют антигенные протеины (аллергены), индуцирующие T2-тип иммунных реакций. Специфическое аллергологическое обследование с использованием кожного тестирования и определения аллерген-специфических IgE выявило сенсибилизацию у 75-80% пациентов с ЭоЭ, что превышает общепопуляционные показатели в три раза. Среди сопутствующих ЭоЭ аллергических заболеваний регистрируются аллергический ринит (АР) у 40-80% больных, бронхиальная астма (БА) – у 14-75%, атопический дерматит (АД) – у 4-60 % пациентов. Нередко в анамнезе больных ЭоЭ отмечаются оральный аллергический синдром как проявление перекрестной пыльцевой/пищевой аллергии и клинические симптомы IgE-опосредованной пищевой сенсибилизации.
По данным систематического обзора и метаанализа, опубликованного в 2023 г и оценивающего эпидемиологию эозинофильного эзофагита с 1976 по 2022 год в мире, заболеваемость ЭоЭ составляет на сегодняшний день 5,31 заболевших на 100000 человек в год (95% ДИ, 3,98-6,63; число исследований – 27, выборка 42191506 человек) [10].
ЭоЭ страдают преимущественно мужчины (75% больных) белой расы (более 90% больных). ЭоЭ встречается во всех возрастных группах, однако чаще в молодом возрасте (средний возраст больных составляет 36-42 года). Прослеживается определенная наследственная предрасположенность: наличие родственников первой степени родства с ЭоЭ повышает риск развития заболевания. ЭоЭ – это хроническое персистирующее заболевание, в связи с чем наблюдается неизбежный ежегодный прирост распространенности ЭоЭ. В среднем распространенность ЭоЭ составляет 40 случаев на 100 000 человек (95% ДИ, 31,10-48,98) [10,111,165].
Распространенность ЭоЭ значительно варьирует в зависимости от географического расположения страны: она максимальна в странах Западной Европы и Северной Америки, значительно ниже в Японии и Китае. Описаны случаи заболевания в Южной Америке, Корее, Турции, Ближнем Востоке, данных по распространенности ЭоЭ в Индии и странах Африки нет [5-16].
Распространенность ЭоЭ варьирует не только в различных географических зонах, но и в группах больных с различными клиническими симптомами. Так, среди лиц, прошедших ЭГДС, ЭоЭ обнаруживается в среднем у 2,4-6,6%. При этом у пациентов с рефрактерной изжогой ЭоЭ выявляется при проведении ЭГДС в 1-8% случаев, у больных с жалобами на некардиальную боль в грудной клетке – в среднем в 6%, у больных с абдоминальной болью – в 4%, при пищевой аллергии – в 5% случаев [10,112].
Среди пациентов с жалобами на дисфагию вероятность обнаружения ЭоЭ при эндоскопическом обследовании значительно выше – 12-23%. У больных с острыми эпизодами вклинения пищи в пищевод ЭоЭ диагностируется не менее чем в 50% случаев [10,112].
В России масштабные эпидемиологические исследования не проводились [5-16,106].
K20 Эзофагит
В настоящее время отсутствует единая классификация эозинофильного эзофагита. С точки зрения клинической значимости стоит выделять эозинофильный эзофагит без осложнений и эозинофильный эзофагит с развитием стриктур и стенозов.
По степени клинико-морфологической активности заболевания выделяют (см. приложение Г4):
Неактивный ЭоЭ;
ЭоЭ слабой степени активности;
ЭоЭ средней степени активности;
ЭоЭ с высокой активностью.
Различают также 3 фенотипа (эндотипа) ЭоЭ [113,114]:
Легкий (ЭoЭ1) – с нормальной эндоскопической картиной или слабо выраженными эндоскопическими и гистологическими изменениями, с хорошим ответом на лечение;
Воспалительный фенотип (ЭoЭ2) – с выраженными воспалительными изменениями, выявляемыми при ЭГДС (отек, экссудат, продольные борозды), выраженной эозинофильной инфильтрацией, экспрессией воспалительных цитокинов, плохим ответом на терапию;
Фибростенозирующий фенотип (ЭoЭ3) – с выраженными фибростенотическими изменениями стенки пищевода, выявляемыми при ЭГДС (кольца, стриктуры, стеноз), развитием фиброза (коллагеновых волокон) в подслизистом слое, обнаруживаемом при патологоанатомическом исследовании и наименьшей экспрессией генов эпителиальной дифференцировки.
Характер и выраженность жалоб значительно отличаются в зависимости от возраста пациента и продолжительности заболевания (таблица 1). Симптомы ЭоЭ у детей раннего возраста неспецифичны и включают срыгивания, тошноту и рвоту, возникающие во время еды, затруднения при проглатывании определенной пищи (орехи, яйца, сухое мясо и др.), боли в животе, отставание в физическом развитии (редко).
Дети подросткового возраста и взрослые предъявляют жалобы на необходимость длительно пережевывать пищу и запивать ее водой («медленно-едящие и много пьющие» пациенты), эпизоды застревания пищи при глотании, часто их беспокоят ГЭРБ -подобные жалобы: изжога и боли за грудиной [115].
Таблица 1. Симптомы ЭоЭ у детей и взрослых
Состояние |
Симптомы у детей первых лет жизни |
Симптомы у детей дошкольного и школьного возраста |
Симптомы у подростков/взрослых |
Нарушение проглатывания пищи |
Поперхивание при кормлении, повторные срыгивания |
Дисфагия |
Дисфагия |
Эпизоды вклинения пищи в пищевод |
Редко |
Часто |
Часто |
Дополнительные симптомы |
Рвота, вздутие живота, боли в животе |
Боль в животе/груди/горле, тошнота, рвота, изжога |
Упорная изжога, ощущение кома в горле |
Психо-эмоциональное состояние |
Беспокойный сон |
Беспокойный сон |
Может не меняться, но возможны страхи и фобии приема некоторых продуктов, нахождения в обществе |
Пищевое поведение |
Отказ от приема пищи |
Снижение аппетита, избирательный подход к еде, длительное пережевывание пищи, обильное питье во время еды, отказ от пищи |
Исключение из рациона твердых и объемных продуктов, измельчение пищи на маленькие кусочки, длительное пережевывание пищи |
Физическое развитие |
От отсутствия набора веса до дефицита массы и развития белково-энергетической недостаточности, возникает необходимость госпитализации для коррекции питания |
Наблюдается дефицит массы тела, вплоть до белково-энергетической и витаминной недостаточности, быстро компенсируется за счет назначения специальных смесей |
Колебания веса небольшие и некритичные, физическое развитие не страдает. |
Для детей характерен преимущественно воспалительный фенотип ЭоЭ, но в подростковом возрасте могут доминировать признаки фибростенотического фенотипа, обусловленного развитием стриктуры пищевода. Взрослые пациенты страдают от симптомов, свидетельствующих о прогрессирующем сужении просвета пищевода: дисфагия, загрудинные боли и эпизоды вклинения пищи в пищевод. Описаны также случаи спонтанного разрыва пищевода, возникшие у больных ЭоЭ на фоне обтурации пищевым комком (синдром Бурхаве) (рисунок 2) [18,20].
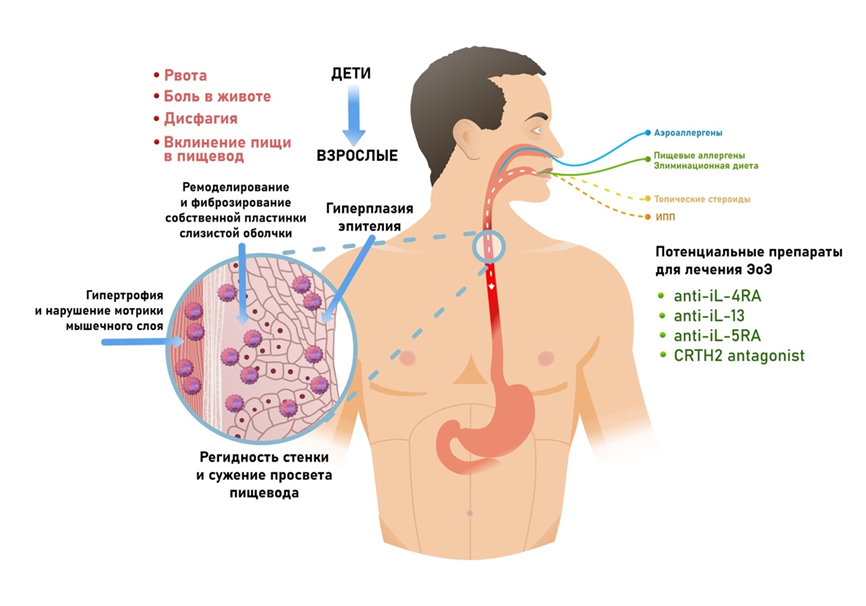
Рисунок 2. Симптомы ЭоЭ у детей и взрослых (адаптировано с O'Shea KM, Aceves SS, Dellon ES, Gupta SK, Spergel JM, Furuta GT, Rothenberg ME. Pathophysiology of Eosinophilic Esophagitis. Gastroenterology. 2018)
Дисфагия у пациентов с ЭоЭ может возникать остро (при застревании пищевого комка твердой консистенции) или беспокоить пациентов постоянно, вынуждая изменять пищевое поведение [1,3,4,17-21,166,167].
Критерии установления диагноза заболевания/состояния:
Диагноз «эозинофильный эзофагит» устанавливают при выявлении совокупности:
клинических симптомов дисфункции пищевода (дисфагия и/или вклинение пищи в пищевод – у взрослых; рвота, упорные срыгивания, трудности при кормлении и глотании, абдоминальная боль – у детей);
характерной эндоскопической картины (отек, кольца, экссудат, продольные борозды, стриктуры);
патоморфологического подтверждения эозинофильной инфильтрации пищевода (с количеством эозинофилов 15 и более в поле зрения при большом увеличении (х400) – (или ≥15 эозинофилов/0,3 мм2 или >60 эозинофилов/мм2 при отсутствии других причин эозинофилии пищевода) [1,2,21,116,166,167,168].
Комментарии: Проведение эндоскопического исследования пищевода у лиц с характерной симптоматикой с обязательным выполнением патологоанатомического исследования не менее 6 биоптатов из дистального и среднего/проксимального отделов пищевода является обязательным диагностическим минимумом для установления диагноза «эозинофильный эзофагит».
Патологоанатомическое исследование включает осмотр биоптатов, окрашенных гематоксилином и эозином. Главным критерием установления диагноза ЭоЭ служит интраэпителиальная эозинофильная инфильтрация с количеством эозинофилов в поле зрения микроскопа высокого разрешения 15 и более при увеличении х 400 (или ≥15 эозинофилов/0,3 мм2 или >60 эозинофилов/мм2) [116].
Важно, что факт обнаружения большого количества эозинофилов в слизистой оболочке пищевода не может служить единственным критерием диагноза «эозинофильный эзофагит». Существует ряд заболеваний, протекающих с эзофагеальной эозинофилией: ГЭРБ, эозинофильный гастроэнтерит, целиакия, болезнь Крона, лучевой и инфекционный эзофагит (грибковые и паразитарные инфекции), гиперэозинофильный синдром, лекарственный эзофагит, васкулиты, ахалазия кардии, системные заболевания соединительной ткани, злокачественные опухоли (таблица 2) [1,2,3,21].
Таблица 2. Заболевания, ассоциированные с эозинофилией пищевода [1,21,116]
Заболевание |
Диагностические критерии |
Эозинофильный гастроэнтерит или колит |
Эозинофильная инфильтрация слизистой оболочки желудка и двенадцатиперстной кишки, толстой кишки |
Болезнь Крона |
Экстраэзофагеальные поражения, подтвержденные данными колоноскопии, компьютерной томографии, морфологического исследования |
Паразитарные и грибковые инфекции |
Экстраэзофагеальные симптомы и данные микробиологических исследований (крови, стула, слюны и т.д.) |
Ахалазия |
Клинические особенности (дисфагия, рвота), данные манометрии пищевода, рентгенологического исследования пищевода |
Гиперэозинофильный синдром |
Число эозинофилов в периферической крови >1,5 x 109/л, эозинофильно-обусловленные поражения внутренних органов (сердечно-сосудистая система, нервная система, кожа, желудочно-кишечный тракт, дыхательная система) |
Лекарственная гиперчувствительность |
Сыпь, лихорадка, лимфаденопатия, мультиорганные поражения, разрешение симптоматики после отмены лекарственного препарата |
Целиакия |
Данные морфологического исследования слизистой оболочки тонкой кишки, данные серологического исследования (антитела к тканевой трансглутаминазе, эндомизию) |
|
Васкулиты; Пемфигоид; Системные заболевания соединительной ткани; Болезнь трансплантат против хозяина |
Системные проявления |
Таким образом, диагноз «эозинофильный эзофагит» может быть установлен только по совокупности клинических симптомов дисфункции пищевода и патологоанатомического подтверждения эозинофильной инфильтрации пищевода, после обязательного исключения заболеваний, сопровождающихся эозинофилией пищевода (алгоритм диагностики представлен в Приложении Б).
Рекомендуется тщательно оценить жалобы и анамнез пациента с подозрением на эозинофильный эзофагит, так как эти данные служат неотъемлемой, а в ряде случаев критически важной частью обследования пациентов [1].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: Клинические проявления ЭоЭ (подробно описаны в разделе 1.6 настоящих рекомендаций) у взрослых пациентов и подростков включают дисфагию при приеме твердой пищи, необходимость длительно жевать пищу, измельчать и блендировать, обильно запивать пищу жидкостью, эпизоды вклинения пищи в пищевод (эпизоды острой обтурационной дисфагии), загрудинную боль, не связанную с глотанием. Для детей раннего и дошкольного возраста более характерны жалобы на срыгивание съеденной пищей, изжогу и отрыжку, рвоту, боль в животе, частый отказ от пищи, задержка физического развития [21-26]. Разработаны опросники для оценки тяжести и активности симптомов, эффективности терапии ЭоЭ (см. приложение Г1).
Пациентам с подозрением на эозинофильный эзофагит рекомендуется физикальное обследование (осмотр кожных покровов, перкуссия, пальпация, аускультация при заболеваниях пищевода, желудка, двенадцатиперстной кишки и органов дыхания), измерение массы тела и роста для определения нутритивного статуса и признаков атопических заболеваний [1].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: Характерные изменения в объективном статусе пациента с ЭоЭ отсутствуют. Однако, при внимательном физикальном обследовании могут быть обнаружены дефицит питания, отставание в физическом развитии, наличие признаков атопических заболеваний кожи, пищевой аллергии, заболеваний органов дыхания (бронхиальная астма). Несмотря на поражение слизистой оболочки пищевода, изменения слизистой оболочки полости рта отсутствуют.
Пациентам с подозрением на эозинофильный эзофагит рекомендуется выполнить общий (клинический) анализ крови развернутый для исключения других заболеваний, сопровождающихся эозинофилией пищевода, оценки эозинофилии периферической крови [115].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: При проведении общего (клинического) развернутого анализа крови эозинофилия наблюдается у 5-50% пациентов с ЭоЭ [116]. Эозинофилия не является специфичной только для ЭоЭ, в связи с чем этот показатель необходимо оценивать с учетом возраста пациента, наличия аллергических заболеваний, времени года (цветение трав и деревьев) и других факторов, способных повлиять на изменение числа эозинофилов в крови [115].
Всем пациентам с подозрением на эозинофильный эзофагит рекомендовано проведение ЭГДС с диагностической целью [1,21,117,166,167].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: Эндоскопическая шкала EREхFS (приложение Г3, приложение А3, рисунки 1, 1а, 1б,1в,1г,1д), оценивает 5 главных эндоскопических признаков ЭоЭ (Edema-отек, Rings-кольца, Exudates-экссудат, Furrows-борозды, Strictures-стриктуры) в баллах [33,118,119,120,121,188]. У 10=25% пациентов с ЭоЭ при эндоскопии пищевода видимых патологических изменений не определяется [117], в связи с чем эндоскопическое исследование пищевода не может служить единственным критерием установления диагноза ЭоЭ без патологоанатомического исследования биоптатов из пищевода [122,123]
Всем пациентам с подозрением на эозинофильный эзофагит рекомендовано при ЭГДС проводить биопсию пищевода с помощью эндоскопии с забором не менее 6 биоптатов из наиболее изменённых участков слизистой оболочки (по 3 из дистального и среднего/проксимального отделов пищевода) с целью установления диагноза [1,21].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Всем пациентам с подозрением на ЭоЭ при проведении ЭГДС должна быть выполнена множественная биопсия пищевода с помощью эндоскопии.
Показаниями для проведения биопсии пищевода с помощью эндоскопии служат:
1. Эндоскопическая картина, характерная для эозинофильного эзофагита;
2. Наличие характерных клинических симптомов ЭоЭ даже в случае нормальной эндоскопической картины;
3. Симптомы ГЭРБ у детей (изжога, загрудинная боль, срыгивание), рефрактерные к терапии ИПН, даже в случае нормальной эндоскопической картины.
Для получения корректных патоморфологических результатов необходимо производить биопсию не менее, чем в 6-8 участках из дистального и среднего/проксимального отделов пищевода (из наиболее измененных участков слизистой оболочки). Биоптат должен включать эпителий на всю его глубину и, по возможности, собственную пластинку слизистой оболочки (для оценки степени субэпителиального фиброза) [1,3,27-33].
Пациентам с подозрением на эозинофильный эзофагит перед проведением диагностической ЭГДС с биопсией пищевода с помощью эндоскопии рекомендуется отмена ИПН и глюкокортикоидов (если позволяет состояние) как минимум за 3 недели до эндоскопического исследования для предотвращения ложных результатов при диагностике ЭоЭ [1,166,167,168].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: Прием ИПН, топических или системных глюкокортикоидов может значительно изменять эндоскопическую и гистологическую картину заболевания. В случае, если пациенту с подозрением на ЭоЭ планируется диагностическая ЭГДС, необходимо (если позволяет состояние пациента) отменять медикаментозную терапию как минимум за 3 недели до эндоскопического исследования [1,168].
Всем пациентам, поступившим в лечебно-профилактическое учреждение в экстренном порядке с дисфагией, связанной с вклинением пищевого комка в пищевод, после извлечения/низведения пищевого комка и устранения дисфагии рекомендуется произвести (даже при отсутствии явных стенотических поражений (опухоль; рубцовая стриктура) и характерных эндоскопических признаков ЭоЭ) множественную биопсию слизистой оболочки дистального и среднего/проксимального отделов пищевода (не менее 6 биоптатов) c помощью эндоскопии с целью установления диагноза и дифференциальной диагностики причины вклинения [1].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Всем пациентам с эпизодом острого вклинения пищевого комка в пищевод, даже в случае спонтанного разрешения непроходимости, рекомендовано проведение ЭГДС для дифференциальной диагностики причины вклинения и биопсии слизистой оболочки пищевода с помощью эндоскопии (не менее 6 биоптатов; по 3 из дистального и среднего/проксимального отделов пищевода) с целью установления диагноза [1].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: Выполнение биопсии в момент извлечения застрявшего пищевого болюса технически невозможно в связи с отсутствием подготовки к эндоскопическому исследованию. В связи с чем пациент должен быть приглашен на плановое повторное эндоскопическое исследование с биопсией из пищевода в ближайшее время [175-184].
Для получения корректных патоморфологических результатов необходимо производить биопсию не менее, чем в 6=8 участках из дистального и среднего/проксимального отделов пищевода (из наиболее измененных участков слизистой оболочки). Биоптат должен включать эпителий на всю его глубину и, по возможности, собственную пластинку слизистой оболочки (для оценки степени субэпителиального фиброза) [1,3,27-33].
Всем пациентам детского возраста с типичными симптомами ГЭРБ, рефрактерными к терапии ИПН и отсутствии иных причин отсутствия эффекта от лечения, рекомендовано проведение ЭГДС с биопсией пищевода с помощью эндоскопии для исключения эозинофильного эзофагита [1,129,130].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: У пациентов детского возраста при ЭоЭ часто наблюдается нормальная эндоскопическая картина в пищеводе (до 21-42,8%), поэтому при проведении ЭГДС у детей с неспецифическими симптомами со стороны верхних отделов пищеварительного тракта следует рассмотреть проведение биопсии из пищевода с помощью эндоскопии (даже при отсутствии визуальных признаков ЭоЭ) [1,32].
Особое внимание следует уделить пациентам детского возраста с типичными симптомами ГЭРБ, рефрактерными к терапии ИПН, поскольку в 30% случаев ЭоЭ у детей сопровождается изжогой [31,129].
Всем пациентам с подозрением на ЭоЭ рекомендовано проведение патологоанатомического исследования биопсийного материала из пищевода с целью подтверждения диагноза [1,21,117,124,166,167].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Патологоанатомическое исследование включает осмотр биоптатов, окрашенных гематоксилином и эозином с подсчетом количества эозинофилов при большом увеличении (х400) [1,21,117,124,125]. Главным критерием установления диагноза ЭоЭ служит интраэпителиальная эозинофильная инфильтрация с количеством эозинофилов в поле зрения микроскопа при большом увеличении – 15 и более (или ≥ 60 эозинофилов на 1 мм2) (приложение А3: рисунок 2а).
Дополнительными гистологическими критериями ЭоЭ являются эозинофильные микроабсцессы, гиперплазия базального слоя эпителия, расширение межклеточных пространств, расположение эозинофилов в поверхностных слоях эпителия, мастоцитарная и лимфоцитарная инфильтрация, удлинение сосочков и фиброз собственной пластинки слизистой оболочки (приложение А3) [1].
Для стандартизации гистологической оценки биоптатов целесообразно использовать систему балльной оценки восьми наиболее характерных гистологических изменений, обнаруживаемых у больных с ЭоЭ (приложение Г4: система балльной оценки биоптатов при ЭоЭ (EoEHSS)) [1,3,123,125-127].
Пациентам с диагнозом «эозинофильный эзофагит» и стойкой дисфагией рекомендовано проведение рентгеноскопии пищевода с контрастированием с целью определения наличия и распространенности стриктур пищевода [1].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: Рентгеноскопия пищевода с контрастированием в диагностике ЭоЭ является дополнительным методом, позволяющим с высокой точностью выявить проксимальные и дистальные стриктуры пищевода, оценить их протяженность, диаметр пищевода в месте сужения, принять решение о необходимости баллонной дилатации стеноза пищевода или бужирования пищевода (приложение А3:рисунок 3) [120,128,129].
Пациентам с ЭоЭ и дисфагией, сохраняющейся несмотря на адекватно проводимое лечение и отсутствие стриктур в пищеводе по данным ЭГДС, рекомендовано проведение функциональных методов исследования (пищеводная манометрия высокого разрешения, рН импедансометрия пищевода, импеданспланиметрия пищевода) с целью оценки функции пищевода и НПС и/или верификации ГЭРБ [1].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: Пищеводная манометрия позволяет оценить сократительную функцию пищевода и НПС. У пациентов с ЭоЭ при проведении манометрии нередко выявляются такие нарушения, как неэффективная моторика пищевода, эзофагоспазм, обструкция пищеводно-желудочного соединения. С помощью манометрии возможно проведение дифференциального диагноза между ахалазией пищевода и ЭоЭ. В некоторых случаях (для верификации сочетанной ГЭРБ) пациентам может быть проведена суточная рН-импедансометрия, которая позволяет выявить эпизоды кислых и некислых рефлюксов в пищевод, длительность экспозиции кислоты и болюса в пищеводе [129,130,131,140].
Пациентам с диагнозом «эозинофильный эзофагит» не рекомендовано рутинное проведение накожных исследований реакций на аллергены, исследование уровня общего иммуноглобулина Е в крови, исследование уровня антител к антигенам растительного, животного и химического происхождения в крови вследствие их низкой информативности при ЭоЭ [1,166,167,168].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Аллергологическое тестирование может быть проведено пациентам с ЭоЭ и сопутствующими аллергическими заболеваниями (аллергический ринит, бронхиальная астма, атопический дерматит), а также пациентам с подозрением на пищевую аллергию. Диагностика коморбидных аллергических заболеваний (БА, АтД, АР/конъюнктивит) рассматривается как необходимый компонент оценки атопической конституции у пациентов с ЭоЭ и проводится врачом-аллергологом-иммунологом. При подозрении на пищевую аллергию выполняются кожные тесты с аллергенами, определение специфических IgE, тесты элиминации-провокации [1,21].
Целями терапии ЭоЭ являются достижение клинической (купирование симптомов ЭоЭ) и гистологической ремиссии заболевания, предотвращение развития осложнений (стриктуры пищевода).
После достижения ремиссии лечение не должно прекращаться с целью поддержания ремиссии и предотвращения рецидива симптомов и осложнений [1,21,166,167,168].
Под гистологической ремиссией ЭоЭ подразумевают разрешение эозинофильного воспаления (5-15 эозинофилов в поле зрения микроскопа высокого разрешения при увеличении х400 (в 0,3 мм)2 или менее 60 эозинофилов в 1 мм2). Под полной гистологической ремиссией понимают уменьшение количества эозинофилов <5 в поле зрения при большом увеличении (или в 0,3 мм2), что соответствует полю зрения при большом увеличении) [1,117,124].
Современная концепция лечения больных ЭоЭ включает медикаментозную терапию, диетические ограничения, и, при необходимости, проведение эндоскопической баллонной дилатации/эндоскопического бужирования стриктур и/или стеноза пищевода.
Диетические ограничения, ИПН и глюкокортикоиды являются терапией первой линии в лечении пациентов с ЭоЭ. Тактика лечения зависит от предпочтений пациента и может быть впоследствии изменена. Эндоскопическая дилатация (баллонная дилатация стеноза пищевода) или бужирование пищевода эндоскопическое проводятся пациентам со стриктурами и тяжелой дисфагией (эпизодами вклинения пищи в пищевод) независимо от типа применяемой базисной терапии [1,166,167].
Комментарии: До 50% больных с ЭоЭ отвечают на терапию ИПН установлением клинической и гистологической ремиссии (<15 эозинофилов в поле зрения микроскопа высокого разрешения). На сегодняшний день ИПН рассматриваются как препараты первой линии в терапии ЭоЭ в связи с высокой эффективностью, удобством применения (по сравнению с топической глюкокортикоидной терапией), безопасностью.
Решение о выборе метода лечения целесообразно принимать совместно с пациентом, обсудив с ним все положительные и отрицательные стороны альтернативных методов лечения (ИПН, топическая глюкокортикоидная терапия, эмпирическая диета) [1,21,166,167].
Топическая глюкокортикоидная терапия и диета являются терапией выбора для пациентов, не достигших ремиссии на фоне приема ИПН. В данном случае решение о тактике лечения должно приниматься исходя из возраста пациента, выраженности его симптомов и тяжести воспалительного процесса в слизистой оболочке пищевода [1,21,117]. Известно, что дети и подростки с трудом придерживаются диетических ограничений, в связи с чем, более рациональным для них будет назначение топических глюкокортикоидов. Справедливо это и для пациентов с тяжелыми симптомами заболевания, у которых диетические ограничения как монотерапия, скорее всего будут неэффективны.
Важно, что терапия пациентов с ЭоЭ может со временем изменяться (при желании пациента, возникновении побочных эффектов и проч.), поскольку существуют данные, показывающие, что достижение ремиссии на фоне ИПН не исключает эффективности глюкокортикоидов или диеты и наоборот [1,21,132,133].
Алгоритм лечения пациентов с ЭоЭ представлен в Приложении Б1 [1].
Всем пациентам с установленным диагнозом «эозинофильный эзофагит» рекомендуется проведение терапии как можно в более ранние сроки с целью предотвращения развития осложнений (стриктуры), требующих эндоскопического лечения [1,166,167].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Отсутствие терапии после манифестации заболевания длительностью 2 года, приводит к развитию стриктур пищевода у 17%-19% больных, начало лечения через 20 лет после появления первых симптомов осложняется стриктурами у 71% пациентов. В то же время своевременное начало лечения позволяет предотвратить развитие фибростенотических изменений в стенке пищевода [35-37].
3.1 Диета
Опубликованный в 2023 г систематический обзор и мета-анализ 34 исследований с участием 1762 человек с использованием различных диетических режимов подтвердил, что диетотерапия является эффективным методом лечения пациентов с ЭоЭ, с общим показателем достижения гистологической ремиссии 53,8-60%. В лечении ЭоЭ диетотерапия лишь немого уступала в эффективности топическим ГКС, применение которых позволяет достичь гистологической ремиссии у 68,3%-76,8% пациентов [169-171].
В лечении ЭоЭ используются элементная диета и эмпирическая диета с исключением с исключением наиболее часто встречающихся пищевых триггеров (приложение Б).
Рекомендовано длительное соблюдение диеты пациентам с ЭоЭ с целью достижения клинической и гистологической ремиссии без медикаментозной терапии [1,21,117,166,167,169,170,171,172].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
Комментарии: Диета может быть назначена в качестве первой линии терапии (монотерапия) ЭоЭ. Может быть использован один из следующих диетических режимов [1,21,47,53,54,117,124,169,170,171,172]:
1. Назначение полного энтерального питания на основе аминокислотной смеси.
2. Назначение эмпирической диеты с исключением 6 групп продуктов (молочные продукты, глютен, яйца, соя, рыба/моллюски и орехи/бобовые);
3. Назначение эмпирической диеты с исключением 4-х групп продуктов (молочные продукты, глютен, яйцо, соя);
4. Назначение эмпирической диеты с исключением 2-х групп продуктов (молочные продукты, глютен или яйца);
5. Назначение эмпирической диеты с исключением только молочных продуктов.
Не рекомендовано рутинное сочетание диеты и медикаментозной терапии всем пациентам с ЭоЭ. Такая комбинация может быть рассмотрена только при неэффективности медикаментозной терапии [1,166,167,172].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: Медикаментозная терапия и диета имеют сопоставимую эффективность в достижении гистологической ремиссии заболевания. Сочетание диеты и медикаментозной терапии может быть рассмотрено только в случае неэффективности монотерапии диетой или медикаментами [1,169-172].
Пациентам с ЭоЭ не рекомендовано применение диет, основанных на данных аллергологического (накожных исследований реакций на аллергены (кожные скарификационные, аппликационные и прик-тесты), исследования уровня антител к антигенам растительного, животного и химического происхождения в крови (определение специфических IgE к продуктам)) тестирования в связи с их невысокой эффективностью в индукции и поддержании ремиссии в большинстве случаев [1,21,39,40,41,44,49,133,134,171,172].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2)
Комментарии: Эффективность (гистологическая ремиссия) элиминационной диеты, основанной на результатах аллергологического тестирования у взрослых пациентов с ЭоЭ составляет 45,5% (данные мета-анализа 2014 г) – 45,7% (данные мета-анализа 2023 г) [39,49,169], причем эффективность данного подхода у взрослых значительно ниже, чем у детей [170,171]. В настоящее время считается нецелесообразным назначение таргетной диеты для лечения ЭоЭ в связи с ее невысокой эффективностью, за исключением случаев пищевой аллергии, доказанной с помощью аллергологического тестирования (кожные тесты, выявление специфических IgE, провокационные тесты) [1,133,172].
Пациентам с ЭоЭ в случае не IgE-опосредованных реакций может быть рекомендована диета с исключением 6 групп продуктов питания (молоко животного происхождения, глютен, рыба и морепродукты, орехи, яйца, соя и бобовые) с целью достижения ремиссии [43-54,169–172].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2)
Пациентам с ЭоЭ в случае не IgE-опосредованных реакций может быть рекомендована диета с исключением 4 групп (молоко животного происхождения, глютен, яйца, соя/бобовые) или 2 групп (молоко животного происхождения и глютен или молоко животного происхождения и яйца) продуктов питания с целью достижения ремиссии. Такая диета характеризуется более высоким уровнем приверженности пациентов, однако несколько меньшей эффективностью, чем диета с исключением 6 групп продуктов [39,43,45,46,47,48,49,52,135,136,169-172].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2)
Комментарии: Назначение эмпирической диеты в качестве монотерапии при исключении 6 продуктов питания (молоко животного происхождения, глютен, рыба/морепродукты, орехи, яйца, бобовые/соя) приводит к индукции гистологической ремиссии у 61,3-63,9% пациентов, независимо от их возраста [39,169,172]. Диета с исключением 4 групп продуктов (молоко, глютен/пшеница, яйца и соя) – у 49,4%-54,7% [39,169], при исключении двух групп продуктов частота гистологической ремиссии составляет 44,3% (36,1-52,8%) [39].
Выбор диеты с исключением одной, 2-х, 4-х или 6 групп продуктов зависит от данных анамнеза, тяжести симптомов и предпочтения пациента и/или родителя. Диета должна назначаться и корректироваться с участием опытного врача-диетолога. При необходимости должны быть использованы специализированные продукты лечебного питания, обогащенные продукты (приложение Б, алгоритм 3) [1,46-52,137,173].
Пациентам с ЭоЭ в случае неэффективности медикаментозной терапии и элиминационных диет рекомендовано рассмотреть назначение элементной диеты (аминокислотные смеси) с целью достижения ремиссии [1,21,141,142].
Для взрослой популяции Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Для детской популяции Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Элементная диета включает употребление в пищу специально приготовленных аминокислотных смесей с минимальной антигенной активностью (на фоне полного исключения из рациона любой другой пищи). Назначение полного энтерального питания (аминокислотная смесь) позволяет достичь клиническую, эндоскопическую и гистологическую ремиссию у 90,8% (95% ДИ 84,7-95,5%) пациентов с ЭоЭ детского и взрослого возраста [38,39,141,142]. Элементные диеты имеют ограниченную роль при эозинофильном эзофагите, они обладают высокой эффективностью, но низким уровнем соблюдения режима лечения и должны применяться для пациентов, невосприимчивых к другим видам лечения [1,38,39]. Назначение аминокислотных смесей может быть рассмотрено в качестве единственного источника питания у детей младше 1 года (в рацион которых еще не вводили густую пищу), а также в качестве дополнительного питания [142,143]. Для лечения ЭоЭ не следует использовать смеси на основе цельного коровьего белка, смеси на основе частичного или полного гидролиза белка, а также смеси на основе козьего молока и сои [1].
При назначении диетических ограничений пациенту с ЭоЭ рекомендован прием (осмотр, консультация) врача-диетолога с целью снижения риска негативных последствий элиминационной диеты [143,144].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: Диетические ограничения могут привести к снижению темпа роста у детей, потере массы тела у взрослых [145], а также к дефицитным состояниям (например, дефицит витамина Д и кальция) [146]. С целью снижения риска негативных последствий элиминационной диеты целесообразно включение в мультидисциплинарную команду, которая должна заниматься лечением пациентов с ЭоЭ, врача-диетолога [144,145]. В том случае, если ремиссия была достигнута на фоне диетотерапии, но продолжение соблюдения диеты неприемлемо для пациента, либо на фоне диетических ограничений развились дефицитные состояния, можно рассмотреть в качестве противорецидивной терапии переход на прием ИПН [132].
3.2. Медикаментозное лечение
Пациентам с ЭоЭ рекомендовано рассмотреть пероральную монотерапию ИПН (#омепразол** или эквиваленты: #эзомепразол** и др.) в стандартной дозе (для взрослых 20 мг 2 раза в сутки, для детей 1 мг/кг 2 раза в сутки) на срок 8-12 недель для индукции клинической и гистологической ремиссии [1,21,55,62,166,167,168].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
В случае достижения клинической и гистологической ремиссии пациентам с ЭоЭ, получающим ИПН, рекомендуется продолжить постоянный прием ИПН в минимально эффективной дозе с целью поддержания ремиссии [1,21,55–65,166,167].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: В терапии взрослых больных ЭоЭ возможно применение #омепразола** в стандартной суточной дозировке дважды в день (20 мг 2 раза в день) или эквивалентных доз других ИПН [1,3,21,59-62]. Для индукции ремиссии эзофагита у детей возможно назначение ИПН (#омепразола** или #эзомепразола**) из расчета 1 мг/кг на 1 прием дважды в день в течение 8 недель. Дозы ИПН у детей не должны превышать следующие: #эзомепразол** 40 мг в день или #омепразол** 40 мг 2 раза в день [1,2,166,167,168].
Мета-анализ по сравнению режима приема ИПН (один раз в день или два раза в день) показал незначительное повышение эффективности лечения при разделении суточной дозировки на 2 приема [62]. Продолжительность курса ИПН для индукции ремиссии – 8-12 недель [1].
ИПН индуцируют клиническую и гистологическую ремиссию у значительной доли взрослых и детей с ЭоЭ (50%-57%) [55,60,61,147,148].
После достижения ремиссии доза ИПН может быть снижена до минимальной эффективной дозы, решение о величине и длительности поддерживающей дозы принимается индивидуально для каждого конкретного пациента [1,3,21,55–65,149,150].
Рекомендовано рассмотреть пероральную монотерапию #будесонидом** в стандартной дозе (для взрослых 2-4 мг в сутки, для детей при росте менее 150 см – 1 мг в сутки, при росте 150 см и более – 2 мг в сутки) на срок 8-12 недель для индукции ремиссии пациентам с ЭоЭ, не достигшим клинической и гистологической ремиссии на фоне приема ИПН [1,3,21,66-78,151–154,166,167].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 1).
В случае достижения клинической и гистологической ремиссии пациентам с ЭоЭ, получающим #будесонид**, рекомендуется продолжить прием #будесонида** в стандартной дозе (для взрослых 1-2 мг в сутки, для детей 1 мг в сутки) с целью поддержания ремиссии длительно (до 1 года и более) [1,3,21,66-78,104,105,137,151–154,166,167].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Препаратами выбора в индукции и поддержании гистологической ремиссии являются топические глюкокортикоиды.
Для лечения больных ЭоЭ используется густая суспензия #будесонида** (смешать 1-2 мг #будесонида** с 5 мг сукралозы (или с сиропом агавы/кленовым сиропом)) [151,152]. Более эффективен прием #будесонида** на ночь уже в постели, так как в горизонтальном положении препарат длительно находится в пищеводе и обеспечивается максимальный контакт со слизистой оболочкой [167].
В течение 30-60 минут после применения топических глюкокортикоидов важно воздержаться от приема пищи и жидкостей во избежание удаления лекарственного препарата со слизистой оболочки пищевода.
Дозы топических глюкокортикоидов для детей необходимо подбирать исходя из антропометрических показателей: для индукции ремиссии при росте менее 150 см назначается 1 мг #будесонида** в сутки, при росте 150 см и более – 2 мг #будесонида** в сутки (в один или два приема). В случае, если на такой дозе не удается достичь гистологической ремиссии, допустимо увеличить дозу до #4 мг в сутки (для детей старше 11 лет, рост более 150 см) [1,151,152,153,154].
После достижения ремиссии, подтвержденной гистологически, через 8-12 недель, возможно применение поддерживающей терапии в дозе 0,5 мг 2 раза в сутки или 1 мг 2 раза в сутки [1,66-79,166,167,168] в течение 1 года и более с последующей эндоскопической и гистологической оценкой [1,137,167]. Для поддерживающей терапии у детей должна подбираться минимально эффективная доза #будесонида** в зависимости от роста, веса и выраженности побочных эффектов [155]. В дальнейшем с целью снижения риска побочных эффектов можно рассмотреть 2 опции: снижение дозы глюкокортикоидов или переход на прием ИПН [1,166,167,168].
В инструкциях к доступным на территории РФ формам для топической глюкокортикоидной терапии отсутствует указание о применении этих препаратов с целью лечения ЭоЭ. В связи с этим перед назначением топической глюкокортикоидной терапии необходимо проведение врачебной комиссии и обсуждение с пациентами и/или законными представителями соотношения пользы и потенциального вреда назначаемых препаратов.
Рекомендуется рассмотреть проведение мониторинга уровня кортизола (исследование уровня общего и свободного кортизола в крови, уровня свободного кортизола в моче) детям, получающим высокие дозы топической глюкокортикоидной терапии в течение длительного времени, а также в случае одновременного использования интраназальных глюкокортикоидов (например, с целью лечения аллергического ринита) – для своевременной диагностики и терапии надпочечниковой недостаточности [1,21].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: Назначение #будесонида** в дозе 0,5-1 мг в сутки в течение 8-43 недель не приводит к снижению уровня кортизола. До настоящего времени не было зафиксировано отрицательного влияния применения топических глюкокортикоидов на темп роста у детей [155]. Тем не менее, имеются данные, что длительная (более 6 месяцев) глюкокортикоидная терапия может приводить к снижению функции коры надпочечников у 10% детей [80] и субоптимальному уровню стимулированного кортизола [81].
Применение глюкокортикоидов (системных) для лечения ЭоЭ не рекомендовано вследствие риска развития побочных эффектов [1,21,66,156].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 1).
Комментарии: Доказано, что системные и топические глюкокортикоиды одинаково эффективны в достижении клинической и гистологической ремиссии ЭоЭ. Однако системные побочные эффекты, такие как повышение аппетита, увеличение массы тела, кушингоид развивались у 40% больных, принимавших преднизолон**. В то время как топическая глюкокортикоидная терапия сопровождалась кандидозом пищевода лишь у 15% больных [66].
Рекомендовано рассмотреть дупилумаб** для лечения пациентов с ЭоЭ в возрасте от 1 года и старше массой тела от 5 кг и выше в дозировке для пациентов с массой тела от 5 до <15 кг по 200 мг каждые 3 недели; для пациентов с массой тела от 15 до <30 кг по 200 мг каждые 2 недели; для пациентов с массой тела от 30 до <40 кг по 300 мг каждые 2 недели; для пациентов с массой тела 40 кг и более по 300 мг 1 раз в неделю) с целью индукции и поддержания ремиссии [1,107,159, 162,166,167,168,174].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
Комментарии: Дупилумаб** представляет собой человеческие моноклональные антитела к субъединице альфа рецептора IL-4Rα – общей для IL-4 и 13 [97-102]. В 2023 г дупилумаб** зарегистрирован в РФ для лечения ЭоЭ. В клинических исследованиях дупилумаб** показал высокую эффективность в достижении клинической и гистологической ремиссии (58-62%) у детей от 1 года и взрослых с ЭоЭ [107,108,159,174]. Доля пациентов с гистологической ремиссией, наблюдаемой через 24 недели, сохранялась до 52-й недели [107,108,159]. Дупилумаб** характеризовался благоприятным профилем безопасности. Терапия дупилумабом** не требует проведения дополнительных лабораторных или инструментальных обследований и рутинного мониторинга лабораторных показателей до и во время лечения [159].
С целью оценки эффективности лечения (индукции ремиссии) дупилумаб** назначают на 12 недель, после чего проводят повторную ЭГДС с биопсией пищевода с помощью эндоскопии с описанием эндоскопической и гистологической динамики [167,168,169].
В случае достижения клинической и гистологической ремиссии пациентам с ЭоЭ, получающим генно-инженерную биологическую терапию, рекомендуется продолжить лечение на постоянной основе (длительно), применявшимся для индукции ремиссии препаратом с целью поддержания ремиссии [1,159,166,167,168,174].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Не рекомендованы ингибиторы фактора некроза опухоли альфа (TNF-α), омализумаб**, меполизумаб**, реслизумаб**, бенрализумаб** для лечения ЭоЭ в связи с недостаточной эффективностью [1,21,91–101,160,166,167].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Использование препаратов бенрализумаб**, омализумаб**, меполизумаб**, реслизумаб** не показало эффективности в лечении пциентов с эозинофильным эзофагитом в клинических исследованиях [91-96,157,158,161, 160].
Бенрализумаб**, меполизумаб**, реслизумаб** не зарегистрированы в РФ и других странах для терапии пациентов с эозинофильным эзофагитом.
Не рекомендовано применение азатиоприна** и меркаптопурина** для лечения ЭоЭ в связи с недостаточной эффективностью [1,21].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: В литературе описано лишь 3 случая стероидо-резистентного течения ЭоЭ, при котором назначение азатиоприна** взрослым пациентам в дозе 2-2,5 мг и меркаптопурина** привело к индукции и поддержанию ремиссии. Однако после отмены терапии наступил рецидив [83].
Не рекомендовано применение антигистаминных средств системного действия, а также монтелукаста и кромоглициевой кислоты** для лечения ЭоЭ в связи с неэффективностью [1,21].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: Антигистаминные средства системного действия, кромоглициевая кислота**, монтелукаст оказались несостоятельны в купировании симптомов и влиянии на выраженность эозинофильного воспаления в слизистой оболочке пищевода у больных ЭоЭ [84-90].
Пациентам с ЭоЭ рекомендовано оценивать эффективность медикаментозной терапии и диетических режимов через 8–12 недель после начала лечения путем проведения ЭГДС с множественной биопсией пищевода с помощью эндоскопии на фоне продолжающегося приема препаратов и/или соблюдения диеты и далее регулярно 1 раз в год или при значительном изменении терапии [1,21, 166, 167, 168].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Степень активности воспалительного процесса в слизистой оболочке пищевода при ЭоЭ не коррелирует с выраженностью симптомов заболевания. Для оценки эффективности лечения и контроля за активностью воспалительного процесса необходимо гистологическое исследование биоптатов. Критерием эффективности лечения служит достижение гистологической ремиссии заболевания (менее 15 эозинофилов в поле зрения при увеличении х400).
3.3. Эндоскопическое лечение
Пациентам, у которых ЭоЭ осложнился развитием стриктур/стеноза просвета пищевода, приводящим к стойкой дисфагии и/или эпизодам вклинения пищевого комка в пищевод, рекомендовано проведение баллонной дилатации или бужирования пищевода эндоскопического для облегчения клинической симптоматики [1,21,166].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Эндоскопическая дилатация (баллонная дилатация стеноза пищевода) или бужирование пищевода показаны пациентам со стриктурами/стенозом просвета пищевода менее 13 мм после курса медикаментозной противовоспалительной терапии.
Баллонная дилатация стеноза пищевода приводит к разрешению дисфагии у 75% (95% CI 58-93%) пациентов [82]. Эндоскопическая дилатация (баллонная дилатацию стеноза пищевода) или бужирование пищевода не оказывают влияния на иммуновоспалительный процесс в слизистой оболочке пищевода, данная процедура проводится с целью снижения выраженности клинических симптомов, вызванных необратимыми фибротическими изменениями стенки пищевода [167,168].
3.4. Иное лечение
Пациентам с ЭоЭ, не отвечающим на медикаментозную терапию и/или со значимыми проявлениями атопических заболеваний, рекомендуется прием (осмотр, консультация) врача-аллерголога-иммунолога с целью уточнения сопутствующей патологии и оптимизации ее терапии [1,166,167].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: сопутствующие атопические заболевания нередко встречаются у пациентов с ЭоЭ, оптимизация их терапии может быть полезна.
При выявлении атопических заболеваний проводится лечение согласно соответствующим клиническим рекомендациям.
Методы реабилитации при ЭоЭ не разработаны.
Первичная профилактика ЭоЭ не разработана. Вторичная профилактика направлена на предотвращение развития осложнений, таких как стриктуры и стенозы.
Рекомендовано включать в программу профилактики своевременную диагностику заболевания, постоянную поддерживающую медикаментозную терапию и проведение ЭГДС с биопсией пищевода с помощью эндоскопии с периодичностью 1 раз в год [1,166,167,168].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
ЭоЭ не является противопоказанием для вакцинации.
Пациентам с ЭоЭ, в зависимости от необходимости, может быть оказана медицинская помощь любого вида, условия, формы, предусмотренных законодательством Российской Федерации.
Ведением пациентов с ЭоЭ обычно занимается врач-гастроэнтеролог с участием других врачей (врач-аллерголог-иммунолог, врач-педиатр, врач-терапевт) при необходимости.
Чаще госпитализация осуществляется в педиатрическое (дети до 18 лет)/терапевтическое или гастроэнтерологическое (взрослые) отделения, при необходимости – в отделение хирургического профиля в зависимости от доминирующих симптомов заболевания.
Показания для плановой госпитализации: нарастание дисфагии, при необходимости – подбор терапии и ее коррекция; системная терапия (в том числе с применением генно-инженерной биологической терапии) в условиях дневного и круглосуточного стационаров (для взрослых и детей).
Показания для экстренной/неотложной госпитализации: острая обтурационная дисфагия (эпизод вклинения пищи в пищевод).
Показания к выписке из стационара: удовлетворительное общее состояние, уменьшение выраженности дисфагии.
Эозинофильный эзофагит был выделен в отдельную нозологию лишь около 30 лет назад, в связи с чем данные о частоте развития осложнений или спонтанных ремиссий, прогнозе заболевания, сроках поддерживающей терапии по сей день остаются скудными и противоречивыми.
В целом ЭоЭ характеризуется доброкачественным течением. В литературе нет данных о развитии рака пищевода на фоне ЭоЭ. Другой особенностью заболевания является крайне медленное его прогрессирование. Скорее всего, это связано с тем, что выраженность дисфагии у пациентов с ЭоЭ зависит в первую очередь от фибротического ремоделирования стенки пищевода, которое при ЭоЭ происходит в течение нескольких лет/десятилетий. Кроме того, больные постепенно адаптируются к возникающим симптомам, более тщательно пережевывают пищу, обильно запивают ее водой, избегают продуктов с твердой и грубой текстурой.
Благоприятное течение заболевания подтверждается также данными о том, что даже кратковременное медикаментозное лечение ЭоЭ приводит к многомесячной ремиссии заболевания. Дилатация стриктур пищевода обеспечивает купирование дисфагии на срок до 1 года даже при отсутствии противовоспалительной медикаментозной терапии.
Существующая модель прогрессирования ЭоЭ отражает постепенный переход от воспалительных изменений к фиброзу и стенозу пищевода с развитием дисфагии у большинства больных ЭоЭ (рисунок 9). В случае своевременного начала медикаментозной терапии и диетических ограничений на ранних стадиях заболевания возможно замедление прогрессирования фибротических изменений. Описаны случаи возникновения спонтанных ремиссий заболевания (без применения медикаментозной терапии или диет), однако они нехарактерны для ЭоЭ и являются скорее исключением. Имеющиеся на современном этапе данные не позволяют сформулировать однозначные рекомендации относительно длительности поддерживающей терапии при ЭоЭ.
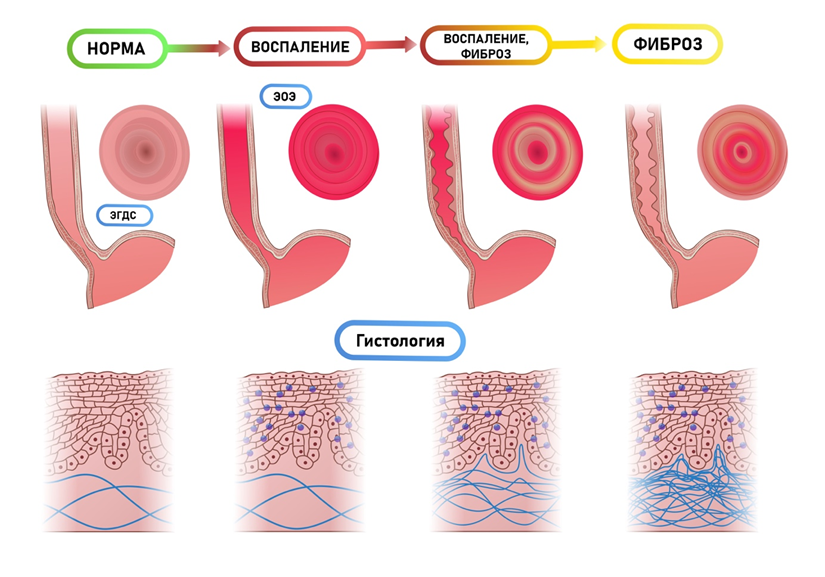
Рисунок 3. Естественное течение (при отсутствии лечения) ЭоЭ













