Синдром Мэллори-Вейсса (желудочно-пищеводный разрывно-геморрагический синдром)Код: 1026 • Редакция: 1
Синдром Мэллори-Вейсса – образование острых линейных разрывов слизистой оболочки брюшного отдела пищевода и кардиального отдела желудка при рецидивирующей рвоте, сопровождающиеся кровотечением.
Причиной разрывов, как правило, является многократная рвота, сопровождающаяся повышением внутрижелудочного или внутрибрюшного давления, а также кардиоэзофагеальным спазмом.
Основные этиологические факторы:
Рвота:
Наиболее частый и распространенный фактор. Рвота, особенно сильная и продолжительная, может быть вызвана различными причинами, включая алкоголь, отравления, заболевания пищеварительной системы и др.
Повышение внутрибрюшного давления:
Помимо рвоты, другие состояния, приводящие к повышению внутрибрюшного давления, также могут способствовать развитию синдрома Мэллори-Вейсса. Это может быть связано с тяжелым кашлем, сильными физическими нагрузками, травмами живота, родами и т.д.
Лекарственные препараты:
Некоторые лекарства, например, ацетилсалициловая кислота**, могут вызвать раздражение слизистой оболочки желудка и, при наличии других факторов риска, способствовать развитию разрывов.
Заболевания ВОПТ:
Хронические заболевания верхнего отдела пищеварительного тракта (гастрит, язвы пищевода), грыжа пищеводного отверстия диафрагмы, портальная гипертензия также могут повышать риск развития синдрома.
Ятрогенные факторы:
Повреждение слизистой оболочки во время эндоскопических манипуляций, введения желудочного зонда или сердечно-легочной реанимации также может стать причиной разрывов.
Факторы риска:
Алкоголизм и булимия:
Эти состояния часто связаны с частой и сильной рвотой, что увеличивает риск развития синдрома.
Гастроэзофагеальная рефлюксная болезнь (ГЭРБ):
Нарушения в работе нижнего пищеводного сфинктера могут способствовать повышению внутрибрюшного давления и развитию разрывов.
Беременность:
Во время беременности могут быть повышенные риски рвоты и изменений в работе пищевода, что увеличивает вероятность развития синдрома.
Патогенез:
Основной реализующей причиной разрывов слизистой оболочки пищеводно-желудочного перехода является рвота. М. Atkinson и соавт. (1962) установили, что у больных во время рвоты давление в желудке достигало 120-150 мм рт. ст., а иногда повышалось до 200 мм рт. ст. [220]. Во время натужных рвотных движений нарушается координация между «запирательной» функцией кардиального жома и привратника и сильными антиперистальтическими сокращениями желудка. В этом случае во время рвоты резко повышается внутрижелудочное давление, что и приводит к разрыву стенки гастроэзофагеального перехода. Патогенез этого заболевания остается не до конца изученным и по настоящее время.
Разрыв Маллори-Вейсса является редкой причиной кровотечения из верхних отделов ЖКТ, составляя примерно 5 % всех случаев. Чаще возникает у мужчин. Данный синдром превалирует среди пациентов в возрасте 40-50 лет, но может возникать и в другом возрасте. Заболеваемость составляет 7,5 случаев на 100 000 человек, внутрибольничная летальность составляет 2,7 %.
К22.6 Желудочно-пищеводный разрывно-геморрагический синдром
Общепринятой классификации СМВ не существует.
Выделяют следующие стадии синдрома Маллори-Вейса:
I стадия - разрыв (трещины) слизистой оболочки нижней трети пищевода, кардиоэзофагиального перехода;
II стадия - разрыв (трещины) слизистой оболочки, подслизистого слоя;
III стадия - разрыв (трещины) с вовлечением циркулярного мышечного слоя. Зона разрыва не спазмируется, не смыкается, интенсивное кровотечение;
IV стадия - разрыв всех слоев пищевода, кардиоэзофагиального перехода, сопровождается перитонитом, медиастинитом, пневмотораксом.
Эндоскопическая картина СМВ:
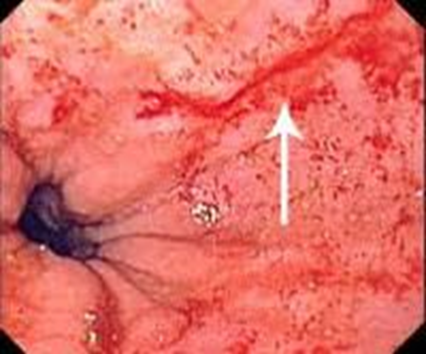
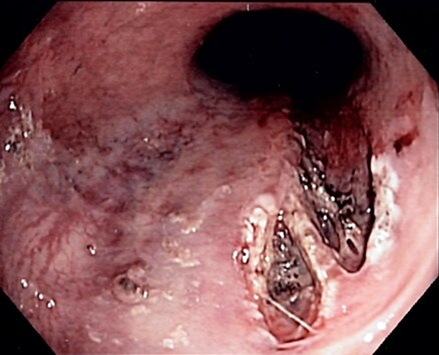
По степени тяжести кровотечения, наиболее распространённой в нашей стране, является классификация А.И. Горбашко 1982 г. (приложение Г1) [16], использующая 3-х степенную градацию, выделяющая лёгкую, среднюю и тяжёлую степень кровотечения, учитывающая при этом, как объём перенесенной кровопотери, так и состояние самого больного. Шкала тяжести кровопотери американского колледжа хирургов (приложение Г2) выделяет 4 класса (степени) кровопотери – лёгкую, умеренную, среднюю и тяжёлую [85].
Клиническая картина синдрома Маллори-Вейсса обычно характеризуется рвотой с кровью (гематемезис): может быть от небольших кровяных прожилок до массивного кровотечения. Цвет крови может варьироваться от ярко-красного до темного, в зависимости от того, насколько долго кровь находится в пищеварительном тракте.
Синдром Маллори-Вейсса часто развивается после эпизодов рвоты, позывам на рвоту, сильного кашля, икоты, а также других факторов, которые могут увеличить давление в брюшной полости и спровоцировать разрывы слизистой.
Клинические проявления пищеводно-желудочных кровотечений при СМВ можно разделить на две группы симптомов:
Общие признаки кровопотери (слабость, головокружение, потеря сознания, холодный липкий пот, снижение артериального давления, тахикардия) и
Симптомы, обусловленные попаданием крови в просвет желудочно-кишечного тракта, которые включают гематемезис и мелену. Кровопотеря в 100 мл может привести к появлению черного, но оформленного кала. «Истинная» мелена (дегтеобразный, т.е. черный и жидкий стул) у взрослого человека возникает при кровопотере объемом около 500 мл. Быстрая и массивная кровопотеря в просвет кишки может проявиться гематохезией – выделением через задний проход крови со сгустками.
При объективном обследовании выявляются: измененное поведение больного (беспокойство, испуг или апатия, сонливость, при тяжелой степени кровопотери – психомоторное возбуждение, бред, галлюцинации); бледность кожных покровов, изменения пульса (частый, слабого наполнения); АД имеет тенденцию к снижению в зависимости от степени кровопотери; дыхание учащено. Пальцевое исследование прямой кишки, являющееся обязательным при подозрении на желудочно-кишечное кровотечение, помогает выявить изменение окраски кала.
Критерии установления диагноза заболевания/состояния:
Диагноз СМВ устанавливается на основании:
1) анамнестических данных (характерные жалобы, выявление язвенной болезни прежде);
2) непосредственного обследования;
3) инструментального обследования (обнаружение разрыва пищевода и/или желудка при эндоскопическом (эзофагогастродуоденоскопия) исследовании).
Диагностическая программа при СМВ должна: 1) установить факт острого кровотечения в просвет верхних отделов ЖКТ; 2) выявить источник кровотечения; 3) определить степень тяжести кровопотери. При угрожающих жизни кровотечениях диагностические исследования должны быть проведены параллельно с неотложными лечебными мероприятиями.
Критерии установления диагноза:
Диагноз СМВ устанавливается на основании совокупности общих клинических признаков кровопотери; признаков кровотечения в просвет ЖКТ; анамнестических и лабораторных данных, подтвержденными результатами ЭГДС. При поступлении в стационар пациент должен быть сразу осмотрен врачом-хирургом и проведена неотложная лабораторная диагностика.
Пациентам с СМВ для определения степени тяжести кровопотери рекомендуется использовать классификацию А.И. Горбашко, 1982 г. [16] (Приложение Г1), оценочную шкалу ACS (American College of Surgeons) [1] (Приложение Г2) [16,19].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Пациентам с СМВ для определения степени тяжести кровопотери рекомендуется использовать Шоковый индекс (Приложение Г6) [221,222].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
У пациентов с СМВ рекомендуется оценить риск рецидива кровотечения по совокупности клинических и эндоскопических данных [21,22].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: критериями высокого риска рецидива кровотечения при СМВ являются клинические (коллапс в анамнезе, тяжелая кровопотеря, тяжелая сопутствующая патология) и лабораторные признаки, отражающие в основном интенсивность кровотечения, а также эндоскопические признаки (глубокие разрывы, продолжающееся кровотечение в момент эндосокпии) [11,15,21]. Для оценки риска рецидива кровотечения и определения дальнейшей лечебной тактики могут быть использованы шкалы AIMS65 (Приложение Г3), Glasgo-Blathford Bleeding Score (Приложение Г4) и многократно валидированная шкала Rockall (Приложение Г5).
Характерные для пациентов с СМВ жалобы и данные анамнеза указаны в подразделе 1.6.
У пациента с признаками кровотечения из верхних отделов ЖКТ рекомендуется выполнить анализ жалоб, анамнеза заболевания и анамнеза жизни на этапе поступления в стационар, но это не должно приводить к задержке неотложных диагностических и лечебных мероприятий [12,14,19,21].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: важно выяснить, как давно началось кровотечение; отмечалось ли предобморочное состояние, потеря сознания; имелись единичные или повторные эпизоды кровавой рвоты, объём и характер рвотных масс (алая или тёмная кровь, сгустки, содержимое типа “кофейной гущи”); частоту эпизодов мелены.
Необходимо выявить состояния, которые могут обусловить развитие острого кровотечения при СМВ: тяжелые сопутствующие заболевания (ИБС, инфаркт миокарда, сердечная недостаточность, нарушение мозгового кровообращения, почечная и печеночная недостаточность, онкологические и гематологические заболевания, алкоголизм); лечение антитромботическими средствами (Код АТХ: B01A).
При поступлении в приёмное отделение пациента с подозрением на СМВ рекомендуется осмотр врача-хирурга с целью исключения или подтверждения данного диагноза и определения дальнейшей тактики [108,110].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
Характерные для пациентов с СМВ данные физикального обследования приведены в подразделе 1.6.
Пациенту с признаками кровотечения из верхних отделов ЖКТ рекомендуется провести обследование при поступлении, включающее оценку всех основных систем организма; трансректальное пальцевое исследование (A01.19.004) [12,13,14,223].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
Комментарии: данные объективного обследования в совокупности с жалобами и анамнезом, уже на этапе поступления пациента позволяют судить о степени тяжести и предполагаемом источнике кровотечения, сопутствующих заболеваниях. Спутанное сознание, резкая бледность кожных покровов и конъюнктивы, частый пульс слабого наполнения и напряжения, снижение артериального и пульсового давления, наличие в желудке большого количества крови и сгустков, а при ректальном исследовании – чёрного жидкого, либо с примесью крови содержимого служат признаками острого массивного кровотечения.
Осмотр кожных покровов и видимых слизистых оболочек может выявить их субиктеричность или желтушность, наличие сосудистых звёздочек, расширение подкожных вен переднебоковых отделов живота, что обычно бывает при заболеваниях печени; внутрикожные или подкожные кровоизлияния, множественные телеангиэктазии при заболеваниях кровеносных сосудов и нарушениях свертывающей системы крови. Клиническими наблюдениями проверено, что АД ниже 100 мм рт. ст. и частота пульса более 100 ударов в минуту у больного с нормальным обычным давлением соответствуют кровопотере около 20 % ОЦК. Перкуссия при заболеваниях пищевода, желудка, двенадцатиперстной кишки (A01.16.004) и пальпация при заболеваниях пищевода, желудка, двенадцатиперстной кишки (A01.16.003) в ряде случаев позволяет выявить опухоль желудка, увеличение печени и селезенки, признаки асцита, увеличенные плотные лимфатические узлы. Осмотр больного необходимо закончить пальцевым исследованием прямой кишки, а затем, при необходимости, зондированием желудка. Полученные при этом объективные данные, независимо от наличия или отсутствия анамнестических указаний на кровавую рвоту и дегтеобразный стул, являются важными признаками, обосновывающими клинический диагноз.
Специфических для СМВ лабораторных признаков не существует. Лабораторные исследования у пациентов с кротечением при СМВ, как правило, включают в экстренном порядке определение основных групп по системе AB0, определение антигена D системы Резус (резус-фактор), определение подгруппы и других групп крови меньшего значения A-1, A-2, D, Cc, E, Kell, Duffy; общий (клинический) анализ крови; исследование уровня натрия в крови, исследование уровня калия в крови, исследование уровня хлоридов в крови, исследование кислотно-основного состояния и газов крови, исследование уровня осмолярности (осмоляльности) крови; исследование уровня мочевины в крови, исследование уровня креатинина в крови, определение протромбинового (тромбопластинового) времени в крови или в плазме, определение международного нормализованного отношения (МНО), исследование уровня фибриногена в крови; исследование уровня глюкозы в крови, исследование уровня общего белка в крови, исследование уровня альбумина в крови, исследование уровня общего билирубина в крови, определение активности аланинаминотрансферазы в крови, определение активности аспартатаминотрансферазы в крови) [12,14,19,21].
Падение уровня гемоглобина, уменьшение числа эритроцитов, снижение гематокрита, несомненно ориентируют в отношении тяжести кровопотери. Однако в первые часы от начала острого кровотечения, даже при его интенсивном характере, гемодилюция не успевает развиться и поэтому все эти показатели могут меняться несущественно. Кроме анемии в результате острой кровопотери и действия крови, излившейся в просвет пищеварительного тракта, нередко отмечается умеренный лейкоцитоз и гипербилирубинемия (за счет непрямой фракции), повышение уровня мочевины при нормальных значениях креатинина, что связано с синдромом всасывания крови в кишечнике.
Исследование ОЦК и его компонентов, с использованием красителей и радиоизотопов, в настоящее время практически не используется. Тяжесть состояния больного и его индивидуальные реакции на перенесенную кровопотерю, достаточно точно характеризует ряд показателей центральной гемодинамики, транспорта кислорода, а также метаболические нарушения (мочевина крови, электролиты, КЩС, осмолярность плазмы и др.).
Кровопотеря, в особенности тяжелой степени, может привести к гипокоагуляции с удлинением времени свертывания крови, снижением уровня протромбина и фибриногена вплоть до развития острого фибринолиза.
Всем пациентам с подозрением на кровотечение при СМВ, при отсутствии противопоказаний, с целью подтверждения диагноза рекомендуется проведение эзофагогастродуоденоскопии (ЭГДС) (А.03.16.001) [2].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: эндоскопическое исследование подтверждает наличие разрыва стенки пищевода и/или желудка, уточняет его локализацию, форму, размеры, глубину, наличие грыжи пищеводного отверстия диафрагмы и рефклюкс-эзофагита.
Экстренное эндоскопическое исследование – эзофагогастродуоденоскопию (ЭГДС) (A03.16.001) рекомендуется выполнять всем пациентам с острым кровотечением из верхних отделов пищеварительного тракта, под процедурной седацией с мониторингом основных параметров жизнедеятельности пациента во время проведения анестезии (B03.003.006), параллельно с проведением инфузионно-трансфузионной терапии [28].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: ЭГДС необходимо выполнить в течение 2 часов от момента госпитализации пациента. Решающее значение для установления источника и характера кровотечения, оценки необходимости и возможности остановки/профилактики кровотечения через эндоскоп, а также для прогнозирования риска рецидива кровотечения принадлежит эндоскопическому методу.
Перед выполнением ЭГДС пациентам с подозрением на пищеводно-желудочное кровотечение рекомендуется выполнить зондирование желудка (A11.16.009) с последующим промыванием желудка (A11.16.008) с целью подготовки к исследованию [19,21,23].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
В ряде случаев, при невозможности адекватно отмыть и эвакуировать содержимое желудка во время зондирования и промывания желудка, рекомендуется использование #Эритромицина (Код АТХ: J01FA01) в парентеральной форме (200 мг однократно) с целью стимуляции моторики желудка [224].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Европейское общество желудочно-кишечной эндоскопии (ESGE) считает возможным для этой цели также использование стимуляторов моторики желудочно-кишечного тракта (Код АТХ: A03F) или #Эритромицина (Код АТХ: J01FA01) в парентеральной форме (200 мг однократно) [224]. Европейское общество желудочно-кишечной эндоскопии (ESGE) также рекомендует выполнять интубацию трахеи перед проведением ЭГДС у пациентов с продолжающейся активной кровавой рвотой, энцефалопатией, возбуждением, с целью защиты дыхательных путей пациента от потенциальной аспирации желудочного содержимого [12,224].
При обнаружении во время ЭГДС в просвете желудка большого количества крови, сгустков, пищевых масс, рекомендуется извлечь эндоскоп медицинский гибкий для обследования желудочно-кишечного тракта и эвакуировать содержимое через зонд желудочный [19,21,23].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии. Биопсия краев разрывов пищевода и желудка (биопсия пищевода с помощью эндоскопии) в большинстве случаев нецелесообразна, может опасна с точки зрения возобновления кровотечения, либо затруднена технически.
Всем пациентам с СМВ с целью определения показаний к эрадикационной терапии рекомендуется проведение тестирования на наличие инфекции Н. рylori с помощью 13С-уреазного дыхательного теста на Helicobacter pylori или определения антигена хеликобактера пилори в фекалиях, а при одновременном проведении ЭГДС - с помощью быстрого уреазного теста (устройство для экспресс-диагностики хеликобактериоза по уреазной активности биоптата (in vitro)) [30].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии: при отсутствии технической возможности первичной диагностики инфекции H. pylori в стационаре, допустимо её проведение на амбулаторном этапе. В соответствии с рекомендациями согласительного совещания «Маастрихт-VI» (2022) наиболее оптимальными тестами первичной диагностики инфекции H. pylori служат 13С-дыхательный уреазный дыхательный тест на Helicobacter pylori и определение антигена H. pylori в кале. Так, согласно последнему Кохрейновскому обзору и мета-анализу, чувствительность 13С-дыхательного уреазного теста составляет 94 % (95 % ДИ: 0,89 - 0,97), а определения антигена хеликобактера пилори в фекалиях – 83 % (95 % ДИ: 0,73 - 0,90) при фиксированной специфичности 90 % [30].
Если пациентам одновременно проводится ЭГДС, то методом первичной диагностики может быть быстрый уреазный тест (устройство для экспресс-диагностики хеликобактериоза по уреазной активности биоптата (in vitro)). При использовании эндоскопических методов диагностики Н. pylori берут, как минимум, 2 биоптата из тела желудка и 1 биоптат из антрального отдела. Серологический метод выявления антител к Н. pylori (определение антител к хеликобактер пилори (Helicobacter pylori) в крови) может применяться для первичной диагностики инфекции H. pylori, однако, только в том случае, если определяемые антитела относятся к классу IgG. Микробиологический (бактериологический) метод (микробиологическое (культуральное) исследование биоптатов слизистой желудка на хеликобактер пилори (Helicobacter pylori) с определением чувствительности к антибактериальным препаратам) применяется в настоящее время для определения индивидуальной чувствительности H. pylori к антибактериальным препаратам системного действия в случаях неэффективности лечения.
Всем пациентам с СМВ рекомендуется рассмотреть возможность контроля эрадикации инфекции Н. рylori для определения дальнейшей лечебной программы [32].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии: для контроля эрадикации через 4–6 недель после окончания эрадикационной терапии целесообразно применять 13С-уреазный дыхательный тест на H.pylori (A07.16.006) и/ или определение антигена хеликобактера пилори в фекалиях (A26.19.020). Прием ИПН необходимо прекратить за 2 недели до предполагаемого контрольного исследования. Отрицательный результат должен быть подтвержден двумя методами диагностики [31,32].
Лечение СМВ должно быть комплексным и включать в себя не только назначение лекарственных препаратов, но и проведение широкого круга различных мероприятий: диетическое питание, прекращение курения и злоупотребления алкоголем, отказ от приема препаратов, обладающих ульцерогенным действием, нормализацию режима труда и отдыха, санаторно-курортное лечение.
3.1 Диетотерапия
Всем пациентам с СМВ с целью ускорения заживления разрывов рекомендуется диетотерапия [34].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: основные принципы диетического питания пациентов с СМВ, выработанные много лет назад, сохраняют свою актуальность и в настоящее время. Остаются в силе рекомендации частого (5-6 раз в сутки), дробного питания, соответствующие правилу: “шесть маленьких приемов пищи лучше, чем три больших”, механического, термического и химического щажения. Из пищевого рациона необходимо исключить продукты, раздражающие слизистую оболочку желудка и возбуждающие секрецию соляной кислоты: крепкие мясные и рыбные бульоны, жареную и наперченную пищу, копчености и консервы, приправы и специи (лук, чеснок, перец, горчицу), соления и маринады, газированные фруктовые воды, пиво, белое сухое вино, шампанское, кофе, цитрусовые.
Следует отдавать предпочтение продуктам, обладающим выраженными буферными свойствами (т.е., способностью связывать и нейтрализовывать соляную кислоту). К ним относятся мясо и рыба (отварные или приготовленные на пару), яйца, молоко и молочные продукты. Разрешаются также макаронные изделия, черствый белый хлеб, сухой бисквит и сухое печенье, молочные и вегетарианские супы. Овощи (картофель, морковь, кабачки, цветная капуста) можно готовить тушеными или в виде пюре и паровых суфле. В пищевой рацион можно включать каши, кисели из сладких сортов ягод, муссы, желе, сырые тертые и печеные яблоки, какао с молоком, некрепкий чай.
Нужно помнить и о таких простых, но в то же время важных рекомендациях, как необходимость принимать пищу в спокойной обстановке, не спеша, сидя, тщательно прожевывать пищу. Это способствует лучшему пропитыванию пищи слюной, буферные возможности которой являются достаточно выраженными.
3.2 Консервативное лечение
Ведение больных с СМВ (как и во всех случаях кровотечений из ВОПТ) на догоспитальном этапе и на этапе поступления в стационар
Всем пациентам с признаками кровотечения из верхних отделов ЖКТ рекомендуется незамедлительно начать интенсивную терапию на догоспитальном этапе и/или при поступлении в стационар [6].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Всем пациентам с клиникой кровотечения при СМВ рекомендуется парентеральное введение ингибиторов протонного насоса (A02BC) при поступлении в стационар [13,19,23,81,102].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 1)
Комментарии: назначение ИПН на догоспитальном этапе и до выполнения первичной ЭГДС уменьшает потребность в проведении эндоскопического гемостаза, но не должно приводить к задержке эндоскопии.
Рекомендуется стратификация больных на этапе поступления в стационар по степени тяжести и вероятности летального исхода для решения вопроса о госпитализации / переводе пациентов с тяжёлым кровотечением в ОРИТ [19].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: с целью стратификации больных с СМВ по степени тяжести кровопотери и вероятности летального исхода могут быть использованы шкалы Glasgow-Blatchford [16,20] (Приложение Г4), AIMС65 (Приложение Г3), Шоковый индекс (> 0,8) [20] (Приложение Г6), шкала ACS (Приложение Г2).
Ведение больных с массивной кровопотерей
Основными задачами интенсивной терапии является обеспечение адекватной доставки кислорода клетке и его потребление, коррекция гемостаза.
У пациентов с СМВ при наличии нестабильной гемодинамики восполнение ОЦК рекомендуется начинать с введения сбалансированных солевых растворов (B05CB) [28].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Пациентам с СМВ при немассивной кровопотере рекомендуется проводить инфузионно- трансфузионную терапию рестриктивного характера [27].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: у пациентов с СМВ необходимо достичь целевых показателей адекватности перфузии после осуществления «хирургического» гемостаза. Либеральная инфузионно-трансфузионная терапия, раннее достижение целевых показателей гемодинамики (до хирургического гемостаза) могут приводить к гемодилюции, повышенному перфузионному давлению, что влечёт за собой увеличение кровопотери [83,84]. В отдельных случаях, у пациентов с отягощенным коморбидным фоном, при необходимости обеспечения персонализированного подхода к инфузионной терапии допустимо использовать такие методы оценки волемического статуса как эхокардиография (оценка сердечного выброса, ударного объема, скорости кровотока) и транспульмональная термодилюция [219].
Пациентам с СМВ рекомендуется проведение гемотрансфузии при уровне гемоглобина менее 70 г/л; пациентам с кардиоваскулярными заболеваниями порог начала гемотрансфузии может быть выше – 90 г/л [13,27,28,235].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Пациентам с СМВ рекомендуется трансфузия свежезамороженной плазмы при наличии гипокоагуляции и продолжающегося кровотечения или высокого риска его возобновления [235].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
У пациентов с СМВ при массивной кровопотере рекомендуется поддерживать уровень тромбоцитов более 50 х 109/л [27].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
У части пациентов с СМВ (с признаками выраженной гипоперфузии) рекомендуется использование норэпинефрина** (Код АТХ: C01CA03) и эпинефрина** (Код АТХ: C01CA24) с целью поддержания необходимого перфузионного давления [27,28,225,226].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Использование норэпинефрина** (Код АТХ: C01CA03) и эпинефрина** (Код АТХ: C01CA24) также может быть рекомендовано при снижении контрактильной функции сердца с целью её улучшения [27,28,225,226].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: критериями восстановления адекватной перфузии служат: состояние кожных покровов (мозаичность, время заполнения капилляров, температура); уровень сознания; величина диуреза; нормализация КЩС, лактата; достижение целевого уровня гемодинамики [13,16].
Критериями адекватности трансфузионной терапии служат: отсутствие патологической кровоточивости (при условии выполненного «хирургического» гемостаза); нормализация гемостаза по глобальным коагулологическим тестам и/или тестированием гемостаза вязкоэластическими методиками (например, тромбоэластография) [16,27,28].
3.3. Эндоскопическое лечение
У пациентов с СМВ при продолжающемся кровотечении из разрывов пищевода и/или желудка рекомендуется выполнить гемостаз (A16.12.020 Остановка кровотечения из периферического сосуда) через эндоскоп (видеогастроскоп гибкий, многоразового использования) [13,19,23,31].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 1)
Комментарии: при остановившемся кровотечении возможно удаление кровяного сгустка с помощью прицельного отмывания [13,19,23,31].
У пациентов с СМВ при остановившемся кровотечении эндоскопическая профилактика рецидива кровотечения рутинно не рекомендуется [13,19,23,31].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: в таких случаях важным является обеспечение адекватной медикаментозной профилактики рецидива кровотечения. Эндоскопическую остановку (профилактику рецидива) кровотечения необходимо выполнить в течение 2 часов от момента госпитализации пациента. У пациентов с СМВ для эндоскопической остановки кровотечения из разрывов и профилактики его рецидива целесообразно применять инъекционный метод гемостаза в сочетании с термическими (диатермокоагуляция, аргоноплазменная коагуляция (A22.30.033.001)) или клипирование (Остановка кровотечения из периферического сосуда; Остановка кровотечения из периферического сосуда эндоскопическая с использованием электрокоагуляции; Остановка кровотечения эндоскопическая с использованием термокоагуляции, Клипирование кровоточащего сосуда эндоскопическое, Коагуляция кровоточащего сосуда аргонплазменная) [13,14,19,23]. Инъекционный гемостаз в качестве монотерапии не обеспечивает должной эффективности и должен применяться только в комбинации с другими методами эндоскопического гемостаза. Как дополнение к комбинированному эндоскопическому гемостазу могут быть использованы и другие местные методы эндоскопического гемостаза [13,14,19,23,31].
У пациентов с СМВ повторное контрольное эндоскопическое исследование/вмешательство рекомендуется выполнить при неполноценном первичном осмотре или при рецидиве кровотечения [86].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 1)
Комментарии: рутинное выполнение контрольного эндоскопического исследования у всех пациентов с СМВ нецелесообразно. При неполноценном первичном осмотре повторное эндоскопическое исследование рекомендуется выполнить в ближайшие часы после первой ЭГДС [87,227].
Пациентам с высоким риском рецидива кровотечения после его эндоскопической остановки/профилактики рекомендуется введение ИПН (например, эзомепразола** в дозировке 80 мг внутривенно болюсно и затем непрерывно по 8 мг в час в течение 72 часов) тотчас после выполнения эндоскопического гемостаза с целью профилактики рецидива кровотечения [13,19,23,81].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии: пациентам с СМВ, которые исходно получали ИПН в парентеральной форме, перевод на пероральные формы производят через 72 часа от начала терапии [13,19,23]. Пациентам с СМВ с низким риском рецидива кровотечения целесообразно парентеральное введение ИПН после выполнения эндоскопии в течение 72 часов с последующим переходом на пероральные формы вплоть до выписки из стационара и далее до полного заживления разрыва – источника перенесенного кровотечения [13,19,23].
Пациентам с низким риском рецидива кровотечения переход на энтеральное питание возможен в ближайшие часы после завершения эндоскопического вмешательства [13,19,23]. Пациентам с высоким риском рецидива кровотечения разрешается пить и принимать жидкую не ранее чем через 24 часа после остановки кровотечения [228,229].
Всем пациентам с СМВ при подтверждении наличия Hp-инфекции рекомендуется проводить эрадикационную терапию с подтверждением проведенной эрадикации [2].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: эрадикационная терапия начинается после перевода пациентов на пероральный прием ИПН [161]. Успешная эрадикация значительно снижает риск возникновения рецидивов кровотечения [162,166].
3.4. Эндоваскулярное лечение
Пациентам при неоднократно рецидивирующих кровотечениях при СМВ, резистентных к эндоскопическому и медикаментозному гемостазу, рекомендуется рассмотреть вопрос о возможной эндоваскулярной эмболизации сосудов (артерий желудка) (A16.12.051), как альтернатива хирургическому лечению [13,19,89-92].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3)
3.5 Хирургическое лечение
Пациентам с продолжающимся или неоднократно рецидивирующем кровотечением при неэффективности (или невозможности) эндоскопического гемостаза рекомендуется оперативное лечение [13,19,23].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: альтернативной хирургическому вмешательству могут является установка зонда-обтуратора (например, зонд-обтуратор резиновый пищеводно-желудочный) или эндоваскулярные вмешательства (эндоваскулярная эмболизация сосудов с помощью адгезивных агентов, эндоваскулярная эмболизация сосудов микроэмболами). Объем хирургического вмешательства включает гастротомию верхней трети тела желудка и прошивание кровотчащих разрывов [217,218].
Лечение больных, находящихся на постоянном приеме антитромботических средств
При возникновении кровотечения у пациентов с СМВ, постоянно принимающих антитромботические средства (Код АТХ: В01А) прием этих препаратов рекомендуется прекратить, однако при этом необходимо учитывать соотношение риска развития кардиоваскулярных осложнений с риском рецидива кровотечения в каждом конкретном случае [231-234].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Прием антитромботических средств рекомендуется возобновить, как только будет достигнут устойчивый гемостаз [231-234].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Пациентам, перенесшим кровотечение при СМВ, рекомендуется санаторно-курортное лечение в санаторно-курортных организациях климатической зоны проживания пациента [230,239].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: пациентам с СМВ рекомендуется санаторно-курортное лечение продолжительностью 14-21 день. Санаторно-курортное лечения проводится в санаториях городов Дорохово, Ессентуки, Железноводск и др. и включает в себя грязевые ванны и торфолечение, хвойно-морские ванны, прием щелочной минеральной воды [230,239].
Всем лицам с наличием инфекции H. pylori при отсутствии противопоказаний рекомендуется проведение эрадикационной терапии [52].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Показанием к экстренной госпитализации является наличие признаков пищеводно-желудочного кровотечения.
Каждая клиника, оказывающая помощь пациентам с острым кровотечением из ВОПТ (включая кровотечения при СМВ) должна располагать локальным протоколом мультидисциплинарного ведения таких пациентов. Протокол диагностики и лечения пациентов должен базироваться на национальных клинических рекомендациях и учитывать особенности структуры оказания неотложной помощи и оснащения конкретного лечебно-профилактического учреждения.
У комплаентных пациентов с СМВ и кровотечением лёгкой степени тяжести, низким риском рецидива кровотечения, отсутствием сопутствующей патологии возможна выписка из стационара в ранние сроки от поступления.
7.1. Особенности течения СМВ у отдельных групп пациентов
7.1.1 Особенности течения СМВ при беременности
Течение СМВ при беременности в целом мало отличается от такового у небеременных женщин. Диагноз устанавливается на основании клинических проявлений, анамнестических данных, результатов ЭГДС [100]. Рентгенологическое исследование желудка и ДПК беременным противопоказано.
Для раннего токсикоза характерны мучительная, почти постоянная тошнота, усиливающаяся на различные запахи, слюнотечение. При этом рвота бывает независимо от еды, особенно по утрам, боль в животе, как правило, отсутствует. Кровотечение, обусловленное СМВ необходимо дифференцировать с таковым при язвенной болезни, эрозивном гастрите, раке желудка, кровотечением из дыхательных путей.
Эрадикационная терапия инфекции Н. pylori у беременных не проводится.
7.1.2 Особенности течения СМВ у лиц пожилого и старческого возраста
В развитии СМВ у пациентов пожилого возраста - помимо инфекции H.pylori и кислотно-пептического фактора – могут также играть роль атеросклеротические изменения сосудов желудка, некоторые фоновые заболевания (например, хронические неспецифические заболевания легких), снижающие защитные свойства слизистой оболочки желудка, прием лекарственных препаратов (в первую очередь, НПВП), обладающих ульцерогенным действием.
При проведении медикаментозной терапии следует соблюдать осторожность, учитывая более высокий риск развития побочных эффектов у пожилых пациентов по сравнению с пациентами молодого и среднего возраста.














