Другие уточненные врожденные аномалии органов дыхания (первичная цилиарная дискинезия)Код: 1028 • Редакция: 1
Первичная цилиарная дискинезия (ПЦД) (OMIM (онлайн база наследственных менделирующих заболеваний у человека) # 242650) – редкое наследственное заболевание из группы цилиопатий, в основе которого лежит дефект ультраструктуры ресничек эпителия респираторного тракта и аналогичных им структур (жгутики сперматозоидов, ворсины фаллопиевых труб, эпендимы желудочков и др.), приводящий к нарушению их двигательной функции. Характеризуется поражением всех отделов респираторного тракта с формированием хронического воспалительного процесса, нарушением фертильности (бесплодие, преимущественно мужское, эктопические беременности у женщин). Около половины пациентов с ПЦД имеют полное или неполное обратное расположение внутренних органов с различными вариантами гетеротаксии (OMIM # 244400) [1, 2, 3, 4, 5].
В литературе встречаются термины, ранее расценивавшиеся как синонимы: синдром Картагенера (Kartagener syndrome; Siewert syndrome; Зиверта-Картагенера), синдром неподвижных ресничек (immotile cilia syndrome), двигательная цилиопатия (the motile ciliopathy) [6].
ПЦД относят к группе цилиопатий - заболеваний, в основе которых лежит генетически детерминированный дефект строения аксонемы ресничек и/или жгутиков [1, 2, 3, 4, 5]. Клетки, имеющие реснички или аналогичные структуры, обнаруживаются во многих системах организма: реснички участвуют в мукоцилиарном клиренсе, движении гамет, перемещении спинномозговой жидкости, сенсорной рецепции, функционировании почечного эпителия, формировании лево-правой асимметрии органов у млекопитающих [7, 8].
Реснички (цилии) разделяют на 2 большие группы в соответствии с их основной функцией - моторные и сенсорные. Реснички мерцательного эпителия респираторного тракта, клеток эпендимы желудочков, сперматозоидов и клеток семявыносящих путей (у мужчин) и фаллопиевых труб (у женщин) выполняют двигательную функцию. Основной компонент реснички/жгутика - аксонема, сложная осевая структруа, состоящая из белковых микротрубочек, которые имеют структуру 9 + 2. Также к группе двигательных относят реснички со структурой 9 + 0, утратившие центральную пару, но имеющие внутренние и наружные динеиновые ручки (ресничка эмбрионального узла). Подробнее о строении ресничек и жгутиков см. Приложение А3.1, варианты нарушений структуры и функции ресничек у пациентов с ПЦД – см. Приложение А3.2.
Первичная цилиарная дискинезия (ПЦД) связана с аномалиями положения внутренних органов грудной и брюшной полости, аномальной подвижностью сперматозоидов и аномальной структурой и функцией ресничек мерцательного эпителия респираторного тракта, которые приводят к нарушению мукоцилиарного клиренса, способствующего размножению бактерий в дыхательных путях, что приводит к хроническому воспалению на протяжении всего респираторного тракта, а также к поражению полостей среднего уха.
У лиц с ПЦД наблюдается респираторный дистресс в младенчестве, постоянный продуктивный кашель с рецидивирующими бронхитами и пневмониями, которые могут прогрессировать до формирования бронхоэктазов. Присоединяется инфекция условно-патогенными микроорганизмами в т.ч., синегнойной палочкой. Микроорганизмы могут культивироваться из секрета дыхательных путей, и носовых пазух. Обратное расположение внутренних органов (situs inversus) присутствует у 50 % пациентов с ПЦД. Стеаторея у пациентов с ПЦД не наблюдается. Задержка развития нехарактерна. ПЦД ассоциирована с патогенными вариантами во множестве генов, кодирующих различные структурные компоненты ресничек, и наследуется преимущественно по аутосомно-рецессивному типу. Дисфункция аксонемной структуры связана с классом заболеваний, известных под общим названием цилиопатии, который включает также синдром Барде-Бидля, гидроцефалию, поликистоз почек, поликистоз печени, нефролитиаз, синдром Меккеля-Грубера и синдром Жубера [271, 272].
В онлайн базе наследственных менделирующих заболеваний у человека – OMIM (244400; 242650) к настоящему времени указано более 45 генетических локусов, участвующих в этиологии ПЦД (Приложение А3.3). Тем не менее, 20-30 % пациентов с хорошо охарактеризованной ПЦД не имеют идентифицируемых патогенных вариантов ни в одном из известных генов. Большинство генетических форм ПЦД наследуются по аутосомно-рецессивному типу, за исключением FOXJ1-PCD (аутосомно-доминантный) и PIH1D3-PCD и OFD1-PCD (X-сцепленный) (Приложение А3.4) [2, 9, 10].
ПЦД – редкое заболевание (ORPHA 244; 98861). Его частота составляет от 1:10 000 до 1:40 000 родившихся живыми [2, 9, 10]. Рассчитанная распространенность ПЦД в среднем составляет 1:7554, при этом расчеты приведены без учета VUS (только патогенные и вероятно патогенные варианты). Оценка распространенности ПЦД рассчитывается на основе предположения, что 65 % больных имеют диагностические варианты генов, которые, как уже известно, участвуют в ПЦД [11].
Широкая вариабельность частоты в различных исследованиях обусловлена как различиями в критериях диагностики, так и популяционными особенностями (географической локализацией различных видов мутаций, частотой кровнородственных браков и т.д.). Среди стран европейского региона самая высокая распространенность на Кипре 1:9 000, а самая низкая - в Эстонии и Болгарии 1:60 000 детей [2, 12]. Относительно более частая встречаемость ПЦД в Великобритании среди популяции выходцев из Южной Азии (1:2265) [9].
Вместе с тем, следует принять во внимание, что диагностика ПЦД нередко существенно запаздывает. Среди детей с рекуррентными воспалительными заболеваниями бронхолегочной системы 5,6 % составляют пациенты с ПЦД [13]; среди пациентов с бронхоэктазами ПЦД выявляется примерно от 7 % [14] до 30 % [15].
На основании обследования населения США с целью выявления обратного расположения внутренних органов и бронхоэктазов заболеваемость предполагается, что частота ПЦД составляет 1 на 10 000–20 000 рожденных детей [16].
В 40 -50 % случаев первичной цилиарной дискинезии наблюдается обратное расположение внутренних органов (situs viscerum inversus) или изолированная декстрокардия, в сочетании с поражением бронхолегочной системы, которая получила название синдром Картагенера (СК). Его распространенность составляет 1:30000-1:60000.
ПЦД не представлена в МКБ-101 как отдельная нозологическая форма. Для кодирования обычно используется следующий код:
Q34.8– Другие уточненные врожденные аномалии органов дыхания
1 - В МКБ 11 для Первичной цилиарной дискинезии используется код LA75.Y (Other specified structural developmental anomalies of lungs/Другие уточненные структурные аномалии развития легких).
Общепринятой классификации первичной цилиарной дискинезии не существует.
○ Первичная цилиарная дискинезия
○ Первичная цилиарная дискинезия с синдромом Картагенера (полный, не полный)
В клинической практике можно рекомендовать классификацию, представленная в таблице 1 [17]
Таблица 1 Клиническая классификация ПЦД
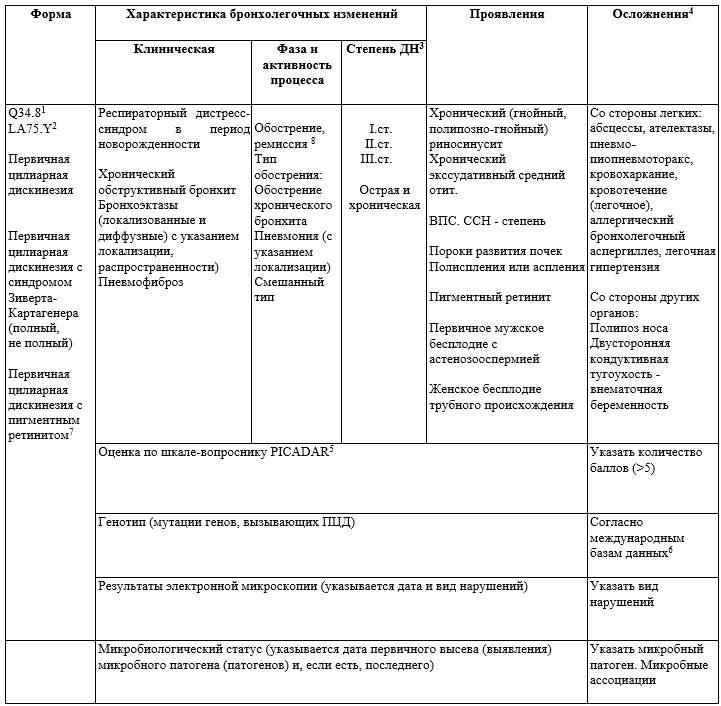
Примечания:
ДН – дыхательная недостаточность; ПЦД – первичная цилиарная дискинезия; ВПС – врожденный порок сердца; ССН – сердечно-сосудистая недостаточность; PICADAR (PrImary CiliAry DyskinesiA Rule) – Предиктивная шкала для выявления симптомов первичной цилиарной дискинезии (Приложение Г1)
1 - Согласно МКБ 10
2 - Согласно МКБ 11
3 - Степень дыхательной недостаточности устанавливается согласно классификации [Chuchalin, A. G. Pulmonology / ed. Chuchalina A. G. - Moscow: GEOTAR-Media, 2020. - 768 p. - ISBN 978-5-9704-5323-0]
4 - Код МКБ рекомендуется использовать из соответствующих разделов.
5 - Оценка по шкале-вопроснику PICADAR [Lucas JS, Gahleitner F, Amorim A, Boon M, Brown P, Constant C, Cook S, Crowley S, Destouches DMS, Eber E, Mussaffi H, Haarman E, Harris A, Koerner-Rettberg C, Kuehni CE, Latzin P, Loebinger MR, Lorent N, Maitre B, Moreno-Galdó A, Nielsen KG, Özçelik U, Philipsen LKD, Pohunek P, Polverino E, Rademacher J, Robinson P, Snijders D, Yiallouros P, Carr SB. Pulmonary exacerbations in patients with primary ciliary dyskinesia: an expert consensus definition for use in clinical trials. ERJ Open Res. 2019 Feb 1;5(1):00147-2018, Behan L, Dimitrov BD, Kuehni CE, Hogg C, Carroll M, Evans HJ, Goutaki M, Harris A,Packham S, Walker WT, Lucas JS. PICADAR: a diagnostic predictive tool for primary ciliary dyskinesia. Eur Respir J. 2016 Apr;47(4):1103-12. doi: 10.1183/13993003.01551-2015. Epub 2016 Feb 25. PMID: 26917608; PMCID: PMC4819882].
6 - Данные на сайтах: Exome Aggregation Consortium [http://exac.broadinstitute.org/ (дата обращения 05.01.2023)], Genome Aggregation Database [http://gnomad.broadinstitute.org (дата обращения 05.01.2023)], Exome Variant Server [http://evs.gs.washington.edu/EVS/ (дата обращения 05.01.2023)], 1000 Genomes Project [http://browser.1000geno-mes.org/index.html (дата обращения 05.01.2023)], dbSNP [http://www.ncbi.nlm.nih.gov/snp (дата обращения 05.01.2023)], dbVar [http://www.ncbi.nlm.nih.gov/dbvar (дата обращения 05.01.2023)], OMIM [http://www.omim.org/ (дата обращения 05.01.2023)], Human Gene Mutation Database [http://www.hgmd.cf.ac.uk/ac/in-dex.php (дата обращения 05.01.2023)], Clin Var [http://www.ncbi.nlm.nih.gov/clin-var/ (дата обращения 05.01.2023)], Human Genome Variation Society [http://www.hgvs.org/dblist/dblist.html (дата обращения 05.01.2023)], DECIPHER [https://decipher.san-ger.ac.uk (дата обращения 05.01.2023)].
7 - Данная форма цеплена с X хромосомой, вызвана мутациями в генах в генах RPGR (20 % всех случаев), PIH1D3 и OFD1.
8 - Обострение хроничеcкого бронхолегочного процесса при наличии 3 и более признаков согласно [Kondratyeva E.I., Avdeev S.N., Mizernitskiy Yu.L., Polyakov A.V., Chernukha M.Yu., Kondratenko O.V., Namazova-Baranova L.S., Vishneva E.A., Selimzyanova L.R., Simonova O.I., Gembitskaya T.E., Bragina E.E., Rachina S.A., Malakhov A.B., Polyakov D.P., Odinaeva N.D., Kutsev S.I. [Primary ciliary dyskinesia: review of the draft clinical guidelines], 2022. PULMONOLOGIYA. 2022;32(4):517-538. (In Russ.) https://doi.org/10.18093/0869-0189-2022-32-4-517-538, Hannah WB, Seifert BA, Truty R, Zariwala MA, Ameel K, Zhao Y, Nykamp K, Gaston B. The global prevalence and ethnic heterogeneity of primary ciliary dyskinesia gene variants: a genetic database analysis. Lancet Respir Med. 2022 May;10(5):459-468. doi: 10.1016/S2213-2600(21)00453-7. Epub 2022 Jan 17. PMID: 35051411; PMCID: PMC9064931].
В будущем, по мере углубления знаний, эта классификация также потребует пересмотра.
Средний возраст постановки диагноза в странах Европы, согласно исследованию, проведенному в 2010 году, составил 5,3 года, при этом пациентам с синдромом Картагенера диагноз подтверждается в более раннем возрасте – 3,5 года. [18]. Медиана возраста установления диагноза в Российской Федерации (57 пациентов): у пациентов с синдромом Картагенера: 4 года (IQR 0,8-7, range 0-14) у пациентов с нормальным расположением внутренних органов: 7,6 лет (IQR 3,1-13, range 0,3-16) [19].
Изменение структуры и функции ресничек респираторного тракта приводит к нарушению мукоцилиарного транспорта. Последующее наслоение инфекции обусловливает формирование хронического воспалительного поражения органов дыхания. Таким образом, в клинической картине заболевания основную роль играют нарушения функции респираторной системы, характеризующиеся тотальностью поражения и ранним началом.
Ведущим проявлением болезни у детей с ПЦД являются частые воспалительные заболевания верхних и нижних дыхательных путей, которые регистрируются у достаточно большой когорты детей, особенно в раннем возрасте. Однако, осведомленность врачей о ПЦД крайне невысока, в связи с чем диагностика данной патологии в большинстве случаев несвоевременна.
Поражение легких в большинстве случаев проявляется уже в первые дни жизни ребенка в виде пневмонии, ателектазов, респираторного дистресса, нередко требующих интенсивной терапии, длительной оксигенотерапии; у пациентов с синдромом Картагенера выявляется обратное расположение внутренних органов; нередко у новорожденных с ПЦД диагностируют пороки сердца. С первых дней жизни отмечают персистирующую ринорею (табл. 1).
У детей более старшего возраста, подростков и взрослых наряду с постоянным влажным кашлем отмечаются повторные воспалительные заболевания дыхательных путей (бронхиты, пневмонии); нередко процесс имеет непрерывно рецидивирующее течение. Патологии бронхолегочной системы сопутствует поражение ЛОР-органов: хронический ринит, риносинусит, повторные отиты, постепенное снижение слуха. У взрослых пациентов отмечают нарушения репродуктивной функции (бесплодие или снижение фертильности) (табл. 2).
Классические проявления ПЦД в зависимости от возраста (адаптировано [20])
Таблица 2. Клинические проявления первичной цилиарной дискинезии в разные возрастные периоды
Возраст |
Клинические проявления |
|---|---|
Период новорожденности |
Пневмония, ателектазы легких Ринит Респираторный дистресс-синдром Пороки сердца и внутренних органов Обратное расположение внутренних органов (у 40-50 % пациентов) |
Детский возраст |
Круглогодичный ринит Хронический/рецидивирующий отит, снижение слуха Полипоз носа Рецидивирующий синусит Рецидивирующий бронхит/пневмония Бронхоэктазы Обратное расположение внутренних органов (у 40-50 % пациентов) |
Подростки и взрослые |
Симптомы, характерные для детского возраста Бронхоэктазы Нарушения фертильности Внематочная беременность Обратное расположение внутренних органов (у 40-50 % пациентов) |
Характер и распространенность бронхолегочных изменений определяют тяжесть заболевания, выраженность воспалительного процесса. Заболевание может протекать по типу тяжелой бронхоэктатической болезни с частыми обострениями, с отделением значительного количества гнойной мокроты, оральной крепитацией, одышкой. У пациентов с бронхитом без бронхоэктазов обострения воспалительного процесса в бронхолегочной системе не столь частые; эндоскопические изменения носят преимущественно катарально-гнойный характер, одышка отсутствует.
Вопрос о частоте и сроках формирования бронхоэктазов у пациентов с ПЦД остается дискуссионным: по мнению некоторых специалистов, морфологический характер бронхолегочных изменений не зависит от длительности течения процесса: бронхоэктазы нередко выявляются у детей уже первых лет жизни, и в то же время наличие бронхита (без сформировавшихся бронхоэктазов) диагностируется иногда у подростков [21, 22]. Вместе с тем, уже к 8-летнему возрасту бронхоэктазы выявляются у 50 % больных ПЦД, достигая почти 100 % их распространенности среди взрослых пациентов [23, 24].
При ПЦД наиболее характерными возбудителями инфекционного процесса являются Haemophilus influenzae и Streptococcus pneumoniae, реже Moraxella catarrhalis, Staphylococcus aureus. Pseudomonas aeruginosa у детей высевается редко, однако с возрастом значение этого патогена у больных с ПЦД постепенно возрастает [1, 25]. У 15 - 47 % пациентов с ПЦД хотя бы один раз в год выделяется P. aeruginosa, а у 39 % пациентов наблюдается хроническая синегнойная инфекция [26]. Распространенность НТМ среди детей с ПЦД составляет 3 % [27], а среди взрослых — 10 % [28].
Показано, что Achromobacter xylosoxidans является патогеном, который в первую очередь идентифицируется среди взрослых пациентов с ПЦД при исследовании смешанной популяции, включающей как детей, так и взрослых с ПЦД, в которой A. xylosoxidans выделен в 6 % образцов мокроты от взрослых пациентов старше 25 лет по сравнению с детьми до 12 лет - в 1 % случаев [26]. Эта проблема мало изучена и в литературе практически отсутствуют данные, касающиеся распространенности, клинического значения и особенностей лечения инфекций легких, вызванных A. xylosoxidans. В литературе также отсутствуют данные, касающиеся распространенности, клинического значения и особенностей лечения при хронической инфекции легких, вызванной Burkholderia cepacia complex. Нельзя исключить, учитывая патогенез ПЦД, что хроническая инфекция легких при ПЦД может быть обусловлена всеми теми же микроорганизмами как при муковисцидозе (МВ).
Впервые в РФ в 2023 г. было проведено исследование в рамках проекта «Бронхоэктазы: муковисцидоз и не только»* (руководители – академик Российской академии наук С.Н. Авдеев, профессор Е.И. Кондратьева) [273]. В феврале–декабре 2023 г. были обследовано 64 пациента с ПЦД ( 24 ребенка в возрасте 0–10 лет; 23 подростка в возрасте 11–18 лет; 17 взрослых в возрасте 19–53 лет) из различных регионов Российской Федерации (Москва, Московская область, Cамара, Екатеринбург, Красноярск, Новосибирск, Омск, Казань, Владимир, Республика Крым). Материалом для изучения стали 170 респираторных образцов (мазки из зева, носа и мокроты). В ходе исследования было выделено 46 видов бактерий, 4 вида вирусов и представители 2 родов грибов. Среди идентифицированных бактерий были представители нормальной микрофлоры респираторного тракта и бактерии, имеющие клиническое значение. Из представителей нормальной микрофлоры наиболее часто из респираторного тракта выделяли Streptococcus spp. (ɑ-гемолитические), относящиеся к группе Viridans, Neisseria spp. (непатогенные), Enterococcus spp., Staphylococcus epidermidis, Corynebacterium spp., Rothia spp. К группе клинически значимых были отнесены микроорганизмы, способные вызывать обострения у пациентов с ПЦД: Staphylococcus aureus, Streptococcus pneumoniae, Streptococcus dysgalactiae, Streptococcus pyogenes, Moraxella spp., а также бактерии, относящиеся к группе НГОБ и порядку Enterobacterales. В группах детей и подростков доминирующим возбудителем, который может вызывать инфекции респираторного тракта, был S. аureus (выделен у 58,3 % детей и 82,6 % подростков). Вторым наиболее часто встречающимся возбудителем в указанных группах были бактерии P. aeruginosa (16,6 и 17,4 % соответственно). В группе взрослых этот возбудитель, наоборот, доминировал (выделен у 52,9 % пациентов), а S. aureus стал вторым по частоте встречаемости (41,2 % случаев). У пациентов с ПЦД выделяли и другие НГОБ. причем наиболее часто – в группе подростков (11 видов НГОБ, тогда как у детей и взрослых – 10 и 4 соответственно). Такие виды, как Pseudomonas montelii, Pseudomonas fluorescens, а также входящие в тот же комплекс Pseudomonas veronii и Pseudomonas rhodesiae, высевали в единичных случаях только в группах детей и подростков. Бактерии Acinetobacter spp. высевали у пациентов всех возрастных групп. Среди других видов бактерий, относящихся к НГОБ, выделен вид Chryseobacterium indologenes, S. maltophilia, Delftia acidovoronas, Ochrobactrum tritici и Pasteurella multocida. Moraxella spp. (M. catarrhalis и M. nonliquefaciens) выделены у взрослых пациентов. M. сatarrhalis обнаружены также у детей. Учитывая, что для пациентов с МВ при ХИЛ клинически значимы бактерии рода Achromobacter и Burkholderia cepacia complex, было решено уделить особое внимание высеву этих микроорганизмов также у пациентов с ПЦД. Achromobacter ruhlandii выделили у ребенка в единичном случае, а Achromobacter xylosoxidans – у взрослого пациента также в единичном случае Бактерии Burkholderia cepacia complex у пациентов с ПЦД не выделены. Порядок Enterobacterales также был представлен многообразием видов. Доминирующими у детей оказались виды Enterobacter cloacae (12,5 %), Klebsiella pneumoniae (8,3 %), Klebsiella oxytoca (8,3 %) детей. У взрослых пациентов выявлены E. coli (23,5 %), K. pneumoniae (11,7 %), Raoultella ornithinolytica (5,8 %). В группе подростков в единичных случаях высевали E. cloacae, Citrobacter freundi, Serratia marcescens. Виды Streptococcus pneumoniae и Streptococcus dysgalactiae выявлены у 8,3 % и 4,1 % детей соответственно, Streptococcus pyogenes был выявлен в единичных случаях у взрослого и подростка. Кроме бактерий, у 48,4 % пациентов из всех возрастных групп выделялись грибы рода Candida 48,4 % и у 7,2 % грибы рода Aspergillus - Исследование микробного пейзажа показало, что у пациентов с ПЦД может встречаться как моно-, так и смешанная инфекция. Моноинфекция обнаружена у 20,3 % пациентов. В остальных случаях инфекция респираторного тракта у пациентов с ПЦД вызвана ассоциациями микроорганизмов. В основном они состояли из 2–3 культур, но в 3 случаях идентифицированы ассоциации из 4 микроорганизмов: P. аeruginosa + S. aureus + A. ruhlandii + C. albicans; P. aeruginosa + S. aureus + S. marcescens + C. albicans и S. aureus + P. monteilii + A. pittii + C. albicans. Доминирующими ассоциациями у пациентов с ПЦД были P. аeruginosa + C. аlbicans, P. аeruginosa + S. aureus, S. aureus + C. albicans (в 10,9 % случаев каждой). P. аeruginosa, S. аureus, C. albicans и Aspergillus spp. – виды, входившие в большинство ассоциаций с видами НГОБ или представителями порядка Enterobacterales. У ряда пациентов с ПЦД, кроме бактерий и грибов, в ассоциации входили вирусы. Среди обследованных пациентов были выделены human Adenovirus (hAdV), human Rhinovirus (hRV), Severe Acute Respiratory Syndrome CoronaVirus 2 (SARS-CoV-2, ранее – 2019-nCoV), Human Coronavirus OC43 (HCoV-OC43). Самым распространенным оказался человеческий риновирус (hRV).
Таким образом, для пациентов с ПЦД характерно наличие инфекции респираторного тракта, вызванной доминирующими возбудителями S. aureus и P. аeruginosa в виде моноинфекции или в ассоциациях с представителями НГОБ, грибов, вирусов. Причем во взрослом возрасте происходит смена доминирующего возбудителя с S. aureus на P. аeruginosa. А также наблюдается разнообразие бактериальных видов, входящих в ассоциации, что необходимо учитывать при диагностике, лечении и профилактике пациентов с ПЦД.
Затруднение носового дыхания и хроническая ринорея обычно присутствуют у детей любых возрастных групп, начиная с новорожденности или грудного возраста. Жалобы носят круглосуточный и круглогодичный характер [29, 30]. Характерна гипосмия или аносмия, как проявление хронического риносинусита. Для > 85 % детей младших возрастных групп характерен рецидивирующий острый средний отит (в т. ч. гнойный перфоративный, с отореей), по поводу которого 38 % пациентов получает более 30 курсов системной антибактериальной терапии. С возрастом у части пациентов прогрессирует кондуктивная тугоухость за счет течения экссудативного среднего отита, формирования ретракционных и адгезивных изменений в среднем ухе. В случае указаний в анамнезе на выполнение тимпаностомии (шунтирования барабанных полостей) по поводу рецидивирующего или хронического экссудативного среднего отита характерна быстрая самостоятельная экструзия вентиляционных трубок. Перфорация барабанной перепонки после шунтирования, по данным ряда авторов, сохраняется у половины больных с ПЦД [31] (в общей популяции подобное явление отмечается у 0,1 % шунтированных). У большой части пациентов имеют место жалобы на прогрессирующее снижение слуха до подросткового возраста с последующей стабилизацией или улучшением [32]. Аналогично с возрастом снижается частота рецидивов острого среднего отита [31].
Дифференциальный диагноз ПЦД требует исключения широкого спектра патологии:
- врожденные пороки развития бронхолегочной системы: дизонтогенетические бронхоэктазы, бронхолегочные кисты, трахео- и бронхо-пищеводные свищи (диагноз подтверждается посредством проведения визуализирующих порок методов диагностики, таких как компьютерная томография, трахеобронхоскопия);
- муковисцидоз (диагноз подтверждается при наличии одного или более характерных фенотипических проявлений МВ в сочетании с доказательствами нарушения функции МВТР, такими как: при положительном результате потовой пробы (исследование уровня хлоридов в поте) и/или выявлении при молекулярно-генетическом исследовании клинически значимых мутаций гена CFTR (МВТР - трансмембранный регулятор проводимости муковисцидоза) (см. Клинические рекомендации «Кистозный фиброз (муковисцидоз)»);
- иммунодефицитные состояния (диагноз подтверждается врачом-аллергологом-иммунологом после проведения иммунологического обследования, включающего в себя, в зависимости от клинической необходимости, определение уровня иммуноглобулинов в крови (A,E,M,G), иммунофенотипирование лимфоцитов, определение определение ДНК TREC (T-cell receptor excision circles – Т-клеточные эксцизионные кольца) и KREC (Kappa-deleting recombination excision circle - Каппа-эксцизионные кольца) в крови методом ПЦР, фагоцитарной активности лейкоцитов, уровня компоненов комплемента, NK-клеток и др.) ;
- длительно находящееся инородное тело в дыхательных путях (диагноз подтверждается посредством проведения трахеобронхоскопии, компьютерной томографии органов грудной полости);
- дефицит альфа-1-антитрипсина (диагноз подтверждается оценкой уровня α-1-антитрипсина в крови, и выявленной значимой заменой в генах ответственных за формирование заболевания, таких как SERPINA1, SERPINA2, SERPINA3);
- пороки развития сердца и сосудов;
- другие врожденные и/или наследственные заболевания и синдромы (синдром Вильямса-Кэмпбелла (ORPHA:411501) и др.);
- бронхиальная астма;
- хроническая обструктивная болезнь легких (ХОБЛ);
- туберкулез;
- легочный микобактериоз;
- идиопатический полипозный риносинусит;
- некоторые формы мужского и женского бесплодия, не связанные с ПЦД;
- цилиопатии, которые могут быть проявлением других синдромов (Сениора-Лукена, Альстрёма, Барде-Бидля) и протекать с или без респираторных проявлений, с обратным расположением внутренних органов (гетеротаксией), поликистозом печени и/или почек, атрезией желчных путей, ретинопатией и др.
Критерии диагностики/исключения ПЦД
В настоящее время нет единого метода - «золотого» стандарта диагностики ПЦД. Диагноз ПЦД устанавливается на основании характерной клинической картины в сочетании с результатами специальных исследований [3].
Оптимальный алгоритм диагностики остается предметом дискуссий [5, 274].
При установлении диагноза учитываются:
характерные данные анамнеза и клиническая картина (см. выше);
результаты скрининга - исследование уровня оксида азота (NO) в выдыхаемом назальном воздухе (Определение уровня оксида азота в выдыхаемом воздухе) (у большинства пациентов с ПЦД он снижен);
анализ частоты и паттерна биения ресничек в биоптате из полости носа или бронха с помощью световой микроскопии/высокоскоростной видеомикроскопии (патолого-анатомическое исследование биопсийного (операционного) материала тканей верхних дыхательных путей/патолого-анатомическое исследование биопсийного (операционного) материала тканей трахеи и бронхов);
электронная микроскопия (патолого-анатомическое исследование биопсийного (операционного) материала тканей верхних дыхательных путей с применением электронно-микроскопических методов/патолого-анатомическое исследование биопсийного (операционного) материала тканей нижних дыхательных путей с применением электронно-микроскопических методов) (обнаружение аномалий строения ресничек в биоптате слизистой оболочки носа или бронха, аномалий строения жгутиков сперматозоидов).
Различают
Дефекты 1 класса:
Дефект наружных динеиновых ручек (ODA)
Комбинированные дефекты наружных и внутренних динеиновых ручек (ODA + IDA)
Дефекты микротрубочек и дефект внутренних динеиновых ручек (IDA)
Дефекты 2 класса:
Дефект центрального комплекса
Неправильная локализация базальных телец с небольшим количеством ресничек или их отсутствием
Отсутствие ODA в 25–50 % сечений
Комбинированные дефекты ODA + IDA в 25–50 % поперечных срезов
При этом, дефекты 1 класса подтверждают диагноз ПЦД
Дефекты 2 класса предполагают ПЦД и требуют подтверждающих данных других диагностических методов.
У лиц с клиническими особенностями ПЦД, у которых не обнаружено патогенных вариантов генов, для подтверждения диагноза ПЦД можно использовать ТЭМ [274].
результаты светооптической микроскопии сперматозоидов (Микроскопическое исследование спермы, спермограмма) (наличие тотальной или субтотальной астенозооспермии);
результаты медико-генетического обследования (анализ родословной, данные молекулярно-генетическое исследования генов, связанных с развитием ПЦД).
Иммуноцитохимическое окрашивание реснитчатых клеток, полученных in vitro (Иммуноцитохимическое исследование биологического материала).
Американское торакальное общество (ATS) и Европейское респираторное общество (ERS) настоятельно рекомендуют сочетание тестов для установления окончательного диагноза ПЦД. Ни один тест не является достаточно чувствительным или специфичным, чтобы исключить ПЦД у всех пациентов.
Высокоскоростная видеомикроскопия, иммунофлуоресцентное тестирование (патолого-анатомическое исследование биопсийного (операционного) материала тканей верхних дыхательных путей/патолого-анатомическое исследование биопсийного (операционного) материала тканей трахеи и бронхов) и исследование уровня оксида азота (NO) в выдыхаемом назальном воздухе (Определение уровня оксида азота в выдыхаемом воздухе, иммуноцитохимическое исследование биологического материала) настоятельно рекомендуются в качестве дополнения к генетическому тестированию и/или трансмиссионной электронной микроскопии (патолого-анатомическое исследование биопсийного (операционного) материала тканей верхних дыхательных путей с применением электронно-микроскопических методов/патолого-анатомическое исследование биопсийного (операционного) материала тканей нижних дыхательных путей с применением электронно-микроскопических методов) для диагностики ПЦД, однако ни один дополнительный тест не подходит в качестве самостоятельного теста для диагностики ПЦД, и ни один отдельный дополнительный или референтный тест не подходит для исключения ПЦД [274].
Исключение диагноза ПЦД
Основываясь на рекомендациях, основанных на фактических данных, при исключении диагноза ПЦД учитывается следующее:
1) При оценке и исключении ПЦД требуется многотестовый подход, поскольку ни один тест не обладает достаточной чувствительностью или специфичностью, чтобы быть самостоятельным.
2) Следовательно, ни один тест не должен использоваться для исключения диагноза ПЦД (включая индексные или референтные тесты).
2) У лиц с симптомами, указывающими на ПЦД, комбинация отрицательных тестов снижает вероятность ПЦД, но диагноз не может быть исключен. Отрицательный тест определяется как: назальный NO > 77 нл/мин., нормальный прямой и восстановительный ход ресничек при высокоскоростной видеомикроскопии, нормальная иммунофлуоресцентная панель, отрицательная генетическая панель известных генов ПЦД, нормальная электронная микроскопия (ТЭМ).
3) Важно подчеркнуть, что невозможно исключить ПЦД у пациента с очень высоким клиническим подозрением (например, situs inversus totalis с бронхоэктазами и неонатальным респираторным дистрессом и хроническими симптомами поражения верхних и нижних дыхательных путей в течение всей жизни) по сравнению с пациентами с низким клиническии проявлениями. Пациентов с высоким клиническим подозрением на ПЦД, но отрицательными тестами (индексным и референтным), следует отнести к категории «Предполагаемая ПЦД» и повторно обследовать во время последующих визитов.
4) Качество и техника проведения теста имеют решающее значение. Тесты должны быть выполнены в соответствии с минимальными стандартами.
Более обширные молекулярно – генетические тесты будут более точными при оценке пациентов на ПЦД.
Обширный генетический тест, такой как полноэкзомное секвенирование, точнее любой панели генов.
5) При оценке пациентов на ПЦД следует рассмотреть возможность более обширного тестирования на альтернативные диагнозы (например, кистозный фиброз (муковисцидоз) и первичный иммунодефицит).
6) У пациента с низким клиническим подозрением на ПЦД чувствительность и специфичность тестирования ниже, и его ценность следует рассматривать в контексте общей оценки. Не все тесты (референтные или индексные) требуются для исключения диагноза у человека с низким клиническим подозрением, и врач может выбрать один тест или не использовать ни одного, если клиническое подозрение очень низкое.
Неубедительные тесты на ПЦД включают:
1) VUS в одном или обоих аллелях известного гена, ассоциированного с ПЦД,
2) Патогенные или вероятно патогенные варианты в генах, обозначенных как умеренные доказательства на ClinGen,
3) Результаты ТЭМ с дефектами 2 класса.
При этом следует учитывать:
1) У пациентов с клиническим подозрением на ПЦД, с VUS в одном или обоих аллелях, или патогенными или вероятно патогенными вариантами в генах со средними доказательствами, диагноз ПЦД с высокой вероятностью может быть поставлен при наличии положительного дополнительного теста (дефект ТЭМ 2 класса или положительный результат HSVA после после культурирования клеток мерцательного эпителия, полученных с помощью биопсии с последующей дифференцировкой в реснитчатые клетки (цилиогенез) (метод ALI-культуры) или положительный иммунофлуоресцентный тест), который согласуется с клинической картиной и известными ассоциациями генотипа и фенотипа.
2) У пациентов с клиническим подозрением на ПЦД и дефектами ПЭМ 2 класса диагноз ПЦД с высокой вероятностью может быть поставлен при наличии положительного дополнительного теста (генетического или иммунофлуоресцентного или HSVA), который согласуется с клиническим анамнезом и известными ассоциациями генотипа и фенотипа.
3) Пациентов с выраженным клиническим анамнезом ПЦД и аномальными дополнительными тестами, но при отсутствии референтных тестов, их неубедительных или нормальных результатах - следует обозначить как «ПЦД с высокой вероятностью».
Например, пациент с характерными клиническими признаками ПЦД с низким содержанием NO в выдыхаемом назальном воздухе и стойкими аномалиями, выявленными при HSVA при оценке после культивирования клеток, несмотря на отрицательные результаты генетического тестирования и ПЭМ. Такие пациенты должны наблюдаться у врача - эксперта по ПЦД (обычно-врач-пульмонолог или иной специалист (например, врач-педиатр/врач-терапевт)).
Диагноз ПЦД следует регулярно пересматривать, по мере появления новых тестов или их доступности, улучшения диагностических тестов или появления новых вариантов генов, связанных с ПЦД.
Рекомендуется направлять пациентов в исследовательские центры, занимающиеся поиском генов ПЦД, ТЭМ, Видеоскоростной микроскопией (HSVA) ALI-культур и иммунофлюоресцентными белками.
4) Важна конкордация между тестами, и если конкордация отсутствует или результаты тестов неубедительны, эти тесты можно повторить в будущем [274].
Так как высокотехнологичные диагностические тесты являются достаточно дорогостоящим и недоступны для широкого использования в неспециализированных стационарах, целесообразен отбор пациентов для их проведения и направление в учреждение, где имеются возможности для обследования. Отбор рекомендуется проводить с учетом приведенных ниже критериев:
Дополнительному обследованию подлежат [3]:
-
Пациенты, имеющие несколько из нижеперечисленных признаков:
- постоянный продуктивный кашель;
- аномалии расположения внутренних органов;
- врожденные пороки сердца;
- персистирующий ринит;
- полипозный риносинусит;
- хронический средний отит со снижением слуха (или без него);
- наличие респираторных нарушений (в том числе – требующих интенсивной терапии) в периоде новорожденности.
Пациенты без аномалий расположения внутренних органов, но имеющие другие характерные клинические проявления ПЦД (см. п.1,4,5,6 и раздел 1.6 «Клиническая картина»).
Сибсы и другие родственники пациентов с ПЦД, особенно – в случае наличия характерных клинических проявлений (см. п.1,4,5,6 и раздел 1.6 «Клиническая картина»).
Нарушение фертильности у взрослых пациентов (в частности, первичное мужское бесплодие, связанное с астенозооспермией).
Внематочная беременность.
Высев из отделяемого/материала, полученного из верхних и нижних дыхательных путей грамотрицательной флоры, MRSA.
Cочетание характерных клинических признаков с положительным результатом оценки по шкале PICADAR (> 5) (см. Приложение Г1).
Алгоритмы диагностики ПЦД представлены в Приложении Б1.
При сборе анамнеза следует обратить внимание на типичные клинические проявления ПЦД: для этих пациентов характерны торпидные к терапии риниты практически с рождения, инфекции нижних дыхательных путей, сопровождающиеся хроническим кашлем, нередко уже в неонатальном периоде или рецидивирующие бронхиты в раннем возрасте. Кроме того, у многих пациентов отмечаются рецидивирующие экссудативные отиты со снижением слуха. Сочетание хронического (рецидивирующего) синусита с хроническим (рецидивирующим) бронхитом является основанием для углубленного обследования ребенка. В семейном анамнезе иногда удается обнаружить случаи мужского бесплодия, хронических бронхитов или синуситов, аномальное расположение внутренних органов, нередки случаи ПЦД у сибсов.
Характерные данные анамнеза и анамнестические признаки ПЦД:
- внематочная беременность в анамнезе;
- бронхоэктазы у родителей;
- рождение после беременности, наступившей в результате экстракорпорального оплодотворения в связи с бесплодием родителей;
- респираторный дистресс-синдром новорожденных, в особенности с ателектазами на рентгенограммах органов грудной клетки, врожденная пневмония;
- практически постоянное «сопение» носом на первом году жизни, хронический ринит, ежедневная заложенность носа;
- хронический влажный кашель (продолжительностью более 4 недель);
- повторные бронхиты, пневмонии, ателектаз, бронхоэктазы (часто – с поражением средней доли легкого);
- повторные отиты, эксудативный отит, снижение уровня слуха;
- повторные синуситы, хронический синусит;
- «зеркальное» расположение внутренних органов (сердца, печени) – у половины больных (синдром Зиверта-Картагенера/синдром Картагенера);
- высев из мокроты MRSA, грамотрицательной флоры;
- бесплодие у мужчин и снижение фертильности у женщин, бесплодие у родственников.
Физикальное обследование подразумевает оценку общего физического состояния, физического развития ребенка (измерение роста, измерение массы тела, подсчет индекса массы тела (ИМТ)), измерение частоты дыхания, измерение частоты сердцебиения, визуальный осмотр терапевтический, пальпация терапевтическая, аускультация терапевтическая (осмотр верхних дыхательных путей и зева, осмотр, пальпацию и перкуссию грудной клетки, аускультацию легких, пальпацию живота).
Проявления ПЦД значительно варьируют в связи с выраженной генетической гетерогенностью.
2.2.1 Общий осмотр
Рекомендовано пациентам с клиническими признаками ПЦД проведение приема (осмотра, консультации) врача-пульмонолога первичного и повторных и/или приема (осмотра, консультации) врача-педиатра первичного и повторных/приема (осмотра, консультации) врача-терапевта первичного и повторных (специализирующихся в отношении пациентов с ПЦД) с целью постановки диагноза, назначения и контроля лечения, наблюдения в динамике [25].
(УУР – C, УДД – 5)
Комментарии: при общем осмотре пациента оценивают тяжесть состояния, физическое развитие).
- кашель - постоянный, преимущественно продуктивный; нередко с отделением значительного количества гнойной мокроты;
- затрудненное носовое дыхание с наличием постоянного отделяемого; нередко назальная обструкция, связанная с наличием полипов, приводящих к видимой деформации лицевого скелета;
- снижение слуха является следствием персистирующего или хронического среднего отита;
- одышка в покое может наблюдаться в стадии обострения заболевания, одышка при физической нагрузке отмечается у абсолютного большинства больных;
- физикальные изменения в легких: как правило, с двух сторон прослушивается множество разнокалиберных влажных хрипов; перкуторный звук над патологически измененными участками легких укорочен, может отмечаться коробочный оттенок звука, наблюдаться признаки бронхиальной обструкции;
- грудная клетка может иметь различные деформации;
- у пациентов с наиболее тяжелыми проявлениями вследствие хронической гипоксии формируется утолщение ногтевых фаланг пальцев («барабанные палочки»), изменение формы ногтей («часовые стекла»).
- при полном обратном расположении внутренних органов тоны сердца прослушиваются в правой половине грудной клетки и со стороны спины; печень пальпируется слева. Могут наблюдаться и другие варианты нарушения расположения органов.
2.2.2 Физикальное обследование ЛОР органов
Рекомендовано пациентам с клиническими признаками ПЦД проведение приема (осмотра, консультации) врача-оториноларинголога первичного и повторных с целью постановки диагноза, назначения и контроля лечения, наблюдения в динамике [25].
(УУР – C, УДД – 5)
- При выполнении передней риноскопии обращает на себя внимание скопление/стагнация отделяемого (чаще гнойного) в нижних носовых ходах, что является достаточно патогномоничным для ПЦД за счет исключительно гравитационно обусловленного транспорта назального секрета в условиях отсутствия мукоцилиарного клиренса [33]. У части пациентов (18 % [34] в конце первой – начале второй декад жизни может развиваться назальный полипоз, который носит характер двустороннего, диффузного.
- При осмотре органа слуха (отоскопии) (осмотр барабанной перепонки с использованием микроскопа (отомикроскопии) вне рецидива острого среднего отита отмечается скопление непрозрачного экссудата за барабанной перепонкой с признаками формирования адгезий и ретракционных карманов расслабленной и натянутой частей барабанной перепонки. В случае наличия стойкой перфорации барабанной перепонки она носит характер центральной (мезотимпанальной) после шунтирования барабанной полости или эпитимпанальной в случае выраженной ретракции расслабленной части (последняя отмечается редко, также как и формирование ретракционной холестеатомы для данной группы пациентов не характерно и отмечается, по данным ряда исследований, от 0 до 11,7 % случаев) [31, 32].
2.2.3 Применение вопросника
Для количественной оценки значимости клинических признаков при подозрении на ПЦД может быть использована шкала PICADAR (Приложение Г1) [35], хотя имеются сообщения о вероятности более низкого предиктивного значения данной шкалы у взрослых [36].
2.3.1 Микробиологическая диагностика
Микробиологическая диагностика у пациентов с ПЦД имеет ряд особенностей, которые необходимо учитывать при организации работы с данной категорией больных.
Хронический воспалительный процесс у пациентов с ПЦД нередко обусловлен патогенами, аналогичными пациентам с кистозным фиброзом (муковисцидозом), что позволило консенсусу экспертов экстраполировать данные, полученные при микробиологических и клинических исследованиях с участием пациентов с кистозным фиброзом (муковисцидозом) на пациентов с ПЦД [28].
Показания для проведения исследования и исследуемые биообразцы
Всем пациентам с ПЦД и пациентам с подозрением на ПЦД рекомендуется регулярное проведение микробиологического исследования респираторных образцов для выделения, идентификации и определения чувствительности клинически значимых возбудителей к противомикробным препаратам (ПМП) с целью оптимизации антимикробной терапии (АМТ) (услуги – см. в Комментариях) [25, 28].
(УУР – C, УДД – 5)
Комментарии: исследование проводится при первичной диагностике и в процессе динамического наблюдения, как правило, не реже 1 раза в 3 мес., по показаниям - чаще. При первичном выявлении P. aeruginosa или хронической инфекции нижних дыхательных путей в период проведения эрадикационной терапии микробиологическое исследование проводится ежемесячно с целью оценки элиминации возбудителя. Также исследование обычно проводится после антимикробной терапии для контроля эрадикации.
Основным методом микробиологической диагностики бронхолегочной инфекции у пациентов с ПЦД является микробиологическое исследование респираторных образцов, включающее культуральное исследование (посев образца на неселективные, селективные и дифференциально-диагностические питательные среды) [25].
В соответствии с Приказом Минздрава России 13 октября 2017 г. № 804н от «Об утверждении номенклатуры медицинских услуг» есть несколько услуг: микробиологическое (культуральное) исследование слизи с миндалин и задней стенки глотки на аэробные и факультативно-анаэробные микроорганизмы, микробиологическое (культуральное) исследование мокроты на аэробные и факультативно-анаэробные микроорганизмы, Микробиологическое (культуральное) исследование лаважной жидкости на аэробные и факультативно-анаэробные микроорганизмы, Определение чувствительности микроорганизмов к антимикробным химиотерапевтическим препаратам.
Рекомендовано проводить пациентам с ПЦД и пациентам с подозрением на ПЦД Микробиологическое (культуральное) исследование мокроты на аэробные и факультативно-анаэробные микроорганизмы, Микробиологическое (культуральное) исследование мокроты на дрожжевые грибы свободно отделяемой мокроты как оптимального биоматериала для микробиологического исследования. Пригодным для исследования также яваляется бронхоальвеолярный лаваж (БАЛ), получаемый при трахеобронхоскопии (Микробиологическое (культуральное) исследование лаважной жидкости на аэробные и факультативно-анаэробные микроорганизмы, Микроскопическое исследование бронхоальвеолярной лаважной жидкости на грибы (дрожжевые и мицелиальные)). При отсутствии продуктивного кашля или затруднении получения мокроты у детей до 6 лет допускается исследование мазка со слизистой оболочки глубоких отделов задней стенки глотки [25].
(УУР – C, УДД – 5)
Комментарий: получение мокроты и БАЛ осуществляется в соответствии со стандартными процедурами при любых инфекциях нижних дыхательных путей. Техника взятия мазка: помещают тампон на заднюю стенку глотки, вызывают кашель и после не менее трех кашлевых толчков удаляют тампон, на который были собраны выделения при кашле.
У пациентов с хроническим синуситом дополнительно к образцам из нижних дыхательных путей рекомендуется микробиологическое исследование мазка, полученного при риноскопии (Микробиологическое (культуральное) исследование смывов из околоносовых полостей на аэробные и факультативно-анаэробные микроорганизмы, Микробиологическое (культуральное) исследование носоглоточных смывов на дрожжевые грибы, Микробиологическое (культуральное) исследование носоглоточных смывов на мицелиальные грибы, Определение чувствительности микроорганизмов к антимикробным химиотерапевтическим препаратам) с целью идентификации микроорганизмов, вызывающих обострение хронического синусита, а также в связи с тем, что ОНП являются резервуаром для инфекций, значимых для нижних дыхательных путей [25, 37].
(УУР – C, УДД – 5)
При наличии продуктивного кашля у пациентов с ПЦД со стабильным течением болезни рекомендовано проведение ежегодного скрининга на НТМБ (выполняется микроскопия с целью выявления кислотоустойчивых бактерий (Микроскопическое исследование мокроты на микобактерии (Mycobacterium spp.)) и культуральное исследование (Микробиологическое (культуральное) исследование мокроты на аэробные и факультативно-анаэробные микроорганизмы, Микробиологическое (культуральное) исследование лаважной жидкости на аэробные и факультативно-анаэробные микроорганизмы)); для выявления НТМБ целесообразно использовать мокроту или другие респираторные образцы (БАЛ) [25, 28].
(УУР – C, УДД – 5)
Хранение и транспортировка образцов для микробиологического исследования
Полученные респираторные образцы от пациентов, проходящих диагностику ПЦД, рекомендовано отправлять в микробиологическую лабораторию в кратчайшие сроки. Если посев биоматериала откладывается более чем на 2 часа, образцы следует хранить при температуре 4–8 °C (но не более 24 ч от момента взятия) с целью получения максимально достоверных результатов исследования [38].
(УУР – C, УДД – 5)
Комментарий: в дополнение к общепринятой маркировке образцов биоматериала для микробиологического исследования необходимо указать, что он собран от пациента с ПЦД с целью обеспечения применения надлежащих процедур исследования в микробиологической лаборатории (питательные среды, режим инкубации и пр.).
Микроскопическое исследование мазков, окрашенных по Граму
В отличие от общих правил микробиологического исследования респираторных образцов (микробиологическое (культуральное) исследование слизи с миндалин и задней стенки глотки на аэробные и факультативно-анаэробные микроорганизмы, микробиологическое (культуральное) исследование мокроты на аэробные и факультативно-анаэробные микроорганизмы, Микробиологическое (культуральное) исследование лаважной жидкости на аэробные и факультативно-анаэробные микроорганизмы, Определение чувствительности микроорганизмов к антимикробным химиотерапевтическим препаратам), у пациентов с ПЦД не рекомендуется отбраковывать образцы мокроты на основании стандартных критериев оценки качества (использования микроскопии мазков, окрашенных по Граму) в связи с их малой информативностью [38].
(УУР – C, УДД – 5)
Комментарий: при ПЦД существует недостаточно доказательств достоверности рутинного использования микроскопии мазков, окрашенных по Граму, в качестве маркера качества мокроты и предполагаемого выделения тех или иных микроорганизмов.
Микробиологическое (культуральное) исследование
Микробиологическое (культуральное) исследование (подготовка, посев образцов на питательные среды, идентификация и оценка клинического значения выделенных микроорганизмов) для диагностики бронхолегочной инфекции у пациентов с ПЦД рекомендуется проводить в соответствии с правилами микробиологической диагностики больных муковисцидозом в связи со сходностью хронического воспалительного процесса [28, 39].
(УУР – C, УДД – 5)
При микробиологической диагностике ПЦД рекомендуется использовать селективные питательные среды для выделения микроорганизмов, требующих особых условий культивирования и выделения: для повышения вероятности обнаружения B. cepacia complex в респираторном образце рекомендуется использование селективной среды для B. cepacia complex (среды, содержащие полимиксин) с целью своевременного обнаружения данного патогена [28, 40].
(УУР – C, УДД – 5)
Комментарий: на селективных средах для B. cepacia complex может быть получен рост и других неферментирующих грамотрицательных бактерий (НГОБ) (B. gladioli, Ralstonia spp., Cupriavidus spp., Pandoraea spp., Inquilinus spp. и др.).
Для всех представителей B. cepacia complex, идентифицированных фенотипическими методами с использованием биохимических/метаболических тест-систем и выделенных от пациентов с клиническими признаками ПЦД, рекомендуется проводить подтверждающую идентификацию физико-химическими (масс-спектрометрическими) методами или молекулярно-генетическими методами с целью более точной диагностики [28, 41].
(УУР – C, УДД – 5)
Рекомендовано проводить более длительную, чем в среднем при обычных респираторных заболеваниях, инкубацию посевов респираторных образцов (микробиологическое (культуральное) исследование слизи с миндалин и задней стенки глотки на аэробные и факультативно-анаэробные микроорганизмы, микробиологическое (культуральное) исследование мокроты на аэробные и факультативно-анаэробные микроорганизмы, Микробиологическое (культуральное) исследование лаважной жидкости на аэробные и факультативно-анаэробные микроорганизмы, Определение чувствительности микроорганизмов к антимикробным химиотерапевтическим препаратам) пациентов с клиническими признаками ПЦД – не менее 5-7 суток с последующей продленной инкубацией чашек с OFPBL-агаром до 28 суток для выявления быстрорастущих НМБ и плесневых грибов, с ежедневным просмотром и изучением всех выросших морфологических типов колоний с целью идентификации всех возможных этиологически значимых микроорганизмов [42].
(УУР – C, УДД – 4)
Комментарий: в большинстве случаев хроническая инфекция нижних дыхательных путей при ПЦД вызывается ассоциациями микроорганизмов. Менее прихотливые и быстро растущие микроорганизмы могут камуфлировать рост более прихотливых и медленнорастущих видов.
Оценка чувствительности выделенных микроорганизмов к ПМП
Для определения чувствительности выделенных микроорганизмов к ПМП при исследовании респираторных образцов (микробиологическое (культуральное) исследование слизи с миндалин и задней стенки глотки на аэробные и факультативно-анаэробные микроорганизмы, микробиологическое (культуральное) исследование мокроты на аэробные и факультативно-анаэробные микроорганизмы, Микробиологическое (культуральное) исследование лаважной жидкости на аэробные и факультативно-анаэробные микроорганизмы, Определение чувствительности микроорганизмов к антимикробным химиотерапевтическим препаратам) пациентов с клиническими признаками ПЦД рекомендовано использовать различные методы: Определение чувствительности микроорганизмов к антимикробным химиотерапевтическим препаратам: Определение чувствительности микроорганизмов к антимикробным химиотерапевтическим препаратам диско-диффузионным методом (ДДМ) или/и методы определения минимальной подавляющей концентрации (МПК) ПМП (Определение чувствительности микроорганизмов к антимикробным химиотерапевтическим препаратам методом градиентной диффузии, Определение чувствительности микроорганизмов к антимикробным химиотерапевтическим препаратам методом разведений, Определение чувствительности микроорганизмов к антимикробным химиотерапевтическим препаратам с использованием автоматических анализаторов) [38].
(УУР – C, УДД – 5)
Комментарии: методы определения минимальной подавляющей концентрации (МПК) ПМП (определение чувствительности микроорганизмов к антимикробным химиотерапевтическим препаратам методом градиентной диффузии, определение чувствительности микроорганизмов к антимикробным химиотерапевтическим препаратам методом разведений (в бульоне), Определение чувствительности микроорганизмов к антимикробным химиотерапевтическим препаратам с использованием автоматических анализаторов) считается референтным методом ПМП с целью получения достоверного результата.
Выбор метода(-ов) определяется возможностями лаборатории и существующими рекомендациями для конкретного возбудителя (комбинации возбудитель-ПМП).
В соответствии с полученными результатами (диаметр зоны подавления роста, значение МПК) определяется клиническая категория чувствительности исследуемого возбудителя к каждому ПМП (если она установлена) [43].
В соответствии с современной методологией оценки чувствительности микроорганизм оценивается как: чувствительный (Ч/S) – если данные in vitro исследования свидетельствуют о высокой вероятности эффективности терапии при использовании стандартной дозы ПМП;
чувствительный при увеличенной экспозиции ПМП (У/I – если данные in vitro исследования свидетельствуют о высокой вероятности эффективности терапии при использовании увеличенной экспозиции ПМП (высокой дозы, увеличенной кратности введения или продленной инфузии);
резистентный (Р/R) – если данные in vitro исследования свидетельствуют о высокой вероятности неэффективности терапии даже при использовании увеличенной экспозиции ПМП.
Выполнение процедуры и интерпретацию результатов исследования рекомендовано проводить в соответствии с актуальной версией рекомендаций по определению чувствительности микроорганизмов к ПМП или новых версий после их вступления в силу с целью получения стандартизированного результата [43].
(УУР – C, УДД – 5)
Комментарий: в ряде ситуаций (для некоторых видов возбудителей, отдельных комбинаций микроорганизм-антибиотик, при лечении ингаляционными формами ПМП) важное значение имеет не только определение клинической категории чувствительности, но и значение МПК ПМП. Если для определения чувствительности использовался метод определения МПК, значение МПК (выраженное в мг/л) следует включить в отчет о микробиологическом исследовании.
При выявлении нескольких морфотипов колоний одного и того же микроорганизма в респираторных образцах пациентов с клиническими признаками ПЦД рекомендовано проводить определение чувствительности к ПМП каждого выделенного морфотипа, так как чувствительность различных морфотипов в пределах одного образца может значительно варьировать [39, 28, 275].
(УУР – C, УДД – 5)
Комментарии: при необходимости наряду со стандартной процедурой определения чувствительности микроорганизмов к ПМП следует использовать дополнительные методы выявления отдельных механизмов резистентности, имеющих клиническое и эпидемиологическое значение (фенотипические и/или молекулярно-генетические, а также другие доступные дополнительные методы выявления детерминант антибиотикорезистентности) [38].
Особенности оценки чувствительности микроорганизмов к ингаляционным ПМП
P. aeruginosa и колистин
Определение чувствительности бактерий в респираторных образцах пациентов с клиническими признаками ПЦД к колистину рекомендуется проводить только методом микроразведений в бульоне (Определение чувствительности микроорганизмов к противомикробным химиотерапевтическим препаратам методом разведений). Другие методы определения чувствительности не обеспечивают получение достоверных результатов [43].
(УУР – C, УДД – 5)
Комментарий: критерии оценки чувствительности к ПМП устанавливаются с учетом сывороточной концентраций ПМП при его системном применении. При применении ингаляционных форм ПМП локальная концентрация может быть существенно выше таковой при внутривенном введении. Критерии оценки чувствительности бактерий при ингаляционном применении ПМП к настоящему времени не разработаны. Следует учитывать, что препарат может сохранять клиническую эффективности и в том случае, если in vitro изолят является устойчивым к колистину.
P. aeruginosa и тобрамицин**
Для ингаляционных форм #тобрамицина** (Согласно инструкции разрешен с 6 лет) наряду с определением категории чувствительности P. aeruginosa выделенных из респираторных образцов пациентов с клиническими признаками ПЦД, рекомендуется определять значение МПК в связи с фармакологическими особенностями вследствие ингаляционного пути введения препарата [44, 45].
(УУР – C, УДД – 5)
Комментарий: испанским советом по стандартизации определения чувствительности к ПМП MENSURA (Mese Espanola de Normalizacion de la Suseptibilitad y Resistencia a los Antimicrobianos) в 2005 году были установлены более высокие пограничные значения МПК для тобрамицина** в случае его ингаляционного введения, в соответствии с которыми изоляты с МПК ≤ 64 мг/л следует оценивать как чувствительные, изоляты P. aeruginosa с МПК ≥ 128мг/л – как резистентные.
Выдача результата микробиологического (культурального) исследования
В заключении о результатах микробиологического исследования целесообразно включать следующую информацию:
- выделенные микроорганизмы в соответствии с ранжированием бактерий по их клиническому значению при ПЦД, наличие мукоидных и немукоидных фенотипов P. aeruginosa аналогично пациентам с МВ;
- результат определения чувствительности к ПМП: значение МПК (если известно), и клиническую категорию чувствительности, используемый стандарт и год издания, в соответствии с которым проводилось исследование (при определении чувствительности ДДМ значения диаметров зон подавления роста не включатся в бланк заключения о результатах микробиологического исследования;
- информацию о выявлении или отсутствии механизмов резистентности, имеющих клиническое и/или эпидемиологическое значение (если проводилось);
- заключение (вероятное клиническое значение выделенных микроорганизмов, комментарии о выявленных особенностях профиля(ей) антибиотикорезистентности возбудителя(ей) и связанных с ним особенностях применения ПМП (если применимо) [39].
В заключение следует включить комментарий о том, что интерпретация значений МПК и/или диаметров зон подавления роста в виде клинической категории осуществляется на основании критериев, рассчитанных для сывороточных концентраций препарата при его системном применении. При использовании ингаляционного пути введения препарата аналогичное значение МПК может быть интерпретировано иначе.
2.3.2 Общеклинические лабораторные методы
Рекомендовано проведение общего (клинического) анализа крови развернутого и Исследование уровня С-реактивного белка в сыворотке крови пациентам при подозрении на ПЦД и далее в процессе динамического наблюдения в целью косвенной оценки активности воспалительного процесса [46, 47].
(УУР – C, УДД – 5)
Комментарии: частота проведения исследований проводится в зависимости от клинической необходимости.
Рекомендовано селективное проведение анализа крови биохимического общетерапевтического при диагностике и при динамическом контроле в связи с вероятностью наличия поликистоза почек у некоторых пациентов с ПЦД (Исследование уровня креатинина в крови, Исследование уровня мочевины в крови, Исследование уровня натрия в крови, Исследование уровня хлоридов в крови) [48, 252].
(УУР – C, УДД – 4)
Комментарии: частота проведения исследований проводится в зависимости от клинической необходимости. Также анализ крови биохимический общетерапевтический (в т.ч., например, Исследование уровня креатинина в крови, Исследование уровня мочевины в крови, Исследование функции нефронов по клиренсу креатинина (проба Реберга) (скорость клубочковой фильтрации) (у детей – определяется по формуле Шварца, у взрослых - по формуле CKD-EPI – подробнее – см. в Клинических рекомендациях по хронической болезни почек), Определение активности аспартатаминотрансферазы в крови, Определение активности аланинаминотрансферазы в крови, Исследование уровня свободного и связанного билирубина в крови и др.) может потребоваться для контроля при лечении противомикробными препаратами, обладающими нефро-и/или гепатотоксичностью в соответствии с Инструкциями.
2.4.1 Методы, применяемые для установления диагноза ПЦД
2.4.1.1 Исследование уровня оксида азота в выдыхаемом назальном воздухе
У пациентов с клиническими признаками ПЦД рекомендовано рассмотреть возможность проведения в качестве скрининга на первом этапе диагностики исследования назального оксида азота (nNO) (Определение уровня оксида азота в выдыхаемом воздухе): у большинства пациентов с первичной цилиарной дискинезией уровень nNO снижен [3, 25, 49, 50, 51, 52, 53].
(УУР – C, УДД – 3)
Комментарии: измерение назального оксида азота (nNO) с помощью хемилюминесцентного анализатора окиси азота в выдыхаемом воздухе проводится в рамках группы диагностических тестов для выявления ПЦД у взрослых и детей старше 5 лет с типичными симптомами данного заболевания [54, 55, 56, 57, 58]; портативные электрохимические газоанализаторы (Портативный ручной монитор окиси азота в выдыхаемом воздухе с принадлежностями) могут использоваться для определения nNO при скрининге на ПЦД, но данный тест должен быть проведен повторно с использованием эталонного стандартного хемилюминесцентного анализатора (хемилюминесцентного анализатора окиси азота в выдыхаемом воздухе) [59, 60].
У детей старше 6 лет и взрослых исследование должно проводиться на хемилюминесцентном анализаторе с задержкой дыхания или сопротивлением на выдохе; у детей младшего возраста проводят тест на непрерывном дыхании.
- У детей старше 5 лет и взрослых, которые могут выполнять необходимые маневры для измерения назального оксида азота, низкое значение nNO (< 77 ppb (*1ppb - 1 частица газа на 109 частиц выдыхаемого воздуха) в двукратных пробах с интервалом не менее 2 месяцев в сочетании с соответствующим клиническим фенотипом (при исключении муковисцидоза, так как 30 % пациентов с муковисцидозом демонстрируют низкий nNO [61]) может быть достаточным для клинического диагноза ПЦД с последующей цилиарной биопсией для электронной микроскопии или высокоскоростной видеомикроскопией и/или генетическим исследованием [3, 25, 51, 52, 53]. Используя значение nNO < 77 ppb (при исключении муковисцидоза), можно обнаружить ПЦД, возникающую в результате дефектов цилиарной аксонемы или мутаций в DNAH11, с чувствительностью и специфичностью 98 % и > 99 % соответственно; но следует помнить, что существуют варианты ПЦД со значениями nNO выше этого порога [62].
- У новорожденных и детей в возрасте до 5 лет показатели nNO не столь надежны для выявления ПЦД (до 36 % ложноположительных результатов у детей дошкольного возраста), поэтому в этой возрастной группе пациентов диагностическое тестирование обычно включает в себя цилиарную биопсию для высокоскоростной видеомикроскопии и электронной микроскопии, а также генетические исследования [25, 49].
- При измерении nNO риск ложноположительных результатов также повышается при острых респираторных инфекциях верхних дыхательных путей, бронхиолите, носовых кровотечениях, ВИЧ и неатопическом синусите, поэтому данное тестирование должно проводиться в здоровом состоянии и повторяться при наличии отклонений в состоянии здоровья на момент обследования [61, 63, 64, 65]; во избежание получения некорректных результатов операторы устройств для определения nNO должны быть хорошо обучены и использовать стандартные рабочие протоколы [52, 55, 66].
Следует отметить, что около 30 % пациентов имеют нормальный или близкий к нормальному результат, например с мутациями CCDC103, RSPH1 [67, 68].
Инвазивные методы оценки строения и/или функции ресничек
Рекомендовано проведение высокоскоростного видео-микроскопического анализа (ВСВМ, HSVA, HSVMA) (Патолого-анатомическое исследование биопсийного (операционного) материала тканей верхних дыхательных путей/Патолого-анатомическое исследование биопсийного (операционного) материала тканей трахеи и бронхов) пациентам с клиническими признаками ПЦД с целью оценки функциональной активности ресничек непосредственно в щеточных биоптатах слизистой носа/бронхов или после культурирования клеток мерцательного эпителия, полученных с помощью биопсии с последующей дифференцировкой в реснитчатые клетки (цилиогенез) (метод ALI-культуры или метод культуры органоидов) с определением частоты биения ресничек – CBF в сочетании с паттерном биения ресничек CBP [3].
(УУР – C, УДД – 5)
Комментарий: метод отличается высокой чувствительностью, но низкой специфичностью; оценка функциональной активности не может производиться изолированно на основе определения частоты биения ресничек.
Самостоятельно не может быть использован ни для подтверждения, ни для исключения диагноза ПЦД; имеет диагностическое значение при использовании совместно с оценкой клинических симптомов и другими специальными методами.
ERS не рекомендует оценивать частоту биений ресничек (CBF) без оценки характера биений ресничек при диагностике ПЦД. Для повышения диагностической точности ВСВМ, оценку CBF следует повторить после культурирования клеток мерцательного эпителия (метод ALI-культуры или метод культуры органоидов).
Возможно применение модифицированного метода световой микроскопии «в темном поле». Компьютеризированная световая микроскопия.
В качестве материала исследования используют щеточные биоптаты слизистой оболочки носа и/или бронхов.
Щеточные биоптаты получают с малоизмененной слизистой оболочки в период ремиссии заболевания. Биоптаты слизистой оболочки незамедлительно после забора помещают в подогретый до 37°С забуференный изотонический раствор натрия хлорида** (натрия хлорид** 0,9 %) и немедленно (не более чем через 20 минут) исследуют нативные препараты. Пригодным для исследования является материал, содержащий цельные пласты эпителия (не менее 12 клеток) с минимальной примесью эритроцитов и слизи.
Для оценки биоптатов цилиарного эпителия методом компьютеризированной световой микроскопии используются нативные препараты или видеоклипы движущихся объектов.
Параметрирование объектов производится в соответствии с алгоритмами, разработанными производителем программы «Мастер Морфология». Параметры движения ресничек предпочтительнее измерять на AVI-изображениях в режиме «Движение» → «Время». При этом учитывается время движения (перемещения) ресничек, затем определяется частота движения в ед/с и проводится статистический анализ с определением среднего значения параметра. Среднее значение длины ресничек определяют в режиме «Подсчет и измерение». При необходимости измеряют длину и ширину эпителиальных клеток, размеры ядра, оценивают ядерно-цитоплазматическое соотношение.
Все параметры подлежат автоматической статистической обработке.
Оборудование для компьютеризированной морфометрии оснащено специальным поворотным устройством конденсора, который позволяет создавать эффект объемного изображения [69].
В РФ зарегистрирована «Программа определения частоты биения реснитчатого эпителия при первичной цилиарной дискинезии» (PCD High-Speed Video Microscopy Analysis (PCD HSVMA)), регистрационный номер программы №2023687245.
Для повышения эффективности диагностики ПЦД на сегодняшний день существуют 3 принципиально разных метода цилиогенеза – метод суспензионной культуры, метод культуры клеток на границе раздела воздух-жидкость (Air-Liquid Interface cell culture – ALI) и метод культуры органоидов. Основу всех методов составляет дифференцировка клеток, выделенных при назальной биопсии, в реснитчатые клетки. Каждый метод цилиогенеза in vitro имеет свои преимущества и недостатки. Получение ALI-культуры является основным методом, при котором образуется больше реснитчатых клеток в сравнении с суспензионной культурой. Однако время цилиогенеза в ALI-культуре значительно больше, а продолжительность поддержания в культуре уступает методу органоидов. Метод ALI-культуры и метод органоидов позволяют проводить повторные анализы ультраструктуры ресничек (ТЭМ) и CBF, что помогает в диагностике ПЦД. Таким образом, клеточные модели реснитчатых клеток имеют хороший потенциал стать инструментом для получения диагностической и терапевтической информации о первичной цилиарной дискинезии и других заболеваниях, связанных с реснитчатыми клетками [70,71,72,73].
Рекомендовано пациентам с клиническими признаками ПЦД селективное (при возможности и необходимости) проведение трансмиссионной электронной микроскопии (ТЭМ) биоптата слизистой оболочки респираторного тракта в качестве дополнительного метода подтверждения диагноза и при сомнительных результатах проведенного обследования (световая микроскопия, высокоскоростной видеомикроскопический анализ) (Патолого-анатомического исследования биопсийного (операционного) материала тканей нижних дыхательных путей с применением электронно-микроскопических методов / Патолого-анатомическое исследование биопсийного (операционного) материала тканей верхних дыхательных путей с применением электронно-микроскопических методов) (с целью выявления ультраструктурных изменений аксонемы ресничек и/или жгутиков [74, 75, 76].
(УУР – C, УДД – 5)
Комментарий: метод ТЭМ доступен только в некоторых крупных научно-исследовательских лабораториях/институтах.
Метод ТЭМ для диагностики ПЦД имеет ряд ограничений: у 10-20 % пациентов с диагнозом ПЦД, установленным с помощью других методов, в том числе, молекулярно-генетического обследования обнаруживается с нормальная ультраструктура аксонемы ресничек либо аномалия не диагностируемая (около 10-20 % пациентов) [76,77,78,79]. Эти случаи были обнаружены с помощью альтернативных диагностических тестов, включая высокоскоростной видеомикроскопический анализ, выявление низкого уровня оксида азота, аномальный профиль цилиарных белков при иммунофлуоресцентном окрашивании и/или патогенные варианты генов, связанных с ПЦД. Таким образом, ультраструктурное выявление аномалий аксонемы ресничек и жгутиков является достаточным, но не необходимым компонентом диагностики ПЦД. Метод входит во все протоколы диагностики ПЦД (Приложение Б1 «Алгоритмы диагностики ПЦД»).
Следует учитывать вероятность вторичных и неспецифических изменений аксонемы реснитчатых клеток дыхательных путей за счет воспалительных и/или инфекционных процессов, а также естественную изменчивость реснитчатых клеток и гетерогенность их морфологии. В связи с этим существенное значение имеет электронно-микроскопическое исследование достаточного количества ресничек в каждом конкретном образце. В случае исследования респираторного эпителия необходимо выявление изменений ультраструктуры не менее 50 ресничек нескольких реснитчатых клеток.
Метод ALI-культуры и метод органоидов позволяют проводить анализ ультраструктуры ресничек (ТЭМ), в т.ч., повторно. Применение методов ALI-культуры или метода органоидов позволяют нивелировать ложноположительные результаты, вызванные повреждением ресничек вследствие воспаления [71].
При ультраструктурных исследованиях ресничек важным моментом является гомогенность (однотипность) выявленных нарушений в конкретном изучаемом образце. Однотипные нарушения должны быть выявлены либо тотально во всех изученных ресничках или жгутиках, либо в подавляющем большинстве.
Учитывая этот факт, метод обладает высокой специфичностью, но ограниченной чувствительностью. Наличие ультраструктурных дефектов достаточно для постановки диагноза и дополнительное обследование нецелесообразно. При отсутствии ультраструктурных дефектов, но при наличии четких клинических признаков, следует продолжить обследование [3].
Пример заключения по результатам ТЭМ в Приложении А3.5.
Рекомендовано проведение эндоскопии носоглотки (Эндоскопическая эндоназальная ревизия полости носа, носоглотки) с забором биоптата (Биопсия слизистой оболочки полости носа / Биопсия слизистой оболочки носоглотки под контролем эндоскопического исследования) или трахеобронхоскопии с биопсией трахеи или бронха (Биопсия трахеи, бронхов при бронхоскопии) пациентам с клиническими признаками ПЦД с целью получения биоптата для проведения высокоскоростного видео-микроскопического анализа и / или ТЭМ и / или анализа частоты и паттерна биения ресничек в биоптате из полости носа или бронха с помощью световой микроскопии [69, 80, 81].
(УУР – C, УДД – 4)
Комментарий:
Забор материала для патологоанатомического исследования:
Щеточные биоптаты получают с малоизмененной слизистой оболочки в период ремиссии заболевания.
Биоптат из полости носа получают с медиальной поверхности среднего отдела нижней носовой раковины с помощью щетки цитологической (для эндоскопа) под контролем передней риноскопии или ригидной эндоскопии. Нежелательным является использование предварительной анемизации слизистой оболочки и аппликационной анестезии из-за цилиотоксического / цилиостатического действия препаратов группы «Деконгестанты и другие назальные препараты для местного применения», анестетиков и входящих в состав препаратов консервантов (имеет значение при исследовании путем нативной световой микроскопии).
Клетки мерцательного эпителия слизистой оболочки полости носа, трахеи или бронхов (при бронхоскопии) для оценки биения ресничек в нативном материале с помощью световой микроскопии могут быть получены с помощью brush (браш)-биопсии (Биопсия слизистой оболочки носоглотки под контролем эндоскопического исследования / Биопсия трахеи, бронхов при бронхоскопии). Биоптаты слизистой оболочки незамедлительно после забора помещают в подогретый до 37°С забуференный 0,9 % раствор натрия хлорида**. Допустимо хранение в теплом 0,9 % растворе натрия хлорида** (37°С) не более 15 минут: при возможности, немедленно исследуют нативные препараты. Пригодным для исследования является материал, содержащий цельные пласты эпителия (не менее 12 клеток) с минимальной примесью эритроцитов и слизи.
Для поведения видеосъемки необходимо применение видеокамеры и инвертированный микроскоп с объективом на 100х с совокупным увеличением 1000х, высокой скоростью съемки. Полученные видеоизображения анализируют в разработанной программе «Программа определения частоты биения реснитчатого эпителия при первичной цилиарной дискинезии» (PCD High-Speed Video Microscopy Analysis (PCD HSVMA)), которая была создана в ФГБНУ «МГНЦ» для оптимизации диагностики ПЦД с помощью световой видеомикроскопии (регистрационный номер №2023687245), нормальная частота биения ресничек считалась более 6 Гц. При увеличении микроскопа (100х, 400х, 1000х), скорость съемки составляла 150 кадров в секунду, время съемки 5 секунд. Полученные видеоизображения анализировали с помощью программы 253]. Программа предназначена для расчета количества активных клеток реснитчатого эпителия и частоты биения ресничек ЧБР (Гц), полученных ex vivo и in vitro (АLI-культуре).
Для проведения трансмиссионной электронной микроскопии материал получают описанным выше методом с помощью браш-биопсии (Биопсия слизистой оболочки носоглотки под контролем эндоскопического исследования/Биопсия трахеи, бронхов при бронхоскопии).
Полученный биоптат для транспортировки первично фиксируется в 2,5 % растворе глутарового альдегида на какодилатном буфере (рН 7,2). Материал хранится в холодильнике при температуре + 4°С, с последующей транспортировкой допустимый срок - до 2-х недель с момента забора [81, 82].
В качестве дополнительного лабораторного метода диагностики и дифференциальной диагностики ПЦД / синдрома Картагенера у мужчин и мальчиков-подростков (в возрасте 15 лет и старше) рекомендовано рассмотреть использование светооптической микроскопии нативного эякулята (стандартное спермиологическое исследование) (Микроскопическое исследование спермы, Спермограмма) [83, 84, 85].
(УУР – C, УДД – 4)
Комментарий: у несовершеннолетних исследование проводят с письменного согласия родителей / законных представителей.
Данное исследование позволяет оценить количественные показатели (объем, концентрация и общее количество сперматозоидов, количество гамет с разной степенью подвижности и неподвижных, количество морфологически нормальных (типичных) сперматозоидов [85].
Существенным фактором при этом является оценка функциональной способности жгутиков сперматозоидов, определяющих их подвижность.
У некоторых пациентов имеются трудности с получением биологического материала.
Забор материала для спермиологического исследования (Микроскопическое исследование спермы, Спермограмма) выполняется путем мастурбации. Рекомендовано сдавать анализ в сроке полового воздержания 3-5 дней. Для ЭМИС строго не регламентировано. Материал собирается в чистые одноразовые пластиковые контейнеры с крышкой. После сдачи образцы термостатируются 20-40 минут для разжижения эякулята при температуре t = 37оC. Кратность выполнения спермиологического исследования у пациентов с ПЦД / подозрением на ПЦД в большинстве случаев достаточно 1 раза, при необходимости – проведение повторного исследования.
Методика оценки подвижности сперматозоидов:
Хорошо перемешать образец спермы. Взять аликвоту эякулята и поместить на предметное стекло, накрыть покровным стеклом. При увеличении 200х или 400х подсчитать 200 сперматозоидов для вычисления доли (%) сперматозоидов различных категорий подвижности. Подвижность каждого сперматозоида оценивается следующим образом: прогрессивно-подвижные (PR, progressive motility) – сперматозоиды, двигающиеся активно, либо линейно, либо по кругу большого радиуса, независимо от скорости; непрогрессивно-подвижные (NP, non-progressive motility) – все другие виды движений с отсутствием прогрессии, то есть плавающие по кругу небольшого радиуса, жгутик с трудом смещает головку или когда наблюдают только биение жгутика; неподвижные (IM, immotility) – отсутствие движения. Повторно взять аликвоту эякулята (предварительно перемешав) и повторить процедуру. Вычислить средние значения и различия между ними для двух аликвот. Определить приемлемость различия (WHO, 2010). Если различие между процентными значениями приемлемо, записать среднее значение. Если различие выше допустимого, приготовить две дополнительные аликвоты спермы и повторить оценку.
Следует отметить, что выявление тотальной и субтотальной астенозооспермии (астенотератозооспермии) и олигоастенотератозооспермии не является обязательным (облигатным) сперматологическим признаком ПЦД, так как они могут быть обусловлены другими причинами. Пациентам с тотальной и субтотальной астенозооспермией (астенотератозооспермией) следует проводить ЭМИС. Для пациентов с ПЦД не характерно наличие тяжелых форм патозоспермии, связанных с отстутствием или крайне низкой концентрацией сперматозооидов (азооспермией и олигозооспермией тяжелой степени). Азооспермия, олигоспермия (объем эякулята менее 1,5 мл), а также кислая реакция эякулята (рH < 7.0), сниженное количество фруктозы эякулята (маркер секрета семенных пузырьков) характерны для мужчин с муковисцидозом и синдромом врожденной двусторонней алазии семявыносящих протоков (CBAVD), но не пациентов с ПЦД/синдромом Картагенера или с обратным расположением внутренних органов. Спермиологическое исследование может быть использовано для дифференциальной диагностики различных заболеваний с поражением органов дыхательной системы, например, у мужчин с брохоэктазами [86, 87]. Нормативные значения показателей эякулята представлены в Приложении А3.6, классификация спермиологических «диагнозов» - в Приложении А3.7.
Рекомендовано рассмотреть возможность проведения ЭМИС в качестве дополнительного метода подтверждения диагноза ПЦД и при сомнительных результатах проведенного обследования (световая микроскопия, высокоскоростной видеомикроскопический анализ (Микроскопическое исследование спермы, Спермограмма)) с целью выявления ультраструктурных изменений аксонемы жгутиков [74, 75, 76, 84,85, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102].
(УУР – B, УДД – 4)
Комментарий:
Метод ЭМИС доступен только в некоторых крупных научно-исследовательских лабораториях / институтах.
Проведение электронной микроскопии сперматозоидов (электронной микроскопии эякулята) возможно только у взрослых мужчин и мальчиков подростков с 15 лет.
Поражение ресничек мерцательного эпителия и жгутиков сперматозоидов у пациентов с ПЦД могут не совпадать, т.е. иметь разную локализацию поражений, как одинаковую в разных клетках, так и различающуюся, например, только нарушение ультраструктуры и подвижности жгутиков сперматозоидов.
Следует учитывать гетерогенность морфологии сперматозоидов. В связи с этим существенное значение имеет электронно-микроскопическое исследование достаточного количества жгутиков в каждом конкретном образце. Для исследования необходимо не менее 50 жгутиков сперматозоидов.
При ультраструктурных исследованиях жгутиков важным моментом является гомогенность (однотипность) выявленных нарушений в конкретном изучаемом образце. Однотипные нарушения должны быть выявлены либо тотально во всех изученных ресничках или жгутиках, либо в подавляющем большинстве.
Европейская комиссия по ПЦД при сравнении точности высокоскоростной видеомикроскопии (HSVM) (патолого-анатомическое исследование биопсийного (операционного) материала тканей верхних дыхательных путей/патолого-анатомическое исследование биопсийного (операционного) материала тканей трахеи и бронхов)), иммунофлуоресценции (IF) (Иммуноцитохимическое исследование биологического материала) и исследования уровня оксида азота (NO) в выдыхаемом назальном воздухе (Определение уровня оксида азота в выдыхаемом воздухе) с эталонным тестом трансмиссионной электронной микроскопии (ТЭМ) и/или молекулярно-генетического исследования, дает убедительные рекомендации по использованию HSVM, IF и nNO в качестве дополнительных тестов к ТЭМ и/или молекулярно-генетических методов для диагностики ПЦД. Однако ни один дополнительный тест не подходит в качестве отдельного теста для диагностики ПЦД и ни один дополнительный или эталонный тест не подходит для исключения ПЦД.
Установление генетического диагноза поощряется из-за его влияния на ведение пациента. Комиссия подчеркивает, что тесты должны соответствовать минимальным стандартам, и предлагает обследовать пациентов в специализированных центрах, имеющих опыт диагностики ПЦД. При интерпретации результатов следует учитывать вероятность предварительного тестирования, основанную на симптомах. У лиц с клиническими особенностями ПЦД, у которых не обнаружено патогенных вариантов генов, для подтверждения диагноза ПЦД можно использовать ТЭМ [274].
2.4.2 Прочие инструментальные методы
Наряду со специальными диагностическими методами, позволяющими установить диагноз, используют рутинные методы инструментальной и лабораторной диагностики, применяющиеся в пульмонологической и оториноларингологической практике, имеющие важное значение как на этапе первичной диагностики, так и при длительном динамическом наблюдении.
2.4.2.1 Определение функции внешнего дыхания
Рекомендовано исследовать функцию внешнего дыхания при подозрении на ПЦД и у пациентов с ПЦД с целью определения и динамического контроля легочной функции при отсутствии возрастных или иных противопоказаний:
- спирометрию (исследование неспровоцированных дыхательных объемов и потоков) - в среднем каждые 3-6 месяцев (при необходимости – дополнительно исследование дыхательных объемов с применением лекарственных препаратов); - бодиплетизмографию - по показаниям, в среднем – ежегодно, с целью определения и динамического контроля статических легочных объемов и бронхиального сопротивления [56, 58, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113].
(УУР – C, УДД – 5)
Комментарий: спирометрия не относится к наиболее чувствительным тестам легочной функции при ПЦД, но она является самым доступным методом тестирования в клинической практике [103, 104, 105, 106, 107, 113]; в целом, качественное проведение спирометрии возможно у детей с 5-6 лет, если пациент может сознательно выполнить маневр форсированного выдоха; диагностическая ценность исследования у детей младше 5 лет ниже [108]. Спирометрия позволяет косвенно оценить легочные объемы [105]; по показаниям возможна более точная оценка статических легочных объемов и бронхиального сопротивления с помощью бодиплетизмографии [56, 58, 114, 115, 116, 117, 118, 119, 120, 121]. Наиболее часто у пациентов с ПЦД выявляют обструктивные или сочетание обструктивных и рестриктивных нарушений вентиляции (в зависимости от объема и характера поражения бронхиального дерева) [109, 110, 112]. Данные исследования проводятся в соответствии с Приказом Минздрава России 13 октября 2017 г. № 804н «Об утверждении номенклатуры медицинских услуг» : исследование неспровоцированных дыхательных объемов и потоков, исследование дыхательных объемов с применением лекарственных препаратов, бодиплетизмография.
Также для оценки легочных объемов и расчета индекса неоднородности вентиляции (LCI - Lung Clearance Index) предлагается использовать тест вымывания инертного газа при множественных выдохах (Multiple-Breath Inert Gas Washout; к примеру, вымывание азота кислородом) (исследование неспровоцированных дыхательных объемов и потоков); считается, что он с большей чувствительностью, нежели спирометрия, позволяет выявлять поражение мелких дыхательных путей, в том числе у детей дошкольного возраста [56, 58, 122, 123, 124, 125].
Рекомендовано проведение пульсоксиметрии и/или исследование газового состава крови (исследование уровня кислорода крови, исследование уровня углекислого газа в крови) всем пациентам с подозрением на ПЦД и всем пациентам с диагностированной ПЦД при каждой госпитализации; по показаниям (обострение хронического бронхолегочного процесса, наличие дыхательной недостаточности, требующей оксигенотерапии) – чаще [58, 126, 127].
(УУР – C, УДД – 5)
2.4.2.2 Лучевые методы
2.4.2.2.1 Методы визуализации легких
Рекомендуется селективное проведение рентгенографии органов грудной клетки (Рентгенография легких / Рентгенография легких цифровая) пациентам с подозрением на ПЦД и пациентам с ПЦД с целью определения характера и объема поражения легочной ткани [128].
(УУР – C, УДД – 5)
Комментарии: рентгенография легких / Рентгенография легких цифровая может выявить такие признаки, как деформация и усиление легочного рисунка, пневмофиброз, перибронхиальная инфильтрация, консолидация (ателектазы), буллы, выявить проявления бронхиальной обструкции: локальные участки вздутия легочной ткани, увеличение ретростернального пространства, уплощение диафрагмы, а также кифоз, утолщение бронхиальных стенок, слизистые пробки, в некоторых случаях - бронхоэктазы.
Частота определяется индивидуально, в среднем, ежегодно, по показаниям – чаще.
Данный метод может быть недостаточно информативен для точного описания характера изменений в легких, но имеет меньшую лучевую нагрузку. В связи с чем рентгенография может быть полезна для оценки состояния легких при изменении респираторных симптомов.
Рекомендуется проведение компьютерной томографии органов грудной полости (КТ органов грудной полости) / спиральной компьютерной томографии легких пациентам с подозрением на ПЦД и пациентам с ПЦД с целью определения характера и объема поражения легочной ткани [25, 129].
(УУР – C, УДД – 5)
Комментарий: в настоящее время компьютерная томография является основным методом диагностики изменений в легких при ПЦД
Компьютерная томография органов грудной полости/Спиральная компьютерная томография легких) - экспертная методика для детализации изменений. Проводится низкодозная компьютерная томография (НДКТ) – снижение силы тока до 1 мА/кг массы для детей и молодых взрослых весом < 50 кг в сочетании с напряжением на трубке 100 кВ. Выполняется на глубине вдоха, при невозможности задержки дыхания, в т.ч., при необходимости – в условиях седации (наркоз – по показаниям).
Частота проведения – в среднем 1 раз в 2 года, при обострении – внеочередное исследование. Функциональная компьютерная томография органов грудной полости (КТ органов грудной полости) / спиральная компьютерная томография легких «на выдохе» для оценки бронхиальной обструкции при невозможности выполнения исследования неспровоцированных дыхательных объемов и потоков (спирометрии) / бодиплетизмографии.
Примеры результатов лучевой диагностики – в Приложении А3.8.
2.4.2.2.2 Методы визуализации околоносовых пазух
Рекомендуется проведение компьютерной томографии придаточных пазух носа (конусно-лучевая или мультиспиральная) (Компьютерная томография придаточных пазух носа, гортани / Спиральная компьютерная томография придаточных пазух носа) при первичной оценке патологического процесса в околоносовых пазухах у пациентов с клиническими признаками ПЦД и при подготовке к каждому ринохирургическому вмешательству [130, 131].
(УУР – C, УДД – 4)
Комментарии: рентгенография ОНП представляется малоинформативной. КТ ОНП производится в аксиальной плоскости с реконструкцией изображения в коронарной и сагиттальной проекциях. Детям не следует выполнять КТ ОНП без клинических показаний (с целью динамического наблюдения), т.к. это в значительной мере увеличивает суммарную лучевую нагрузку (в связи с необходимостью периодического выполнения КТ органов грудной клетки). Взрослым КТ ОНП проводится 1 раз в 1-2 года или чаще по показаниям. Помимо КТ-картины хронического риносинусита с полипами или без полипов характерным является аплазия или гипоплазия лобных и клиновидных пазух.
Должны оцениваться: степень нарушения пневматизации околоносовых пазух, наличие полипов носа, послеоперационные костные изменения. Рентгенография ОНП не является информативным методом диагностики хронического риносинусита (ХРС) при ПЦД. Магнитнорезонансная томография (МРТ) околоносовых пазух также не может быть альтернативой КТ, т.к. не позволяет оценить состояние костных структур.
В соответствии с приказом Минздрава России 13 октября 2017 г. № 804н «Об утверждении номенклатуры медицинских услуг»: компьютерная томография придаточных пазух носа, гортани, спиральная компьютерная томография придаточных пазух носа.
2.4.3 Эндоскопическая оценка состояния околоносовых пазух
Рекомендовано пациентам с подозрением на ПЦД и пациентам с ПЦД проведение эндоскопии носоглотки (Эндоскопическая эндоназальная ревизия полости носа, носоглотки) с целью диагностики и динамического контроля воспалительного процесса в ОНП [25, 132, 133].
(УУР – C, УДД – 4)
Комментарий: при динамическом обследовании частота определяется индивидуально.
2.4.4 Оценка состояния органов репродуктивной системы и репродуктивной функции
Поскольку для первичной цилиарной дискинезии характерно нарушение фертильности, всем взрослым пациентам с ПЦД или с подозрением на ПЦД проводится репродуктологическое обследование: у пациентов мужского пола – урологическое/андрологическое обследование, у пациентов женского пола – гинекологическое обследование, при необходимости выполнение ультразвукового исследования половых органов (Ультразвуковое исследование органов малого таза (комплексное)), а также энодокринологического и других методов репродуктологического обследования.
Всем лицам мужского пола с ПЦД или с подозрением на ПЦД в возрасте старше 15 лет рекомендовано проведение стандартного спермиологического исследования спермограммы: светооптическое микроскопическое исследования (Микроскопическое исследование спермы / Спермограмма) с целью выявления нарушений подвижности жгутиков сперматозоидов, оценки возможности сохранения фертильности и тактики решения вопроса репродукции в случае нарушений фертильности [128, 134, 135].
(УУР – C, УДД – 4)
Комментарии: при отсутствии азооспермиии / криптозооспермиии спермиологическое исследование (спермограмму) также следует выполнять взрослым пациентам с установленным диагнозом ПЦД в процессе динамического наблюдения с частотой, в среднем, 1 раз в год.
Пациентам с астенозооспермией с астенотеатозооспермией с общей подвижностью сперматозоидов 0-10 % (показатель общей подвижности «PR» + «NP») прогрессивно подвижные – progressive motility «PR» и непрогрессивно подвижные – non-progressive motility, NP) и количеством неподвижных сперматозоидов – 90-100 % после повторной(ых) спермограммы менее) следует рассмотреть проведение исследования ультраструктуры жгутиков сперматозоидов методом ЭМИС (ТЭМ) (Электронная микроскопия эякулята) (см. подраздел 2.4.2.2), при возможности, молекулярно-генетического исследования на патогенные варианты в генах (см. подраздел 2.5.1), связанных с развитием ПЦД и медико-генетического обследования и консультирования и их супругов.
При выявлении патогенных вариантов в генах, ответственных за развитие ПЦД, супругам может быть рекомендовано молекулярно-генетическое обследование (на носительство мутаций в соответствующих генах) перед планированием деторождения, в том числе с помощью методов вспомогательных репродуктивных технологий (ВРТ) с целью рождения здорового потомства.
ВРТ-методы: экстракорпоральное оплодотворение методом ЭКО (экстракорпорального оплодотворения ооцитов)/ИКСИ (от англ. ICSI — IntraCytoplasmic Sperm Injection, букв. введение сперматозоида в цитоплазму, интрацитоплазматическая инъекция сперматозоида) - инъекция сперматозоида в цитоплазму ооцита (ИКСИ).
Медико-генетическое обследование при ПЦД должно включать проведение клинико-генетического обследования (прием и консультация врача-генетика), а также молекулярно-генетического исследования (анализ генов, ответственных за развитие ПЦД). Его необходимо выполнять до планирования беременности или проведения программ ЭКО / ИКСИ.
При необходимости - выполнять другие генетические тесты, репродуктологические исследования.
По результатам лабораторных генетических исследований – необходимо повторное консультирование у врача-генетика.
При выявлении мутаций у пациентов с ПЦД (кроме доминантныхх форм) следует рекомендовать обследование супруга(и), а также родственников на носительство мутаций, связанных с развитием ПЦД.
В случаях высокого генетического риска супружеским парам может быть рекомендовано преимплантационное генетическое тестирование на моногенные заболевания (ПГТ-М) методом высокопроизводительного секвенирования или методом полимеразной цепной реакции или соответствующая пренатальная ДНК-диагностика (Преимплантационная генетическая диагностика эмбриона) [128].
2.4.5 Оценка состояния сердечно-сосудистой системы
Рекомендовано проведение эхокардиографии и электрокардиографии (регистрация электрокардиограммы, расшифровка, описание и интерпретация электрокардиографических данных) пациентам с подозрением на ПЦД и пациентам с ПЦД с целью оценки состояния сердечно-сосудистой системы [25].
(УУР – C, УДД – 5)
Комментарий: средняя частота проведения ЭКГ и Эхо-КГ – 1 р./год (представлена в п.5.2).
2.4.6 Исследование слуха и состояния среднего уха
Рекомендуется прием (осмотр, консультация) врача-сурдолога-оториноларинголога первичный и повторные с проведением тональной аудиометрии (тональной пороговой аудиометрии) всем пациентам с ПЦД и отоскопическими признаками поражения полостей среднего уха, а также при субъективном снижении слуха и/или появлении ушн
2.5.1 Молекулярно-генетическое исследование
Рекомендовано проведение молекулярно-генетического исследования пациентам с подозрением на ПЦД с целью верификации диагноза и установления конкретной генетической формы [3, 128].
(УУР – C, УДД – 5)
Комментарий:
Генотипирование – диагностически значимым считают выявление биаллельной мутации (гомозиготной или компаунд-гетерозиготной).
К настоящему моменту наличие генетических вариантов (мутаций) генов, ответственных за развитие ПЦД, выявлено лишь у 50-75 % пациентов с ПЦД. На сегодняшний день отсутствуют исследования, указывающие на возможность использования генетического обследования для установления диагноза. Вместе с тем, при наличии технических возможностей, проведение генотипирования целесообразно всем пациентам с ПЦД.
Генетическое тестирование идентифицирует ген и его генетический вариант примерно в ~ 65 % случаев [3, 142].
Диагноз конкретной генетической формы первичной цилиарной дискинезии устанавливается у пробанда с вышеуказанными клиническими характеристиками и двуаллельными патогенными вариантами (или гетерозиготным патогенным вариантом в FOXJ1, или гемизиготным патогенным вариантом в PIH1D3 или OFD1 у мужчин), идентифицированными в одном из генов, перечисленных в Приложении А3.3.
Подходы к молекулярному тестированию могут включать:
o целевой анализ наиболее частых патогенных вариантов в конкретном гене (актуально в первую очередь для лиц определенной этнической принадлежности (Приложение А3.4);
o целевое тестирование определенного гена;
Однако в силу генетической гетерогенности предпочтительным является алгоритм:
1. Комплексное геномное тестирование (секвенирование экзома, реже - секвенирование генома).
2. Анализ протяженных изменений в генах (делеций / дупликаций), поскольку простое секвенирование не идентифицирует такой тип изменений.
Мультигенная панель, созданная для определённых популяций, с наибольшей вероятностью идентифицирует генетическую причину заболевания. Однако требуется создание мультигенной панели для РФ, в настоящее время она не может применяется в виду отсутствия знаний о характерных для РФ генах и их вариантах.
Резюме консенсуса Рабочей группы по опубликованным данным о генетическом тестировании в диагностике первичной цилиарной дискинезии (ПЦД) адаптировано из [3].
1. Генетическое тестирование для подтверждения диагноза может быть выполнено у лиц с ПЦД, диагностированных другими способами (например, ВСВМ и ТЭМ.), или у лиц с явными клиническими признаками на ПЦД (типичные клинические данные, низкий nNO) и при отсутствии других исследований, таких как как ВСВМ и ТЭМ. Отрицательный генетический тест не исключает ПЦД. |
|---|
2. Генетическое тестирование также может быть выполнено для верификации диагноза и установления конкретной генетической формы у пациентов с явными клиническими признаками ПЦД и у которых ВСВМ и ТЭМ не подтвердили диагноз, как это может быть в случае пациентов с мутациями генов DNAH11, CCNO, MCIDAS или RSPH. |
3. Генетическое тестирование и интерпретация результатов должны соответствовать национальным и международным рекомендациям [3, 25]. |
4. Анализ сегрегации аллелей в семье (особенно у обоих родителей) важен для подтверждения генотипа у пробандов (для различения гомозиготности и гемизиготности, а также сложной гетерозиготности и сложного аллеля). |
5. Генетическое тестирование пациентов и их родственников может быть необходимо для генетического консультирования и планирования деторождения. |
6. В будущем генетическое тестирование может быть важным для лечения пациентов с учетом генотипа. |
Примечание: ВСВМ -анализ с помощью высокоскоростной видеомикроскопии; ТЭМ-трансмиссионная электронная микроскопия; nNO- назальный оксид азота.
2.5.2 Консультации специалистов
Рекомендуется при диагностике и ведении пациентов с ПЦД использовать мультидисциплинарный подход в виду того, что заболевание характеризуется поражением многих органов и систем, требует комплексной терапии, что диктует необходимость совместного ведения пациента специалистами разных профилей (услуги указаны в комментарии) [68,128].
(УУР – С, УДД – 5)
Комментарии: диагностику и ведение / наблюдение пациентов с ПЦД осуществляет врач-пульмонолог (и / или, в детской практике, врач-педиатр, во взрослой – врач-терапевт), иногда – врач-инфекционист, а также врач-генетик, врач-оториноларинголог, (прием (осмотр, консультация) врача-пульмонолога, врача-педиатра, врача-терапевта, врача-инфекциониста, врача-генетика, врача-оториноларинголога первичный и повторные)) (динамическое наблюдение за течением хронического экссудативного среднего отита и хронического риносинусита, внеплановая консультация при остром среднем отите, возникновении отореи, гнойном обострении хронического риносинусита), врач-сурдолог-оториноларинголог (прием (осмотр, консультация) врача-сурдолога-оториноларинголога) – при необходимости контроля слуховой функции у пациентов с хроническим экссудативным средним отитом и получающих препараты, обладающие ототоксичностью, врач по лечебной физкультуре (или врач по медицинской реабилитации, или врач-физиотерапевт (прием (осмотр, консультация) врача по лечебной физкультуре, врача по медицинской реабилитации, врача-физиотерапевта первичный и повторные) или специалист с высшим (немедицинским) образованием (инструктор-методист по лечебной физкультуре; или специалист со средним профессиональным (медицинским) образованием (инструктор по лечебной физкультуре, медицинская сестра по массажу, медицинская сестра по физиотерапии) - для обучения ингаляционной терапии, кинезитерапии, дыхательными тренажерами, прием (осмотр, консультация) врача-кардиолога (врача-детского кардиолога) первичный и повторные при наличии синдрома Картагенера и/или легочной гипертензии (легочного сердца), прием (осмотр, консультация) врача-клинического фармаколога первичный и повторные для решения сложных вопросов по терапии и предотвращению / лечению нежелательных явлений лекарственной терапии, прием (осмотр, консультация) врача-фтизиатра первичный и повторные при диагностике и терапии легочного микобактериоза, прием (осмотр, консультация) врача-хирурга / врача-детского хирурга / врача-торакального хирурга первичный и повторные, в т. ч., со специализацией по трансплантологии, и др. по клинической необходимости. Пациентам мужского пола в возрасте с 15 лет – прием (осмотр, консультация) врача-уролога / врача-детского уролога-андролога первичные и повторные для оценки состояния репродуктивной системы и определения тактики дальнейшего наблюдения. Пациенткам женского пола показаны приемы (осмотры, консультации) врача-акушера-гинеколога первичные и повторные в декретированные сроки и при планировании и ведении беременности. Консультирование врачами-специалистами в процессе динамического наблюдения осуществляется по мере необходимости.
Подход к терапии пациента с ПЦД должен быть мультидисциплинарным в связи с полиорганностью поражений. Специфических методов лечения ПЦД в настоящее время не существует. Следует соблюдать общие принципы очистки дыхательных путей и антибиотикотерапии, используемые при муковисцидозе (МВ) или бронхоэктазах без МВ [25].
Основными целями терапии являются
o максимально возможное предупреждение прогрессирования и/или развития бронхоэктазов;
o восстановление / сохранение нормальной легочной функции;
o восстановление / сохранение носового дыхания и слуха;
o обеспечение максимально высокого качества жизни пациента;
o предупреждение и лечение обострения хронического инфекционно-воспалительного процесса в бронхолёгочной системе, верхних дыхательных путях и среднем ухе;
o предупреждение и лечение обострения инфекционно-воспалительного процесса в околоносовых пазухах (ОНП) для уменьшения степени нисходящей контаминации бронхолегочной системы;
o терапия хронического среднего отита;
o обеспечение профилактики осложнений;
o лечение осложнений.
Обострение хроничеcкого бронхолегочного процесса при ПЦД диагностируется при наличии 3 и более признаков [143]:
- усиление кашля;
- изменение объема и/или цвета мокроты;
- усиление одышки (по ощущениям пациента или законных представителей);
- решение начать / изменить лечение противомикробными препаратами из-за предполагаемых легочных симптомов;
- недомогание, слабость, ощущение усталости или вялость;
- появление или усиление кровохарканья;
- повышение температуры > 38°C;
Основные составляющие лечения:
o Дренирование бронхиального дерева и кинезитерапия;
o Противомикробная терапия;
o Муколитическая терапия;
o Противовоспалительная терапия;
o Мероприятия, направленные на предупреждение и лечение обострения инфекционно-воспалительного процесса в околоносовых пазухах (ОНП) для уменьшения степени нисходящей контаминации бронхолегочной системы;
o Терапия хронического среднего отита;
o Терапия осложнений;
o Индивидуальная коррекция рациона на основе оценки нутритивного статуса.
3.1 Консервативное лечение
3.1.1 Муколитическая терапия
Рекомендовано всем пациентам с ПЦД (за исключением имеющих медицинские противопоказания) проведение активной муколитической терапии с целью уменьшения вязкости мокроты и облегчения ее эвакуации [144, 254].
(УУР – C, УДД – 5)
Комментарии: выбор лекарственных средств определяется индивидуально.
Выбор пути введения: предпочтение отдается ингаляционному введению.
Оценка эффективности лечения: клинически (оценка суточного количества мокроты, изменений ее консистенции, оценка степени дыхательной недостаточности).
Оценка безопасности лечения: клинически (специальных стандартизованных методик оценки безопасности этих лекарственных средств не существует).
Дополнительные замечания: все способы разжижения мокроты необходимо комбинировать с удалением ее из дыхательных путей, используя методы кинезитерапии. Перед сеансом кинезитерапии желательно, а при наличии бронхообструкции – обязательно, перед муколитическим препаратом - провести ингаляцию препаратом c бронхолитическим эффектом из групп: селективные бета2-адреномиметики или адренергические средства в комбинации с антихолинергическими средствами или антихолинергические средства либо другой препарат для лечения обструктивных заболеваний дыхательных путей.
В клинической практике для муколитической терапии используются:
3 % или 6 % или 7 % гипертонический раствор натрия хлорида** с 0,01 % и 0,1 % натрием гиалуронатом [145] (зарегистрирован как медицинское изделие - раствор для ингаляционной терапии с органическими веществами) применяется ингаляционно через небулайзер по 5 мл 2 раза в день, улучшает клиренс дыхательных путей и является базисной муколитической терапией с быстрым муколитическим эффектом. Может применяться 3 % гипертонический раствор натрия хлорида**, особенно у детей младшего возраста, у пациентов старшего поколения и для назального душа [144].
Рекомендовано рассмотреть для отдельных пациентов с ПЦД с частыми рецидивами или длительными респираторными обострениями ингаляторное применение #дорназы альфа** с муколитической целью [25, 109, 128, 133, 140, 146].
(УУР – C, УДД – 5)
Комментарий: имеются отдельные работы, в которых показана эффективность ингаляторного применения #дорназы альфа** [147]. Дозировки аналогичны назначаемым пациентам с кистозным фиброзом (муковисцидозом). Длительность терапии определяется индивидуально.
Ацетилцистеин** не рекомендован пациентам с ПЦД для применения с муколитической целью в связи с отсутствием доказательств эффективности. Рекомендован только при использовании аминогликозидов для профилактики снижения слуха [109, 133, 140].
(УУР – C, УДД – 5)
3.1.2 Бронхолитическая терапия
Рекомендовано назначение ингаляционной бронхолитической терапии пациентам с ПЦД при наличии обратимой или частично обратимой бронхиальной обструкции с целью улучшения эвакуации мокроты, перед применением ингаляцией противомикробных препаратов системного действия, гипертонического раствора натрия хлорида**, перед кинезитерапией [140, 148].
(УУР – C, УДД – 5)
Комментарий: противопоказанием является индивидуальная непереносимость.
Пациентам с ПЦД в качестве бронхолитической терапии назначают препарат c бронхолитическим эффектом из групп: селективные бета2-адреномиметики или адренергические средства в комбинации с антихолинергическими средствами или антихолинергические средства либо другой препарат для лечения обструктивных заболеваний дыхательных путей по индивидуальным показаниям в режиме «по требованию».
Используется селективный бета2-адреномиметик сальбутамол** в монотерапии или в сочетании с антихолинергическими средствами (R03BB) (R03BB) (ипратропия бромид**) или фиксированная комбинация фенотерол + ипратропия бромид** или препараты пролонгированного действия (тиотропия бромид** (противопоказан детям до 18 лет по показанию хронический бронхит)) либо другой препарат для лечения обструктивных заболеваний дыхательных путей по индивидуальным показаниям.
Использование дозированных аэрозольных ингаляторов обязательно со спейсером, при назначении ингаляционных бронхолитиков (препаратов для лечения обструктивных заболеваний дыхательных путей) (селективный бета2-адреномиметик сальбутамол** в монотерапии или в сочетании с антихолинергическими средствами (R03BB) (ипратропия бромид**) или фиксированная комбинация фенотерол + ипратропия бромид** или препараты пролонгированного действия (тиотропия бромид** (противопоказан детям до 18 лет по показанию хронический бронхит)) либо другого препарата для лечения обструктивных заболеваний дыхательных путей по индивидуальным показаниям) пациентам с тяжелой бронхообструкцией (ОФВ1 < 30 % от должного) ингаляции должны проводиться при помощи небулайзера.
Выбор пути введения препарата для лечения обструктивных заболеваний дыхательных путей: предпочтение отдается ингаляционному пути введения.
Оценка эффективности лечения: клинически (симптомы бронхообструкции) и по данным спирометрии.
Оценка безопасности лечения: клинически и по результатам объективного осмотра (частота сердечных сокращений, сердечный ритм).
применение лекарственного препарата в соответствии с показателями (характеристиками), не указанными в инструкции по его применению (off-label), осуществляется по решению врачебной комиссии при условии подписанного информированного добровольного согласия (согласно ФЗ № 323-ФЗ от 21.11.2011 г. с изменениями).
Пациентов с ПЦД в сочетании с ХОБЛ или астмой рекомендовано лечить согласно соответствующим рекомендациям. Документирование обратимой обструкции воздушного потока должно выполняться с использованием соответствующих возрасту методик [109, 140].
(УУР – C, УДД – 5)
3.1.3 Консервативное лечение риносинусита и отита
Рекомендуется проведение терапии хронического риносинусита назальных полипов согласно соответствующим клиническим рекомендациям с целью достижения оптимального результата лечения [128].
(УУР – C, УДД – 5)
Комментарии: в том числе, могут быть назначены промывания носовых ходов солевыми растворами, противомикробная терапия при обострениях, кортикостероиды (R01AD) (для интраназального применения) при назальном полипозе). Алгоритм первичной оценки и лечения риносинусита у пациентов с ПЦД – в Приложении Б.
Рекомендуется пациентам с ПЦД промывание полости носа #гипертоническим (3 %, 6 %) и изотоническим (0,9 %) раствором натрия хлорида**, применение назального душа с целью очистки носовых ходов [25, 140].
(УУР – C, УДД – 5)
Комментарий: ирригационная терапия оказывает положительное влияние при назальных симптомах (заложенность носа, постоянное выделение слизи).
Рекомендуется лечение экссудативного среднего отита у пациентов с ПЦД в соответствии с клиническими рекомендациями «Острый средний отит» [128].
(УУР – C, УДД – 5)
Комментарии: применяется консервативное лечение, в т.ч., антимикробная терапия по показаниям.
3.1.4 Антимикробная терапия
3.1.4.1 Общие вопросы антимикробной терапии у пациентов с ПЦД
Согласно консенсусу экспертов, данные, полученные при микробиологических и клинических исследованиях с участием пациентов с кистозным фиброзом (муковисцидозом) можно экстраполировать на пациентов с ПЦД [28].
При обострении хронического бронхолегочного процесса всем пациентам ПЦД рекомендована системная антимикробная терапия (АМТ), с целью сокращения продолжительности симптомов и повышения эффективности лечения [25, 28, 140].
(УУР – C, УДД – 5)
Комментарии: антимикробная терапия проводится пациентам с ПЦД с обострением хронического бронхолегочного процесса (включая обострения на фоне острой респираторной инфекции). Также антимикробная терапия проводится в случаях, если выявляются новые высокопатогенные возбудители респираторной инфекции при плановом микробиологическом исследовании (см. табл. 3,4,5) [128, 148, 149, 150].
o Противопоказания: определяются индивидуально и зависят от индивидуальной непереносимости (в том числе аллергии), характера сопутствующих заболеваний (главным образом заболевания печени и почек) и возраста пациента.
o Выбор лекарственных средств определяется: видом возбудителя, выявленного у пациента; чувствительностью возбудителя (in vitro) к данному ПМП; фазой заболевания (обострения – ремиссия); продолжительностью инфекционного процесса (хроническая инфекция – впервые выявленный возбудитель); эффективностью терапии предшествующего обострения легочной инфекции.
o Комбинированнная АМТ. При назначении АМТ и необходимости применения нескольких препаратов - следует использовать комбинации ЛС с различным механизмом действия (например, бета-лактамные антибактериальные препараты, пенициллины / Другие бета-лактамные антибактериальные препараты в комбинации с аминогликозидами). При выделении в мокроте пациента одновременно двух микроорганизмов выбор АМТ зависит от свойств более резистентного возбудителя.
o Выбор пути введения определяется: видом возбудителя, выявленного у пациента; фазой заболевания (обострение – ремиссия); продолжительностью инфекционного процесса (хроническая инфекция – впервые выявленный возбудитель); местом оказания медицинской помощи (амбулаторная – стационарная); эффективностью предшествующей антибактериальной терапии. Одновременно назначать препараты для ингаляционного и внутривенного путей введения одной фармакологической группы не следует. Возможно назначение ингаляционной и внутривенной АМТ одновременно по решению консилиума специалистов и с учетом фармакологической группы препаратов.
o При частых обострениях инфекционно-воспалительного процесса в бронхолёгочной системе следует увеличивать продолжительность курсов антибактериальной терапии до 3 недель и более, использовать внутривенный способ введения и / или сокращать интервалы между курсами и/или рассмотреть, в зависимости от возбудителя, в индивидуальном порядке между курсами в/в терапии применение ципрофлоксацина** в таблетках. Ципрофлоксацин** может применяться также при каждой острой респираторной инфекции и обострении бронхолегочного процесса легкой степени) [25, 151, 152]. У детей с ПЦД назначать #ципрофлоксацин** по решению врачебной комиссии в случае отсутствия альтернативного ПМП (дозы – см. табл. 4).
o Оценка эффективности АМТ: клинически (лихорадка, респираторные симптомы), по данным лабораторных методов обследования (лейкоцитоз, уровень С-реактивного белка, по показаниям - прокальцитонина (исследование уровня прокальцитонина в крови)) и по данным микробиологического исследования (эрадикация возбудителя, персистирование, суперинфекция, снижение выделения возбудителя < 104 колониеобразующих единиц или отрицательный результат посева и т.д.).
o Оценка безопасности лечения: зависит от применяемого лекарственного средства (ЛС) и проводится с учетом возможных нежелательных явлений.
Дополнительные замечания:
1. Применение ПМП внутрь используется для терапии обострений ПЦД в домашних условиях или для профилактического лечения пациентов, хронически инфицированных P. aeruginosa, В.cepacia, MRSA, НТМБ.
2. Внутривенное введение ПМП
Применение ПМП внутривенно показано:
- при тяжелых обострениях (лечение в условиях медицинской организации) (одним, а при необходимости - двумя препаратами в соответствии с результатами микробиологического исследовании);
- в тех случаях, когда применение ПМП внутрь и ингаляционно оказалось неэффективным;
- для плановой терапии пациентов, инфицированных P. aeruginosa, MRSA, нетуберкулезных микобактерий (см табл. 3 и Приложение А3.9).
- при ухудшении течения заболевания и появлении новых симптомов у пациентов, получающих ПМП внутрь.
Внутривенное введение ПМП начинается в стационаре с курсом лечения до 14 и более дней. Введение осуществляется через периферический венозный катетер (катетер периферический) или через порт-систему (порт инфузионный / инъекционный, имплантируемый***), которые устанавливаются согласно методическим руководствам «Венозный доступ, 2019 (https://msestra.ru/download/file.php?id=4763) с использованием необходимых лекарственных средств. Порт-системы устанавливаются согласно Распоряжению Правительства Российской Федерации от 31.12.2018 г. № 3053-р «Об утверждении перечня медицинских изделий, имплантируемых в организм человека при оказании медицинской помощи в рамках программы государственных гарантий бесплатного оказания гражданам медицинской помощи, а также перечня медицинских изделий, отпускаемых по рецептам на медицинские изделия при предоставлении набора социальных услуг». Лечение может проводиться в стационаре и в амбулаторных условиях.
Организация внутривенной терапии в амбулаторных условиях способствует повышению комплаентности, профилактике обострений. Пребывание в больнице отягощается риском перекрестного и суперинфицирования резистентными к антибиотикам штаммами микроорганизмов, стрессом, пропуском школьных занятий. Кроме того, пребывание пациента в стационаре значительно дороже, чем амбулаторное лечение. Катетеризация вен давно стала рутинной медицинской процедурой в мире для обеспечения различных видов внутривенной терапии. Проведение внутривенной терапии через периферический венозный катетер (катетер периферический) или порт-систему (порт инфузионный/инъекционный, имплантируемый***) является практически безопасным, если соблюдаются основные условия: метод должен стать постоянным и привычным в практике, должен быть обеспечен безупречный уход за катетером. Катетер устанавливается в условиях дневного стационара или выездной бригадой на дому.
3. Применение ПМП в виде ингаляций через небулайзер:
- может проводиться как в стационаре, так и в домашних условиях;
- для решения вопроса о назначении ингаляционной терапии следует провести спирометрию до первой ингаляции ПМП и через несколько минут после ингаляции (для выявления возможного бронхоспазма (при отсутствии возрастных и/или иных противопоказаний)) (см. раздел «Бронхолитическая терапия») - перед ингаляцией ПМП необходимо провести ингаляцию препарата для лечения обструктивных заболеваний дыхательных путей (группа АТХ R03) (бронхолитика): ). cелективные бета2-адреномиметики, например, сальбутамол** 2,5 мг через небулайзер (или дозированный аэрозольный ингалятор по 200 – 400 мкг с использованием спейсера) за 15-30 минут до ингаляции антибиотика в монотерапии или в сочетании с антихолинергическими средствами (R03BB) (ипратропия бромид**) или фиксированная комбинация фенотерол + ипратропия бромид** или препараты пролонгированного действия (тиотропия бромид**) (по Инструкции – противопоказан пациентам до 18 лет, за исключением бронхиальной астмы)) или другие препараты для лечения обструктивных заболеваний дыхательных путей, муколитических препаратов, а также дренаж;
- при ингаляции ПМП в домашних условиях желательно использовать небулайзер, оснащенный фильтром для выдыхаемого воздуха;
- при ингаляции ПМП предпочтительнее применять мундштук, по сравнению с маской. Следует рекомендовать пациентам переходить на применение мундштука в максимально ранние сроки, как правило, с 3-х летнего возраста [153]. Вдыхание препарата лучше осуществлять через рот, применение носовых зажимов во время ингаляции увеличивает эффективность лечения;
- при проведении ингаляций в условиях медицинской организации и амбулаторно пациенты с ПЦД, должны пользоваться индивидуальным небулайзером с возможностью замены каждые 3 месяца комплекта распылителя и трубки воздуховода и фильтра;
- ингаляционная система с низкопоточным компрессором (уровень потока сжатого воздуха до 6 л/мин.), с производительностью 0,15 мл-0,25 мл/мин., снабженная системой контроля инспираторного потока и системой клапанов вдоха и выдоха, позволяющей сократить потери медикамента в окружающую среду, обеспечивающий максимальную эффективность терапии, приспособленный к химической и термической дезинфекции и к автоклавированию;
- для введения медикамента в ОНП применяется ингаляционная система с функцией пульсирующей подачи аэрозоля;
- в качестве мобильного устройства возможно использование мэш-небулайзера - ингаляционного прибора, состоящего из блока управления и аэрозольного модуля, включающего в себя резервуар для медикамента, аэрозольную головку, спейсер\накопитель, оснащенный системой клапанов вдоха и выдоха и мундштуком. Скорость распыления в диапазоне 0,3-0,7 мл/мин., а нераспыляемым (остаточным) объемом не более 0,5 мл. Все части аэрозольного модуля должны подлежать термической дезинфекции. Для пациента с ПЦД важно производить замену компонентов мэш-небулайзера каждые 3 месяца.
4. Профилактические курсы АМТ
- У пациентов с частыми обострениями и снижением функции легких следует рассмотреть возможность проведения регулярной 1 раз в квартал внутривенной терапии. Однако контролируемых испытаний этого подхода при ПЦД не проводилось.
- Профилактические пероральные противомикробные препараты системного действия не следует назначать всем пациентам с ПЦД, но их необходимо рассмотреть, если требуются частые повторные курсы пероральных ПМП при обострении заболевания и при хронической колонизации нижних дыхательных путей P. аeruginosa, для увеличения продолжительности жизни пациентов [25, 26, 28, 154, 155, 156].
- Следует помнить, что проведение профилактических курсов антимикробной терапии практически не сказывается на устойчивости штаммов микроорганизмов только при своевременной смене применяемых препаратов.
Системная АБТ рекомендована пациентам с ПЦД при обострении хронического синусита в случае отсутствия эффекта от местного лечения (ирригационная терапия, кортикостероиды (R01AD) и др.) с терапевтической целью. Выбор АБ и принципы АБТ соответствуют таковым при лечении синусита в общей популяции [148].
(УУР – C, УДД – 5)
Комментарии: при необходимости применения небулайзера для введения медикамента в ОНП применяется небулайзер с универсальной ингаляционной системой функции пульсирующей подачи аэрозоля;
До начала АМТ у всех пациентов необходимо получить респираторный образец (для детей 6 лет и старше и взрослых – мокроту или БАЛ) для микробиологического (культурального) исследования с целью дальнейшей коррекции АМТ с учетом выделенного возбудителя и его чувствительности к ПМП [25, 28, 141].
(УУР – C, УДД – 5)
Рекомендовано при отсутствии результатов микробиологического исследования пациентам с ПЦД стартовую АМТ назначать эмпирически, но при выборе АБ целесообрано учитывать анамнез (практику лечения предыдущих обострений) и результаты предшествующего микробиологического (культурального) исследования респираторного образца с целью повышения эффективности лечения [25, 26, 141].
(УУР – C, УДД – 5)
Комментарий: наиболее частыми возбудителями обострения ПЦД являются нетипируемая H. influenzae, S. pneumoniae, S. aureus (в том числе MRSA), P. aeruginosa. У детей раннего возраста в структуре возбудителей преобладают H. influenzae, S. pneumoniae, S. aureus. Среди взрослых и подростков, напротив, чаще выявляются P. aeruginosa и другие НФГОБ, например, B. cepacia complex, S. maltophilia, Аchromobacter spp.[157]. В настоящее время данные о роли S. maltophilia противоречивы [28].
Для грамотрицательной микрофлоры (в т.ч., P. aeruginosa), MRSA, нетуберкулезных микобактерий или при их хроническом высеве значение имеет любое количество колоний, определенное по результатам микробиологического исследования.
Для эмпирической АМТ обострения хронического бронхолегочного процесса при ПЦД в случае отсутствия недавних результатов микробиологического (культурального) исследования респираторного образца в большинстве случаев следует использовать пенициллины широкого спектра действия (аминопенициллины)), в том числе комбинации пенициллинов, включая комбинации с ингибиторами бета-лактамаз (ингибиторозащищеные), цефалоспорины второго поколения,цефалоспорины третьего поколения, цефалоспорины четвертого поколения, доксициклин** (взрослые и дети > 8 лет), левофлоксацин** (взрослые)), при необходимости, по жизненным показаниям - #левофлоксацин** - детям [158,159] – табл. 2 и 3.
Стартовый режим АМТ должен быть скорректирован при наличии результатов недавнего микробиологического исследования респираторного образца: например, в случае выявления S.aureus или P.aeruginosa назначаются препараты, активные в отношении данных возбудителей – табл. 3,4.
Препараты в соответствии с чувствительностью выделенной микрофлоры назначают в максимально допустимых (для данного возраста) дозах и используют парентерально или внутрь (в зависимости от состояния пациента), также используется ступенчатый метод введения. При высеве P. aeruginosa терапия проводится аналогично протоколам лечения больных муковисцидозом.
Следует использовать модифицированные критерии Лидса при установлении диагноза хронической инфекции легких, вызванной Pseudomonas aeruginosa [26].
Согласно консенсусу «BEAT-PCD» (Better Experimental Approaches to Treat PCD) [28]:
○ при наличии высева P. aeruginosa назначают антибактериальную терапию независимо от симптомов и результатов микроскопии;
○ антимикробную терапию при высеве H. influenzae, M. catarrhalis, S. pneumoniae, S. aureus (MSSA) назначают, если у пациента есть симптомы, свидетельствующие об обострении хронической инфекции;
○ при высеве метициллинрезистентного золотистого стафилококка (MRSA) и/или B. cepacia complex антимикробная терапия назначается независимо от симптомов и результатов микроскопии;
○ необходимо отделять пациентов с инфекцией, вызванной P. aeruginosa в амбулаторных и стационарных условиях;
○ диагноз хронической инфекции легких, вызванной НТМ, необходимо устанавливать на основании
1) легочных симптомов;
2) узловых или полостных процессов на рентгенограмме грудной клетки и/или бронхоэктазов;
3) положительных результатов посева, по крайней мере, из двух отдельных проб секрета из дыхательных путей или положительного посева образцов по крайней мере одной промывки или лаважа бронхов или на основании результата патолого-анатомического (гистологического) исследования – обнаружение микобактерий в материале трансбронхиальной биопсии или биопсии легкого вместе с положительным высевом НТМ;
При нетяжелом обострении у пациентов с ПЦД (не требуется госпитализация) рекомендуется назначать ПМП (пероральные); при тяжелом обострении, неэффективности стартовой пероральной АМТ, наличии сопутствующих заболеваний/состояний, нарушающих всасывание в ЖКТ, лечение следует начинать с ПМП (в/в лекарственных форм); в дальнейшем возможен переход на пероральный прием того же ПМП или близкого по спектру активности и механизму действия препарата до завершения полного курса АМТ [25, 141, 160].
(УУР – А, УДД – 1)
Комментарий: комбинированная АБТ, использование разных путей доставки препаратов (например, в/в и ингаляционный) не имеют доказанных преимуществ перед монотерапией; назначение комбинаций АБ (например, в случае выявления поли-и экстремально резистентных грам (-) возбудителей) должно определяться консилиумом специалистов и учитывать потенциальный синергизм в отношении выделенного возбудителя, фармакокинетические взаимодействия препаратов.
Высокие дозы ПМП (пероральных) следует назначать при первых признаках ухудшения респираторных симптомов или ухудшения функции легких. Если отсутствует улучшение со стороны респираторных симптомов на пероральные ПМП, следует назначить внутривенную терапию [109, 133, 141].
Рекомендованная длительность АМТ при обострении у пациентов с ПЦД в случае выявления P. aeruginosa – в среднем 14 дней, в остальных случаях продолжительность приема АБ может быть сокращена до 10 дней (нетяжелое обострение, быстрый клинический эффект при назначении АБ). При тяжелом обострении, осложнениях, неэффективности стартовой АМТ и др. может быть увеличена до 21 дня с целью эффективной эрадикации причиннозначимого возбудителя [25, 141, 148].
(УУР – C, УДД – 5)
Таблица 3. Рекомендации по АБТ обострений хронической инфекции при ПЦД [25, 149, 151,161]
Возбудитель |
Нетяжелое обострение (предпочтительно амбулаторное лечение) |
Тяжелое обострение (лечение в стационаре) |
|
|---|---|---|---|
|
Начальная эмпирическая терапия1
|
Амоксициллин**, Амоксициллин + Клавулановая кислота** Цефуроксим** Доксициклин**2 Левофлоксацин**3 |
Ампициллин**, Амоксициллин + Клавулановая кислота** Ампициллин + [Сульбактам]** Цефотаксим** Цефтриаксон** Цефтаролина фосамил** Цефепим** Левофлоксацин**3 |
|
Этиотропная терапия | |||
|
H. influenzae Ампициллин-Ч
Ампициллин-Р
|
Амоксициллин**
Амоксициллин + Клавулановая кислота** Доксициклин** 2 Цефиксим** Ципрофлоксацин**3 Левофлоксацин**3 |
Ампициллин**
Амоксициллин + Клавулановая кислота** Ампициллин + [Сульбактам]** Цефотаксим** Цефтриаксон** Цефтаролина фосамил** Ципрофлоксацин**3 Левофлоксацин**3 |
|
|
S. pneumoniae Пенициллин-Ч
Пенициллин-Р
|
Амоксициллин** Азитромицин**4 Кларитромицин**4
Амоксициллин** (высокая доза) Линезолид** Левофлоксацин**3 Моксифлоксацин**3 |
Ампициллин**
Цефтаролина фосамил** Цефотаксим** Цефтриаксон** Линезолид** Левофлоксацин**3 Моксифлоксацин**3 |
|
M. catarrhalis |
Амоксициллин + Клавулановая кислота** Цефиксим** Азитромицин** Кларитромицин** Ципрофлоксацин**3 Левофлоксацин**3 Моксифлоксацин**3 |
Амоксициллин + Клавулановая кислота** Ампициллин + [Сульбактам]** Цефотаксим** Цефтриаксон** Ципрофлоксацин**3 Левофлоксацин**3 Моксифлоксацин**3 |
|
|
S. aureus MSSA
МRSA¶ |
Амоксициллин + Клавулановая кислота** Клиндамицин** #Цефалексин** [255, 256] Левофлоксацин**3 Моксифлоксацин**3 Цефуроксим**
Линезолид** Ко-тримоксазол [Сульфаметоксазол + Триметоприм]** |
Оксациллин** Цефазолин** Линезолид**
Линезолид** Цефтаролина фосамил** Ванкомицин** #Телаванцин**(противопоказан детям до 18 лет) [276, 277] |
|
P. aeruginosa |
Ципрофлоксацин**3 #Тобрамицин** (ингаляционно) Колистиметат натрия (ингаляционно)
|
Цефтазидим** Цефепим** Пиперациллин+[Тазобактам] Меропенем** Имипенем** Дорипенем**(противопоказан детям до 18 лет) Биапенем** (противопоказан детям до 18 лет) Цефтазидим + [Авибактам]** Цефталозан + [Тазобактам]** +/- Амикацин**5 #Тобрамицин**5 [178] Фосфомицин** Азтреонам Полимиксин В** Колистиметат натрия |
|
|
Enterobacterales БЛРС (-)
БЛРС (+) Карбапенемаза (-)
Карбапенемаза (+) |
Цефиксим** Ципрофлоксацин**3 Левофлоксацин**3 Моксифлоксацин**3
Эртапенем**
Цефтазидим + [Авибактам]** +/- Азтреонам Тигециклин**(высокая доза)
|
Цефотаксим** Цефтриаксон** Цефепим** Ципрофлоксацин**3 Левофлоксацин**3 Моксифлоксацин**3
Меропенем** Имипенем** Дорипенем (противопоказан детям до 18 лет) Цефтазидим + [Авибактам]** Пиперациллин + [Тазобактам]6 Цефепим + [Сульбактам]**6
Цефтазидим + [Авибактам]** +/- Азтреонам Тигециклин** (высокая доза) Полимиксин В** +/- фосфомицин** Колистиметат натрия +/- фосфомицин** |
|
S. maltophilia |
Ко-тримоксазол** Тигециклин** Миноциклин (противопоказан детям до 8 лет) Левофлоксацин** |
Комбинация 2-х из нижеперечисленных препаратов: Ко-тримоксазол [Сульфаметоксазол + Триметоприм]** Тигециклин** Левофлоксацин** Цефтазидим + [Авибактам]** |
|
Achromobacter spp.7 |
Ко-тримоксазол [Сульфаметоксазол + Триметоприм]** Колистиметат натрия (ингаляционно) Цефтазидим** |
Комбинация 2-х или 3-х из нижеперечисленных препаратов (не назначать > 1 препарата групп «Бета-лактамные антибактериальные препараты, пенициллины» / «Другие бета-лактамные антибактериальные препараты» ): Пиперациллин + [Тазобактам] Меропенем** Ко-тримоксазол [Сульфаметоксазол + Триметоприм]** Цефтазидим** Цефепим** Тигециклин** Полимиксин В** Колистиметат натрия Левофлоксацин** |
|
B. cepacia complex |
Ко-тримоксазол** Доксициклин** Миноциклин (противопоказан детям до 8 лет) Цефтазидим** Меропенем** Дорипенем (противопоказан детям до 18 лет) Цефтазидим + [Авибактам]** |
Ко-тримоксазол** Цефтазидим** Меропенем** Дорипенем (противопоказан детям до 18 лет) Цефтазидим + [Авибактам]** |
|
Примечание:
1 Помимо клинической тяжести выбор стартовой АМТ определяется результатами культурального исследования респираторных образцов (мокрота, БАЛ и др.: микробиологическое (культуральное) исследование слизи с миндалин и задней стенки глотки на аэробные и факультативно-анаэробные микроорганизмы, микробиологическое (культуральное) исследование мокроты на аэробные и факультативно-анаэробные микроорганизмы, Микробиологическое (культуральное) исследование лаважной жидкости на аэробные и факультативно-анаэробные микроорганизмы, Определение чувствительности микроорганизмов к антимикробным химиотерапевтическим препаратам), локальными данными чувствительности ключевых возбудителей к ПМП и предшествующим ответом на АМТ; необходима консультация клинического фармаколога, если в анамнезе имеется гиперчувствительность к ПМП или серьезные НЛР при назначении ПМП, а также высокий риск значимых лекарственных взаимодействий.
2 Доксициклин** применяется только у взрослых и детей > 8 лет; необходимо учитывать, что в России повсеместно отмечается высокий уровень резистентности S. pneumoniae к доксициклину**.
3 Ципрофлоксацин**, левофлоксацин** / моксифлоксацин** – лицам 18 лет и старше, детям – по жизненным показаниям (#ципрофлоксацин**, #левофлоксацин**, #моксифлоксацин**) [158, 159]. Левофлоксацин** и моксифлоксацин** следует назначать в максимальных терапевтических дозах.
4 Назначаются только при известной чувствительности возбудителя.
5 Убедительных доказательств преимуществ комбинированной АМТ не получено. Комбинация назначается при недостаточной эффективности монотерапии, при выявлении поли- / панрезистентных изолятов P. aeruginosa.
6 Возможно только при выявлении E. coli.
7 Реальная эффективность и влияние на исходы различных режимов АБТ при инфекциях, вызванных Achromobacter spp., не установлена
применение лекарственного препарата в соответствии с показателями (характеристиками)
Для улучшения общего состояния пациента следует соблюдать меры профилактики обострений, а лечебные мероприятия должны проводиться комплексно и в полном объеме, включать регулярные курсы реабилитации.
Рекомендуется: регулярное проведение курсов реабилитации всем пациентам с ПЦД с целью улучшения функции легких, увеличения толерантности к физическим нагрузкам, снижения количества обострений и госпитализаций, улучшения качества жизни (услуги перечислены в комментарии) [2, 141].
(УУР – С, УДД –5)
Комментарии: медицинскую реабилитацию можно начинать на любой стадии заболевания с целью сведения к минимуму тяжести болезни и симптомов, она должна быть индивидуализированной и ориентированной на потребности пациента.
Реабилитация проводится согласно приказу Минздрава России от 31 июля 2020 г. № 788н «Об утверждении Порядка организации медицинской реабилитации взрослых» (у взрослых) или согласно приказу Минздрава России от 23 октября 2019 г. № 878н «Об утверждении Порядка организации медицинской реабилитации детей» с соблюдением всех описанных в них принципов и включает: модификацию образа жизни, самообразование по вопросам особенностей течения заболевания, физическую реабилитацию (кинезитерапию), использование физических факторов, использование методов основанных на БОС, корректировку питания и психологическую поддержку. Возможно включать в программу реабилитацию в санаторно-курортных учреждениях в местных санаториях и на климатолечебных курортах.
Медицинская реабилитация пациентов данного профиля осуществляется специалистами мультдисциплинарной бригады включающей, например: врача-педиатра/врача-терапевта, врача-пульмонолога, врача по медицинской реабилитации / врача физической и реабилитационной медицины / врача по лечебной физкультуре / врача-физиотерапевта, медицинскую сестру, при возможности - медицинского психолога, врача-диетолога, специалиста по эргореабилитации (эргоспециалиста) / специалиста по физической реабилитации (кинезиоспециалиста).
Рекомендуется селективное включение в программу реабилитации пациентов с ПЦД дыхательные и релаксационные тренинги на основе БОС по контролю фаз дыхания и частоты сердечных сокращений (Лечебная физкультура с биологической обратной связью при заболеваниях бронхолегочной системы) с целью укрепления дыхательной мускулатуры, повышения эмоционального тонуса пациента [220, 221, 222].
(УУР – C, УДД – 5)
Психолого-педагогическая реабилитация семьи ребенка с первичной цилиарной дискинезией
Согласно результатам анализа ряда современных научных исследований качества жизни детей и подростков с первичной цилиарной дискинезией, большинство авторов считают наиболее значимыми негативными психофизическими последствиями болезни, ограничивающими социальное функционирование больного, следующие: расстройство дыхательной функции и нарушение газообмена, патология сна и высокий риск апноэ, периодически возникающие головные боли и воспаления среднего уха различной степени выраженности [223, 224].
В силу хронической астении у детей наблюдаются неустойчивость эмоционально-волевой регуляции и концентрации внимания, ухудшение динамических показателей мышления, снижение работоспособности. В случае тяжелого рецидивирующего течения болезни и отсутствия своевременного лечения у детей развивается кондуктивная тугоухость, что приводит к нарушению речевого развития и коммуникативным трудностям, проблемам социальной адаптации [225, 226].
По мере взросления социальные проблемы трансформируются и к старшему подростковому возрасту у лиц с первичной цилиарной дискинезией нередко появляется пессимистическое отношение к профессиональному будущему и отказ от планирования семьи в силу ограничения фертильности и невозможности иметь детей [227].
Исследования психологического состояния родителей детей с первичной цилиарной дискинезией свидетельствуют о высоком уровне стресса (тревоги, депрессии), особенно в первые годы жизни ребенка, на этапе постановки диагноза, что может продолжаться несколько месяцев, а также проблемам адаптации к новой жизненной ситуации, необходимости приобретения специальных навыков по уходу за ребенком с редким заболеванием и подбором оптимального для него стиля воспитания [228].
Целью психолого-педагогической помощи является создание соответствующих психофизическим возможностям ребенка психолого-педагогических условий для удовлетворения индивидуальных психологических и особых образовательных потребностей.
Рекомендовано пациентам с ПЦД при возможности проведение приема (тестирования, консультации) медицинского психолога первичного / повторных с целью улучшения адаптации пациента [223, 224, 226, 229].
(УУР – C, УДД – 5)
Комментарии: психолого-педагогическая помощь реализуется по следующим направлениям: психолого-педагогическая диагностика, разработка индивидуальной программы психолого-педагогического сопровождения и ее реализация, оценка эффективности психолого-педагогической помощи и внесение изменений в содержание индивидуальной программы.
Диагностическое обследование включает следующие направления:
- анализ и оценка физического функционирования ребенка и степени ограничений жизнедеятельности по результатам изучения медицинской документации, оценка познавательного развития для определения актуального способа мышления, особых образовательных потребностей и правильного выбора образовательного маршрута и содержания обучения (при необходимости АООП) с помощью методики диагностики познавательного развития (Стребелева Е.А., Лазуренко С.Б., Закрепина А.В.); теста интеллекта Дж. Векслера [230, 231];
- изучение индивидуально-личностных характеристик и психологического состояния с целью установления возрастных и индивидуальных психологических потребностей [«Лист наблюдений» (Check-list) Т. Ахенбаха; опросник самоотношения Пирса-Харриса; методика «Три желания» (А.М. Прихожан, Н.Н. Толстых)]; «Незаконченные предложения» (В. Михал), Методика изучения самооценки Т.В. Дембо, С.Я. Рубинштейн [232, 233, 234];
- оценка социальной ситуации развития и ее соответствия потребностям и психофизическим возможностям ребенка («Родительское сочинение» А.А. Шведовской, методика Рене Жиля, анкета комплаентности Мориски-Грина) [234, 235, 236].
Содержание психолого-педагогической помощи определяется физическим функционированием, возрастными и психологическими потребностями ребенка, социальной ситуацией развития, а также организацией процесса лечения.
Для пациентов с достаточным психофизическим функционированием, преимущественно с легким либо среднетяжелым течением болезни в стадии медикаментозной ремиссии, незначительными социальными ограничениями, обусловленными снижением работоспособности и режимом лечения, психолого-педагогическая помощь включает в себя мониторинг психологического состояние и решение актуальных психологических трудностей, профилактику возникновения устойчивых социально-психологических проблем. Особое внимание уделяется оценке степени соответствия образа жизни, режима педагогической нагрузки, жизненных и профессиональных планов психофизическим возможностям ребенка и формированию приверженности лечению.
Детям с ограничением психофизического функционирования, что обусловлено рецидивирующим течением болезни, психолого-педагогическое сопровождение реализуется регулярно как в очной, так и дистанционной формах с целью оптимизации социальной ситуации развития и удовлетворения индивидуальных психологических и образовательных потребностей. Содержание, форма и режим педагогических и психологических занятий определяется индивидуально на каждом этапе возрастного развития с учётом состояния здоровья, методов и организации медицинской помощи.
Пациенты с низким психофизическим функционированием в силу тяжелого физического и психологического состояния, вплоть до выраженного истощения и приглушения психологических потребностей, нуждаются в психологической помощи для улучшения эмоционального состояния, поддержании и активизации возрастных видов деятельности, в том числе общении со сверстниками, удовлетворении индивидуальных интересов и способностей. Деятельность специалистов педагогического профиля направлена на расширение кругозора ребенка и освоение содержания образовательной программы, рекомендованной медико-психолого-педагогической комиссией с учетом мнения родителей.
Для оптимизации социальной ситуации развития, формирования конструктивного отношения родителей к ситуации болезни ребенка, повышения качества ухода и выполнения врачебных назначений на всех этапах его лечения осуществляется семейное консультирование, просветительская и образовательная работа с родителями/законными представителями [228].
Психолого-педагогическое сопровождение семьи ребенка с первичной цилиарной дискинезией реализуется командой специалистов с высшим психологическим и педагогическим образованием: детские и семейные психологи, медицинские психологи.
5.1 Профилактика
Рекомендуется генетическое консультирование родителей детей с ПЦД (прием (осмотр, консультация) врача-генетика первичный / повторный) при планировании последующих беременностей с целью минимизации риска рождения больного ребенка [237].
(УУР – C, УДД – 5)
5.2 Вакцинация, профилактика обострений и противоэпидемические меры
Вакцинацию у пациентов с ПЦД рекомендовано проводить в соответствии с национальным календарем прививок, в том числе, против коклюшной инфекции. Рекомендуется также иммунизация против пневмококка и гемофильной инфекции, а также ежегодная вакцинация от гриппа [25].
(УУР – C, УДД – 5)
Комментарии: пациентам с ПЦД иммунизацию проводят в свободном от обострений периоде, в том числе на фоне длительной антибактериальной и иной (кроме высоких доз иммуносупрессивной) терапии.
Пациентам с ПЦД рекомендована вакцинация против коронавирусной инфекции нового типа (COVID-19) в соответствии с инструкциями к препаратам с целью профилактики данной инфекции [238].
(УУР – C, УДД – 5)
Комментарии: у пациентов с ПЦД отсутствуют особые противопоказания для вакцинации коронавирусной инфекции нового типа (COVID-19).
Рекомендовано пациентам с ПЦД избегать курения (в т.ч., пассивного), воздействия других аэрополлютантов и веществ, раздражающих дыхательные пути с целью предотвращения повреждения слизистой оболочки дыхательных путей и стимулирования гиперпродукции слизи [237].
(УУР – C, УДД – 5)
Рекомендовано соблюдение противоэпидемического режима, проведение контроля и мониторирования инфекции у пациентов с ПЦД с целью предотвращения перекрестного инфицирования, своевременного выявления и адекватной терапии [28].
(УУР – C, УДД – 5)
Комментарии: отсутствие в РФ данных, касающихся эпидемиологии инфекционных осложнений при ПЦД, не позволяет разработать строгие рекомендации для профилактики инфекции при ПЦД. В связи с этим в данных клинических рекомендациях представлены некоторые положения из первого международного консенсуса по профилактике и контролю инфекции при ПЦД, принятого в 2020 году «BEAT-PCD» (Better Experimental Approaches to Treat PCD), включающего значимые положения, которые касаются микробиологической диагностики, показаний для лечения инфекций и действий, направленных на улучшение профилактики и инфекционного контроля у пациентов с ПЦД [28]. Основные положения консенсуса:
- регулярно проводить исследование на селективных средах для Pseudomonas aeruginosa каждого образца мокроты или секрета из дыхательных путей;
- все центры для пациентов с ПЦД должны иметь возможность отправлять образцы мокроты для идентификации и генотипирования микроорганизмов в референс лаборатории;
- осуществлять посевы образцов секрета из дыхательных путей от пациентов с ПЦД не менее 4 раз в год;
- осуществлять исследование на НТМ не реже одного раза в год и дополнительно при любом необъяснимом ухудшении функции легких;
- осуществлять обязательное генотипирование при первом положительном посеве Burkholderia cepacia complex;
- необходимо отделять пациентов с инфекцией, вызванной P. aeruginosa в амбулаторных и стационарных условиях;
- необходимо отдельно принимать и госпитализировать пациентов с НТМБ инфекцией в амбулаторных и стационарных условиях;
- также необходимо отдельно принимать и госпитализировать пациентов с MRSA в амбулаторных и стационарных условиях;
- пациентов с инфекцией B. cepacia complex в амбулаторных и стационарных условиях необходимо принимать и госпитализировать отдельно;
-лечебные центры, где осуществляют прием пациентов с ПЦД, должны иметь инструкции, где описаны правила разделения пациентов с ПЦД с хроническими инфекциями легких различной этиологией;
- во время пандемии COVID-19 в отношении мероприятий за пределами больницы: если более одного пациента с ПЦД посещают мероприятия в помещении, они должны держаться на расстоянии не менее 2 м и носить маску независимо от статуса заражения;
- пациенты с выявленной вирусной инфекцией или с симптомами респираторной инфекции должны быть временно изолированы в амбулаторных и стационарных условиях или, по крайней мере, носить маску;
- необходимо подвергать дезинфекции процедурные кабинеты и кабинеты, где осуществляется прием пациентов, между приемом пациентов и в конце дня, с использованием дезинфицирующих / моющих средств;
- пациентов, из верхних и нижних дыхательных путей которых высевают H. influenzae, M. catarrhalis, S. pneumoniae и S. aureus (MSSA), нет необходимости разделять в амбулаторных и госпитальных условиях.
Таким образом, может быть достигнут консенсус по микробиологической диагностике, показаниям для лечения инфекций, и учитывающим аспекты разделения пациентов с инфекциями различной этиологии, включая возбудителя COVID-19.
По микробиологической диагностике консенсус может быть достигнут относительно ряда профилактических мер, принимаемых для ограничения распространения инфекций, вызываемых условно-патогенными микроорганизмами, такими как P. aeruginosa, B. cepacia complex и НТМ, включая раннее выявление инфекции путем исследования не менее четырех образцов секрета из дыхательных путей пациентов с ПЦД в течение года в соответствии с модифицированными критериями Лидса для определения хронической инфекции P. aeruginosa [26] и использования конкретных микробиологических лабораторных методов, таких как культивирование на селективных средах и проведение генотипирования для повышения точности микробиологической диагностики.
Относительно разделения пациентов был достигнут консенсус, включающий разделение внутри и за пределами больницы, если у пациента есть идентифицированная инфекция, вызванная P. aeruginosa, B. cepacia complex, НТМБ или MRSA, даже при первом положительном высеве. В настоящее время нет четких доказательств передачи P. aeruginosa от пациента к пациенту между пациентами с ПЦД. Однако передача мультирезистентных штаммов P. aeruginosa между пациентами с МВ является хорошо известной проблемой [238]. Из опыта лечения МВ также известно, что некоторые типы клонов могут передаваться другим пациентам, например пациентам с ХОБЛ. Поэтому рекомендуется избегать любого прямого контакта между пациентами с МВ, как в больнице, так и за ее пределами [239, 240].
Поскольку также необходимо исследовать не менее четырех образцов секрета из дыхательных путей в год, последний положительный результат посева секрета из дыхательных путей может быть получен 3 месяца назад или более. Следовательно, существует потенциальный риск передачи патогенов, если ими пациент был инфицирован позже, чем исследован последний образец секрета из дыхательных путей. Чтобы свести к минимуму этот риск, необходимо, чтобы пациент прислал образец секрета из дыхательных путей за неделю до амбулаторного визита, чтобы можно было узнать о любом изменении инфекционного статуса в день приема пациента. Однако следует отметить, что медленнорастущие патогены в образце могут не определяться из-за чрезмерного роста более быстрорастущих бактерий, если они присутствуют в небольших количествах.
30-минутный перерыв между посещениями пациентов с ПЦД независимо от инфекционного статуса, который мог бы минимизировать передачу, не привел к достижению консенсуса, поскольку такой перерыв слишком сложно соблюдать из-за логистики в различных местах.
В некоторых медицинских организациях могут быть общие помещения для пациентов с МВ и пациентов с ПЦД, и в этих организациях следует учитывать соблюдение строгих правил разделения пациентов с ПЦД согласно консенсусу «BEAT-PCD» (Better Experimental Approaches to Treat PCD) [28]:
Консенсус был достигнут в отношении необходимости сегрегации, если пациенты были инфицированы P. aeruginosa и B. cepacia complex, MRSA и NTM, тогда как не было достигнуто консенсуса в отношении предложения сегрегации для пациентов, инфицированных A. xylosoxidans, или пациентов с положительными результатами посева H. influenzae, M. catarrhalis, S. pneumoniae и S. aureus (MSSA). Социальное дистанцирование не менее 2 м между пациентами с ПЦД и использованием лицевых масок пациентами во время встреч в помещении, включая более одного пациента с ПЦД, было предложено после вспышки COVID-19 [28] и широко используемым среди большинства людей во всех повседневных жизненных ситуациях[241].
Консенсус относительно профилактических мероприятий касался методов дезинфекции. Во избежание общего распространения микроорганизмов на других пациентов было предложено дезинфицировать палату пациента между посещениями и в конце дня зарегистрированным дезинфицирующим/моющим средством. В соответствии с руководящими принципами Всемирной организации здравоохранения (ВОЗ) медицинский персонал также должен соблюдать гигиену рук перед входом в палату и при выходе из комнаты пациента, до или после прямого контакта с пациентом, перед надеванием перчаток и после снятия перчаток при медицинских процедурах, после контакта с кожей пациента, слизистыми оболочками, мокротой или другими биологическими жидкостями, а также после контакта с медицинским оборудованием рядом с пациентом, которое может быть загрязнено биологическими жидкостями из дыхательных путей [242].
Обеспечение профилактики перекрестной инфекцией, например, P. aeruginosa между пациентами с ПЦД привела к использованию масок. Ранее было показано, что использование масок для лица эффективно для уменьшения выделения потенциально инфекционных аэрозолей, содержащих P. aeruginosa, у пациентов с МВ [243, 244], как в амбулаторных, так и в госпитальных условиях [245].
5.3 Ведение пациентов и диспансерное наблюдение
Первичная диагностика и подбор терапии осуществляется в условиях специализированного пульмонологического стационара или отделения (пациенты с нетяжелым течением, особенно при катамнестическом наблюдении могут быть госпитализированы в дневной стационар), ведение пациентов совместно со специалистом врачом-оториноларингологом и, по показаниям, с врачом-сурдологом-оториноларингологом, при наличии признаков легочной гипертензии – с врачом-детским кардиологом / врачом-кардиологом. Срок пребывания в среднем может составить 14-21 день.
В амбулаторно-поликлинических учреждениях при подозрении на ПЦД участковые врачи-педиатры направляют больных на консультацию к врачу-пульмонологу.
Частота визитов пациента с первичной цилиарной дискинезией устанавливается индивидуально в зависимости от тяжести течения. В среднем контрольные осмотры пациентов с ПЦД должны проводиться не реже 2-х раза в год (по показаниям - чаще), с одновременным исследованием функции внешнего дыхания, проведением пульсоксиметрии. Проведение ЭхоКГ с допплеровским анализом и контроль КТ легких рекомендуется в среднем 1 раз в 2 года).
Рекомендовано диспансерное наблюдение пациентов с ПЦД (диспансерный прием (осмотр, консультация) врача-педиатра / врача-терапевта / врача-пульмонолога) с целью проведения адекватной своевременной терапии, контроля за лечением, улучшения качества и продолжительности жизни (Примерный план динамического наблюдения и мониторирования пациентов с ПЦД представлен в таблице 9) [25].
(УУР – C, УДД – 5)
Комментарии:
Таблица 9. Перечень лабораторных и инструментальных исследований и консультаций специалистов, осуществляемых в среднем при динамическом наблюдении пациентов с ПЦД
Вид обследования |
При первичном обращении |
Плановый визит (каждые 3 мес. При наличии бронхоэктазов и дыхательной недостаточности |
Плановый визит (каждые 6 месяцев при отсутствии бронхоэктазов и ДН) |
Ежегодно |
Каждые 2 года |
По показаниям |
|---|---|---|---|---|---|---|
Жалобы, анамнез |
+ |
+ |
+ |
|||
Антропометрия с оценкой по процентильным рядам и динамикой |
+ |
+ |
+ |
|||
Клинический осмотр (прием (осмотр, консультация) врача-пульмонолога (или врача-педиатра / врача-терапевта) первичный и повторные |
+ |
+ |
+ |
|||
|
Спирометрия1 (исследование неспровоцированных дыхательных объемов и потоков) |
+ |
+ |
+ |
|||
|
Спирометрия с пробой с бронхолитиком1 (исследование дыхательных объемов с применением лекарственных препаратов) |
+ |
+ |
||||
Бодиплетизмография1 |
+ |
+ |
||||
Пульсоксиметрия |
+/- |
+ |
+ |
|||
|
Общий анализ крови (Общий (клинический) анализ крови развернутый) |
+ |
+ |
+ |
|||
|
Биохимический анализ крови1 (анализ крови биохимический общетерапевтический, исследование уровня глюкозы в крови) |
+ |
+ |
+ |
|||
|
Микробиологический анализ мокроты (наименования услуг в соответствии с Номенклатурой медицинских услуг услуг см. комментарий в разделе 2.3 «Лабораторная диагностика») |
+ |
+ |
+ |
+ |
||
Обследование на НТМБ (услуги - см. подраздел 2.3.1) |
+ |
|||||
Исследование уровня общего иммуноглобулина Е в крови |
+ |
|||||
Электрокардиография (ЭКГ) |
+ |
+ |
+ |
|||
Эхокардиография (ЭХО-КГ) |
+ |
+ |
||||
|
Рентгенография органов грудной клетки (рентгенография легких) |
+ |
+ |
||||
Компьютерная томография органов грудной полости / Спиральная компьютерная томография легких |
+/- |
+ |
||||
Магнитно-резонансная томография органов грудной полости |
+ |
|||||
|
КТ пазух носа (с 5 лет) (компьютерная томография придаточных пазух носа, гортани)1 |
+ |
+ |
||||
Прием (осмотр, консультация) врача-оториноларинголога первичная / повторные |
+ |
+2 |
||||
Эндоскопия носоглотки (эндоскопическая эндоназальная ревизия полости носа, носоглотки) |
+ |
+2 |
+ |
|||
Тональная пороговая аудиометрия (регистрация вызванной отоакустической эмиссии и / или регистрация коротколатентных слуховых вызванных потенциалов, ASSR-тест)1 |
+ |
+2 |
+ |
|||
Прием (тестирование, консультация) медицинского психолога первичный / повторные |
+ |
|||||
Контроль навыков кинезитерапии и использования дыхательных тренажеров и приборов |
+ |
+ |
||||
Прием (осмотр, консультация) врача-хирурга / врача-детского хирурга первичный / повторные, специализирующегося в трансплантологии |
+ |
|||||
Прием (осмотр, консультация) врача-кардиолога (врача-детского кардиолога) первичный / повторные |
+ |
+ |
||||
Прием (осмотр, консультация) врача-уролога (врача-уролога-андролога детского) первичный и повторные |
+ |
|||||
Прием (осмотр, консультация) врача-акушера-гинеколога первичная и повторные |
+ (только лицам женского пола) |
|||||
Рекомендации по лекарственному обеспечению, внесение изменений заявку по лекарственному обеспечению |
+ |
|||||
Годовой эпикриз (выписка для МСЭ) с рекомендациями и планом наблюдения на год |
+ |
|||||
Подписание информированного согласия и внесение данных пациента в регистр |
+ |
Примечания:
1 В отдельных возрастных группах с учетом возраста и возможности выполнения маневра
2 При наличии полисинусита и полипов носа – чаще
При оказании медицинской помощи пациентам с ПЦД необходимо использовать мультидисциплинарный подход, что обусловлено как тяжестью состояния, так и поражением различных органов и систем.
Пациентам с ПЦД, в зависимости от необходимости, может быть оказана медицинская помощь любого вида, условия, формы, предусмотренных законодательством Российской Федерации.
Ведение пациентов с ПЦД предпочтительно проводить в специализированных центрах. Следует, при возможности, использовать стационарозамещающие технологии.
Динамическое наблюдение в амбулаторно-поликлинических условиях при оказании первичной медико-санитарной помощи осуществляет врач-педиатр участковый (врач-педиатр, или врач-пульмонолог, которые прошли соответствующий тематический курс в рамках программ непрерывного медицинского образования, и/или имеют опыт ведения пациентов с данной нозологией; консультации специалистов – по показаниям) с частотой, определяемой тяжестью состояния пациента и имеющимися осложнениями болезни (1 раз в 1-3 месяца или по показаниям). Впервые диагностированные пациенты или пациенты с тяжелыми формами заболевания должны наблюдаться чаще (ежемесячно), пациенты с легким или атипичным течением ПЦД могут наблюдаться реже (каждые 6-12 мес.).
Наблюдение за пациентом и контроль состояния необходимо осуществлять регулярно в условиях дневного стационара. Госпитализация проводится по показаниям в круглосуточный стационар (в пульмонологическое, инфекционное или иное отделение, в штате которого есть специалисты, имеющие опыт ведения пациентов с данной нозологией). Пациента госпитализируют в палату с учетом подтвержденного ранее микробиологического пейзажа (особенно для Р. aeruginosa, В. cepacia comрlex, MRSA, Achromobacter spp., нетуберкулезных микобактерий, хронический аспергиллеза), при возможности – индивидуальный бокс. В зависимости от состояния пациента срок госпитализации может составить от 4 до 21 дня.
Пациенты с ПЦД, нуждающиеся в стационарном лечении в рамках первичной специализированной медико-санитарной помощи, направляются по медицинским показаниям в пульмонологическое, инфекционное или иное отделение (по показаниям, условия – указаны выше) медицинской организации врачом скорой медицинской помощи, врачом-педиатром участковым / врачом-терапевтом участковым, врачом-пульмонологом или иным специалистом амбулаторно-поликлинического звена.
Пациентов с ПЦД, нуждающихся в оказании специализированной медицинской помощи, в том числе высокотехнологичной, в стационарных условиях, по медицинским показаниям направляют в соответствующее отделение медицинской организации врач-пульмонолог или врач-педиатр.
Маршрутизация пациента детского возраста во взрослую сеть – во взрослый центр ПЦД, осуществляется к 18 годам.
Пациенты с ПЦД получают:
- в рамках первичной медико-санитарной помощи – плановую и неотложную амбулаторно-поликлиническую и первичную специализированную помощь (соответствующего профиля, по показаниям и в зависимости от тяжести состояния, а также, при необходимости, в т.ч., при неотложных / экстренных ситуациях - скорую медицинскую помощь);
- в рамках специализированной медицинской помощи – специализированную, в том числе высокотехнологичную медицинскую помощь, в соответствующих условиях дневного или круглосуточного стационара.
При направлении в отделение (центр или кабинет), специализирующийся на пациентах с ПЦД, врачом-педиатром участковым или врачом другой специальности предоставляется выписка из амбулаторной карты (истории болезни) с указанием предварительного (или заключительного) диагноза, сопутствующих заболеваний, а также имеющихся результатов лабораторных и функциональных исследований.
7.1 Исходы и прогноз
Определяющими факторами являются своевременное установление диагноза и адекватная терапия.
Прогноз зависит от объема и характера поражения легких и, у большинства пациентов при правильном систематическом лечении и регулярном проведении реабилитационных мероприятий относительно благоприятный. При дыхательной недостаточности может быть показана трансплантация легких.
Обострения хронического воспалительного процесса в легких и околоносовых пазухах могут существенно снижать качество жизни пациентов.
Для взрослых пациентов мужского пола характерно первичное бесплодие или сниженная фертильность вследствие отсутствия или недостаточного количества (%) подвижных сперматозоидов.
Женщины с ПЦД могут иметь нормальную фертильность, однако в некоторых случаях способность к репродукции (фертильность) снижена, при этом отмечаются случаи внематочной беременности [20].













