Сахарный диабет 1 типа (СД 1) — это полигенное многофакторное заболевание, в основе которого лежит иммуноопосредованная или идиопатическая деструкция β-клеток поджелудочной железы, приводящая к абсолютной инсулиновой недостаточности [1].
СД 1 развивается при наличии генетической предрасположенности, для реализации которой необходимы факторы внешней среды, выступающие в роли триггера аутоиммунного поражения β-клеток поджелудочной железы [2]. Триггерами могут являться как инфекционные, так и неинфекционные факторы [3,4].
Инфекционные: энтеровирусы, ретровирусы. Неинфекционные: диетические составляющие – глютен, соя; коровье молоко (вскармливание), глюкоза; ненасыщенные жиры, антиоксиданты, тяжелые металлы, нитриты/нитраты, вещества, токсичные для β-клеток, психосоциальные факторы (стресс), ультрафиолетовая радиация, температура/сезонность.
У большинства лиц изменение в секреции инсулина и толерантности к глюкозе происходят в течение одного - трёх месяцев после обнаружения островковых антител. После того как критическая масса (точно неизвестно, какая именно) β-клеток разрушена, происходит манифестация заболевания с необходимостью во введении экзогенного инсулина. Манифестация происходит после «скрытой фазы», которая длится от нескольких месяцев до многих лет, которую у лиц с генетической предрасположенностью и несколькими видами антител можно рассматривать как бессимптомный СД 1.
Основными механизмами действия триггерных факторов являются: активация поликлональных лимфоцитов (например, инфекционными агентами); молекулярная мимикрия — идентичность участков белковых последовательностей инфекционного или химического агента и аутоантигенов; повышенная иммуногенность, индуцирующая иммунный ответ. Эти механизмы в конечном счете запускают развитие аутоиммунных процессов, а также приводят к продукции различных аутоантител, наиболее значимыми из которых являются аутоантитела к глутаматдекарбоксилазе (GADА), островковым клеткам (ICA), инсулину (IAA), тирозинфосфатаза-подобному белку (IA-2), транспортеру цинка (Zn-T8А) [5,6].
Во всем мире происходит увеличение распространенности СД. По данным Международной Диабетической Федерации численность пациентов с СД в возрасте 20-79 лет в мире в 2024 г. составила 588,7 млн., из них количество пациентов с СД 1 – 9,1 млн. (старше 20 лет – 1,8 млн.) [7]. В Российской Федерации (РФ) по данным Федеральной службы государственной статистики (Росстат) количество пациентов с зарегистрированным СД на 01.01.2025 г. составило 5 835 984 человек, из них с СД 1 типа - 349 543 пациентов [8].
E10.2 - Инсулинзависимый сахарный диабет с поражением почек;
E10.3 - Инсулинзависимый сахарный диабет с поражениями глаз;
E10.4 - Инсулинзависимый сахарный диабет с неврологическими осложнениями;
E10.5 - Инсулинзависимый сахарный диабет с нарушениями периферического кровоснабжения;
E10.6 - Инсулинзависимый сахарный диабет с другими уточненными осложнениями;
E10.7 - Инсулинзависимый сахарный диабет с множественными осложнениями;
E10.8 - Инсулинзависимый сахарный диабет с неуточненными осложнениями;
E10.9 - Инсулинзависимый сахарный диабет без осложнений.
В РФ используется классификация Всемирной организации здравоохранения (ВОЗ) 1999 г. с дополнениями (табл. 1).
Таблица 1. Классификация сахарного диабета (Всемирная Организация Здравоохранения, 1999, с дополнениями) [9,10]
|
СД 1 типа • Иммуноопосредованный • Идиопатический |
Деструкция β-клеток поджелудочной железы, обычно приводящая к абсолютной инсулиновой недостаточности |
|---|---|
СД 2 типа |
- с преимущественной инсулинорезистентностью и относительной инсулиновой недостаточностью или - с преимущественным нарушением секреции инсулина с инсулинорезистентностью или без нее |
Другие специфические типы СД |
- Генетические дефекты функции β-клеток - Генетические дефекты действия инсулина - Заболевания экзокринной части поджелудочной железы - Эндокринопатии - СД, индуцированный лекарственными препаратами или химическими веществами - Инфекции - Необычные формы иммунологически опосредованного СД - Другие генетические синдромы, иногда сочетающиеся с СД |
Гестационный СД |
Возникает во время беременности1 |
1 Кроме манифестного СД.
В отличие от классификации МКБ-10, в отечественной и зарубежной практике используются термины СД 1 (вместо инсулинзависимый СД) и СД 2 (вместо инсулиннезависимый СД).
В 2019 г. ВОЗ опубликовала новую классификацию СД, в которой появились гибридные формы СД, неклассифицируемый СД [11]. В настоящее время Российская ассоциация эндокринологов рекомендует продолжать использовать классификацию 1999 г., с учетом возможных сложностей кодирования по МКБ-10.
Понятие тяжести СД в формулировке диагноза исключено. Тяжесть СД определяется наличием осложнений, характеристика которых указана в диагнозе.
В связи с введением индивидуализированных целей терапии понятия компенсации, субкомпенсации и декомпенсации в формулировке диагноза у пациентов с СД нецелесообразны. После полной формулировки диагноза следует указать индивидуальный целевой уровень гликемического контроля (см. в разделе 3.1 «Терапевтические цели»).
СД 1 характеризуется острым началом заболевания, быстрым развитием метаболических нарушений. Заболевание обычно начинается в детском и подростковом возрасте, но может развиться в любом возрасте, в том числе в старческом. Часто отмечается сочетание с другими аутоиммунными заболеваниями [5,12].
Генетическая предрасположенность необходима для развития заболевания, но реализуется далеко не всегда. В семьях пациентов максимальный риск имеют родственники первой степени родства пациентов с СД 1: братья, сестры, дети, родители.
Выделяют доклиническую стадию заболевания, когда еще до появления первых клинических симптомов заболевания могут быть выявлены антитела. Нередко клинической манифестации заболевания предшествует вирусная инфекция, стресс или перегрузка легкоусвояемыми углеводами, ускоряющие клинические проявления болезни.
Клиническая картина СД 1 варьирует от умеренных или выраженных признаков гипергликемии до тяжелой дегидратации, диабетического кетоацидоза (ДКА) вплоть до развития коматозного состояния и обусловлена абсолютным дефицитом инсулина.
Симптомы классического СД 1 развиваются достаточно быстро. Как правило, через 2–4 нед. после перенесенной инфекции у пациентов появляется сухость во рту, жажда до 3–5 л/сут., (полидипсия), повышенный аппетит (полифагия), мочеизнурение (полиурия), особенно в ночные часы. При обследовании выявляют гипергликемию и глюкозурию. Гипергликемия обусловлена снижением утилизации глюкозы периферическими тканями вследствие недостатка инсулина. Гипергликемия, в свою очередь, приводит к глюкозурии. Полиурия – первый манифестный симптом глюкозурии. Известно, что глюкоза полностью реабсорбируется в канальцах почек при её концентрации в плазме крови до 10 ммоль/л. Превышение этого порога приводит к выведению глюкозы с мочой. Полиурия, обычно сопровождающая высокую глюкозурию, — следствие осмотического диуреза. Сухость во рту и жажда связаны с обезвоживанием организма вследствие избыточного выделения жидкости через почки, а также с повышением содержания в крови глюкозы, мочевины, натрия. Степень выраженности полиурии может быть различной, может превышать 5 литров в сутки. Моча бесцветная, с высоким удельным весом. Полидипсия возникает в результате раздражения центра жажды в головном мозге вследствие гиперосмолярности крови и обезвоживания. Жажда более заметна в ночные часы и утром.
Клиническая симптоматика сопровождается выраженной потерей массы тела, слабостью. Механизм развития клинических проявлений острой недостаточности инсулина, помимо нарушения углеводного обмена, включает дисбаланс белкового и жирового обменов. Это приводит к гипераминоацидемии, гиперлипидемии и кетоацидозу. Дефицит инсулина стимулирует глюконеогенез и гликогенолиз, а также подавляет гликогеногенез в печени.
Гиперлипидемия проявляется повышением содержания холестерина, триглицеридов, липопротеинов. Повышенное поступление липидов в печень, где они усиленно окисляются, приводит к увеличению продукции кетоновых тел и гиперкетонемии.
Накопление кетоновых тел (ацетона, β-оксимасляной и ацетоуксусной кислот) вызывает ДКА, уменьшение рН и развитие тканевой гипоксии. Прогрессирование метаболических нарушений, обусловленное дефицитом инсулина, усиливает тканевую дегидратацию, гиповолемию, гемоконцентрацию с тенденцией к развитию синдрома диссеминированного внутрисосудистого свертывания, гипоксии и, в конечном итоге, развитию диабетической комы.
Полиурия и жажда, обусловленные высоким содержанием глюкозы в плазме крови, наблюдаются далеко не у каждого пациента с декомпенсацией обмена веществ [9,13]. Некоторые пациенты не ощущают проявлений высокого уровня глюкозы в плазме крови. Однако те из них, у которых отмечают прогрессирующее повышение этого показателя, предъявляют жалобы на слабость, тяжесть в голове, нарушение зрения. Причина снижения остроты зрения — набухание хрусталика и слабость аккомодации, вызванные гипергликемией.
ВОЗ утверждены следующие критерии диагностики СД и других нарушений гликемии (табл. 2) [9,10].
Таблица 2. Диагностические критерии сахарного диабета и других нарушений гликемии (Всемирная Организация Здравоохранения, 1999–2013)
|
Время определения |
Концентрация глюкозы, ммоль/л1 |
|
|---|---|---|
|
Цельная капиллярная кровь |
Венозная плазма2 |
НОРМА | ||
|
Натощак и Через 2 часа после ПГТТ |
< 5,6 |
< 6,1 |
< 7,8 |
< 7,8 |
|
Сахарный диабет3 | ||
|
Натощак или Через 2 часа после ПГТТ или Случайное определение4 |
³ 6,1 |
³ 7,0 |
³ 11,1 |
³ 11,1 |
|
³ 11,1 |
³ 11,1 |
|
Нарушенная толерантность к глюкозе | ||
|
Натощак (если определяется) и Через 2 часа после ПГТТ |
< 6,1 |
< 7,0 |
³ 7,8 < 11,1 |
³ 7,8 < 11,1 |
|
Нарушенная гликемия натощак | ||
|
Натощак и Через 2 часа после ПГТТ (если определяется) |
³ 5,6 < 6,1 |
³ 6,1 < 7,0 |
< 7,8 |
< 7,8 |
|
Норма у беременных | ||
|
Натощак и Через 1 час после ПГТТ и Через 2 часа после ПГТТ |
|
< 5,1 |
|
< 10,0 |
|
|
< 8,5 |
|
Гестационный сахарный диабет | ||
|
Натощак или Через 1 час после ПГТТ или Через 2 часа после ПГТТ |
|
³ 5,1 < 7,0 |
|
³ 10,0 |
|
|
³ 8,5 < 11,1 |
|
Сокращения: ПГТТ – пероральный глюкозотолерантный тест.
1 Диагностика проводится на основании лабораторных определений уровня гликемии.
2 Возможно использование сыворотки.
3 Диагноз СД всегда следует подтверждать повторным определением гликемии в последующие дни, за исключением случаев несомненной гипергликемии с острой метаболической декомпенсацией или с очевидными симптомами. Диагноз гестационного СД может быть поставлен на основании однократного определения гликемии.
4 При наличии классических симптомов гипергликемии.
Перевод глюкозы крови из ммоль/л в мг/дл: ммоль/л × 18,02 = мг/дл.
Натощак – означает уровень глюкозы в крови утром после предварительного голодания в течение не менее 8 часов и не более 14 часов.
Случайное – означает уровень глюкозы в крови в любое время суток вне зависимости от времени приема пищи.
ПГТТ – пероральный глюкозотолерантный тест. Проводится в случае сомнительных значений гликемии для уточнения диагноза.
Правила проведения ПГТТ:
ПГТТ следует проводить утром на фоне не менее чем 3-дневного неограниченного питания (более 150 г углеводов в сутки) и обычной физической активности. Тесту должно предшествовать ночное голодание в течение 8–14 часов (можно пить воду). Последний вечерний прием пищи должен содержать 30–50 г углеводов. После забора крови натощак испытуемый должен не более чем за 5 мин. выпить 75 г безводной глюкозы или 82,5 г моногидрата глюкозы, растворенных в 250–300 мл воды. В процессе теста не разрешается курение. Через 2 часа осуществляется повторный забор крови.
Для предотвращения гликолиза и ошибочных результатов определение концентрации глюкозы проводится сразу после взятия крови, или кровь должна быть центрифугирована сразу после взятия, или храниться при температуре 0–4°С, или быть взята в пробирку с консервантом (флуорид натрия).
ПГТТ не проводится:
на фоне острого заболевания;
на фоне кратковременного приема препаратов, повышающих уровень гликемии (глюкокортикостероиды (АТХ-классификация S01BA), тиазидные диуретики (АТХ-классификация С03АА), бета-адреноблокаторы (АТХ-классификация С07) и др.).
Транзиторная гипергликемия
Гипергликемия, выявленная на фоне острой инфекции, травмы, стресса, инфаркта миокарда, острого нарушения мозгового кровообращения, обширных оперативных вмешательств, может быть транзиторной (стресс-индуцированной), обычно спонтанно нормализуется после исчезновения вызвавшего ее фактора и не должна сама по себе относиться к диагнозу СД. На период гипергликемии назначается терапия соответственно клинической ситуации. Через 4–12 недель после устранения возможной причины транзиторной гипергликемии у лиц с уровнем глюкозы венозной плазмы натощак < 7,0 ммоль/л проводится ПГТТ и/или определение гликированного гемоглобина (HbA1c) для реклассификации степени нарушения углеводного обмена.
Пациенты могут предъявлять жалобы на жажду (до 3–5 л/сут.); запах ацетона в выдыхаемом воздухе; кожный зуд; учащенное мочеиспускание, в том числе ночное; плохое заживление ран; фурункулез, кандидоз; резкое и значительное снижение массы тела, слабость, утомляемость.
СД 1 чаще развивается в молодом или детском возрасте. Заболеванию, как правило, предшествует острое вирусное заболевание или стресс. При позднем выявлении возможно развитие кетоацидотической комы.
Специфических признаков СД 1, которые можно было бы выявить при физикальном осмотре, не существует. Необходимо соблюдать общие пропедевтические принципы обследования пациентов. У взрослых манифестация СД 1 типа, как правило, менее выраженная, чем у детей. Клиническая симптоматика может быть ограничена такими признаками, как снижение веса, рецидивирующие кожные инфекция (фурункулез, кандидоз), иногда выявляются признаки сенсорной или болевой полинейропатии.
Здесь и далее: соответствие терминов (медицинских вмешательств), используемых в тексте клинических рекомендаций, номенклатуре медицинских услуг (в том числе для случаев с возможной неоднозначной интерпретацией) представлено в приложении А3.
Рекомендуется проведение одного из следующих исследований: исследование уровня глюкозы плазмы натощак , случайное исследование уровня глюкозы плазмы, исследование уровня гликированного гемоглобина (HbA1c) в крови - всем лицам с подозрением на СД 1 для уточнения диагноза [14,15].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: гипергликемия, выявленная при наличии острой инфекции, травмы или стресса, может быть транзиторной и не должна сама по себе относиться к диагнозу СД. Диагноз СД у лиц без симптомов не может быть установлен после однократного выяления повышенного уровня глюкозы. В этом случае необходимо повторное подтверждение значения глюкозы в «диабетическом» диапазоне либо натощак, либо случайно, либо в процессе ПГТТ.
Рекомендуется проведение ПГТТ с 75 г глюкозы лицам с подозрением на СД 1 в сомнительных случаях для уточнения диагноза [14,15].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Рекомендуется использование уровня HbA1c в крови ≥ 6,5 % (≥ 48 ммоль/ммоль) у лиц с подозрением на СД 1 для установления диагноза СД [15–17].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: исследование уровня HbA1c в крови должно быть выполнено с использованием метода, сертифицированного в соответствии с National Glycohemoglobin Standardization Program (NGSP) или International Federation of Clinical Chemists (IFCC) и стандартизованного в соответствии с референсными значениями, принятыми в Diabetes Control and Complications Trial (DCCT). Нормальным считается уровень HbA1c ≤ 6,0 % (≤ 42 ммоль/моль).
Согласно рекомендациям Всемирной Организации Здравоохранения, уровень HbA1c > 6,0 и < 6,5 % (> 42 и < 48 ммоль/моль) сам по себе не позволяет ставить какие-либо диагнозы, но не исключает возможности диагностики СД по уровню глюкозы крови.
В случае отсутствия симптомов острой метаболической декомпенсации диагноз должен быть поставлен на основании двух цифр, находящихся в диабетическом диапазоне, например, дважды определенный HbA1c или однократное определение HbA1c + однократное определение уровня глюкозы крови.
Ограничения в использовании HbA1c:
- При стремительном развитии СД, например, в некоторых случаях СД 1 типа у детей, уровень HbA1c может не быть значимо повышенным, несмотря на наличие классических симптомов СД и гипергликемии.
- Лабораторная и индивидуальная вариабельность, в связи с чем решения об изменении терапии должны проводиться с учетом других данных оценки гликемического контроля.
- Негликемические факторы, искажающие уровень HbA1c.
Повышают уровень HbA1c: анемии (дефицит железа, витамина В12, фолиевой кислоты), некоторые гемоглобинопатии, хроническое употребление алкоголя, употребление салицилатов, опиодов, спленэктомия, выраженная гипербилирубинемия.
Понижают уровень HbA1c: беременность (II и III триместры), гемолитические анемии, назначение препаратов железа, витамина В12, эритропоэтинов, прием витамина Е, С и других антиоксидантов в больших дозах, антиретровирусная терапия, лечение рибавирином и интерфероном-α, острая кровопотеря, переливание крови или эритроцитарной массы, ретикулоцитоз, спленомегалия, ревматоидный артрит, хронические заболевания печени, выраженная гипертриглицеридемия.
Повышают или понижают уровень HbA1c: гемоглобинопатии, терминальная почечная недостаточность, генетические факторы, фетальный гемоглобин, метгемоглобин.
В этом случае возможно определение уровня фруктозамина, который оценивает уровень глюкозы плазмы за 3 недели, но его диагностические и целевые значения пока не разработаны.
Рекомендуется определение (обнаружение) кетоновых тел в крови или в моче пациентам с диагностированным СД 1 для определения степени метаболических нарушений [13,18].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: при обнаружении кетоновых тел в моче ≥ 5 ммоль/л у лиц с СД 1 показана госпитализация.
У пациентов с классическими симптомами гипергликемии (жажда до 3–5 л/сут.; запах ацетона в выдыхаемом воздухе; кожный зуд; полиурия; плохое заживление ран; фурункулез, кандидоз; резкое и значительное снижение массы тела) повышения измеренного уровня глюкозы плазмы достаточно для постановки диагноза СД 1. Проведение дифференциальной диагностики требуется при стертой клинической симптоматике (в сомнительных случаях).
Рекомендуется общий (клинический) анализ крови (гемоглобин, гематокрит, количество эритроцитов, скорость оседания эритроцитов, цветовой показатель, дифференцированный подсчет лейкоцитов (лейкоцитарная формула)) не реже 1 раза в год пациентам с диагностированным СД 1 для исключения или подтверждения наличия сопутствующего воспалительного процесса и анемии [15,19].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: при выявлении снижения уровня гемоглобина пациентов следует направлять к врачу-терапевту для проведения дообследования.
Рекомендуется анализ крови биохимический общетерапевтический (исследование уровня общего белка в крови; исследование уровня общего кальция в крови; исследование уровня холестерина в крови; исследование уровня холестерина липопротеинов низкой плотности; исследование уровня холестерина липопротеинов высокой плотности в крови; исследование уровня триглицеридов в крови; исследование уровня общего билирубина в крови; исследование уровня мочевины в крови; исследование уровня креатинина в крови; определение активности аланинаминотрансферазы в крови; определение активности аспартатаминотрансферазы в крови; исследование уровня калия в крови; исследование уровня натрия в крови), исследование уровня глюкозы плазмы натощак не реже 1 раза в год пациентам с диагностированным СД 1 для уточнения наличия осложнений [13,15,20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Рекомендуется оценка расчетной скорости клубочковой фильтрации (рСКФ) или определение СКФ клиренсовыми методами (проба Реберга) при наличии показаний не реже 1 раза в год пациентам с диагностированным СД 1 для оценки функции почек [21–23].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 2)
Комментарии: рСКФ вычисляется на основании исследования уровня креатинина в крови с дальнейшим проведением расчета с использованием валидизированной формулы (предпочтительно формула CKD-EPI, наилучшим образом соотносящаяся с референсными (клиренсовыми) методами определения, доступно на https://www.kidney.org/professionals/gfr_calculator). Показания к оценке функции почек клиренсовыми методами перечислены в разделе 7 «Диабетическая нефропатия».
Рекомендуется общий (клинический) анализ мочи не реже 1 раза в год пациентам с диагностированным СД 1 для исключения заболеваний мочевых путей [15,19].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: при выявлении инфекции мочевых путей необходимо её лечение.
Рекомендуется исследование уровня C-пептида в крови пациентам с впервые выявленным СД 1 для определения остаточной секреции инсулина [15,24,25].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: С-пептид является белком, который отщепляется от молекулы проинсулина в процессе выделения инсулина в эквимолярных количествах. Не обладая гормональной активностью, С-пептид является дополнительным биологическим маркером эндогенной секреции инсулина. Базальный уровень С-пептида у здоровых людей 1,1–4,4 нг/мл. При СД 1 уровень С-пептида снижен или не определяется, что важно для дифференциальной диагностики с другими типами СД. После стимуляции глюкозой или стандартным углеводистым завтраком уровень С-пептида у пациентов с СД 1 значимо не повышается, а при СД 2 — значительно возрастает.
Рекомендуется определение содержания антител к антигенам островков клеток поджелудочной железы в крови (АТ к глутаматдекарбоксилазе – GADA; АТ к тирозинфосфатазе – IА-2; АТ к транспортеру цинка 8 – ZnT8, АТ к инсулину в крови – IAA, АТ к структурам островковых клеток – ICA) пациентам с подозрением на СД 1 для дифференциальной диагностики с другими типами СД [26,27].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: аутоантитела к антигенам β-клеток (ICA, GADA, IAA, IA-2, Zn-T8A) — иммунологические маркеры аутоиммунного инсулита. Исследование проводится для дифференциальной диагностики СД 1 и латентного аутоиммунного диабета взрослых с СД 2, моногенными и другими типами СД, а также при необходимости у родственников 1 степени родства с целью оценки риска развития СД 1. Присутствие двух и более специфичных аутоантител характерно для развития СД 1.
Рекомендуется выполнить молекулярно-генетическое исследование мутаций пациентам с нетипичной картиной СД 1 для исключения моногенных типов СД [28–30].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: при подозрении может потребоваться дифференциальная диагностика с моногенными типами СД (например, MODY).
Рекомендуется исследование уровня тиреотропного гормона (ТТГ) в крови пациентам с СД 1 для определения функции щитовидной железы [31–33].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
Комментарии: при нарушении функции щитовидной железы показано проведение дообследования: проведение ультразвукового исследования щитовидной железы, исследование уровня аутоантител к тиреопероксидазе.
Используются для скрининга и диагностики осложнений заболевания (информация представлена в разделе 7 «Дополнительная информация»).
Используются для скрининга и диагностики осложнений заболевания (информация представлена в разделе 7 «Дополнительная информация»).
Лечение СД 1 включает в себя:
инсулинотерапию;
самоконтроль гликемии;
обучение принципам управления заболеванием.
3.1 Терапевтические цели
3.1.1 Показатели контроля углеводного обмена (индивидуальные цели лечения)
Рекомендуется выбор индивидуальных целей гликемического контроля не реже 1 раза в год пациентам с СД 1 с целью безопасной терапии, обеспечивающей профилактику или замедление прогрессирования осложнений СД [15,34–36].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: индивидуальные цели гликемического контроля выбираются в зависимости от возраста пациента, ожидаемой продолжительности жизни, функциональной зависимости, наличия атеросклеротических сердечно-сосудистых заболеваний (АССЗ) и риска тяжелой гипогликемии. Алгоритм индивидуализированного выбора целей терапии по HbA1c представлен в табл. 3. Данные целевые значения не относятся к детям, подросткам и беременным женщинам.
Таблица 3. Алгоритм индивидуализированного выбора целей терапии по HbA1c1, 2
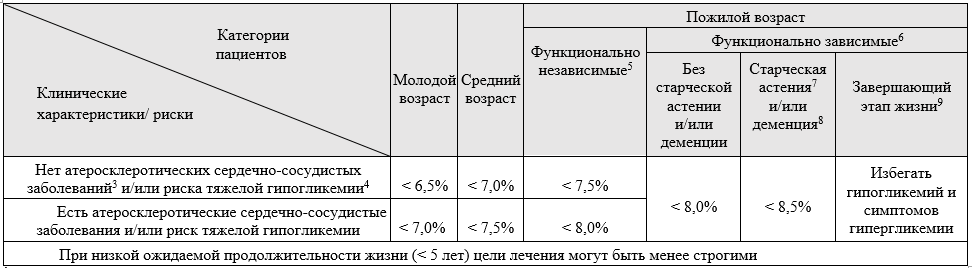
1 Данные целевые значения не относятся к беременным женщинам.
2 Нормальный уровень в соответствии со стандартами DCCT: ≤ 6 %.
3 ИБС (инфаркт миокарда в анамнезе, шунтирование/стентирование коронарных артерий, стенокардия); нарушение мозгового кровообращения в анамнезе; заболевания артерий нижних конечностей (с симптоматикой).
4 Основными критериями риска тяжелой гипогликемии являются: тяжелая гипогликемия в анамнезе, бессимптомная гипогликемия, большая продолжительность СД, ХБП С3-5, деменция.
5 Функционально независимые - пациенты, которые могут проживать независимо, не нуждаются в посторонней поддержке в мероприятиях повседневной активности (либо в минимальном объеме).
6 Функционально зависимые - пациенты, которые имеют нарушения в выполнении обычных мероприятий повседневной активности (например, одевание, процедуры личной гигиены), что увеличивает потребность в дополнительной медицинской и социальной поддержке и риск госпитализаций.
7 Старческая астения - пациенты с этим синдромом характеризуются повышенной утомляемостью, снижением массы тела, ограничением мобильности и мышечной силы, увеличением риска падений. Для скрининга синдрома старческой астении может быть использован опросник «Возраст не помеха» [37,38] (Приложение Г).
8 Деменция - у пациентов с деменцией имеются когнитивные нарушения, которые приводят к потере возможности самообслуживания (снижение памяти, ориентации во времени и пространстве, изменения личности). Соматически пациенты с деменцией могут длительно оставаться сохранными. Для оценки риска выраженных когнитивных нарушений можно использовать тест Mini-Cog (Приложение Г).
9 Завершающий этап жизни - ожидаемая продолжительность жизни менее 6 мес.
Примечание: следует учитывать, что биологический и паспортный возраст часто не совпадают, поэтому определения молодого, среднего и пожилого возраста относительно условны. В то же время существует понятие «ожидаемой продолжительности жизни» (ОПЖ), которая в большей степени, чем возраст, позволяет определить общее состояние пациента и клиническую значимость развития у него осложнений. Даже в пожилом возрасте ОПЖ может быть достаточно высокой и в этих случаях не следует допускать завышения индивидуальных целей лечения.
Соответствие HbA1c целевым значениям пре- и постпрандиального уровня глюкозы плазмы приведено в табл. 4.
Таблица 4. Соответствие HbA1c целевым значениям пре- и постпрандиального уровня глюкозы плазмы1
HbA1c, %2 |
Уровень глюкозы плазмы натощак/перед едой/ на ночь/ночью, ммоль/л |
Уровень глюкозы плазмы через 2 ч после еды, ммоль/л |
|---|---|---|
< 6,5 |
< 6,5 |
< 8,0 |
< 7,0 |
< 7,0 |
< 9,0 |
< 7,5 |
< 7,5 |
< 10,0 |
< 8,0 |
< 8,0 |
< 11,0 |
< 8,5 |
< 8,5 |
< 12,0 |
1 Данные целевые значения не относятся к беременным женщинам.
2 Нормальный уровень в соответствии со стандартами DCCT: ≤6 %.
После формулировки диагноза следует указать индивидуальные цели гликемического контроля (уровень HbA1c, уровень глюкозы плазмы натощак/перед едой/на ночь/ночью и через 2 ч после еды).
В табл. 5 представлено соответствие HbA1c среднесуточному уровню глюкозы плазмы за последние 3 мес.
Таблица 5. Соответствие HbA1c среднесуточному уровню глюкозы плазмы за последние 3 мес.
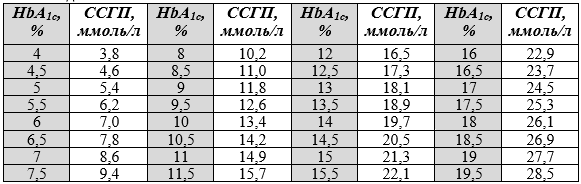
ССГП - среднесуточный уровень глюкозы плазмы.
ССГП (ммоль/л) = 1.5944 × HbA1c (%) – 2.594 [39].
Рекомендуется использование амбулаторного гликемического профиля и стандартизированных показателей при непрерывном мониторировании глюкозы (НМГ), включая время в диапазонах глюкозы (время в целевом диапазоне, время в диапазоне выше целевого, время в диапазоне ниже целевого) у пациентов с СД 1 для оценки степени достижения целевого гликемического контроля и безопасности терапии, обеспечивающей профилактику или замедление прогрессирования осложнений СД [40–49].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: стандартизованные показатели НМГ и их целевые значения у пациентов с СД 1 представлены в табл. 6 [40]. Для пациентов, проводящих НМГ, после формулировки диагноза, в качестве индивидуальных целей гликемического контроля, кроме уровня HbA1c, уровня глюкозы плазмы натощак/перед едой/на ночь/ночью и через 2 ч после еды, следует указать как минимум рекомендуемое время в целевом диапазоне.
Таблица 6. Стандартизованные показатели непрерывного мониторирования глюкозы и их целевые значения у пациентов с сахарным диабетом 1 типа
Показатель |
Целевое значение |
|
|---|---|---|
|
Пациенты молодого и среднего возраста и без факторов риска |
Пациенты пожилого возраста или с факторами риска |
Основные | ||
Количество дней ношения устройства НМГ |
≥ 14 дней |
|
Доля времени с активным устройством НМГ |
≥ 70 % |
|
Среднее значение уровня глюкозы |
- |
|
Время выше целевого диапазона: % измерений (время) в диапазоне > 10,0 ммоль/л (Уровень 1)1 |
< 25 % (< 6 ч) |
< 50 % (< 12 ч) |
Время в целевом диапазоне: % измерений (время) в диапазоне 3,9-10,0 ммоль/л |
> 70 % (> 16 ч 48 мин.) |
> 50 % (> 12 ч) |
Время ниже целевого диапазона: % измерений (время) в диапазоне < 3,9 ммоль/л (Уровень 1)2 |
< 4 % (< 1 ч) |
< 1 % (< 15 мин.) |
Дополнительные | ||
Индикатор контроля уровня глюкозы |
- |
|
Коэффициент вариабельности уровня глюкозы |
≤ 36 % |
|
Время выше целевого диапазона: % измерений (время) в диапазоне > 13,9 ммоль/л (Уровень 2) |
< 5 % (< 1 ч 12 мин.) |
< 10 % (< 2 ч 24 мин.) |
Время ниже целевого диапазона: % измерений (время) в диапазоне < 3,0 ммоль/л (Уровень 2) |
< 1% (<15 мин.) |
- |
1Включая значения > 13,9 ммоль/л, 2Включая значения < 3,0 ммоль/л.
У пациентов с достигнутыми целевыми параметрами контроля глюкозы (в том числе при использовании систем автоматического введения инсулина с замкнутым контуром) возможно рассмотреть время в узком целевом диапазоне (3,9-7,8 ммоль/л) в качестве критерия, дополнительного к стандартным метрикам НМГ.
3.1.2 Целевые уровни показателей липидного обмена
Рекомендуется выбор целевых уровней ХЛНП пациентам с СД 1 с учетом индивидуальных особенностей пациента для снижения риска сердечно-сосудистых событий и осложнений [50–55].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: выбор целевых уровней ХЛНП представлен в табл. 7.
Таблица 7. Выбор целевых уровней холестерина липопротеидов низкой плотности у пациентов с сахарным диабетом 1 типа
Категория риска |
Категория пациентов |
ХЛНП, ммоль/л1 |
|---|---|---|
Очень высокого риска |
|
< 1,4 |
Высокого риска |
|
< 1,8 |
Среднего риска |
|
< 2,6 |
Примечание: ХЛНП - холестерин липопротеинов низкой плотности.
1 Перевод из ммоль/л в мг/дл: ммоль/л × 38,67 = мг/дл.
2 Протеинурия, рСКФ < 45 мл/мин./1,73 м2, рСКФ 45-59 мл/мин./1,73 м2 + микроальбуминурия, гипертрофия левого желудочка (ЛЖ) или ретинопатия.
3 Возраст пациента (СД 1 типа ≥ 35 лет или СД 2 типа ≥ 50 лет), артериальная гипертензия, дислипидемия, курение, ожирение.
3.1.3 Целевые уровни показателей артериального давления
Рекомендуется выбор индивидуальных целевых уровней систолического и диастолического артериального давления (АД) пациентам с СД 1 с учетом возраста и переносимости для снижения риска сердечно-сосудистых событий [56–63].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: целевые уровни показателей АД представлены в табл. 8.
Таблица 8. Выбор целевых уровней артериального давления (при условии хорошей переносимости) у пациентов с сахарным диабетом 1 типа
Возраст |
Систолическое АД, мм рт.ст.1 |
Диастолическое АД, мм рт.ст.1 |
|---|---|---|
18 – 65 лет |
≥ 120 и < 130 |
≥ 70 и < 80 |
> 65 лет |
≥ 130 и < 140 |
1Нижняя граница целевых показателей АД относится к лицам на антигипертензивной терапии.
3.2 Контроль уровня глюкозы
Для самоконтроля уровня глюкозы крови рекомендуется применять глюкометры, предназначенные для индивидуального использования. В настоящее время существуют глюкометры с настройкой индивидуального целевого диапазона гликемии, а также глюкометры с функцией беспроводной передачи данных об уровне глюкозы медицинским специалистам, родственникам или в установленное на смартфон пациента специальное приложение (с внесением дополнительной информации о приемах пищи и дозах сахароснижающих препаратов) для использования при дистанционном наблюдении. Контроль уровня глюкозы крови может проводиться с применением методики ДНСД с использованием СИС ДН или модулей медицинских информационных систем, предназначенные для автоматической интерпретации данных.
Индивидуальные глюкометры должны соответствовать ГОСТ Р ИСО 15197-2015 по аналитической и клинической точности [64]. При уровне глюкозы плазмы < 5,6 ммоль/л 95 % измерений должны отклоняться от эталонного анализатора не более чем на ± 0,8 ммоль/л, при уровне глюкозы плазмы ≥ 5,6 ммоль/л 95 % измерений должны отклоняться от эталонного анализатора не более чем на ±15 %.
В условиях лечебно-профилактических учреждений, помимо лабораторных анализаторов, необходимо использовать глюкометры для профессионального применения (многопользовательские, госпитальные).
Системы длительного (непрерывного) мониторирования глюкозы (НМГ) измеряют глюкозу в интерстициальной жидкости непрерывно с частотой 5-15 минут с помощью устанавливаемых подкожно датчиков (сенсоров). Существует разница между отображаемым значением интерстициальной и капиллярной глюкозы (в среднем на 8-10 минут, максимально до 20 минут). Таким образом, в случае стабильного уровня глюкозы в крови отображаемые уровни будут близки к уровням капиллярной глюкозы. Однако во время быстрого повышения или понижения уровня глюкозы в крови отображаемое значение, как правило, будет ниже или выше, соответственно.
Доступные в настоящее время системы НМГ могут быть разделены на три категории:
1) НМГ в реальном времени отражает текущий уровень глюкозы, тенденции (направления и скорости) изменения глюкозы, график глюкозы за предыдущее время (в том числе вариабельность). Они имеют сигналы тревоги, которые активируются при достижении гликемией пороговых значений, прогнозировании этих значений, а также при достижении порогового уровня скорости изменения гликемии. Некоторые модели систем НМГ в реальном времени передают данные об уровне глюкозы на смартфон, откуда они могут быть сохранены на сервере в сети Интернет и использованы для удаленного мониторинга.
2) периодически сканируемое/просматриваемое НМГ или флеш-мониторирование глюкозы (ФМГ) не отображает данные об уровне глюкозы автоматически, а только при приближении на короткое расстояние сканера (ридера) или смартфона с установленным специальным приложением к датчику (сенсору). ФМГ предоставляет информацию о текущем уровне глюкозы, тенденции (направления и скорости) изменения глюкозы, график глюкозы за предыдущее время (в том числе вариабельность).
3) Комбинированный вариант работы НМГ (ФМГ второго поколения): мониторирование в реальном времени с автоматическим отображением данных об уровне глюкозы и обновлением данных на смартфоне пациента с частотой 1 раз в минуту, без необходимости в проведении рутинной глюкометрии пациентами для выполнения калибровок и принятия решений, например, расчета дозы инсулина, дополненный также ФМГ с возможностью для пациентов осуществлять сканирование датчика в случае потери связи.
Некоторые системы НМГ требуют т.н. калибровки, то есть внесения данных об уровне глюкозы в капиллярной крови. В то же время некоторые новые системы уже имеют т.н. «заводскую калибровку», когда проведение ручной калибровки (измерение глюкозы глюкометром) не требуется.
Также отдельные системы НМГ могут быть рекомендованы для самостоятельного применения, то есть для принятия терапевтических решений (например, расчета доз инсулина, при купировании гипогликемии и др.) без необходимости подтверждения с помощью глюкометра. При использовании таких систем потребность в использовании глюкометра меньше по сравнению с системами без таких показаний.
В то же время, пациенты, использующие НМГ должны иметь доступ к самоконтролю глюкозы крови для калибровки (при необходимости), при потере связи с НМГ, для принятия решений по лечению - для тех систем, которые не могут быть использованы для самостоятельного применения. Необходимая частота проведения самоконтроля гликемии на фоне применения таких систем НМГ должна соответствовать рекомендациям производителя. Таким образом, самоконтроль гликемии с помощью глюкометра продолжает оставаться необходимым при использовании НМГ.
С учетом большого объема информации, накапливаемого в процессе использования, и возникающими трудностями в их наглядной интерпретации специалистами, необходимо периодическое считывание данных НМГ и ФМГ с последующим анализом, с использованием специализированного программного обеспечения (в том числе амбулаторного профиля глюкозы). Могут быть проанализированы различные показатели вариабельности глюкозы, а также время нахождения в целевом, гипогликемическом и гипергликемическом диапазоне.
Рекомендуется проведение самоконтроля гликемии не менее 4 раз в сутки с помощью глюкометра: перед едой, через 2 ч после еды, на ночь, периодически ночью всем пациентам с СД 1 со своевременной коррекцией доз инсулина в целях достижения целевого уровня гликемического контроля и профилактики или замедления прогрессирования осложнений СД [15,34,35,65–69].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 2)
Комментарии: рекомендуется дополнительное проведение самоконтроля гликемии перед физическими нагрузками и после них, при подозрении на гипогликемию, а также если предстоят какие-то действия, потенциально опасные для пациента и окружающих (например, вождение транспортного средства или управление сложными механизмами). Увеличение частоты самоконтроля может улучшить показатели гликемии, а снижение частоты самоконтроля ведет к ухудшению показателей гликемии. При нахождении пациента в стационаре необходимость увеличения частоты контроля гликемии определяется индивидуально с учетом клинической ситуации, выраженности декомпенсации углеводного обмена и причины госпитализации.
Рекомендуется использовать глюкометры для профессионального применения (согласно инструкции по применению многопользовательские, госпитальные) у пациентов с СД 1 в условиях медицинских организаций для контроля гликемии [70–74].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: многопользовательские глюкометры обладают более высокой точностью измерений по сравнению с индивидуальными глюкометрами и выдерживают многократные циклы дезинфекции в соответствии с хорошо валидированными методами, представленными производителем. Многопользовательский глюкометр необходимо дезинфицировать после каждого измерения уровня глюкозы крови у каждого пациента средствами, обладающими фунгицидной, антибактериальной и противовирусной активностью, и не влияющими на функциональные свойства глюкометра.
Рекомендуется исследование уровня HbA1c в крови 1 раз в 3 месяца пациентам с СД 1 с целью определения степени достижения целевых показателей гликемического контроля и стратификации риска развития осложнений СД [15,34,36,75,76].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2)
Рекомендуется применение НМГ пациентам с СД 1 для оценки гликемического профиля и эффективности проводимого лечения в определенных клинических ситуациях [40,77–80].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
Комментарии: НМГ может быть проведено кратковременно (<15 дней) как амбулаторно, так и в условиях стационара, с целью:
- выявления ночной гипо- и гипергликемии (феномен «утренней зари»);
- оценки расширенного перечня показателей гликемического контроля в том числе: время в целевом диапазоне / гипогликемии / гипергликемии / вариабельность гликемии и др.;
- выявления индивидуальных постпрандиальных профилей гликемии (ускоренное или замедленное всасывание углеводов из ЖКТ);
- уточнения влияния физической нагрузки, гиподинамии, стресса и других факторов на гликемию;
- формирования индивидуальных рекомендаций в отношении инсулинотерапии и оптимальных алгоритмов снижения вариабельности гликемии (в том числе предупреждения гипогликемий и выраженной гипергликемии);
- полноценной оценки эффекта лекарственных средств на гликемию в рамках клинических исследований.
Рекомендуется применение НМГ пациентам с СД 1 для достижения индивидуальных целевых показателей гликемического контроля, снижения риска гипогликемии (в том числе тяжелой) и вариабельности гликемии, увеличения времени в целевом диапазоне, повышения качества жизни [40,77–80].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
Комментарии:
У взрослых пациентов с СД применение НМГ в реальном времени, ФМГ или НМГ с комбинированным вариантом работы целесообразно при желании, возможности и способности пациента и/или законного представителя активно его использовать, проводить регулярный самоконтроль гликемии и выполнять рекомендации лечащего врача. Применение НМГ в реальном времени или ФМГ или НМГ с комбинированным вариантом работы может быть рассмотрено у пациентов при:
• HbA1с > 7,5 % или другого индивидуального целевого показателя;
• тяжелых гипогликемиях (≥ 1 раза за последний год);
• частых эпизодах легкой гипогликемии (≥ 1 раза в день);
• при нарушении распознавания гипогликемии;
• высокой вариабельности гликемии независимо от уровня НbА1с;
• во время беременности;
• отказ пациента или законного представителя от НМГ;
• отсутствие возможности и способности пациента и/или законного представителя активно использовать НМГ, проводить регулярный самоконтроль и выполнять рекомендации лечащего врача;
• индивидуальная непереносимость НМГ: выраженные кожные реакции или другие нежелательные явления, связанные с методом и препятствующие его использованию;
• недостаточное использование НМГ ( < 60 % времени);
• при отсутствии клинической эффективности в течение 6 месяцев использования НМГ (при отсутствии объективных причин):
o Если исходный показатель HbA1c превышает индивидуальный целевой уровень менее чем на 1.0 %, эффективным считается темп снижения НbA1c ≥ 0,5 % (за 6 месяцев наблюдения);
o Если исходный показатель HbA1c превышает индивидуальный целевой уровень на 1.0-2.5 %, эффективным считается темп снижения НbA1c ≥ 1,0 % (за 6 месяцев наблюдения);
o Если исходный показатель HbA1c превышает индивидуальный целевой уровень более чем на 2.5 %, эффективным считается темп снижения HbA1с ≥ 1,5 % (за 6 месяцев наблюдения).
Рекомендуется проведение самоконтроля гликемии при помощи индивидуального глюкометра не менее 4 раз в сутки при использовании НМГ в реальном времени или не менее 2 раз в сутки при использовании ФМГ пациентам с СД 1 для оценки точности и/или калибровки данных мониторирования и решения вопроса о коррекции лечения [40,77,78,80–84].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: НМГ в реальном времени и ФМГ не исключают традиционный самоконтроль гликемии при помощи глюкометров. Рост точности измерений в современных системах НМГ в реальном времени и ФМГ позволяет значительно сократить частоту традиционного самоконтроля гликемии глюкометром. ФМГ может быть использовано вместо глюкометра для принятия клинических решений, за исключением отдельных случаев (гипогликемии, быстрого изменения гликемии или если симптомы не соответствуют показателям системы).
3.3 Инсулинотерапия
Заместительная инсулинотерапия является единственным методом лечения пациентов с СД 1. Характеристики препаратов инсулина, применяемых при лечении пациентов с СД 1 в РФ, указаны в табл. 9.
Таблица 9. Характеристика препаратов инсулина, применяемых при лечении пациентов с сахарным диабетом 1 типа [15]
АТХ-классификация |
Вид инсулина |
Международное непатентованное наиме-нование |
Начало действия |
Пик действия |
Длитель-ность действия |
|---|---|---|---|---|---|
A10AB инсулины короткого действия и их аналоги для инъекционного введения |
Сверхбыстрого действия (аналоги инсулина человека), ИСБД |
Инсулин аспарт** (имеющий в составе вспомогательное вещества никотинамид) |
Через 1-10 мин. |
Через 45-90 мин. |
3-5 ч |
|
Инсулин лизпро** 100 ЕД/мл (имеющий в составе вспомогательное вещество трепростинил) | |||||
|
Инсулин лизпро** 200 ЕД/мл1 (имеющий в составе вспомогательное вещество трепростинил) | |||||
Ультракороткого действия (аналоги инсулина человека), ИУКД |
Инсулин аспарт** |
Через 5–15 мин. |
Через 1–2 ч |
4-5 ч |
|
Инсулин глулизин** | |||||
Инсулин лизпро** 100 ЕД/мл | |||||
Инсулин лизпро 200 ЕД/мл1 | |||||
Короткого действия, ИКД |
Инсулин растворимый (человеческий генно-инженерный)** |
Через 20–30 мин. |
Через 2–4 ч |
5–6 ч |
|
A10AC инсулины средней продолжительности действия и их аналоги для инъекционного введения |
Средней продолжительности действия (НПХ-инсулины) 2 |
Инсулин-изофан (человеческий генно-инженерный)** |
Через 2 ч |
Через 6–10 ч |
12–16 ч |
A10AE инсулины длительного действия и их аналоги для инъекционного введения |
Длительного действия (аналоги инсулина человека) |
Инсулин гларгин** 100 ЕД/мл |
Через 1–2 ч |
Не выражен |
До 29 ч |
Инсулин гларгин** 300 ЕД/мл |
До 36 ч |
||||
Инсулин детемир** |
До 24 ч |
||||
Сверхдлительного действия (аналоги инсулина человека) |
Инсулин деглудек** |
Через 30-90 мин. |
Отсут-ствует |
Более 42 ч |
1 Не использовать для в/в введения, помповой инсулинотерапии и набора в инсулиновый шприц.
2 Перед введением следует тщательно перемешать.
В реальной клинической практике перевод с одного инсулина на другой происходит достаточно часто. При переводе пациента с одного инсулина на другой необходимо соблюдать следующий алгоритм требований для наилучшего обеспечения безопасности пациента [85]:
1. В случае разных МНН
• Перевод с одного препарата инсулина на другой должен осуществляться строго по медицинским показаниям, только при участии врача, требует более частого самоконтроля уровня глюкозы, обучения пациента и коррекции дозы вновь назначенного инсулина.
• Перевод может быть осуществлен с одного препарата инсулина на другой как в рамках одной группы по АТХ-классификации, так и со сменой АТХ-группы (например, перевод с человеческого инсулина на аналог инсулина и наоборот).
2. В случае одного и того же МНН
• Перевод пациентов с одного инсулина на другой с подтвержденной взаимозаменяемостью (т.е. подтвержденной биоэквивалентностью в отношении фармакокинетики, фармакодинамики и безопасности действия), как правило, не требует более частого самоконтроля уровня глюкозы, обучения пациента и коррекции дозы вновь назначенного инсулина. При подтвержденной биоэквивалентности все показания, противопоказания, нежелательные реакции, применение у особых групп экстраполируются на биосимиляр из инструкции по медицинскому применению референтного препарата.
• Перевод пациентов с одного инсулина на другой в рамках одного МНН, но с разной фармакокинетикой и фармакодинамикой должен осуществляться по правилам, указанным для препаратов с разными МНН.
3. В случае развития нежелательных явлений как при назначении инсулинотерапии, так и переводе с одного препарата инсулина на другой, к которым относятся ухудшение гликемического контроля, существенное изменение потребности/дозы инсулина, развитие аллергических реакций, обязательно сообщение в Федеральную службу по надзору в сфере здравоохранения [85].
4. Решение о переводе с одного препарата инсулина на другой принимает врач с учетом актуальной инструкции по применению.
Для всех пациентов с СД 1 препаратами первого ряда являются аналоги инсулина человека сверхбыстрого, ультракороткого, длительного и сверхдлительного действия.
Рекомендуется назначение интенсифицированной (базис-болюсной) инсулинотерапии путем многократных инъекций ИКД (ИУКД, ИСБД) и базального инсулина или путем непрерывной (постоянной) подкожной инфузии инсулина (НПИИ) пациентам с СД 1 для достижения целевых показателей гликемического контроля [15,34].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 2)
Комментарии: в большинстве случаев рекомендуется интенсифицированная инсулинотерапия с разделением инсулина на:
• фоновый или базальный (используются препараты инсулина средней продолжительности, длительного и сверхдлительного действия, при помповой инсулинотерапии – ИУКД (ИСБД));
• пищевой или прандиальный (используются ИКД (ИУКД, ИСБД)). Следует вычислить углеводной коэффициент - количество единиц инсулина на 1 ХЕ или количество граммов углеводов на 1 единицу инсулина;
• коррекционный – для снижения повышенного уровня гликемии (используются ИКД (ИУКД, ИСБД)). Следует вычислить фактор чувствительности к инсулину - на сколько ммоль/л снижает уровень глюкозы крови 1 ЕД инсулина.
Рекомендуется назначение аналогов ИУКД (ИСБД) пациентам с СД 1 для уменьшения риска гипогликемических состояний и/или вариабельности гликемии [86,87].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии: по сравнению с ИУКД препараты ИСБД обладают более быстрым началом действия и более ранним пиком, что позволяет уменьшить интервал между инъекцией и приемом пищи, а также снизить постпрандиальную экскурсию гликемии [88,89]. Инсулины сверхбыстрого действия имеют преимущества у лиц с активным образом жизни, частыми перекусами и др.
Рекомендуется назначение аналогов инсулина длительного и сверхдлительного действия пациентам с СД 1 для уменьшения риска гипогликемических состояний и/или вариабельности гликемии [90–101].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии: инсулин гларгин** 300 ЕД/мл и инсулин деглудек**, по сравнению с инсулином гларгин** 100 ЕД/мл характеризуются более низким риском развития гипогликемий [92,94,102].
Рекомендуется определение соответствия дозы ИКД (ИУКД, ИСБД) приему углеводов, уровню глюкозы в крови перед едой и ожидаемой физической активности пациентам с СД 1 для улучшения гликемического контроля [15,34,35,103–114].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
Комментарии: коррекция дозы инсулина должна осуществляться ежедневно с учетом данных самоконтроля гликемии в течение суток и количества углеводов в пище, до достижения индивидуальных целевых показателей гликемического контроля. Ограничений в дозе инсулина не существует. При планировании обеспечения пациента инсулином следует использовать условную среднесуточную дозу инсулина, включающую в себя не только базальный и прандиальный инсулин, но и инсулин для коррекции гипергликемии и проверки проходимости инсулиновой иглы.
Рекомендованные устройства для введения инсулина:
➣ инсулиновые шприцы 100 ЕД/мл (концентрация на флаконе инсулина должна совпадать с концентрацией на инсулиновом шприце);
➣ инсулиновые шприц-ручки:
1) с шагом дозы 1 или 0,5 ЕД;
2) готовые к употреблению (предзаполненные инсулином) или со сменными инсулиновыми картриджами.
➣ инсулиновые помпы*** (носимые дозаторы инсулина), в том числе с непрерывным мониторированием глюкозы.
Все пациенты с СД 1 должны быть обеспечены инъекторами инсулина (шприц-ручками) или помпами!
3.3.1 Техника инъекций инсулина [15]
ИКД при близком к нормальному уровню гликемии вводится за 20–30 минут до приема пищи. ИУКД (ИСБД) при близком к нормальному уровню гликемии вводится непосредственно перед приемом пищи, при необходимости можно вводить сразу после приема пищи.
При повышенном уровне гликемии перед приемом пищи рекомендуется увеличивать интервал времени от инъекции ИКД (ИУКД, ИСБД) до приема пищи.
Рекомендуемыми местами подкожных (п/к) инъекций являются:
а) живот в пределах следующих границ: примерно 1 см выше лонного сочленения, примерно 1 см ниже нижнего ребра, примерно 1 см в сторону от пупка и латерально до средне-боковой линии. Смещаться латерально по поверхности передней брюшной стенки у худых пациентов не рекомендуется, так как толщина подкожно-жировой клетчатки уменьшается, что повышает риск внутримышечного (в/м) введения. Также не следует делать инъекции/инфузию в область пупка и средней линии живота, где подкожно-жировая клетчатка тонкая;
б) передне-наружная часть верхней трети бедер;
в) верхне-наружная часть ягодиц и наружная часть поясничной области;
г) средняя наружная (боковая) треть плеч. Обычно область плеча не рекомендуется для самостоятельных инъекций из-за высокого риска в/м введения препарата (невозможно сформировать складку кожи).
При выборе мест инъекций следует учитывать тип инсулина. Предпочтительное место введения человеческого ИКД – область живота, так как в этом месте всасывание инсулина самое быстрое. НПХ-инсулины должны вводиться в ягодицу или бедро, так как эти места имеют более медленную скорость всасывания.
ИУКД (ИСБД), аналоги инсулина длительного и сверхдлительного действия можно вводить во все рекомендуемые места инъекций.
Инсулин должен вводиться в здоровую подкожно-жировую клетчатку, следует избегать внутрикожных и в/м инъекций, а также шрамов и участков липодистрофии.
В некоторых случаях предпочтительным может быть разделение относительно больших доз инсулина на две инъекции, которые выполняются одна за другой в разные места. Нет универсальной пороговой величины для разделения доз, но, как правило, за нее принимают величину 40–50 ЕД инсулина с концентрацией 100 ЕД/мл.
Всегда следует соблюдать правильное чередование мест инъекций, чтобы не допустить развития участков липодистрофии (липогипертрофии), приводящих к нарушению всасывания инсулина увеличению доз инсулина, повышению вариабельности гликемии и риска гипогликемии. Следует избегать многократного использования инсулиновых игл из-за опасности развития липодистрофии в местах инъекций. Важно делать каждую последующую инъекцию на расстоянии минимум 1 см от предыдущей инъекции и использовать все возможные места для инъекций.
Во избежание передачи инфекционных заболеваний инсулиновые шприц-ручки, картриджи для инсулиновых шприц-ручек и флаконы инсулина предназначены исключительно для индивидуального использования.
Запас инсулина должен храниться при температуре +2-8°С. Флаконы с инсулином или инсулиновые шприц-ручки, которые используются для ежедневных инъекций, могут храниться при комнатной температуре (до +30°С) в течение 4 недель (инсулин детемир** - 6 недель, инсулин деглудек** - 8 недель); перед введением инсулин должен иметь комнатную температуру.
НПХ-инсулин и готовые смеси инсулина перед введением следует тщательно перемешать, перекатывая флакон между ладонями, но не встряхивая.
Рекомендуется использовать иглы для инсулиновых шприц-ручек длиной 4-5 мм / 6-мм инсулиновые шприцы или самые короткие доступные иглы пациентам с СД 1 для минимизации риска в/м введения [115–127].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2)
Комментарии: инъекции инсулина 4-мм иглами для инсулин
Специфической медицинской реабилитации пациентам с СД 1 не требуется. В круг реабилитационных мероприятий пациентам с СД 1 могут быть включены занятия с медицинским психологом, социальная адаптация с участием специалистов и социальных работников.
Специфические методы реабилитации при наличии осложнений указаны в соответствующих разделах.
Рекомендуется рассмотреть возможность санаторно-курортного лечения пациенту с СД 1 в отсутствие значимой метаболической декомпенсации и без выраженных стадий осложнений (без синдрома диабетической стопы, хронической болезни почек (ХБП) С5) для улучшения общего состояния здоровья [183–185].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: могут быть рекомендованы санаторно-курортные организации - бальнеологические курорты с питьевыми минеральными водами и водами минеральными природными для наружного бальнеотерапевтического применения. Целесообразно использование таких факторов как диетическая терапия, ЛФК. Следует соблюдать осторожность при наличии ХБП С4, пролиферативной ДР.
На настоящий момент лекарственных препаратов для модификации течения болезни или профилактики СД 1 типа в РФ не зарегистрировано.
У родственников 1 линии родства пациентов с СД 1 типа (особенно детей) определение аутоантител может быть целесообразно для ранней диагностики СД 1 типа и профилактики манифестации заболевания с диабетическим кетоацидозом (в случае определения ≥ 2 аутоантител полезным будет обращение к врачу).
Мониторинг компенсации углеводного обмена и скрининг осложнений СД являются необходимым условием профилактики развития и прогрессирования осложнений заболевания.
Рекомендуется оценка степени выраженности нарушений углеводного обмена у родственников 1 линии родства пациентов с СД 1 типа при наличии у этих родственников ≥ 2 аутоантител с целью профилактики манифестации заболевания с диабетическим кетоацидозом [15,186,187].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: при наличии ≥ 2 аутоантител (аутоантител к инсулину (IAA), глутаматдекарбоксилазе (GAD), тирозинфосфатазе (IA-2), поверхностным антигенам (ICA), транспортеру цинка (ZnT-8) для дальнейшей диагностики у бессимптомных пациентов могут быть использованы исследование уровня гликированного гемоглобина в крови (HbA1c), исследование глюкозы плазмы натощак, проведение ПГТТ.
Рекомендуется диспансерное наблюдение у врача-эндокринолога пациентам с СД 1 типа для профилактики развития и прогрессирования осложнений заболевания и предупреждения декомпенсации углеводного обмена [15,188].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: пациенты с СД 1 типа должны находиться на диспансерном наблюдении у врача-эндокринолога с момента установления диагноза пожизненно.
Рекомендуется исследование уровня HbA1c 1 раз в 3 месяца всем пациентам с СД 1 для оценки степени достижения целевых показателей гликемического контроля и стратификации риска развития осложнений СД [15,16,34,36,76].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2)
Рекомендуется выполнение анализа крови биохимического общетерапевтического (исследование уровня общего белка в крови; исследование уровня общего кальция в крови; исследование уровня холестерина в крови; исследование уровня холестерина липопротеинов низкой плотности; исследование уровня холестерина липопротеинов высокой плотности в крови; исследование уровня триглицеридов в крови; исследование уровня общего билирубина в крови; исследование уровня мочевины в крови; исследование уровня креатинина в крови; определение активности аланинаминотрансферазы в крови; определение активности аспартатаминотрансферазы в крови; исследование уровня калия в крови; исследование уровня натрия в крови), исследование уровня глюкозы плазмы натощак всем пациентам с СД 1 не реже 1 раза в год для оценки наличия и выраженности осложнений и сопутствующих заболеваний [14,15,21].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: дополнительные биохимические исследования назначаются по показаниям. При наличии изменений в результатах анализов частота контрольных исследований и консультации специалистов определяется индивидуально.
Рекомендуется оценка рСКФ (или определение СКФ клиренсовыми методами (проба Реберга) при наличии показаний) всем пациентам с СД 1 не реже 1 раза в год для оценки функции почек [20–22].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
Комментарии: для пациентов с СД 1 и рСКФ < 60 мл/мин./1,73 м2 целесообразно проводить оценку этого показателя 2 раза в год.
Рекомендуется оценка соотношения альбумин/креатинин в моче в разовой порции (предпочтительно) или определение альбумина в разовой порции мочи (или в суточной моче) пациентам с СД 1 не реже 1 раза в год для оценки функции почек (не позднее чем через 5 лет от дебюта заболевания) [20–22].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
Комментарии: биохимический анализ утренней порции мочи проводится через 5 лет после установки диагноза, далее не реже 1 раза в год. Для пациентов с СД 1 и альбуминурией ≥ 3 мг/ммоль и/или рСКФ < 60 мл/мин./1,73 м2 целесообразно проводить оценку этого показателя 2 раза в год. Исследование проводится при отсутствии воспалительных изменений в общем анализе мочи или анализе мочи по Нечипоренко. Для расчета соотношения альбумин/креатинин в номенклатуре медицинских услуг используется «определение альбумина в моче» и «исследование уровня креатинина в моче». Оценку соотношения альбумин/креатинин в моче предпочтитеьно проводить в утренней порции.
Рекомендуются осмотры врачом-офтальмологом пациентов c СД 1 не позднее, чем через 5 лет от дебюта СД, далее не реже 1 раза в год, с целью выявления диабетических изменений сетчатки [15,189–197].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: осмотры врачом-офтальмологом могут проводиться по показаниям чаще.
Рекомендуется проведение комплексного обследования стоп (визуальный осмотр, оценка вибрационной, тактильной и температурной чувствительности нижних конечностей, определение пульсации на артериях стоп) пациентам с СД 1 не реже 1 раза в год для оценки периферической чувствительности и состояния периферических артерий [198,199].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
Комментарии: осмотр и оценка вибрационной, тактильной и температурной чувствительности нижних конечностей, определение пульсации на артериях стоп проводится не позднее, чем через 5 лет после установки диагноза СД 1, далее не реже 1 раза в год, по показаниям - чаще.
Рекомендуется регистрация ЭКГ в покое пациентам с СД 1 не реже 1 раза в год для скрининга сердечно-сосудистой патологии [15].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Рекомендуется дистанционное наблюдение врача-эндокринолога с применением телемедицинских технологий пациентов с СД 1 с целью динамического наблюдения и достижения целевых показателей гликемии, в том числе с использованием СИС ДН [200–205].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 1)
Форма - плановая; условия - стационар, дневной стационар:
➣ необходимость коррекции инсулинотерапии при декомпенсации заболевания;
➣ инициация помповой инсулинотерапии;
➣ наличие инфицированного раневого дефекта любой этиологии;
➣ критическая ишемия конечности у пациентов с заболеванием артерий нижних конечностей;
➣ развитие нефротического синдрома и значительное снижение фильтрационной функции почек;
➣ клинически значимое ухудшение основного заболевания, его осложнений и сопутствующей патологии.
Форма - экстренная, неотложная; условия - стационар:
➣ ДКА, прекома, гиперосмолярное гипергликемическое состояние (прекома, кома), гипогликемическая кома;
➣ гипогликемическое состояние, сопровождающееся дезориентацией нарушением координации движений, речи, судорог, нарушением сознания;
➣ необходимость назначения инсулина (при впервые выявленном СД 1);
➣ СД 1 при появлении признаков аллергии к препаратам инсулина;
➣ любые жизнеугрожающие состояния у пациентов с СД 1.
Показания к выписке пациента из медицинской организации:
стойкое улучшение состояния, когда пациент может без ущерба для здоровья продолжить лечение в амбулаторно-поликлиническом учреждении или домашних условиях;
при необходимости перевода пациента в другую организацию здравоохранения;
грубое нарушение режима;
по письменному требованию пациента либо его законного представителя, если выписка не угрожает жизни пациента и не опасна для окружающих. В этом случае выписка может быть произведена только с разрешения главного врача медицинского учреждения или его заместителя по лечебной работе.
Наибольшее влияние на прогноз жизни у пациентов СД оказывают развитие и прогрессирование осложнений заболевания. Принципы диагностики, лечения, реабилитации и профилактики поздних осложнений СД изложены в настоящем разделе. У пациентов с СД некоторые заболевания и состояния (например, сердечно-сосудистые заболевания) имеют отличия от таковых лиц без СД, что должно быть учтено при определении тактики ведения. Лечение пациентов с СД во время беременности имеет особенности как при выборе индивидуальных целей лечения, так и оптимальных (безопасных) схем терапии.
7.1. Острые осложнения (неотложные состояния)
Вопросы диагностики, клиники и лечения острых осложнений СД 1 излагаются в соответствующих клинических рекомендациях.
Клиника, диагностика и лечение гипогликемии изложены в разделе 3.6 «Гипогликемия».
7.2 Диабетическая нефропатия
Диабетическая нефропатия (ДН) – или диабетическая болезнь почек (ДБП) — это специфическое поражение почек при СД под воздействием метаболических, гемодинамических, воспалительных, генетических, эпигенетических факторов, приводящее к развитию терминальной почечной недостаточности (ТПН), требующей проведения заместительной почечной терапии (ЗПТ): диализа, трансплантации.
Хроническая болезнь почек (ХБП) – наднозологическое понятие, определяется как нарушение структуры или функции почек, сохраняющееся более 3 месяцев и имеющее последствия для здоровья. В случае диабетического генеза поражения почек рекомендуется применение термина «пациенты с СД и ХБП» или «ХБП при СД». ХБП классифицируется на основе причины, категории расчетной скорости клубочковой фильтрации (рСКФ) (С1-С5) (табл. 10) и категории альбуминурии (А1-А3) (табл. 11) [23].
ДН развивается у 20-40 % пациентов с СД 1 [20], в типичном случае - при длительности заболевания более 10 лет, однако при неблагоприятных факторах возможно более раннее развитие. ДН существенно повышает риск сердечно-сосудистой патологии и стоимость лечения [206].
Согласно концепции ХБП, оценка стадии почечной патологии осуществляется по величине рСКФ, признанной наиболее полно отражающей количество и суммарный объем работы нефронов, в том числе связанной с выполнением неэкскреторных функций (табл. 10). Кроме того, выделяют три категории альбуминурии (табл. 11) [23].
Таблица 10. Стадии хронической болезни почек по уровню скорости клубочковой фильтрации
Стадия |
Определение |
рСКФ (мл/мин./1,73 м2) |
|---|---|---|
11 |
Высокая и оптимальная |
≥ 90 |
21 |
Незначительно сниженная |
60-89 |
3а |
Умеренно сниженная |
45-59 |
3б |
Существенно сниженная |
30-44 |
4 |
Резко сниженная |
15-29 |
5 |
Терминальная почечная недостаточность |
< 15 |
1Для установления ХБП в этом случае необходимо наличие также и маркеров почечного повреждения. При их отсутствии ХБП не диагностируется.
Таблица 11. Классификация хронической болезни почек по уровню альбуминурии
Категория |
А/Кр1 мочи |
СЭА2 (мг/24 часа) |
Описание |
|
|---|---|---|---|---|
мг/ммоль |
мг/г |
|||
А1 |
< 3 |
< 30 |
< 30 |
Норма или незначительно повышена |
А2 |
3-30 |
30-300 |
30-300 |
Умеренно повышена |
А3 |
> 30 |
> 300 |
> 300 |
Значительно повышена3 |
1А/Кр – соотношение альбумин/креатинин в разовой порции мочи.
2 СЭА – суточная экскреция альбумина.
3 Включая нефротический синдром (СЭА > 2200 мг/24 часа [А/Кр > 2200 мг/г; > 220 мг/ммоль]).
Формулировка диагноза ДН в соответствии с классификацией ХБП:
1) ДН, ХБП С1 (2, 3, 4 или 5) А2.
2) ДН, ХБП С1 (2, 3, 4 или 5) А3.
3) ДН, ХБП С3 (4 или 5) А1 (т.е. независимо от уровня альбуминурии).
4) ДН, ХБП С5 (лечение заместительной почечной терапией).
5) В случае нормализации показателей альбуминурии на фоне нефропротективной терапии у пациентов с сохранной рСКФ ≥ 60 мл/мин./1,73 м2 - диагноз ДН, ХБП сохраняется с формулировкой: ДН, ХБП С1-2 А1 (регресс альбуминурии на фоне нефропротективной терапии).
После указания стадии ХБП необходимо указать осложнения ХБП (АГ, анемия, минерально-костные нарушения (МКН) - ХБП, электролитные нарушения) при их наличии.
Специфические симптомы ДН на стадии ХБП С1-3 А1-2 отсутствуют у большинства пациентов с СД 1 (редко отмечают эпизоды повышения АД). На стадии ХБП С4-5 отмечают слабость, сонливость, быструю утомляемость, выраженные стойкие отеки, стабильно повышенное АД, тошноту, иногда рвоту без облегчения состояния. На стадии ХБП С3-5 А3 отмечают отеки стоп, голеней, иногда бедер, лица, снижение аппетита, нарастание и постоянно повышенное АД.
Диагностика
Рекомендуется оценка соотношения альбумин/креатинин в моче в разовой порции (предпочтительно) или определение альбумина в моче (в разовой порции мочи или в суточной моче) и рСКФ у пациентов с СД 1 не позднее, чем через 5 лет от дебюта СД, далее не реже 1 раза в год, для выявления ДН [23].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: у пациентов с СД 1 и альбуминурией ≥ 3 мг/ммоль и/или рСКФ <60 мл/мин./1,73 м2 целесообразно проводить оценку этих показателей 2 раза в год. Соотношение альбумин/креатинин в разовой (предпочтительно утренней) порции мочи с высокой чувствительностью и специфичностью соотносится с суточной экскрецией альбумина с мочой. Определение в разовой порции мочи только альбумина без креатинина не дает такого точного соотношения, так как не учитывает влияние разведения мочи в силу различной гидратации. Поскольку в клинической практике продолжается оценка в разовой порции мочи только альбумина, то результаты этого исследования необходимо интерпретировать следующим образом (значения, соответствующие уровням альбуминурии согласно классификации ХБП): не более 20 мг/л – А1; >20 до 200 мг/л - А2; > 200 мг/л - А3.
Комбинированный риск сердечно-сосудистых событий и терминальной почечной недостаточности у пациентов с ХБП в зависимости от категории рСКФ и альбуминурии представлен в Приложении Г [207].
Рекомендуется оценка потенциальных осложнений ХБП у пациентов с СД 1 и рСКФ < 60 мл/мин./1,73 м2 (АГ, перегрузка объемом, электролитные нарушения, метаболический ацидоз, анемия, минеральные и костные нарушения) для своевременной инициации их терапии [208].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Рекомендуется незамедлительное обращение пациентов с СД 1 к врачу-нефрологу при быстром прогрессировании почечной патологии для определения этиологии и терапии [209].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии: диагностика ДН основывается на наличии повышенной альбуминурии и/или снижении рСКФ при отсутствии симптомов первичной почечной патологии. Типичная картина включает длительный анамнез заболевания, наличие ДР, альбуминурию без гематурии и быстрого снижения рСКФ. Однако нередко у пациентов с СД 1 снижение рСКФ может происходить на фоне нормоальбуминурии [210]. С учетом вариабельности для установления диагноза ДН необходимо не менее, чем 2-кратное исследование соотношения альбумин/креатинин или концентрации альбумина в разовой порции мочи (только количественными методами) в период от 1 до 3 месяцев. Преходящее повышение экскреции альбумина возможно при значительной гипергликемии, интенсивной физической нагрузке, высокобелковом питании, лихорадке, менструации. рСКФ вычисляется с учетом уровня креатинина плазмы с использованием валидизированной формулы (предпочтительно формула CKD-EPI, наилучшим образом соотносящаяся с референтными (клиренсовыми) методами определения). Согласно обновленной версии Клинического практического руководства KDIGO (Kidney Disease: Improving Global Outcomes 2024) если доступен цистатин C, категорию рСКФ следует оценивать по комбинации креатинина и цистатина C [рСЕФ кр-цис] [23]. Обоснование использования комбинации креатинина и цистатина С в уравнении рСКФ заключается в том, что ни одно из этих двух соединений не является идеальным маркером для оценки клиренса. Креатинин, напрямую связанный с мышечной массой, может вводить в заблуждение при крайних вариантах телосложения или определенных состояниях (травмы спинного мозга, саркопения). На цистатин С также влияют различные факторы: употребление стероидов, патология щитовидной железы, онкологические заболевания. Комбинация креатинина и цистатина С в расчетной формуле дает более точные оценки рСКФ по сравнению с измерениями с использованием отдельно каждого. Определение СКФ клиренсовыми методами (включая исследование функции нефронов по клиренсу креатинина (проба Реберга)) необходимо при беременности, морбидном ожирении (ИМТ ≥40 кг/м2), дефиците массы тела (ИМТ ≤15 кг/м2), вегетарианстве, миодистрофии, параплегии, квадриплегии, нестандартных размерах тела (ампутированные конечности), почечном трансплантате, назначении нефротоксичных препаратов, определении начала заместительной почечной терапии. При быстро нарастающей альбуминурии, внезапном развитии нефротического синдрома, быстром снижении рСКФ, отсутствии ДР, изменении осадка мочи (гематурия, лейкоцитурия, цилиндрурия) можно предположить альтернативную или дополнительную причину почечной патологии.
Лечение
Всех пациентов с СД 1 и ХБП следует лечить по комплексному плану для оптимизации питания, физической активности, отказа от курения и снижения веса (при избытке или ожирении). Фармакологические методы лечения, основанные на доказательствах, направлены на сохранение функции органов, улучшение кардиоваскулярного прогноза, нормализацию активности РААС и достижение промежуточных целевых показателей гликемии, АД и липидов, контроль хронического воспаления и фиброза, предотвращение развития и прогрессирования осложнений ХБП (анемии, электролитных нарушений, минерально-костных нарушений и др.), отсрочку инициации ЗПТ.
Рекомендуется потребление белка не более 0,8 г/кг массы тела в сутки недиализным небеременным пациентам с СД 1 с ХБП С3-5 и/или А3 для замедления прогрессирования осложнения [211].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии: потребление такого количества белка в сравнении с большим уровнем замедляет снижение рСКФ. Диета, содержащая более 1,3 г/кг/сут. ассоциирована с усилением альбуминурии, быстрым снижением почечной функции, кардиоваскулярной смертностью. Потребление белка не более 0,8 г/кг/сут не влияет на контроль гликемии, сердечно-сосудистый риск и снижение рСКФ. Для пациентов на диализе необходимо более высокое потребление белка, так как нарушение питательного статуса – важная проблема диализных пациентов [212].
У пожилых людей целевые показатели суточного потребления белка следует устанавливать после тщательной индивидуальной оценки питания и метаболического статуса. Допустимо потребление белка в количестве 1,0–1,2 г/ кг массы тела в сутки пожилым пациентам со стабильной или медленно прогрессирующей ХБП для предотвращения развития белково-энергетической недостаточности и саркопении [213,214].
Рекомендуется пациентам с СД 1 и ХБП, проходящим лечение на диализе, увеличить потребление белка до 1,0-1,2 г/кг массы тела в сутки для предотвращения его усиленного катаболизма и потери в диализате [215–217].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: потери аминокислот во время гемодиализа и в особенности перитонеального диализа были многократно задокументированы в различных РКИ. В дополнение, возникающая уремия у пациентов с ХБП приводит к снижению аппетита, и, как следствие, потере не только жировой, но и мышечной массы.
Рекомендуется ограничение потребления натрия до 2,3 г/сут. пациентам с СД 1 и ХБП для контроля АД, снижения сердечно-сосудистого риска [218,219].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии: 2,3 г натрия соответствует 5 г поваренной соли.
Рекомендуется ограничение потребления калия пациентам с СД 1 и ХБП для снижения риска гиперкалиемии [220].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
Комментарии: потребление натрия и калия необходимо индивидуализировать с учетом коморбидности, применяемых препаратов, уровня АД и лабораторных данных.
Рекомендуется физическая активность умеренной интенсивности соответственно сердечно-сосудистой и физической толерантности пациентам с СД 1 и ХБП для снижения риска прогрессирования ДН, общей и сердечно-сосудистой смертности [221,222].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
Комментарии: у пациентов с СД 1 и ХБП, как и в общей популяции, регулярная и достаточная физическая активность обеспечивает кардиометаболические, ренальные и когнитивные преимущества, повышает качество жизни, улучшает чувствительность к инсулину, понижает уровень маркеров воспаления и улучшает функцию эндотелия. Однако пациенты с ХБП имеют ограничения, препятствующие участию в регулярных упражнениях и в деятельности высокой интенсивности, прежде всего, связанные с возрастом и, следовательно, с риском падения. Потеря мышечной массы и развитие таких осложнений, как анемия, периферическая нейропатия, автономная нейропатия, лимитируют функциональные способности этих пациентов параллельно снижению почечной функции. Несмотря на такие ограничения, рекомендация физической активности во время обычного визита важна для пациентов практически во всех ситуациях, несмотря на конкурирующие проблемы и недостаток конкретных ресурсов. До реализации программы физической активности необходимо провести оценку физической толерантности, риска нежелательных явлений (прежде всего, падения), а также доступности с учетом выраженности АССЗ.
Рекомендуется оптимизировать контроль гликемии пациентам с СД 1 для снижения риска или замедления прогрессирования ДН [34,35,223,224].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
Комментарии: у пациентов с выраженными стадиями ХБП целевой уровень HbA1c должен быть индивидуализирован с учетом высокого риска гипогликемии. Целевой уровень HbA1c для пациентов, получающих диализную терапию, не установлен в связи с тем, что достоверность HbA1c как показателя компенсации углеводного обмена ограничена из-за уменьшения периода полужизни эритроцитов, изменения их свойств под воздействием метаболических и механических факторов, влияния терапии. Тем не менее, необходимость контроля гликемии очевидна при большой осторожности при его интенсификации с учетом повышенного риска сердечно-сосудистой смертности в соответствии с выраженностью почечной дисфункции. Контроль гликемии при проведении сеансов гемодиализа должен проводиться ежечасно. Возможно проведение исследования уровня глюкозы в крови методом непрерывного мониторирования с целью оптимизации гликемического контроля.
Рекомендуется оптимизировать контроль АД пациентам с СД 1 для снижения риска или замедления прогрессирования ДН [225].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4)
Рекомендуется прием ингибиторов ангиотензинпревращающего фермента (иАПФ) (АТХ - классификация C09AA Ингибиторы АПФ) для небеременных пациентов с СД 1 и АГ, и/или повышенным соотношением альбумин/креатинин в моче (≥ 3 мг/ммоль) для замедления прогрессирования ДН [15,208,225,226].
Уровень убедительности рекомендаций А (уровень убедительности доказательств – 2)
Комментарии: режим дозирования иАПФ должен быть индивидуальным с учетом показателей рСКФ пациента и особенностей фармакокинетики препаратов, указанных в инструкции.
Рекомендуется прием иАПФ или блокаторов рецепторов ангиотензина II (БРА) (АТХ - классификация C09CA Антагонисты рецепторов ангиотензина II) для небеременных пациентов с СД 1 и АГ и/или повышенным соотношением альбумин/креатинин в моче (≥ 3 мг/ммоль) и/или рСКФ < 60 мл/мин./1,73 м2 для замедления прогрессирования ДН [15,208].
Уровень убедительности рекомендаций C (уровень убедительности доказательств – 5)
Комментарии: рекомендации профильных международных ассоциаций не разделяют лечение ДН при СД 1 и СД 2 и рекомендуют пациентам вышеупомянутой группы прием иАПФ и БРА, экстраполируя на обе группы результаты рандомизированных клинических исследований (РКИ), доказавших нефропротективный эффект этих препаратов [208]. Следует избегать комбинированной терапии иАПФ и БРА пациентам с СД 1 и ДН для профилактики гиперкалиемии или острого повреждения почек.
Рекомендуется исследование в динамике уровня креатинина в крови и уровня калия в крови пациентам с СД 1, получающим иАПФ или БРА и диуретики (АТХ-классификация С03) для оценки безопасности терапии [220,227].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии. Не следует отменять иАПФ или БРА при повышении креатинина ≤ 30 % в отсутствие гиповолемии.
Рекомендуется контроль соотношения альбумин/креатинин в моче в разовой порции (предпочтительно) или определение альбумина в моче (в разовой порции мочи или в суточной моче) пациентам с СД 1 с альбуминурией, получающим иАПФ или БРА для оценки эффективности лечения и прогрессирования ДН [228].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Не рекомендуется прием иАПФ или БРА пациентам с СД 1 при нормальном АД, соотношении альбумин/креатинин мочи < 3 мг/ммоль или альбуминурии < 20 мг/л (30 мг/сут.), нормальной рСКФ для первичной профилактики ДН ввиду отсутствия доказательств эффективности [229].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
Комментарии: АГ – значимый фактор риска развития и прогрессирования ХБП. Антигипертензивная терапия снижает риск альбуминурии и сердечно-сосудистых событий. У пациентов с установленной ХБП (рСКФ < 60 мл/мин./1,73 м2 и соотношением альбумин/креатинин мочи > 30 мг/ммоль) иАПФ и БРА снижают риск прогрессирования до терминальной ХБП. Уровень АД менее 130/80 мм рт.ст. может рассматриваться как целевой на основе индивидуальных преимуществ и рисков. иАПФ и БРА – препараты первой линии для лечения АГ у пациентов с СД 1, АГ, рСКФ < 60 мл/мин./1,73 м2 и соотношением альбумин/креатинин мочи > 30 мг/ммоль, поскольку имеют доказанные преимущества в профилактике прогрессирования ХБП. иАПФ и БРА имеют сопоставимые преимущества и риски. При более низком уровне альбуминурии (соотношение альбумин/креатинин 3-30 мг/ммоль) терапия иАПФ и БРА демонстрирует снижение прогрессирования до более высокого уровня альбуминурии (соотношение альбумин/креатинин мочи > 30 мг/ммоль) и сердечно-сосудистых событий, но не прогрессирования до терминальной ХБП. При отсутствии ХБП, иАПФ и БРА используются для контроля АД, но не имеют преимуществ по сравнению с другими классами антигипертензивных препаратов, включая блокаторы кальциевых каналов, тиазидные диуретики. В исследованиях, включавших пациентов с СД 1 без АГ и альбуминурии, иАПФ и БРА не предотвращали развитие диабетической гломерулопатии, оцененной по биопсии почки. Антагонисты рецепторов минералокортикоидов эффективны в лечении резистентной АГ, снижают альбуминурию по данным непродолжительных исследований пациентов с ХБП и могут иметь дополнительные сердечно-сосудистые преимущества. Однако они увеличивают риск эпизодов гиперкалиемии в двойной терапии (в комбинации с иАПФ или БРА).
Рекомендуется терапия ингибиторами 3-гидрокси-3-метилглутарил-коэнзим А-( ГМГ-КоА) редуктазы (АТХ-классификация С10АА Ингибиторы ГМГ-КоА-редуктазы) (статинами) умеренной интенсивности для всех пациентов с СД 1 и ХБП для первичной профилактики АССЗ или высокой интенсивности для пациентов с известными АССЗ и множественными факторами риска АССЗ с подключением эзетемиба (АТХ-классификация С10АХ другие гиполипидемические препараты) или ингибиторов пропротеиновой конвертазы субтилизин-кексина типа 9 (PCSK9) (АТХ-классификация С10АХ другие гиполипидемические препараты) при недостижении целевого уровня ЛПНП [230].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: дислипидемия является частым осложнением ХБП, а ее коррекция – сложная задача. Уремическое состояние приводит к различным изменениям количества и качества циркулирующих липопротеинов. Даже небольшое снижение рСКФ связано с более высокими уровнями триглицеридов и снижением концентрации ЛПВП в сыворотке. Дислипидемия связана с прогрессированием ХБП. Липиды, в свою очередь, могут откладываться в почках, что приводит к изменениям, которые включаются в термин «липоидная нефротоксичность» с прямым повреждением подоцитов. В консенсусном документе ADA (American Diabetes Association) и KDIGO (Kidney Disease: Improving Global Outcomes) контроль липидов занял очень сильные позиции. Ингибиторы 3-гидрокси-3-метилглутарил-коэнзим А-редуктазы (статины) в первую очередь нацелены на снижение уровня холестерина ЛПНП. Их преимущества для первичной и вторичной профилактики сердечно-сосудистых событий были надежно установлены для населения в целом. Результаты РКИ, включавших пациентов с ХБП, показали необходимость терапии статинами для снижения риска сердечно-сосудистых заболеваний, несмотря на снижение ее эффективности при прогрессировании ХБП и отсутствие существенного влияния на функцию почек [231]. Некоторым пациентам рекомендуется интенсификация терапии статинами, добавление эзетимиба и/или ингибиторов PCSK-9 (на основании риска АСССЗ и достигнутых концентраций холестерина ЛПНП). Использование ингибиторов PCSK-9 следует расширять при условии нарастания доказательств РКИ. Влияние фармакологических вмешательств, отличных от статинов, на прогрессирование ХБП в значительной степени еще не определено.
Рекомендуется терапия омега-3 кислотами этиловыми эфирами (АТХ классификация С10АХ другие гиполипидемические препараты) в сочетании с интенсификацией изменения образа жизни, оптимизацией гликемического контроля для пациентов с СД 1 и ХБП и гипертриглицеридемией для снижения уровня триглицеридов [230].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: пациентам с высоким уровнем триглицеридов или низким уровнем ЛПВП необходима интенсификация изменения образа жизни, оптимизация гликемического контроля, а затем рассмотрение вопроса о назначении омега-3 кислот этиловых эфиров (АТХ классификация С10АХ другие гиполипидемические препараты). Метаанализ 10 РКИ с участием 344 участников с СД1 и СД2 продемонстрировал, что применение омега-3 жирных кислот в течение минимум 24 недель снижает уровень триглицеридов. Кроме того, у участников метаанализа с СД1 продемонстрировано значимое повышение ЛПВП по сравнению с группой плацебо (р=0,04) [232]. В РФ зарегистрирован препарат Омега-3 кислот этиловых эфиров, содержащий полиненасыщенные жирные кислоты семейства омега-3: эйкозапентаеновую и докозагексаеновую кислоты.
Рекомендуется терапия осложнений ХБП у пациентов с СД 1 и рСКФ < 60 мл/мин./1,73 м2 для замедления их прогрессирования [208].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: подробные рекомендации по лечению осложнений ХБП (включая немедикаментозные) см. в соответствующих клинических рекомендациях.
Рекомендуется оценить сроки и возможности заместительной почечной терапии у пациентов с СД 1 и рСКФ < 30 мл/мин./1,73 м2 для ее плановой инициации [209].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 3)
Комментарии: консультации врача-нефролога пациентов с СД 1 и ХБП С4 (рСКФ < 30 мл/мин./1,73 м2) могут снизить затраты, улучшить обслуживание и отсрочить диализную терапию [209].
Профилактика ДН возможна только при своевременном определении и коррекции факторов риска развития и прогрессирования осложнения.
Диспансерное наблюдение включает мониторинг в зависимости от стадии ДН (табл. 12).
Таблица 12. Мониторинг в зависимости от стадии диабетической нефропатии [15]
Стадия ДН |
Параметры контроля |
Частота определений |
|---|---|---|
ХБП C1-2 А2-А3 |
|
1 раз в 3 мес. |
|
2 раза в год |
|
|
Ежедневно |
|
|
1 раз в год |
|
|
1 раз в год при нормальных значениях; через 4-12 нед. в случае инициации терапии статинами (АТХ-классификация C10AA Ингибиторы ГМГ-КоА-редуктазы) или изменения дозы, далее – 1 раз в год |
|
|
1 раз в год при наличии анемии |
|
|
Рекомендации врача-кардиолога |
|
|
Рекомендации врача-офтальмолога |
|
|
При каждом посещении врача |
|
|
ХБП С3 А1-А3 |
|
1 раз в 3 мес. |
|
2 раза в год |
|
|
Ежедневно |
|
|
1 раз в 6-12 мес. |
|
|
1 раз в год По показаниям |
|
|
1 раз в год при нормальных значениях; через 4-12 нед. в случае инициации терапии статинами или изменения дозы, далее – 1 раз в год |
|
|
1 раз в 6 мес. (чаще – в начале лечения средствами, стимулирующими эритропоэз (АТХ-классификация B03XA Другие антианемические препараты), и препаратами железа) |
|
|
Рекомендации врача-кардиолога |
|
|
Рекомендации врача-офтальмолога |
|
|
Рекомендации врача-невролога |
|
|
При каждом посещении врача |
|
|
ХБП С4 А1-3 |
|
1 раз в 3 мес. |
|
2 раза в год |
|
|
Ежедневно |
|
|
1 раз в 3 мес. |
|
|
1 раз в 6-12 мес. |
|
|
1 раз в год По показаниям |
|
|
1 раз в 6 мес. год при нормальных значениях; через 4-12 нед. в случае инициации терапии статинами или изменения дозы, далее – 1 раз в 6 мес. |
|
|
1 раз в 3 мес. (1 раз в мес. в начале лечения средствами, стимулирующими эритропоэз, и препаратами железа) |
|
|
Рекомендации врача-кардиолога |
|
|
Рекомендации врача-офтальмолога |
|
|
Рекомендации врача-невролога |
|
|
При каждом посещении |
|
|
1 раз в 6 мес. |
|
|
1 раз в 6 мес. |
|
|
ХБП С5 А1-3 (без ЗПТ) |
|
1раз в 3 мес. |
|
1 раз в 3 мес. |
|
|
Ежедневно |
|
|
1 раз в мес. 1 раз в 3 мес. |
|
|
1 раз в 3 мес. 1 раз в 6 мес. |
|
|
1 раз в год По показаниям |
|
|
1 раз в 6 мес. При нормальных значениях; через 4-12 нед. В случае инициации терапии статинами или изменения дозы, далее – 1 раз в 6 мес. |
|
|
1 раз в 3 мес. (1 раз в мес. – в начале лечения средствами, стимулирующими эритропоэз и препаратами железа) |
|
|
Рекомендации врача-кардиолога |
|
|
Рекомендации врача-офтальмолога |
|
|
Рекомендации врача-невролога |
|
|
При каждом посещении |
|
|
1 раз в 3 мес. |
|
|
1 раз в 6 мес. |
Рекомендуется сочетанная трансплантация почки и панкреато-дуоденального комплекса (СТПиПДК) пациентам с СД 1 и терминальной стадией ХБП для предотвращения развития диабетической нефропатии почечного трансплантата и улучшения качества жизни [233–241].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
Комментарии: продемонстрировано, что успешная СТПиПДК снижает риск развития диабетической нефропатии в почечном трансплантате. Так, в долгосрочной перспективе у пациентов после СТПиПДК отмечается лучшая выживаемость аллотрансплантата почки вследствие поддержания стойкой нормогликемии, что сопровождается снижением риска сердечнососудистых событий по сравнению с пациентами после изолированной трансплантации почки [235]. Успешная СТПиПДК приводит к достижению и поддержанию нормогликемии без инсулинотерапии, а также нормализации почечной функции, что как правило сопровождается положительной динамикой течения осложнений ХБП и значимо улучшает качество жизни пациентов с СД1 и терминальной стадией ХБП. Рекомендуется выполнение СТПиПДК у пациентов с СД 1 и терминальной стадией ХБП квалифицированными врачами-хирургами, имеющими большой опыт в выполнении таких операций, основывая решение о проведении операции, включая подготовку к ней, на мнении мультидисциплинарной команды (включая врача-эндокринолога, врача-нефролога, врача-хирурга, врача-терапевта/врача-кардиолога, при необходимости - других специалистов) с целью улучшения исходов [241].
7.3 Диабетическая ретинопатия
При СД поражение сетчатки проявляется виде диабетической ретинопатии (ДР) и/или диабетического макулярного отека (ДМО). Подробные данные по ведению пациентов с диабетической ретинопатией и ДМО представлены в соответствующих клинических рекомендациях [242]. Для врача-эндокринолога принципиально обеспечить своевременную выявляемость, регулярное наблюдение пациентов с ДР и ДМО и коррекцию факторов риска.
Диабетическая ретинопатия (ДР) — специфичное позднее нейромикрососудистое осложнение СД, развивающееся, как правило, последовательно от изменений, связанных с повышенной проницаемостью и окклюзией ретинальных сосудов до появления новообразованных сосудов и фиброглиальной ткани.
Диабетический макулярный отек (ДМО) — утолщение сетчатки, связанное с накоплением жидкости в межклеточном пространстве нейроэпителия вследствие нарушения гематоретинальных барьеров и несоответствия между транссудацией жидкости и способности к ее реабсорбции. ДМО может развиться при любой стадии ДР.
В основе патогенеза ДР лежит ишемия, развивающаяся из-за окклюзии капилляров сетчатки. Причиной нарушения перфузии сетчатки является поражение эндотелия сосудов (эндотелиальный стресс) в условиях гипергликемии, приводящее к образованию тромбов в капиллярном русле. Ишемия сетчатки приводит к повышению экспрессии сосудистого эндотелиального фактора роста VEGF (vascular endothelial growth factor). Увеличение выработки VEGF выше критического уровня способствует развитию основных клинических проявлений диабетического поражения сетчатки – ДМО и неоваскуляризации [243,244].
Частота развития ДР определяется длительностью СД. При длительности СД 1 более 20 лет ДР диагностируется более чем у 88 % пациентов [190], при этом почти у половины выявляется пролиферативная ДР. Частота ДМО увеличивается с тяжестью ДР и с длительностью СД: при непролиферативной ДР - в 2-6 %, при препролиферативной – в 20-63 %, при пролиферативной – в 70-74 % случаев. В РФ на 01.01.2023 г. ДР была зарегистрирована у 28,92 % пациентов с СД 1 [245].
Классификация ДР, предложенная Kohner E. и Porta M. (1991), выделяет три основных стадии заболевания [246]:
непролиферативная ДР;
препролиферативная ДР;
пролиферативная ДР.
Клинические изменения, характерные для каждой стадии ДР, п













