Рак легкого (РЛ) – собирательное понятие, объединяющее различные по происхождению, гистологической структуре, клиническому течению и результатам лечения злокачественные эпителиальные опухоли из покровного эпителия слизистой оболочки бронхов, бронхиальных слизистых желез бронхиол и легочных альвеол [1, 2].
У подавляющего большинства пациентов, страдающих от РЛ (85-90%) развитие заболевания связано с курением, как активным, так и пассивным. Кроме того, к факторам риска можно отнести облучение (проведенную ранее лучевую терапию (ЛТ) по поводу других опухолей внутригрудной локализации), воздействие радона, асбеста, мышьяка [3].
По заболеваемости РЛ занимает 1-е место среди других злокачественных опухолей у мужчин в России, а по смертности – 1-е место среди мужчин и женщин как в России, так и в мире.
В России в 2022 г. с впервые выявленным установленным диагнозом РЛ взято на учет 44981 случай. Летальность на первом году составляет 44,8% [4]. От него ежегодно умирает больше пациентов, чем от рака простаты, молочной железы и толстой кишки вместе взятых [5].
Злокачественное новообразование бронхов и легкого (C34)
C34.0 Злокачественное новообразование главного бронха
C34.1 Злокачественное новообразование верхней доли, бронхов или легкого
C34.2 Злокачественное новообразование средней доли, бронхов или легкого
C34.3 Злокачественное новообразование нижней доли, бронхов или легкого
C34.8 Злокачественное новообразование бронхов или легкого, выходящее за пределы одной и более вышеуказанных локализаций
C34.9 Злокачественное новообразование бронхов или легкого неуточненной локализации
Международная гистологическая классификация (2021) [6]
Код МКБ-О Классификация эпителиальных опухолей легкого ВОЗ (2021)
Папилломы
8052/0 Плоскоклеточная папиллома БДУ
8053/0 Плоскоклеточная папиллома инвертированного типа
8260/0 Железистая папиллома
8560/0 Смешанная плоскоклеточно-железистая папиллома
Аденомы
8832/0 Склерозирующаяся пневмоцитома
8251/0 Альвеолярная аденома
8260/0 Папиллярная аденома
8140/0 Бронхиолярная аденома/реснитчатая микронодулярная муконодулярная папиллярная опухоль*
8470/0 Муцинозная цистаденома
8480/0 Аденома слизистых желез
Прединвазивные железистые процессы
8250/0 Атипичная аденоматозная гиперплазия
8250/2 Аденокарцинома in situ немуцинозная
8253/2 Аденокарцинома in situ муцинозная
Аденокарциномы
8256/3 Минимально инвазивная аденокарцинома, немуцинозная
8257/3 Минимально инвазивная аденокарцинома, муцнозная
8250/3 Стелющаяся аденокарцинома
8551/3 Ацинарная аденокарцинома
8260/3 Папиллярная аденокарцинома
8265/3 Микропапиллярная аденокарцинома
8230/3 Солидная аденокарцинома
8253/3 Инвазивная муцинозная аденокарцинома
8254/3 Смешанная инвазивная муцинозная и немуцинозная аденокарцинома
8480/3 Коллоидная аденокарцинома
8333/3 Фетальная аденокарцинома
8144/3 Аденокарцинома кишечного типа
8140/3 Аденокарцинома БДУ
Прединвазивные плоскоклеточные процессы
8070/2 Плоскоклеточный рак in situ
8077/0 Слабая плоскоклеточная дисплазия
8077/2 Умеренная плоскоклеточная дисплазия
8077/2 Тяжелая плоскоклеточная дисплазия
Плоскоклеточные карциномы
8070/3 Плоскоклеточный рак БДУ
8071/3 Плоскоклеточный ороговевающий рак
8072/3 Плоскоклеточный неороговевающий рак
8083/3 Базалоидный плоскоклеточный рак
8082/3 Лимфоэпителиальный рак
Нейроэндокринные новообразования Прединвазивный процесс
8040/0 Диффузная идиопатическая легочная нейроэндокринноклеточная гиперплазия
Нейроэндокринные опухоли
8240/3 Карциноид БДУ/нейроэндокринная опухоль БДУ
8240/3 Типичный карциноид/нейроэндокринная опухоль G1
8249/3 Атипичный карциноид/нейроэндокринная опухоль G2
Нейроэндокринные карциномы
8041/3 Мелкоклеточный рак
8045/3 Комбинированный мелкоклеточный рак
8013/3 Крупноклеточный нейроэндокринный рак
8013/3 Комбинированный крупноклеточный нейроэндокринный рак
Другие эпителиальные опухоли
8012/3 Крупноклеточный рак БДУ
8560/3 Железисто-плоскоклеточный рак
8022/3 Плеоморфный рак
8032/3 Веретеноклеточный рак
8031/3 Гигантоклеточный рак
8980/3 Карциносаркома
8972/3 Легочная бластома
8023/3 NUT-карцинома
8044/3 Торакальная SMARCA4-дефицитная недифференцированная опухоль*
Опухоли по типу новообразований слюнных желез
8430/3 Мукоэпидермоидный рак
8200/3 Аденокистозный рак
8562/3 Эпителиально-миоэпителиальный рак
8940/0 Плеоморфная аденома
8982/0 Миоэпителиома
8982/3 Миоэпителиальный рак
8310/3 Гиалинизирующийся светлоклеточный рак
Клинико-анатомическая классификация
Центральный рак легкого локализуется в бронхах (главном, промежуточном, долевом, сегментарном, субсегментарном). По направлению роста различают экзофитный (эндобронхиальный) рак, при котором опухоль растет в просвет бронха; эндофитный (экзобронхиальный) рак, при котором опухоль растет преимущественно в толщу легочной паренхимы; разветвленный рак с муфтообразным перибронхиальным ростом опухоли вокруг бронхов, а также опухоли со смешанным характером роста с преобладанием того или иного компонента [1, 2].
Периферический рак легкого локализуется в периферических отделах легкого.
Различают узловую форму опухоли, пневмониеподобный рак и рак верхушки легкого с синдромом Панкоста [1, 2].
Атипичные формы рака легкого: медиастинальная форма, милиарный канцероматоз [8, 9]
Стадирование
Для определения стадии РЛ используется Международная классификация стадий злокачественных новообразований TNM (от Tumor, Nodus и Metastasis) (9-е издание, 2024) [6, 7] (табл. 1).
T – первичная опухоль
Tх – первичная опухоль не может быть оценена или опухоль верифицирована путем обнаружения злокачественных клеток в мокроте или лаваже, при этом опухоль не визуализируется при бронхоскопии.
Т0 – первичная опухоль не определяется.
Tis – карцинома in situ.
Т1 – опухоль достигает 30 мм в диаметре или менее в наибольшем измерении, окружена легочной паренхимой или висцеральной плеврой, нет признаков инвазии проксимальнее долевого бронха при бронхоскопии (это значит, что опухоль не расположена в главном бронхе).
Т1mi – минимально инвазивная аденокарцинома.
T1а – опухоль 10 мм в диаметре или менее в наибольшем измерении.
T1b – опухоль от 10 до 20 мм в диаметре в наибольшем измерении.
Т1с – опухоль от 20 до 30 мм в диаметре в наибольшем измерении.
Т2 – опухоль от 31 до 50 мм в диаметре в наибольшем измерении или опухоль в сочетании с вовлечением главного бронха, независимо от расстояния до карины, но без ее поражения; с поражением висцеральной плевры; с ателектазом или обструктивным пневмонитом, который располагается в прикорневых отделах, вовлекает часть или все легкое.
Т2а – опухоль от 31 до 40 мм в диаметре в наибольшем измерении или опухоль, размер которой не может быть определен (например, если опухоль неотделима от ателектаза).
Т2b – опухоль от 41 до 50 мм в диаметре в наибольшем измерении.
Т3 – опухоль от 51 до 70 мм в диаметре в наибольшем измерении или прямая инвазия в грудную стенку (включая париетальную плевру и опухоли верхней борозды), диафрагмальный нерв, париетальный перикард, а также метастатические узлы (узел) в той же доле.
Т4 – опухоль более 70 мм в диаметре в наибольшем измерении или поражение диафрагмы, средостения, сердца, крупных сосудов, трахеи, возвратного гортанного нерва, пищевода, тела позвонка, бифуркации трахеи, висцерального перикарда, а также метастатические узлы (узел) в других ипсилатеральных долях.
N – вовлечение регионарных лимфатических узлов
Nx – невозможно дать оценку регионарных лимфатических узлов.
N0 – нет метастазов в регионарных лимфатических узлах.
N1 – метастазы в ипсилатеральных перибронхиальных и/или ипсилатеральных корневых лимфатических узлах или метастазы во внутрилегочных лимфатических узлах, включая прямое поражение лимфатических узлов
N2 – метастазы в ипсилатеральных медиастинальных и/или субкаринальных лимфатических узлах.
N2а – поражены лимфатические узлы одного коллектора N2
N2b – множественное вовлечение лимфатических узлов коллектора N2
N3 – метастазы в контралатеральных медиастинальных, контралатеральных корневых, ипсилатеральных или контралатеральных любых лестничных или надключичных лимфатических узлах.
M – отдаленные метастазы
М0 – нет отдаленных метастазов.
М1 – отдаленные метастазы есть.
М1а – опухолевые узлы в контралатеральном легком, опухолевое узелковое поражение плевры, метастатический плевральный или перикардиальный выпот.
M1b – одиночный отдаленный опухолевый узел.
М1с – множественные внелегочные метастазы в одном или нескольких органах.
М1с1 – множественные метастазы в пределах одного органа или системы
М1с2 – множественные метастазы в нескольких органах
Для уточнения локализации отдаленного метастатического очага (М) применяют дополнительную градацию:
PUL – легкое PER – брюшная полость
MAR – костный мозг BRA – головной мозг
OSS – кости SKI – кожа
PLE – плевра LYM – лимфатические узлы
ADP – почки SADP – надпочечники
HEP – печень OTH – другие
При клинической оценке распространенности опухолевого процесса перед символами TNM ставится «с», а при патогистологической классификации – «р». Требования к определению категории pT, pN, pM аналогичны таковым для категории сT, сN, сM. Символ рN может быть оценен при исследовании не менее 6 лимфатических узлов, 3 из которых средостенные, из них 1 – бифуркационный.
Таблица 1. Стадирование рака легкого по международной классификации стадий злокачественных новообразований TNM (9-е издание, 2024)
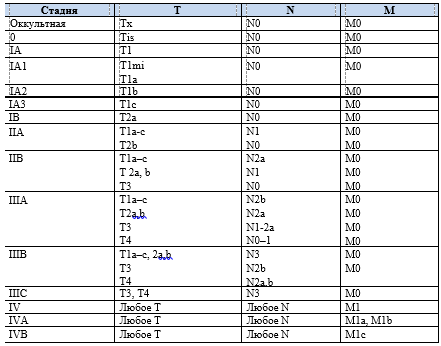
Сокращения: T – первичная опухоль, N – вовлечение регионарных лимфатических узлов, M – отдаленные метастазы.
Для мелкоклеточного рака легкого (МРЛ) может применяться упрощенная классификация по степени распространенности: локализованная форма и распространенная форма. Локализованная форма характеризуется распространенностью опухолевого процесса в одном легком и средостении, в пределах гемиторакса и возможностью облучения одним полем.
Клинические симптомы опухолевого поражения могут сочетаться с симптомами сопутствующих осложнений. Первичные симптомы – кашель, одышка, боль в груди, кровохарканье, общие симптомы – слабость, утомляемость, снижение аппетита. Вторичные симптомы появляются в результате сопутствующих воспалительных осложнений, регионарного или отдаленного метастазирования, инвазии прилежащих органов [9]. К клиническим проявлениям относятся также паранеопластические синдромы. Возможно и бессимптомное течение РЛ.
Критерии установления диагноза: при наличии результатов комплексного обследования по оценке распространенности опухолевого процесса и морфологической верификации диагноз «рак легкого» считается доказанным. Если в силу каких-либо обстоятельств провести морфологическую верификацию диагноза не представляется возможным, то на основании клинико-рентгенологической картины, по решению консилиума, может быть определена тактика лечения.
Наименования медицинских услуг по НМУ представлены в Приложении А3 (Таблица А3-1. Термины, описывающие процедуры в клинической рекомендации и возможные (наиболее близкие) термины из действующей номенклатуры медицинских услуг).
Выраженность клинической симптоматики при РЛ зависит от клинико-анатомической формы новообразования, его гистологической структуры, локализации, размеров и типа роста опухоли, характера метастазирования, сопутствующих воспалительных изменений в бронхах и легочной ткани [1,9].
Кашель при центральном РЛ у большинства пациентов сухой, временами надсадный. С нарастанием обтурации бронха кашель может сопровождаться мокротой слизистого или слизисто-гнойного характера.
Кровохарканье может проявляться в виде прожилок алой крови в мокроте или в виде диффузно окрашенной мокроты.
Одышка выражена тем ярче, чем крупнее просвет пораженного бронха при центральном раке, или ее выраженность зависит от размера периферической опухоли, т.е. степени сдавления анатомических структур средостения, особенно крупных венозных стволов, бронхов и трахеи.
Боль в грудной клетке различной интенсивности на стороне поражения может быть обусловлена локализацией новообразования в плащевой зоне легкого, особенно при прорастании опухолью плевры и грудной стенки, а также наличием плеврального выпота или ателектаза легкого с признаками обтурационного пневмонита.
При наличии периферического рака верхушки легкого может наблюдаться симптомокомплекс, описанный Панкостом (H. Pancoast) в 1924 г. (боль в участке плечевого сустава и плеча, атрофия мышц предплечья, синдром Горнера). Рентгенологическими особенностями этой формы считают локализацию опухолевого узла в области верхушки, сравнительно быстрое прорастание в плевру, деструкцию I, II ребер, а иногда и поперечных отростков позвонков.
Синдром сдавления верхней полой вены (цианоз, отек лица, шеи, верхних конечностей, развитые подкожные венозные коллатерали на туловище) наиболее характерен для медиастинальной формы РЛ и МРЛ, при котором часто наблюдается массивное поражение лимфатических узлов средостения и, как следствие, сдавление верхней полой вены.
Перечисленные симптомы и синдромы не патогномоничны для РЛ и могут иметь место при неопухолевой легочной и общесоматической внелегочной патологии. Так, кровохарканье может наблюдаться при туберкулезе легкого и декомпенсированной кардиальной патологии, одышка – при хронической обструктивной болезни легких, боли в грудной клетке – при воспалительных плевритах, радикулитах, межреберной невралгии, кашель – при простудных, вирусных инфекциях, туберкулезе и гнойных процессах в легких, а симптомы общей интоксикации присущи большой группе заболеваний.
У некоторых пациентов выявляются паранеопластические синдромы, связанные с гиперпродукцией гормонов (синдромы секреции адренокортикотропного, антидиуретического, паратиреоидного гормонов, эстрогенов, серотонина).
РЛ может сопровождаться тромбофлебитом, различными вариантами нейро- и миопатии, своеобразными дерматозами, нарушениями жирового и липидного обмена, артралгическими и ревматоидноподобными состояниями. Нередко проявляется остеоартропатией (синдромом Мари-Бамбергера), заключающейся в утолщении и склерозе длинных трубчатых костей голеней и предплечий, мелких трубчатых костей кистей и стоп, припухлости суставов (локтевых, голеностопных), колбовидном утолщении концевых фаланг пальцев кистей (синдроме «барабанных палочек») [1]. При периферическом раке верхушки легкого возможно появление синдрома Бернара-Горнера (птоза, миоза, энофтальма) в сочетании с болями в плечевом суставе и плече, прогрессирующей атрофией мышц дистальных отделов предплечья, обусловленными непосредственным распространением опухоли через купол плевры на плечевое сплетение, поперечные отростки и дужки нижних шейных позвонков, а также симпатические нервы [2].
Возможно бессимптомное развитие заболевания, при котором оно становится случайной рентгенологической находкой.
При сборе анамнеза у всех пациентов рекомендуется обращать внимание на стаж курения и количество потребляемых сигарет, профессиональные вредности (п/п. 1, табл. А3-1) [1–3, 9].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5)
Рекомендуются всем пациентам: тщательный физикальный осмотр (п/п. 2, табл. А3-1), включающий измерение частоты дыхания и пульсоксиметрию, определение наличия и характера одышки, выявление симптомов сдавления верхней полой вены, пальпацию шейно-надключичных и других зон лимфоузлов, перкуссию и аускультацию органов грудной клетки и др. Кроме того, проводится оценка общего и нутритивного статуса, выявление паранеопластических синдромов. При проведении физикального обследования следует учитывать многообразие клинических проявлений опухолей легких и различные клинико-анатомические формы роста [1, 2, 9].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
-
Рекомендуется всем пациентам в целях дифференциальной диагностики на этапе установки диагноза и в целях оценки эффективности лечения определять уровень следующих онкомаркеров (в зависимости от гистологической структуры РЛ):
Исследование уровня нейронспецифической енолазы в крови при МРЛ [1];
Исследование уровня растворимого фрагмента цитокератина 19 (CYFRA 21-1) в крови, антигена плоскоклеточной карциномы (squamous cell carcinoma antigen, SCC) в крови;
Исследование уровня растворимого фрагмента цитокератина 19 CYFRA 21-1 в крови, антигена аденогенных типов рака CA-125 в крови при аденокарциноме [10];
Исследование уровня растворимого фрагмента цитокератина 19 CYFRA 21.1 и антигена плоскоклеточной карциномы SCC в крови, ракового эмбрионального антигена при крупноклеточном раке [10].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 3).
Рекомендуется пациентам с подозрением на РЛ проводить общий (клинический) анализ крови развернутый и анализ крови биохимический общетерапевтический (включая: исследование уровня глюкозы, креатинина, общего билирубина, альбумина в крови, определение активности аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ), щелочной фосфатазы в крови), исследование свертывающей системы крови (п/п. 5, табл. А3-1) (включая оценку активированного частичного тромбопластинового времени (АЧТВ), исследование уровня фибриногена в крови, определение международного нормализованного отношения (МНО), определение протромбинового (тромбопластинового) времени в крови или в плазме), общий (клинический) анализ мочи на наличие системной воспалительной реакции и определение уровня ее выраженности, установление функционального статуса кроветворной, гемостатической, детоксикационной и выделительной систем [11,12].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
-
При выявлении неплоскоклеточного (в том числе, диморфного) НМРЛ рекомендовано проведение молекулярно-генетических и ИГХ исследований (гистологический или цитологический материал) на наличие активирующих мутаций и экспрессии PD-L1 в зависимости от стадии:
при I-III стадии после радикального хирургического лечения «обязательный объем тестирования» включает определение мутаций гена EGFR 18-21 экзоны (молекулярно-генетическое исследование мутаций в гене EGFR в биопсийном (операционном) материале) и молекулярно-генетическое исследование транслокаций гена ALK (п/п. 7, табл. А3-1);
при II-III стадии «обязательный объем тестирования» после радикального хирургического лечения включает определение экспрессии белка PDL1 иммуногистохимическим методом;
при неоперабельной III стадии и IV стадии – «обязательный объем тестирования» [мутации гена EGFR 18-21 экзоны (молекулярно-генетическое исследование мутаций в гене EGFR в биопсийном (операционном) материале, либо молекулярно-генетическое исследование мутаций в гене EGFR в цитологических образцах, либо молекулярно-генетическое исследование мутаций в гене EGFR в крови методом ПЦР), транслокации ALK (молекулярно-генетическое исследование транслокаций гена ALK), транслокации ROS1 (молекулярно-генетическое исследование транслокаций гена ROS1) и мутации BRAF V600E (молекулярно-генетическое исследование мутаций в гене BRAF в биопсийном (операционном) материале); при отсутствии перечисленных активирующих мутаций ИГХ – определение экспрессии белка PD-L1 иммуногистохимическим методом и «возможный объем тестирования» [транслокации RET (молекулярно-генетическое исследование мутаций в гене RET в биопсийном (операционном) материале, молекулярно-генетическое исследование мутаций в гене RET в крови), мутации c-MET, мутации 20 экзона HER2 (п/п. 12, табл. А3-1) (определение амплификации гена HER2 методом флюоресцентной гибридизации in situ (FISH)), мутации KRAS (молекулярно-генетическое исследование мутаций в гене KRAS в биопсийном (операционном) материале) и транслокации генов семейства NTRK, определение последовательности вставок (инсерций) в 20 экзоне гена EGFR (молекулярно-генетическое исследование мутаций в гене EGFR в биопсийном (операционном) материале, либо молекулярно-генетическое исследование мутаций в гене EGFR в цитологических образцах, либо молекулярно-генетическое исследование мутаций в гене EGFR в крови методом ПЦР)] [347].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5).
Комментарии: в настоящее время выделено несколько биомаркеров, которые помогают выделить подгруппу пациентов со значимым ответом на определенную терапию. Данные биомаркеры включают: ALK, ROS1 транслокацию генов, EGFR (18-21-й экзоны), BRAF V600E, определение последовательности вставок (инсерций) в 20 экзоне гена EGFR и PD-L1 экспрессию. Молекулярно- генетическое тестирование может быть оправдано и в случае плоскоклеточного рака или при затруднении (при малом количестве материала) в определении гистологического подтипа у некурящих молодых пациентов [6,12].
Расширенное молекулярно-генетическое тестирование может быть полезным не только для определения тактики лечения в рамках стандартов, но и для включения пациента в клинические исследования по изучению новых противоопухолевых препаратов, что может обеспечить значимую выгоду для пациента в сравнении со стандартным лечением. Молекулярно-генетическое и ИГХ исследование может быть оправдано и при затруднении (мало материала) в определении гистологического подтипа или в случаях плоскоклеточного рака у некурящих молодых больных (<50 лет). С учетом гетерогенности опухолей и появления новых мутаций в процессе терапии при прогрессировании целесообразны повторные биопсии с целью изменения лечебной тактики.
При необходимости возможно использовать NGS как метод молекулярного профилирования рака легкого для тестирования биомаркеров с учетом текущей доступности лекарственных препаратов «направленного действия» и индивидуализировать подходы к назначению иммунотерапии.
С целью оптимизации использования NGS кандидатами для данного вида исследования следует считать пациентов с распространенным неплоскоклеточным НМРЛ при наличии показаний к проведению лекарственного лечения [347].
При выявлении неплоскоклеточного (в том числе диморфного) рака при отсутствии возможности проведения молекулярно-генетического исследования в биопсийном (операционном) материале (в том числе цитологическом) рекомендовано исследование свободно-циркулирующей опухолевой ДНК плазмы крови в целях детектирования мутаций в генах EGFR (молекулярно-генетическое исследование мутаций в гене EGFR в крови методом ПЦР) [11, 175].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5).
Комментарии: исследование свободно-циркулирующей опухолевой ДНК плазмы крови (или «жидкостная биопсия») не следует проводить вместо молекулярно-генетического исследования биопсийного материала. Для исследования мутаций с использованием жидкостной биопсии характерны низкая чувствительность и высокая специфичность, обусловленная незначительным и нестабильным количеством циркулирующей опухолевой ДНК. В соответствии с исследованиями, вероятность ложноотрицательного результата при проведении жидкостной биопсии по сравнению с традиционной биопсией может составлять до 30% [176,177,178,179]. Несмотря на указанные ограничения жидкостной биопсии, молекулярно-генетическое исследование мутаций в гене EGFR в крови методом ПЦР необходимо выполнять для выявления мутаций гена EGFR и определения эффективности таргетной терапии в двух случаях: 1) при неоперабельном раке, когда тканевый образец недоступен для молекулярно-генетического исследования: 2) когда невозможно провести молекулярно-генетическое исследование по тканевому образцу ввиду низкого его качества или количества [176].
При проведении молекулярно-генетического исследования рекомендуется проводить анализ мутаций гена EGFR (молекулярно-генетическое исследование мутаций в гене EGFR в биопсийном (операционном) материале, либо молекулярно-генетическое исследование мутаций в гене EGFR в цитологических образцах, либо молекулярно-генетическое исследование мутаций в гене EGFR в крови методом ПЦР) как в отношении распространенных генетических нарушений (делеции в 19-м экзоне; точечная замена p.L858R в 21-м экзоне), так и в отношении менее распространенных генетических нарушений в 18-21-х экзонах (в частности, вставки в 19-м экзоне, инсерций 20 экзона, а также точечные замены p.L861Q, p.G719X, p.S768I) [180,181,182, 183,184].
Уровень убедительности рекомендаций – B (уровень достоверности доказательств – 3).
Комментарии: в гене EGFR описаны генетические нарушения, ассоциированные как с потенциальной эффективностью ингибиторов тирозинкиназы EGFR, так и с резистентностью к ингибиторам тирозинкиназы EGFR. В случае использования высокопроизводительного секвенирования могут быть обнаружены дополнительные мутации гена EGFR, значимость которых в отношении назначения таргетной терапии может быть неопределенной. Таким образом, результаты молекулярно-генетического исследования мутаций гена EGFR должны включать информацию о том, какое именно генетическое нарушение обнаружено.
Определять дальнейшую лечебную тактику следует на междисциплинарном консилиуме.
Комментарии: Мутационная нагрузка является относительным показателем общего количества мутационных событий, произошедших в опухолевой ткани, и в ряде случаев расценивается, как коррелирующая с появлением неоантигенов, способных активировать противоопухолевый иммунный ответ [229]. Высокая мутационная нагрузка часто регистрируется при НМРЛ, ассоциированном с курением.
Предварительные данные Checkmate 227 (рандомизированного исследования 3 фазы по применению комбинированного режима ниволумаб** + #ипилимумаб**) позволили предположить, что мутационная нагрузка может быть валидным маркером чувствительности опухоли к иммуноонкологической терапии [210]. Однако окончательный анализ показал, что эффективность этой терапии не зависит ни от степени мутационной нагрузки, ни от уровня экспрессии PDL1, ни от сочетания этих маркеров. Общая выживаемость в результате применения комбинации ниволумаба** и #ипилимумаба** повышалась у всех пациентов с НМРЛ [219].
Исследование Keynote 158 (исследование 2 фазы по эффективности пембролизумаба** у пациентов во второй линии терапии) определило мутационную нагрузку как маркер эффективности иммуноонкологических препаратов для ряда онкологических заболеваний, но не для НМРЛ [230]. Кроме того, серьезными препятствиями к использованию мутационной нагрузки как валидного маркера являются отсутствие стандартизации методов исследований и несовпадение в пороговых значениях, разделяющих низкую и высокую мутационную нагрузку в различных исследованиях [231]
Таким образом, в настоящее время мутационная нагрузка не может быть использована как маркер чувствительности к иммунноонкологической терапии при НМРЛ
2.4.1. Визуализация
Рекомендуется проведение стандартной рентгенографии легких (или рентгенография легких цифровая) всем пациентам при подозрении на РЛ по клиническим данным (клинические симптомы) [5,11].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Рекомендуется проведение КТ органов грудной полости (компьютерная томография грудной полости с внутривенным болюсным контрастированием, мультипланарной и трехмерной реконструкцией) от уровня выше верхней апертуры до уровня окончания реберных синусов (включая надпочечники) всем пациентам с подозрением на РЛ, по данным рентгенографии легких, или при невозможности исключить РЛ на основе клинического обследования при отсутствии изменений на рентгенограммах [8, 9, 195].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Комментарии: КТ является основной методикой визуализации для оценки патологических изменений, установленных при рентгенографии. При КТ органов грудной полости могут быть выявлены изменения, не видимые на обзорных рентгенограммах, имеющих важное значение для определения тактики лечения пациентов с РЛ. При локализации изменений в области средостения и корней легких, а также при необходимости дифференциальной диагностики выявленных изменений, целесообразно применять КТ органов грудной полости с внутривенным болюсным контрастированием.
При центральном расположении опухоли КТ позволяет выявить изменения в бронхах до развития воспаления легких и формирования обтурационного ателектаза. В сравнении с бронхоскопией точность КТ выше при перибронхиально расположенных образованиях и ниже – при поверхностных эндобронхиальных опухолях.
Периферическая опухоль может иметь вид одиночного очага различной плотности, полости распада или участка инфильтрации некруглой формы (пневмониеподобная форма рака). Реже на этапе первичной диагностики выявляют опухоль, которая врастает в грудную стенку (кортикоплевральная форма), средостение (медиастинальная форма), верхнюю апертуру (опухоль Панкоста) или представляет собой очаговую диссеминацию в легком.
В зависимости от плотности очаг периферического рака может быть солидного типа, частично солидного типа или очагом по типу «матового стекла». Солидный очаг чаще имеет бугристые и/или лучистые контуры, стенки дренирующего бронха утолщены, висцеральная плевра втянута в опухоль и локально утолщена.
Для дифференциальной диагностики с доброкачественными гранулемами (туберкулема) может иметь значение накопление контрастного средства в опухоли (при динамической КТ).
ПЭТ как метод диагностики солидных очагов оценивается неоднозначно, особенно в странах с высоким бременем туберкулеза. Очаг по типу «матового стекла» характерен для аденокарциномы со стелющимся ростом, в том числе in situ. Очаги по типу «матового стекла» увеличиваются медленнее солидных очагов. При ПЭТ-КТ с флудезоксиглюкозой [18F] (18ФДГ) (позитронная эмиссионная томография, совмещенная с компьютерной томографией с туморотропными РФП) такие очаги отличаются низким уровнем накопления изотопа. Субсолидный очаг имеет центральный солидный компонент и периферическую зону «матового стекла». Солидная часть очага ассоциируется с инвазивным ростом и имеет значение для определения прогноза и оценки Т-стадии опухолевого роста.
Рекомендуется всем пациентам для определения стадии (распространенности) опухолевого процесса при РЛ применять следующие методы визуализации:
1. Для оценки первичной опухоли в грудной полости проведение КТ органов грудной полости с внутривенным болюсным контрастированием от уровня выше верхней апертуры до уровня окончания реберных синусов (включая печень и надпочечники) [197, 198, 199];
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 3).
Комментарий: при невозможности проведения КТ органов грудной полости (неисправность оборудования и проч.) или при невозможности применения внутривенного контрастирования (тяжелая аллергическая реакция на рентгеноконтрастные средства, содержащие йод, в анамнезе, отсутствие автоматического инжектора и пр.) возможно выполнение МРТ органов грудной клетки (или магнитно-резонансная томография органов грудной клетки с внутривенным контрастированием) при наличии оборудования и подготовленных специалистов.
2. Для оценки регионарных лимфатических узлов (N) и выявления отдаленных метастазов (M) проведение совмещенного ПЭТ-КТ-исследования всего тела (п/п 17, табл. А3-1) [198, 200, 201].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Комментарии: совмещенное ПЭТ-КТ с 18ФДГ (позитронная эмиссионная томография, совмещенная с компьютерной томографией с туморотропными РФП, в том числе с контрастированием) в целом является более эффективным исследованием в сравнении с УЗИ, КТ и МРТ (ультразвуковое исследование органов брюшной полости (комплексное), ультразвуковое исследование забрюшинного пространства, ультразвуковое исследование лимфатических узлов, компьютерная томография органов грудной полости, компьютерная томография органов брюшной полости и забрюшинного пространства с внутривенным болюсным контрастированием, магнитно-резонансная томография органов брюшной полости с внутривенным контрастированием, магнитно-резонансная томография забрюшинного пространства) в выявлении распространенности опухолевого процесса, в том числе в выявлении метастазов в лимфатических узлах, солидных органах, костях и костном мозге, серозных оболочках. Применение ПЭТ-КТ с 18ФДГ позволяет у 1/3 пациентов изменить стадию опухолевого процесса. Совмещенное ПЭТ-КТ с 18ФДГ исследование не позволяет достоверно выявлять метастазы в головном мозге, что определяется необходимость применения МРТ или КТ с внутривенным контрастированием (компьютерная томография головного мозга с внутривенным контрастированием, магнитно-резонансная томография головного мозга с контрастированием). При невозможности выполнения ПЭТ-КТ с 18ФДГ это исследование может быть заменено КТ с внутривенным контрастированием области живота и таза (компьютерная томография органов брюшной полости и забрюшинного пространства с внутривенным болюсным контрастированием, спиральная компьютерная томография органов малого таза у женщин с внутривенным болюсным контрастированием, спиральная компьютерная томография органов таза у мужчин с внутривенным болюсным контрастированием) в сочетании остеосцинтиграфией костей скелета (ОФЭКТ/КТ) (сцинтиграфия костей всего тела, однофотонная эмиссионная компьютерная томография, совмещенная с компьютерной томографией костей всего тела).
3. Для выявления метастазов РЛ в головном мозге проведение МРТ головного мозга с контрастированием [391].
Уровень убедительности рекомендаций – B (уровень достоверности доказательств – 2).
Комментарии: внутривенное контрастирование достоверно повышает чувствительность метода в выявлении очагов метастазов в головном мозге, особенно небольшого размера. При невозможности проведения МРТ, исследование может быть заменено на КТ головного мозга с внутривенным контрастированием.
Рекомендуется при динамическом наблюдении пациента после хирургического, лучевого и химиотерапевтического лечения РЛ проведение КТ органов грудной полости, в том числе при наличии показаний, с внутривенным болюсным контрастированием [8, 9].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Рекомендуется применение низкодозной КТ органов грудной полости (НДКТ) для скрининга РЛ в группах риска [200–203].
Уровень убедительности рекомендаций – А (уровень достоверности доказательств – 1).
Комментарии: ряд проспективных рандомизированных исследований показал, что применение НДКТ в группах риска по РЛ с частотой раз в год приводит к снижению смертности от этого заболевания в популяции на 20% и более [200–202]. Группы риска включают пациентов в возрасте 55-80 лет, курящих в настоящее время (индекс курения – 30 пачка/лет) или бросивших курить не более 15 лет назад.
Программа скрининга РЛ предусматривает три основных этапа: 1) организационно-методический (информирование населения, выявление групп риска, составление плана-графика обследований, ведение картотеки и пр.); 2) диагностический (проведение диагностического теста в соответствии с международными и отечественными рекомендациями, и стандартами, с учетом региональных особенностей системы здравоохранения); 3) онкологический (возможность дообследования или наблюдения пациентов с выявленной при НДКТ патологией в легких в условиях специализированной онкологической медицинской помощи).
Возможность реализации программы НДКТ скрининга РЛ определяется региональными возможностями системы здравоохранения, в том числе технологическими, организационными, географическими, экономическими и пр. При ограниченных ресурсах внедрение такой формы скрининга нецелесообразно.
Популяционный скрининг РЛ с использованием НДКТ не должен применяться для пациентов без доказанных факторов риска, в частности для лиц старше 80 и младше 55 лет, с меньшей интенсивностью курения, а также с хроническими заболеваниями легких (хроническая обструктивная болезнь легких, интерстициальные заболевания легких, профессиональные заболевания, хронические инфекции, в частности туберкулез, и пр.), поскольку эффективность скрининга для этих групп населения не доказана.
Рентгенографию легких не следует проводить для популяционного скрининга РЛ, поскольку проведенные проспективные рандомизированные исследования не выявили достоверного снижения смертности от РЛ при использовании этой методики. При этом рентгенография легких по-прежнему является основной методикой первичного выявления РЛ при проведении диагностического исследования по клиническим показаниям.
Рекомендуется пациентам с подозрением на РЛ проведение бронхологического исследования (бронхоскопии) при центральном расположении опухолевого узла в легком или периферическом расположении новообразования, но с наличием «дренирующего» бронха с целью оценки локализации, распространенности опухолевого процесса и получения материала для патолого-анатомического исследования биопсийного (операционного) материала (в том числе цитологического исследования) [1, 2].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Комментарии: бронхологическое исследование относят к основным и обязательным методам диагностики РЛ. Оно позволяет не только визуально исследовать гортань, трахею и все бронхи, непосредственно увидеть локализацию опухоли, определить границы ее распространения, косвенно судить об увеличении лимфатических узлов корня легкого и средостения, но и провести биопсию, для гистологического исследования (биопсия трахеи, бронхов при бронхоскопии, биопсия легких при бронхоскопии), получить материал (браш-биоптаты, мазки-отпечатки, соскоб или смыв из бронхиального дерева) для цитологического изучения (цитологическое исследование микропрепарата тканей трахеи и бронхов, цитологическое исследование микропрепарата тканей легкого, цитологическое исследование микропрепарата тканей нижних дыхательных путей), т.е. морфологически подтвердить диагноз, и уточнить гистологическую структуру опухоли.
В последние годы все шире используются диагностические аппараты, объединяющие в себе возможности рентгеноэндоскопии, эндосонографии и флюоресцентной эндоскопии (центр ультразвуковой эндоскопический, видеобронхоскоп гибкий, эндоскопы гибкие для обследования верхних дыхательных путей и др.). Наиболее перспективным методом выявления скрытых микроочагов рака слизистой оболочки считается бронхоскопия аутофлюоресцентная, которая основана на эффекте аутофлюоресценции и при которой регистрируется концентрация в опухоли эндогенных фотосенсибилизаторов [1, 2].
Рекомендуется пациентам с подозрением на РЛ проведение трансторакальной биопсии (биопсия трансторакальная легкого рентгенохирургическая) под рентгенологическим или ультразвуковым контролем периферического образования в легком (за исключением образований менее 1 см – T1a), если совокупность результатов перечисленных выше методов диагностики не позволяет верифицировать процесс, а вероятность злокачественной опухоли остается высокой. В случае неэффективности и при высоких рисках осложнений трансторакальной биопсии под контролем КТ (биопсия трансторакальная легкого рентгенохирургическая) может быть использована торакоскопия для верификации диагноза [8, 9].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Проведение трансбронхиальной или трансэзофагеальной пункции (EBUS/EUS) (эндосонография средостения чреспищеводная), медиастиноскопии, торакоскопии [8, 9] рекомендуется пациентам при подозрении на метастатическое поражение лимфатических узлов средостения (N2-3) для оценки распространенности процесса. Методики EBUS и EUS могут быть использованы и для верификации первичных периферических парамедиастинальных новообразований.
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Диагностическую видеоторакоскопию (A03.10.001 – торакоскопия) проводят:
при отсутствии результатов бронхологического и/или других исследований для получения морфологического материала из лимфатических узлов средостения или первичной опухоли у неоперабельных пациентов;
с целью дифференциальной диагностики медиастинальной формы РЛ и опухоли переднего средостения (в случае неинформативности трансторакальной биопсии); o при экссудативном плеврите неясной этиологии;
с целью стадирования РЛ;
при метастазах опухоли в легком и по плевре (при невозможности применения малоинвазивных методов диагностики).
Комментарии: после интраоперационной торакоскопической ревизии и срочного патолого-анатомического исследования биопсийного (операционного) материала в зависимости от клинической ситуации операцию завершают удалением адекватного объема легочной ткани, а при злокачественном процессе дополняют ее медиастинальной лимфаденэктомией.
Всем пациентам c подозрением на РЛ рекомендуется ультразвуковое исследование органов брюшной полости (комплексное) или КТ органов брюшной полости с внутривенным болюсным контрастированием для уточнения распространенности заболевания [8, 9].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Пациентам c установленным диагнозом РЛ II-III стадии рекомендуется выполнение остеосцинтиграфии (сцинтиграфия костей всего тела) для уточнения распространенности заболевания и для контроля эффективности лечения, если не проводилось ПЭТ-КТ с 18ФДГ всего тела [11,12].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Рекомендуется выполнение регистрации электрокардиограммы всем пациентам с подозрением на РЛ для выявления сопутствующей патологии [11,12].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Рекомендуется при подготовке пациента к хирургическому, лучевому и химиотерапевтическому лечению с целью оценки функционального статуса по показаниям проводить дополнительное обследование: эхокардиографию, холтеровское мониторирование электрокардиографических данных исследование функции внешнего дыхания, сцинтиграфию легких вентиляционную, ультразвуковую допплерографию сосудов шеи и сосудов (артерий и вен) нижних конечностей, эзофагогастродуоденоскопию, прием (осмотр, консультация) врача-невролога первичный, прием (осмотр, консультация) врача-кардиолога первичный, прием (осмотр, консультация) врача-эндокринолога первичный и т.п. [11,12].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Рекомендуется использование технологий искусственного интеллекта для анализа изображений с целью выявления признаков злокачественных новообразований бронхов и легкого у взрослых [293].
Уровень убедительности рекомендаций – В (уровень достоверности доказательств – 3).
Рекомендуется проведение цитологического (цитологическое исследование микропрепарата тканей трахеи и бронхов, цитологическое исследование микропрепарата тканей легкого, цитологическое исследование микропрепарата тканей нижних дыхательных путей) и/или патолого-анатомического исследования биопсийного (операционного) материала с применением иммуноцитохимического или иммуногистохимического исследования (ИЦХ/ИГХ) для уточнения морфологической формы РЛ и исследования биомаркёров, имеющих прогностическое и предсказательное значение [6, 232].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Комментарии: приблизительно в 70% случаев морфологический диагноз у пациентов с нерезектабельным или метастатическим раком легкого ставится на основании исследования цитологического или биопсийного материала. Основными целями исследования малого диагностического материала являются: а) установления возможно более точной нозологической принадлежности опухоли в соответствии с классификацией ВОЗ 2021 и б) сохранить ткань для молекулярно-генетических исследований, особенно у пациентов с продвинутыми стадиями заболевания. В случае низкодифференцированных опухолей объёма материала может оказаться недостаточно для точного определения гистологической формы РЛ даже с использованием ИЦХ/ИГХ. Поэтому в отсутствии морфологических признаков нейроэндокринной дифференцировки оптимальной для ИЦХ/ИГХ является панель из двух маркёров: TTF1 и р63 (или р40) [ВОЗ, IASLC]. Это поможет минимизировать количество подрезок блока и сохранить биоматериал для молекулярно-генетических исследований. При наличии морфологических признаков нейроэндокринной дифференцировки при выполнении ИЦХ/ИГХ можно пользоваться антителами к CD56, синаптофизину или хромогранину А. Более широкими панелями антител следует пользоваться если гистогенез опухоли не ясен или подозревается метастатический характер поражения легкого.
-
Рекомендуется при проведении патолого-анатомического исследования биопсийного (операционного) материала опухоли, полученной при первичной биопсии (биопсия трахеи, бронхов при бронхоскопии, биопсия легких при бронхоскопии, биопсия трансторакальная легкого рентгенохирургическая) с целью верификации диагноза, отражать в заключении следующие параметры [6,12]:
1) Гистологический тип опухоли в соответствии с классификацией ВОЗ 2021 [6],
2) Долю опухолевой ткани в биоптате в процентах.
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5).
Комментарии: при исследовании малого диагностического материала вероятность некорректного определения гистологического типа опухоли выше, чем при исследовании операционного материала. Поэтому допустимы следующие формулировки диагноза: «низкодифференцированный рак, вероятно аденокарцинома», «низкодифференцированный рак, вероятно плоскоклеточный рак», «низкодифференцированный рак без достоверных признаков нейроэндокринной и плоскоклеточной дифференцировки». Также при исследовании малого объёма биопсийного материала не следует указывать нижеперечисленные гистологические типы РЛ в рубрике патологоанатомический диагноз: аденокарцинома in situ, минимально инвазивная аденокарцинома, крупноклеточный рак, железисто- плоскоклеточный рак, карциносаркома, саркоматоидный (веретеноклеточный) рак, гигантоклеточный рак [ВОЗ].
-
Рекомендуется при проведении патолого-анатомического исследования биопсийного (операционного) материала опухолей, опухолеподобных образований мягких тканей, полученных при повторной биопсии (биопсия трахеи, бронхов при бронхоскопии, биопсия легких при бронхоскопии, биопсия трансторакальная легкого рентгенохирургическая, трепанбиопсия опухолей наружных локализаций, лимфатических узлов под визуальным контролем, биопсия опухолей, опухолеподобных образований мягких тканей) на фоне прогрессирования/появления новых очагов, отражать в заключении следующие параметры [12]:
1) Соответствует ли гистологический тип опухоли исходному гистологическому типу в первичной биопсии,
2) долю опухолевой ткани в биоптате в процентах.
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5).
Комментарии: при повторной биопсии опухолей, опухолеподобных образований мягких тканей на фоне прогрессирования или появления новых очагов следует сравнить её тип гистологического строения с опухолью в материале первичной биопсии, выполненной с целью верификации диагноза. Т.к. приоритетным исследованием на материале повторной биопсии является молекулярно-генетическое исследование с целью определения механизмов резистентности к проведённой терапии, то ИЦХ/ИГХ выполняется только в ситуации морфологической трансформации опухоли. Например, в случае трансформации аденокарциномы в нейроэндокринный рак.
-
Рекомендуется при проведении патолого-анатомического исследования операционного материала отражать в макроописании следующие параметры [233, 234,235]:
1) Тип образца, присланного на исследование,
2) Сторона поражения,
3) Расположение узловых образований в образце,
4) Максимальный размер инвазивной части опухоли в двух измерениях,
5) Наличие нескольких образований.
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5).
-
Рекомендуется при проведении патолого-анатомического исследования операционного материала отражать в микроописании следующие параметры [233, 235]:
1) Гистологический тип опухоли,
2) Гистологическая степень злокачественности,
3) Распространение по воздухоносным путям (наличие/отсутствие),
4) Инвазия висцеральной плевры (наличие/отсутствие),
5) Сосудистая инвазия (наличие/отсутствие),
6) Инвазия опухоли в смежные структуры,
7) Наличие или отсутствие инвазивной опухоли в крае резекции,
8) Расстояние от инвазивной опухоли до ближайшего края резекции (мм),
9) Наличие или отсутствие других опухолевых узлов (метастазы) в легких,
10) Наличие или отсутствие иных патологических процессов в лёгочной ткани,
11) Число исследованных лимфатических узлов,
12) Число лимфатических узлов с метастатическим поражением,
13) Степень морфологического регресса опухоли в случае проведения специализированного противоопухолевого лечения,
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5).
Комментарии: гистологический тип рака легкого следует указывать в соответствии с классификацией ВОЗ 2021 (см. табл. №1 Кодирование по МКБ)). Гистологическая степень злокачественности не валидирована для плоскоклеточного рака, имеет очень ограниченное прогностическое значение для аденокарциномы, но её обязательно указывать для нейроэндокринных опухолей легкого.
Для пациентов, получавших неоадъювантную химиотерапию и/или лучевую терапию перед оперативным лечением, следует проводить количественную оценку степени морфологического регресса опухоли. Следует вычислять долю, приходящуюся на жизнеспособные опухолевые клетки, от всего опухолевого ложа. Пороговым значением выраженного морфологического регресса является <10% жизнеспособных опухолевых клеток.
При выявлении двух и более первичных узлов РЛ, отразить содержание пунктов 1-8 и 12-13 для каждого узла.
Рекомендуется проводить определение экспрессии белка PD-L1 иммуногистохимическим методом для выявления пациентов наиболее чувствительных к анти-PD-1/PD-L1 терапии [236].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5).
Комментарий: для тестирования PD-L1 методом ИГХ были разработаны различные клоны антител. Часть из них, сопоставимы по интенсивности и доле окрашенных клеток, часть нет. Однако при высоком уровне экспрессии PD-L1 данные тестов с антителами 22С3, SP263, SP142 сопоставимы в большом проценте случаев и эти тесты взаимозаменяемы. Критерии позитивности зависят от используемого антитела и платформы для окрашивания. Для тестов с антителами клонов 22С3 и SP263 следует указывать процент позитивных опухолевых клеток. Для теста с антителами клона SP142 следует указывать процент позитивных опухолевых клеток и процент позитивных иммунных клеток. Использование нескольких ИГХ-тестов одновременно обычно не приветствуется. В протоколе иммуногистохимического исследования следует указывать каким тестом было произведено исследование и по каким критериям оценивалась экспрессия PD-L1.
В настоящее время накоплено мало свидетельств в пользу определения PD-L1 статуса опухоли методом ИЦХ.
3.1. Лечение пациентов с немелкоклеточным раком легкого
Один из основных методов лечения РЛ для I-II, частично III стадии – хирургический. Объем операции определяется распространенностью опухолевого процесса, гистологической формой опухоли и функциональным состоянием пациента.
При карциноидных опухолях хирургический метод является основным. Карциноидные опухоли, особенно их типичные формы, характеризуются менее агрессивным местным инфильтративным ростом и отдаленным метастазированием, чем другие (более часто встречающиеся) формы НМРЛ – плоскоклеточный и железистый рак. Карциноиды развиваются чаще в крупных бронхах 1, 2 и 3-го порядка и характеризуются преимущественно экзофитным, внутрипросветным ростом, без распространения опухоли по стенке бронха, что часто позволяет выполнить органосохраняющую радикальную операцию в объеме лоб-, билобэктомии с использованием резекции и реконструкции бронхов и трахеи или изолированную радикальную резекцию бронхов, трахеи и ее бифуркации с сохранением функции всего легкого (A16.09.018.001. Пластика бронха. Реконструктивные операции на трахее и бронхах). При получении планового гистологического заключения типичной нейроэндокринной опухоли после диагностической атипичной резекции лёгкого с тотальным удалением опухоли и гистологически подтверждённым отрицательным краем резекции (R0) у больных с ограниченными функциональными резервами выполненный объём резекции следует считать достаточным. Эндоскопическое, эндобронхиальное удаление карциноидных опухолей может быть проведено у пациентов без прорастания опухолью всей стенки бронха, у которых по тем или иным причинам нельзя провести радикальную резекцию легкого и бронха открытым способом или через торакоскопический доступ. При обследовании до операции всегда сложно установить истинную глубину поражения опухолью стенки бронха [14,17].
3.1.1. Принципы лечения пациентов с 0-IIIА стадиями заболевания
Пациенты 0-IIIА стадиями НМРЛ, с IIIB (T3N2) – являются потенциально операбельными (при возможности R0-резекции), с учетом функциональных показателей [1, 2].
Пациентам с 0-IIIA стадиями НМРЛ рекомендуется хирургическое лечение с целью повышения выживаемости данных пациентов при условии соблюдения требований к радикальной операции (R0 резекция), и функциональной операбельности. При планировании операции в объеме пневмонэктомии следует обсудить возможные варианты терапии на мультидисциплинарном консилиуме с участием, в том числе, пациента [7,12].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Комментарии: стандартный объем операции включает анатомическую резекцию легкого (сегмент-, лоб-/билобэктомию или пневмонэктомию) с ипсилатеральной систематической медиастинальной лимфодиссекцией (удалены минимум 6 лимфатических узлов: не менее 3 корневых или бронхопульмональных, не менее 3 – медиастинальных (средостенных) из 3-х разных групп (в том числе минимум 1 лимфатический узел из бифуркационной группы))
Для пациентов с Т3 (отсев в ту же долю) может быть предложено хирургическое лечение
Для пациентов с Т4 (отсев в другую долю) хирургическое лечение может рассматриваться как возможная опция.
Торакоскопические операции при клинической форме РЛ I стадии могут быть рассмотрены как стандартный вариант хирургического лечения наряду с обычными открытыми вмешательствами [15- 20].
Торакоскопические операции при II стадии оптимально выполнять только в лечебных учреждениях с большим опытом подобных хирургических вмешательств.
Не рекомендуются адъювантная химиотерапия (ХТ) и ЛТ пациентам с I стадией заболевания (кроме Ib стадией высокого риска) [12].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5)
Пациентам группы высокого риска с IB стадией (вовлечение висцеральной плевры, сосудистая инвазия, низкая степень дифференцировки, хирургическое лечение в объеме атипичной резекции, Nх, возраст моложе 75 лет) рекомендуется адъювантная химиотерапия (ХТ) с целью повышения выживаемости данных пациентов [20].
Уровень убедительности рекомендаций – A (уровень достоверности доказательств – 1)
Пациентам с распространенностью заболевания сT1-2N0 в случае невозможности проведения хирургического лечения или отказа пациента рекомендуется дистанционная лучевая стереотаксическая гипофракционная терапия (A07.30.009.001 конформная дистанционная лучевая терапия, в том числе IMRT, IGRT, ViMAT, стереотаксическая) по радикальной программе (высокодозированное облучение) с использованием крупных доз за фракцию (РОД 10-18 Гр, СОД 50-54 Гр) с целью повышения выживаемости данных пациентов [11,24].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5)
В случае отсутствия морфологической верификации решение о проведении стереотаксической лучевой терапии данной категории больных может быть принято расширенным консилиумом медицинской организации на основании динамики рентгенологических данных (КТ или ПЭТ-КТ). Подтверждение биопсии перед SBRT настоятельно рекомендуется, но не является обязательным условием, если эта процедура сопряжена с высоким риском осложнений.
Возможные режимы фракционирования:
7,5 Гр 8 Фр ультрацентральные опухоли*
12 Гр 5Фр центральные опухоли
20 Гр 3Фр периферические опухоли
* При облучении ультрацентрических опухолей (планируемый целевой объем примыкает к или накладывается на проксимальную часть бронхиального дерева, пищевод или трахею), целесообразно использовать схему со стандартным фракционированием [7, 12, 19,32].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5)
Комментарий: лечение проводится с использованием методов контроля дыхания.
Пациентам со II стадией НМРЛ рекомендуется проведение адъювантной лекарственной противоопухолевой терапии в целях повышения показателей выживаемости (см. табл. 3). Предоперационное противоопухолевое лечение данной группе пациентов не рекомендуется в связи с отсутствием доказательств влияния этого лечения на их выживаемость [20–23].
Уровень убедительности рекомендаций – B (уровень достоверности доказательств – 2).
Комментарии: режимы адъювантной лекарственной противоопухолевой терапии см. табл. 3.
Пациентам со II стадией НМРЛ в случае невозможности проведения хирургического лечения рекомендуется ХТ, или ЛТ, или ХЛТ с целью повышения выживаемости данных пациентов [7, 12, 19].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Неоадъювантная лекарственная терапия (2-4 курса) рекомендуется операбельным пациентам с IIIA (со статусом лимфатических узлов N2) и операбельной IIIB (T3N2) стадией, доказанной по данным патолого-анатомического исследования биопсийного (операционного) материала или ПЭТ/КТ, в качестве этапа комбинированного лечения [294].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 4).
Пациентам, которые являются кандидатами для неоадьювантной лекарственной терапии (операбельным пациентам с IIIA (со статусом лимфатических узлов N2), операбельной IIIB (T3N2) стадией, доказанной по данным патолого-анатомического исследования биопсийного (операционного) материала или ПЭТ-КТ, имеющих экспрессию PD-L1 >1% при постановке первичного диагноза, показано проведение НАХТ в комбинации с ингибиторами контрольных точек иммунитета (ИКТ, L01F Моноклональные антитела и конъюгаты антител): #ниволумаб** 360 мг 1 раз в 3 нед [334], или #пембролизумаб** 200 мг 1 раз в 3 нед или #дурвалумаб** 1500 мг 1 раз в 3 нед. [347] (для пациентов с погранично резектабельными стадиями) + платиносодержащие режимы ХТ (режимы неоадьювантной лекарственной терапии см. таблица 2). Противопоказания для назначения ИКТ могут включать активные или ранее документированные аутоиммунные поражения, иммуносупрессивную терапию, драйверные мутации, ассоциированные с меньшим выигрышем от ИТ (мутации EGFR, транслокации ALK).
Таблица 2. Рекомендуемые схемы комбинированной неоадъювантной лекарственной терапии при немелкоклеточном раке легкого
Препарат |
Схема лечения |
|---|---|
Гемцитабин** + цисплатин** |
1250 мг/м2 в/в в 1-й и 8-й дни цикла. 80 мг/м2 в/в в 1-й день цикла. Цикл – 21 день; до 4 циклов [29] |
Винорелбин** + цисплатин** |
30 мг/м2 в/в (максимум 60 мг/м2 внутрь) в 1-й и 8-й дни цикла. 80 мг/м2 в/в в 1-й день цикла. Цикл – 21 день; до 4 циклов [20, 27, 347] |
#Паклитаксел** + карбоплатин** |
175 мг/м2 в/в в 1-й день цикла. AUC 5 в/в в 1-й день цикла. Цикл – 21 день; до 4 циклов [29] |
#Доцетаксел** + карбоплатин** |
75 мг/м2 в/в в 1-й день цикла. AUC 6 в/в в 1-й день цикла. Цикл – 21 день; до 4 циклов [29] |
#Доцетаксел** + цисплатин** |
75 мг/м2 в/в в 1-й день цикла. 75 мг/м2 в/в в 1-й день цикла. Цикл – 21 день; до 4 циклов [31] |
|
#Ниволумаб** + 1) карбоплатин** + #паклитаксел** (для любого гистологического подтипа) или 2) цисплатин** + гемцитабин** (для плоскоклеточного НМРЛ) или 3) цисплатин** + #пеметрексед** (для неплоскоклеточного НМРЛ) |
360 мг в/в кап. в 1-й день в комбинации с одним из режимов ХТ [334,335]: AUC 5-6 в/в в 1-й день 175-200 мг/м2 в/в в 1-й день Цикл 21 день, 3 цикла 75 мг/м2 в/в в 1-й день 1250 мг/м2 в/в в 1-й и 8-й дни Цикл 21 день, 3 цикла 75 мг/м2 в/в в 1-й день 500 мг/м2 в/в в 1-й день Цикл 21 день х 3 цикла |
|
#Пембролизумаб** 1) цисплатин** + гемцитабин** (для плоскоклеточного НМРЛ) или 2) цисплатин** + #пеметрексед** (для неплоскоклеточного НМРЛ) Адъювантный этап: #пембролизумаб** 200 мг в/в каждые 3 нед. до 13 циклов [336] |
200 мг в/в в 1-й день в комбинации с одним из режимов ХТ [336]: 75 мг/м2 в/в в 1-й день 1000 мг/м2 в/в в 1-й и 8-й дни Цикл 21 день х 4 цикла 75 мг/м2 в/в в 1-й день 500 мг/м2 в/в в 1-й день Цикл 21 день х 4 цикла |
|
#Дурвалумаб** 1) цисплатин** + гемцитабин** (для плоскоклеточного НМРЛ) или 2) #паклитаксел+** карбоплатин** (для плоскоклеточного НМРЛ) 3) цисплатин** + #пеметрексед** (для неплоскоклеточного НМРЛ) Адъювантный этап: #дурвалумаб** 1500 мг в/в каждые 4 нед. 12 циклов [347] |
1500 мг в/в 60-минутная инфузия + ХТ [337]: 75мг/м2 в/в в 1й день 1250 мг/м2 в/в в 1 й и 8-й дни Цикл 21 день х 4 цикла 200 мг/м2 в/в в 1-й день AUC 5-6 в/в в 1-й день Цикл 21 день х 4 цикла [337] 75 мг/м2 в/в в 1-й день 500 мг/м2 в/в в 1-й день Цикл 21 день х 4 цикла |
** Жизненно необходимые и важнейшие лекарственные препараты;
# – препарат, применяющийся не в соответствии с показаниями к применению и противопоказаниями, способами применения и дозами, содержащимися в инструкции по применению лекарственного препарата.
Примечание: фактическая доза карбоплатина** рассчитывается индивидуально, исходя из показателя креатинина в анализе крови пациента накануне проведения лечения.
Адъювантная ХТ, при отсутствии противопоказаний, рекомендуется пациентам во всех случаях N+ с целью повышения выживаемости данных пациентов [2].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5).
ЛТ рекомендуется пациентам с НМРЛ при нерадикальной операции (R+), так как уменьшает риск рецидива у данных пациентов [7].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5).
Относительными показаниями к послеоперационной ЛТ у пациентов с НМРЛ могут являться:
экстракапсулярное распространение при N2;
поражение самого высокого из резецированных лимфатических узлов (потенциально не радикальная резекция);
неадекватная лимфаденэктомия и/или N2 с выходом опухоли за пределы капсулы: я c целью улучшения локорегионарного контроля рекомендуется ХЛТ (последовательный вариант) до 54 Гр в режиме стандартного фракционирования [11].
Послеоперационная ЛТ не влияет на ОВ пациентов НМРЛ.
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5).
Таблица 3. Рекомендуемые режимы адъювантной лекарственной терапии, в т.ч. периоперационные схемы лечения
Препарат |
Схема лечения |
Цисплатин** + #Винорелбин** |
50 мг/м2 в/в в 1-й и 8-й дни 25 мг/м2 в/в в 1-й, 8-й, 15-й, 22-й дни, каждые 4 нед., 4 цикла [21] |
Цисплатин** + #Винорелбин** |
100 мг/м2 в/в в 1-й день 30 мг/м2 в/в в 1-й, 8-й, 15-й, 22-й дни, каждые 4 нед., 4 цикла [33] |
Цисплатин** + Винорелбин** |
80 мг/м2 в/в в 1-й день 25 мг/м2 в/в или 60 мг/м2 внутрь в 1-й и 8-й дни, каждые 3 нед., 4 цикла [347] |
Цисплатин** + Этопозид** |
100 мг/м2 в/в в 1-й день 100 мг/м2 в/в в 1-3-й дни, каждые 4 нед., 4 цикла [33] |
Цисплатин** + Гемцитабин** |
75 мг/м2 в/в в 1-й день 1250 мг/м2 в/в в 1-й и 8-й дни, каждые 3 нед., 4 цикла [347] |
Цисплатин** + #Доцетаксел** |
75 мг/м2 в/в в 1-й день 75 мг/м2 в/в в 1-й день, каждые 3 нед., 4 цикла [347] |
Цисплатин** + #Пеметрексед** |
75 мг/м2 в/в в 1-й день 500 мг/м2 в/в в 1-й день, каждые 3 нед., 4 цикла на фоне премедикации фолиевой кислотой** и цианокобаламином** (для неплоскоклеточного НМРЛ) [340] |
Карбоплатин** + #Паклитаксел** |
AUC 5-6 в/в в 1-й день 175-200 мг/м2 в/в в 1-й день, каждые 3 нед., 4 цикла [30, 347] |
Карбоплатин** + #Гемцитабин** |
AUC 5 в/в в 1-й день 1000 мг/м2 в/в в 1-й и 8-й дни, каждые 3 нед., 4 цикла [342] |
Карбоплатин** + Винорелбин** |
AUC 5 в/в в 1-й день 25 мг/м2 в/в или 60 мг/м2 внутрь в 1-й и 8-й дни, каждые 3 нед., 4 цикла [348]. |
Карбоплатин** + #Пеметрексед** |
AUC 5 в/в в 1-й день 500 мг/м2 в/в в 1-й день, каждые 3 нед., 4 цикла на фоне премедикации фолиевой кислотой** и цианокобаламином** (для неплоскоклеточного НМРЛ) [343] |
Осимертиниб** |
80 мг внутрь ежедневно до 3 лет или развития непереносимой токсичности, после адъювантной ХТ или без нее (при делеции 19 экзона или мутации L858R в 21 экзоне) |
Атезолизумаб** |
1200 мг в/в в 1-й день каждые 3 нед. или 840 мг в/в каждые 2 нед. или 1680 мг в/в каждые 4 нед. до 1 года или развития непереносимой токсичности, после адъювантной ХТ (при гиперэкспрессии PD-L1 в ≥50% опухолевых клеток). Возможно использование лекарственной формы атезолизумаба** для подкожного введения в дозе 1875 мг/15 мл (независимо от массы тела пациента) 1 раз в 3 нед. [286] |
|
Неоадъювантный этап: #пембролизумаб** в комбинации с одним из режимов ХТ: цисплатин** + гемцитабин** или цисплатин** + #пеметрексед** Адъювантный этап: #пембролизумаб** |
200 мг в/в в 1-й день 75 мг/м2 в/в в 1-й день 1000 мг/м2 в/в в 1-й и 8-й дни (для плоскоклеточного НМРЛ) [347] 75 мг/м2 в/в в 1-й день 500 мг/м2 в/в в 1-й день каждые 3 нед., 4 цикла (для неплоскоклеточного НМРЛ [336] 200 мг в/в каждые 3 нед. до 13 циклов [237] |
#Пембролизумаб** |
200 мг в/в каждые 3 нед. длительно, до 1 года [237] (PD-L1 1- 49%) |
Алектиниб** |
600 мг х 2 раза в день до 2х лет (при транслокации ALK) [239] |
|
Неоадъювантный этап: #Ниволумаб** + Любой гистологический подтип: #Паклитаксел** + Карбоплатин** Неплоскоклеточный НМРЛ: #Пеметрексед** + Цисплатин** - Или Карбоплатин** Плоскоклеточный НМРЛ: #Доцетаксел**+ Цисплатин** |
360 мг в/в каждые три недели [335,347] 175 мг/м2 в/в кап в 1й день AUC 5-6 в/в кап в 1й день Цикл 21 день х 4 цикла [347] 500 мг/м2 в День 1 75 мг/м2 в День 1 AUC 5-6 в/в кап в День 1 [347] 75 мг/м2 в День 1 75 мг/м2 в День 1 Цикл 21 день х 4 цикла [349]. |
Адъювантный этап: #Ниволумаб** |
480 мг каждые 4 недели в адъювантном режиме до прогрессирования заболевания, рецидива или непереносимой токсичности или максимально до 13 курсов (до 1 года терапии) [334] |
|
#Дурвалумаб** 1) цисплатин** + гемцитабин** (для плоскоклеточного НМРЛ) или 2) #паклитаксел+** карбоплатин** (для плоскоклеточного НМРЛ) 3) цисплатин** + #пеметрексед** (для неплоскоклеточного НМРЛ) Адъювантный этап: #дурвалумаб** 1500 мг в/в каждые 4 нед. 12 циклов [347] |
1500 мг в/в 60-минутная инфузия + ХТ [337]: 75мг/м2 в/в в 1й день 1250 мг/м2 в/в в 1 й и 8-й дни Цикл 21 день х 4 цикла 200 мг/м2 в/в в 1-й день AUC 5-6 в/в в 1-й день Цикл 21 день х 4 цикла [337] 75 мг/м2 в/в в 1-й день 500 мг/м2 в/в в 1-й день Цикл 21 день х 4 цикла |
После завершения 1-4 курсов платиносодержащей ХТ пациентам с положительной экспрессии PD-L1 в ≥50% опухолевых клеток без активирующих мутаций в генах EGFR, ALK, рекомендуется поддерживающая ИТ атезолизумабом** (если не проводилась неоадъювантная терапия с включением ИТ) [240].
Уровень убедительности рекомендаций – A (уровень достоверности доказательств – 2).
Пациентам с Ib-IIIA стадией при выявлении активирующих мутаций гена EGFR (делеции в 19-м экзоне; точечная замена p.L858R в 21-м экзоне) рекомендуется адъювантная таргетная терапия ингибиторами рецептора эпидермального фактора роста 3-го поколения осимертинибом** (L01E ингибиторы протеинкиназы) в течение 3 лет, с целью улучшения безрецидивной и общей выживаемости у данных пациентов. Таргетная терапия может быть начата после адъювантной ПХТ (до 26 недель после операции) или вместо адъювантной ПХТ (до 10 недель после операции) [204].
Уровень убедительности рекомендаций – А (уровень достоверности доказательств – 2).
У пациентов с Ib-IIIA с выявленной ALK транслокацией адъювантная терапия препаратом алектиниб** 600 мг 2 р/сут в течение 2 лет улучшала показатели безрецидивной выживаемости [239]. При исходно нерезектабельной опухоли у пациентов в удовлетворительном общем состоянии (0-1 балл по шкале ECOG, приложение Г3) при IIIА стадии заболевания на 1-м этапе рекомендуется одновременная химиолучевая терапия; у пациентов с оценкой 2 балла по шкале оценки общего состояния пациента Восточной объединенной онкологической группы ECOG (Eastern Cooperative Oncology Group Performance Status) предпочтительнее последовательное использование 2 методов в целях повышения выживаемости данных пациентов [2]. Рекомендуемые подходы к проведению ХЛТ и ведению пациентов после завершения ХЛТ описаны в разделе 3.1.2.
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Пациентам с IIIA стадией заболевания после завершения одновременной ХЛТ пациентам, не имеющим признаков прогрессирования болезни (контрольное КТ [компьютерная томография органов грудной полости с внутривенным болюсным контрастированием, компьютерная томография органов брюшной полости и забрюшинного пространства с внутривенным болюсным контрастированием] целесообразно проводить непосредственно после окончания ХЛТ), без активирующих мутаций в гене EGFR/ALK и при уровне экспрессии PD-L1 более 1%, рекомендуется поддерживающая иммунотерапия дурвалумабом**. С началом поддерживающего этапа не позже 60 дней от окончания лучевой терапии с целью улучшения выживаемости без прогрессирования и общей выживаемости у этих пациентов. Препарат назначается в дозе 10 мг/кг в виде 60-минутной внутривенной инфузии каждые 2 нед., либо в дозе 1500 мг 1 раз в 4 недели в течение не менее 12 мес., или до прогрессирования, или до развития непереносимой токсичности [40,42].
Уровень убедительности рекомендаций – В (уровень достоверности доказательств – 2).
3.1.2. Принципы лечения пациентов с IIIB-IIIC стадией заболевания
Пациентам с IIIB-IIIC стадией НМРЛ на 1-м этапе рекомендуется одновременная химиолучевая терапия для достижения ремиссии и увеличения выживаемости [23,35]. Важнейшими целями современной ЛТ являются достижение максимального контроля опухоли и минимизация токсичности лечения. Минимальным технологическим стандартом является 3D-ХЛТ.
Уровень убедительности рекомендаций – A (уровень достоверности доказательств – 1).
Комментарии: Стадии IIIB и IIIC являются неоперабельными, IIIB (T3N2) – является потенциально операбельной (при возможности R0-резекции), для данной категории пациентов возможно проведение одновременной (предпочтительно) или последовательной ХЛТ в качестве основного метода лечения. Планируемая СОД ЛТ в рамках ХЛТ должна составлять 60 Гр (± 10 %) в течение 6 нед. (перерывы в лечении снижают эффективность); рекомендуемые режимы ХТ при одновременной ХЛТ представлены в табл.4. Режимы ХТ включают соединения платины: цисплатин** или карбоплатин** при противопоказаниях к цисплатину**.
Одновременная ХЛТ дает более высокие результаты по сравнению с последовательной у пациентов с нерезектабельным НМРЛ III стадии, однако, она более токсична и назначается только пациентам в удовлетворительном общем состоянии (по шкале ECOG 0-1 балл). При ослабленном состоянии пациента (по шкале ECOG 2 балла) целесообразно последовательное применение ХТ и ЛТ. Вопрос о тактике ведения решается индивидуально на мультидисциплинарном консилиуме.
Важнейшими целями современной ЛТ являются максимизация контроля опухоли и минимизация токсичности лечения. Минимальным технологическим стандартом является 3D-ХЛТ.
Более «продвинутые» технологии уместны, когда это необходимо для безопасного подведения дозы ЛТ. Эти технологии включают (но не ограничиваются ими) 4D-КТ и/или ПЭТ-КТ, IMRT, VMAT, IGRT (конформная дистанционная лучевая терапия, в том числе IMRT, IGRT, ViMAT, стереотаксическая), синхронизацию дыхания.
Рандомизированные исследования применяемых сегодня технологий ЛТ демонстрируют снижение токсичности и улучшение выживаемости по сравнению с более старыми методами. В проспективном исследовании «радикальных программ» ХЛТ для пациентов с НМРЛ III стадии (RTOG 0617) IMRT ассоциировалась с почти 60%-ым снижением (с 7,9% до 3,5%) частоты лучевых пневмонитов, а также аналогичными улучшениями выживаемости и контроля опухоли по сравнению с 3D-ХЛТ.
Дистанционная ЛТ первичной опухоли и пораженных лимфатических узлов: ЛТ с IMRT, VMAT, IGRT, синхронизацией дыхания (минимально необходимые требования: 3D конформная ЛТ) РОД 2 Гр, СОД 60Гр +/- 10%Гр (КТ, ПЭТ).
Проведение индукционной ХТ не целесообразно, так как этот подход не позволяет достичь преимуществ в эффективности над стандартной ХЛТ. Индукционную ХТ следует рассматривать при значительных размерах опухоли и невозможности достижения запланированных объемов облучения. Не показано проведение консолидирующей ХТ после ХЛТ в связи с отсутствием преимуществ в ВБП. Режимы химиотерапии, применяемые в комбинации с лучевой терапией указаны в таблице 4.
Таблица 4. Режимы химиотерапии, часто применяемые в лечении IIIА, IIIB, IIIC стадий НМРЛ в комбинации с лучевой терапией
Схема лечения |
#Паклитаксел** 175-200 мг/м2 в/в в 1-й день + карбоплатин** AUC 5 (фактическая доза карбоплатина** рассчитывается индивидуально, исходя из уровня креатинина в крови пациента накануне проведения лечения) в/в капельно в 1-й день, интервал 3 нед., 3-4 курса [350, 351, 352]. |
#Пеметрексед** 500 мг/м2 в/в капельно в 1-й день + цисплатин** 75 мг/м2 (или карбоплатин** AUC 5 (фактическая доза карбоплатина** рассчитывается индивидуально, исходя из уровня креатинина в крови пациента накануне проведения лечения)) в/в капельно в 1-й день каждые 3 нед., 3 курса одновременно с ЛТ (при неплоскоклеточном НМРЛ) [38] |
Этопозид** 50 мг/м2 в/в в 1-5-й, 29–33-й дни + цисплатин** 50 мг/м2 в 1, 8, 29, 36-й дни одновременно с ЛТ [39,40] |
#Паклитаксел** 50 мг/м2 в/в + карбоплатин** AUC 2 (фактическая доза карбоплатина** рассчитывается индивидуально, исходя из уроня креатинина в крови пациента накануне проведения лечения) в/в капельно еженедельно на фоне ЛТ |
Примечание: фактическая доза карбоплатина** рассчитывается индивидуально, исходя из уровня креатинина в крови пациента накануне проведения лечения.
После завершения ХЛТ в одновременном или последовательном вариантах пациентам, не имеющим признаков прогрессирования заболевания (контрольное КТ органов грудной полости и УЗИ органов брюшной полости (комплексное), другие дополнительные исследования по показаниям целесообразно проводить непосредственно после окончания ХЛТ) и противопоказаний к иммунотерапии, без активирующих мутаций в гене EGFR/ALK и при уровне экспрессии PD-L1 более 1% рекомендуется иммунотерапия дурвалумабом**. С началом поддерживающего этапа не позже 60 дней** независимо от окончания лучевой терапии, уровня экспрессии PD-L1. [42].
Уровень убедительности рекомендаций – A (уровень достоверности доказательств – 2).
Комментарии: Препарат назначается в дозе 10 мг/кг в виде 60-минутной в/в инфузии каждые 2 нед. либо в дозе 1500 мг в виде 60-минутной в/в инфузии каждые 4 нед. в течение не менее 12 мес. или до прогрессирования или развития непереносимой токсичности. Поддерживающая терапия дурвалумабом** у больных с драйверными мутациями в генах EGFR или ALK может быть ассоциирована с более низкой эффективностью [42].
У больных с активирующими мутациями в гене EGFR (делеция в 19 экзоне и мутация L858R) рекомендуется поддерживающая терапия осимертинибом** (80 мг в сут внутрь до прогрессирования или непереносимой токсичности) после ХЛТ улучшает безрецидивную выживаемость [241, 345].
Уровень убедительности рекомендаций – A (уровень достоверности доказательств – 2).
Пациентам с неоперабельными локорегиональными рецидивами после радикального хирургического лечения возможно проведение ХЛТ. Возможно проведение 3-4 циклов ХТ перед ЛТ, либо 2-4 циклов ХТ одновременно с ЛТ. После окончания ЛТ в отсутствие признаков прогрессирования процесса необходимо рассмотреть вопрос о проведении консолидирующей иммунотерапии дурвалумабом** в течение 12 месяцев. Для достижения максимальной эффективности и безопасности комбинированного лечения (ХЛТ + иммунотерапия) крайне важным является мультидисциплинарное планирование стратегии лечения пациентов с III стадией НМРЛ, преемственность между специалистами, сокращение сроков между окончанием ХЛТ и началом иммунотерапии.
При противопоказаниях к ХЛТ рекомендуется проводить системное лекарственное лечение (см. раздел 3.1.3.1), включая молекулярно-направленное и иммунотерапию. При наличии противопоказаний к проведению химиотерапии возможно рассмотреть вариант проведения ЛТ в монорежиме [317].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
3.1.3. Принципы лечения пациентов с IV стадией заболевания
Рекомендуется проводить противоопухолевую лекарственную терапию. Лечение пациентов с IV стадией НМРЛ следует расценивать как паллиативное, направленное на увеличение продолжительности жизни, улучшение ее качества и эффективный контроль за симптомами болезни. Раннее начало противоопухолевой терапии, поддерживающей и сопроводительной симптоматической терапии увеличивает продолжительность жизни [7, 12].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Пациентам с IV стадией рекомендуется назначать лечение с учетом предиктивных и прогностических факторов [43, 44].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5).
Комментарии: режимы 1-й линии комбинированной платиносодержащей химиотерапии немелкоклеточного рака легкого IV стадии представлены в табл. 5.
При выявлении активирующих мутаций гена EGFR (18-21-й экзоны) или транслокаций ALK, ROS1, мутации BRAF V600E, рекомендуется назначение таргетной терапии [43–51] (см. 3.1.3.4.).
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
При отсутствии драйверных молекулярно-генетических нарушений рекомендуется ХТ, химиоиммунотерапия или ИТ в зависимости от ряда клинических и лабораторных параметров, в некоторых случаях с учетом уровня экспрессии PD-L1 опухолевыми клетками (см. 3.1.3.1 Химиотерапия 1-й линии) [12].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
3.1.3.1. Химиотерапия 1-й линии
Рекомендации по применению активных режимов 1-й линии комбинированной платиносодержащей ХТ для лечения пациентов с IV стадией НМРЛ (табл. 5) представлены ниже.
Таблица 5. Активные режимы 1-й линии комбинированной платиносодержащей химиотерапии немелкоклеточного рака легкого IV стадии
Препарат |
Схема лечения |
Источник |
Этопозид** + цисплатин** |
100 мг/м2 в/в в 1, 2, 3-й дни. 100 мг/м2 в/в в 1-й день каждые 3 нед |
[76] |
Этопозид** + карбоплатин** AUC 5 |
100 мг/м2 в/в в 1-3-й дни. В/в в 1-й день каждые 3 нед |
[295, 397, 398] |
Винорелбин** +цисплатин** |
25 мг/м2 в/в (или 60-80 мг/м2 внутрь) в 1-й и 8-й дни. 80 мг/м2 в/в в 1-й день каждые 3 нед |
[55] |
#Паклитаксел** + карбоплатин** AUC 6 ± бевацизумаб** |
175-200 мг/м2 в 1-й день. В/в в 1-й день каждые 3 нед. 15 мг/кг 1 раз в 3 нед до прогрессирования (только при аденокарциноме) |
[56, 296] |
Гемцитабин** + цисплатин** |
1250 мг/м2 в 1-й и 8-й дни. 80 мг/м2 в 1-й день каждые 3 нед |
[55, 57] |
Гемцитабин** + карбоплатин** AUC 5 |
1250 мг/м2 в 1-й и 8-й дни. В/в в 1-й день каждые 3 нед |
[353,399] |
|
Пеметрексед** + цисплатин** или #Пеметрексед + карбоплатин**AUC5 с премедикацией фолиевой кислотой** и цианкобаламином** для уменьшения токсичности ± бевацизумаб** |
500 мг/м2 в 1-й день. 75 мг/м2 в 1-й день каждые 3 нед. Фолиевая кислота** по 350-1000 мкг, в среднем 400 мг как минимум за 5 дней до начала лечения пеметрекседом** и цианкобаламин** (витамин В12) в дозе 1000 мкг в/м в период за 7 дней до начала лечебного цикла). 7,5-15 мг/кг 1 раз в 3 нед до прогрессирования (только при аденокарциноме) |
[59, 60, 354] |
** Жизненно необходимые и важнейшие лекарственные препараты;
# – препарат, применяющийся не в соответствии с показаниями к применению и противопоказаниями, способами применения и дозами, содержащимися в инструкции по применению лекарственного препарата.
Примечание: фактическая доза карбоплатина** рассчитывается индивидуально, исходя из показателя креатинина в анализе крови пациента накануне проведения лечения.
Сокращения: в/в – внутривенно, AUC – площадь под фармакологической кривой.
Комментарий: комбинация цисплатина** с пеметрекседом** у пациентов с неплоскоклеточным НМРЛ в метаанализе показала преимущество по сравнению с комбинацией с гемцитабином**[60].
Всем пациентам с IV стадией НМРЛ без активирующих мутаций в состоянии, оцениваемом в 0-2 балла по шкале ECOG (см. приложение Г3), при отсутствии противопоказаний рекомендуется проведение комбинированной платиносодержащей ХТ [62–64].
Уровень убедительности рекомендаций – A (уровень достоверности доказательств – 1).
Комментарии: режимы представлены в таблице 5. Целесообразны 4 цикла ХТ при контроле роста опухоли (стабилизации, полном или частичном регрессе); число циклов может быть увеличено до 6 при нарастающем объективном эффекте и удовлетворительной переносимости [65]. При неплоскоклеточном РЛ при отсутствии признаков прогрессирования заболевания после 4-6 циклов лечения возможна поддерживающая терапия пеметрекседом**, или бевацизумабом**, или их комбинацией, если эти препараты входили в схему 1-й линии лечения. Для контроля эффективности лечения необходимо проводить обследование с использованием методов объективной визуализации (КТ, рентгенографии, МРТ, ПЭТ-КТ, сцинтиграфии костей скелета) до начала лечения, после каждых 2 циклов ХТ в сроки около 2 нед от 1-го дня четного циклов и далее 1 раз в 6-12 нед с учетом клинических показаний. Представляется целесообразным применять тот же метод оценки, что и до начала лечения.
Рекомендуется рассмотреть возможность проведения монохимиотерапии (винорелбин**, гемцитабин**, этопозид**, пеметрексед**) для лечения пациентов, состояние которых оценивается в 2 балла по шкале ECOG (см. приложение Г3); в качестве минимального варианта лечения.
этопозидом** 50 мг/м2 внутрь в течение 14-21 дня с повторением циклов каждые 28 дней [54; 273, 297];
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 4).
винорелбином** (прием внутрь или внутривенное введение), пеметрекседом** (при неплоскоклеточном НМРЛ), таксанами, гемцитабином** [67–69].
Уровень убедительности рекомендаций – B (уровень достоверности доказательств – 2).
Комментарии: режимы см. табл. 6.
моноиммунотерапия пембролизумабом** при уровне экспрессии PD-L1 >50% [78],
Уровень убедительности рекомендаций – A (уровень достоверности доказательств – 2).
При непереносимости ХТ и экспрессии PD-L1 >1% может быть рекомендован пембролизумаб** [242].
Уровень убедительности рекомендаций – B (уровень достоверности доказательств – 2).
При непереносимости ХТ и ECOG 2 при любом уровне PD-L1 может быть рекомендован атезолизумаб** [242]
Уровень убедительности рекомендаций – B (уровень достоверности доказательств – 2).
Таблица 6. Режимы терапии для лечения пациентов, состояние которых оценивается в 2 балла по шкале ECOG
4.1. Предреабилитация
Пациентам перед проведением оперативного вмешательства рекомендуется проведение физической предреабилитации, которая значительно улучшает функциональное состояние дыхательной мускулатуры и биомеханику дыхания, что увеличивает вентиляционную способность легких, повышает бронхиальную проходимость, ускоряет функциональное восстановление дыхательной системы, значительно сокращает сроки пребывания в стационаре после операции, а также снижает частоту развития осложнений и летальных исходов на фоне лечения онкологического заболевания [145].
Уровень убедительности рекомендаций – А (уровень достоверности доказательств – 2).
Комментарий: аэробная направленность физической предреабилитации улучшает крово- и лимфообращение, вентиляционную активность легких, повышает толерантность к физическим нагрузкам, а также качество жизни [146].
Пациентам перед проведением оперативного вмешательства рекомендуется выполнение комплекса физических упражнений на этапе предреабилитации, что достоверно увеличивает жизненную емкость легких на 630 мл и объем форсированного выдоха на 420 мл, а также сокращает продолжительность госпитального лечения на 4,83 дня и риск развития послеоперационных осложнений на 45% [147].
Уровень убедительности рекомендаций – В (уровень достоверности доказательств – 1).
Комментарии: эффективное применение дыхательной гимнастики в ходе предреабилитации снижает частоту послеоперационных легочных осложнений и сокращает срок пребывания в стационаре [148].
-
Для диагностики нутритивной недостаточности рекомендуется регулярно оценивать количественный и качественный состав рациона питания, динамику МТ, индекса МТ (ИМТ), начиная с момента постановки диагноза и далее, на протяжении всего противоопухолевого лечения. При выявлении недостаточности питания необходимо оценить количественный и качественный состав пищевого рациона, диспепсические проблемы, мышечную массу, физическую работоспособность и степень системного воспаления. Энергетические потребности, если они не измерялись индивидуально, следует считать равными 25-30 ккал/кг массы тела в день. Потребности в белке должны составлять 1,0-1,5 г/кг массы тела в день. Объём витаминов и минералов равен стандартным дневным нормам. Назначение высоких доз микроэлементов возможно только при доказанной недостаточности конкретного нутриента.
С целью сохранения энергетической плотности и снижения гликемической нагрузки при сочетании нутритивной недостаточности и инсулинорезистетности необходимо увеличение в рационе питания количества жиров на фоне снижения количества углеводов.
У больных с различной степенью недостаточности питания или риском её развития, способных питаться самостоятельно, рекомендуется коррекция пищевого рациона, лечение диспепсических расстройств, а при недостижении целевых значений энергетического и белкового обеспечения – использование специализированного лечебного питания в виде сипинга. Не рекомендуется использование любых низкокалорийных диет [281].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств 5).
Рекомендуется всем пациентам как можно раньше отказаться от табакокурения, поскольку отказ от курения на любом этапе постановки диагноза или проведения специфического лечения способствует улучшению его результатов и повышает общую выживаемость [282,283]
Уровень убедительности рекомендаций – А (уровень достоверности доказательств – 2).
4.2 Первый этап реабилитации после хирургического лечения
Пациентам в раннем послеоперационном периоде рекомендуется использовать тактику fast track rehabilitation («быстрый путь») и ERAS (early rehabilitation after surgery – медицинская реабилитации пациента, перенесшего операцию по поводу онкологического заболевания), включающую комплексное обезболивание, раннее энтеральное питание, отказ от рутинного применения зондов и дренажей, раннюю мобилизацию пациентов в 1-е сутки после операции [148, 149].
80
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Комментарии: данная тактика снижает риск ранних послеоперационных осложнений, уменьшает длительность пребывания в стационаре и частоту повторных госпитализаций [150]. Кроме того, ранняя мобилизация в комплексе с применением антикоагулянтов (антитромботические средства) и эластической компрессии нижних конечностей способствует профилактике тромбоэмболических осложнений в послеоперационном периоде [150]. Дополнительное энтеральное питание, позволяющее обеспечить суммарную калорийность пищевого рациона из расчета 25 ккал/кг МТ в день, положительно влияет на восстановление дыхательной функции в послеоперационном периоде, способствует улучшению общих результатов лечения и снижает общую летальность в течение первого года после оперативного вмешательства [284].
Пациентам после проведения лобэктомии рекомендуется рассматривать возможность кинезиологического тейпирования, которое достоверно снижает интенсивность болевого синдрома в послеоперационном периоде [149].
Уровень убедительности рекомендаций – A (уровень достоверности доказательств – 2).
Пациентам после проведения лобэктомии рекомендуется глубокая высокочастотная осцилляция и вибрационный массаж грудной клетки, проводимые в раннем послеоперационном периоде, которые увеличивают объем форсированного выдоха в раннем послеоперационном периоде, способствуя возрастанию парциального давления кислорода в артериальной крови [315,316].
Уровень убедительности рекомендаций – A (уровень достоверности доказательств – 2).
4.3. Второй этап реабилитации после хирургического лечения
Пациентам, перенесшим оперативные вмешательства по поводу РЛ, рекомендуется адекватная физическая активность, чередование аэробных и анаэробных нагрузок, сочетание дыхательных статических и динамических упражнений с целью улучшения показателей внешнего дыхания, повышения общей физической работоспособности, расширения адаптивных возможностей организма, улучшения качества жизни пациентов [153].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Пациентам, перенесшим оперативные вмешательства по поводу РЛ, рекомендуются регулярные занятия лечебной физкультурой, которая улучшает функцию внешнего дыхания, увеличивает выносливость, положительно влияет на психологический статус пациента, уменьшает выраженность тревожности и депрессии, слабости, болевого синдрома, улучшает настроение [154, 155].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 4).
Комментарии: после комбинированного лечения злокачественных новообразований легких работа с медицинским психологом, методики релаксации, методы когнитивно-поведенческой терапии снижают симптомы депрессии и тревоги [156–159].
4.4. Третий этап реабилитации после хирургического лечения
Пациентам после комплексного лечения РЛ рекомендуется вести активный образ жизни с целью достижения компенсированного функционального состояния, ускорения социальной адаптации и предотвращения формирования хронического стрессорного состояния [155], поддерживать оптимальную МТ (ИМТ 18,5-25 кг/м2), соблюдать диету, включающую достаточное количество овощей, фруктов и цельнозерновых продуктов (400-600 г в день) с низким содержанием жиров, красного мяса и алкоголя [281].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Комментарии: Лечебная физкультура и повышение физической активности сопровождаются уменьшением слабости, повышением мобильности пациента, снижают уровень депрессии, улучшают качество жизни и являются мерой профилактики сердечно-сосудистых и легочных осложнений [160, 162]. Применение методик аудиовизуальной релаксации достоверно уменьшает выраженность болевого синдрома, усталости, тревожности, улучшает качество жизни и социальную адаптацию пациента [162].
Рекомендуется отказаться от табакокурения, поскольку это увеличивает общую выживаемость больных [283].
Уровень убедительности рекомендаций – А (уровень достоверности доказательств – 2).
4.5. Реабилитация при химиотерапии
Пациентам, получающим ХТ, рекомендуется обеспечить адекватное питание и поддержание физической активности. Если при проведении химиотерапии, несмотря на консультации врача-диетолога и назначение сипинга, пациент не получает достаточное количество нутриентов, рекомендуется дополнительное энтеральное питание, а если его недостаточно или его проведение невозможно, то парентеральное питание [281].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Комментарии. Различные варианты химиотерапии вызывают нутритивную недостаточность разной степени. Например, потеря МТ является частым побочным эффектом таргетной терапии. Доказано, что стабилизация МТ у пациентов с новообразованиями лёгких коррелирует со значительным улучшением выживаемости, однако в настоящее время исследований, анализирующих взаимосвязь между улучшением нутритивного статуса, эффективностью химиотерапии и увеличением выживаемости, немного [281].
Пациентам, получающим ХТ, рекомендуется проведение сеансов акупунктуры, которая увеличивает уровни ИЛ-2, CD3+ и CD4+, уменьшает супрессию костного мозга, а также снижает слабость и тошноту, улучшает показатели качества жизни [161].
Уровень убедительности рекомендаций – B (уровень достоверности доказательств – 2).
При возникновении индуцированной ХТ полинейропатии пациентам рекомендуется выполнять физические упражнения, практиковать терренное лечение (лечение ходьбой) с целью контроля клинических проявлений полинейропатии [162].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 3).
Комментарий: упражнения на тренировку баланса более эффективны для коррекции полинейропатии, чем сочетание упражнений на выносливость и силовых упражнений [163]; регулярное выполнение комплексов лечебной физкультуры на фоне ХТ снижает частоту развития кардиальных осложнений [165].
В комплексном лечении периферической полинейропатии на фоне ХТ пациентам рекомендуется применение по показаниям физиотерапевтических методов лечения: низкоинтенсивной лазеротерапии, низкочастотной магнитотерапии, чрескожной короткоимпульсной электростимуляции (ЧЭНС) [163, 164, 165].
Уровень убедительности рекомендаций – В (уровень достоверности доказательств – 2).
Для профилактики мукозита полости рта на фоне ХТ пациентам рекомендуется проведение низкоинтенсивной лазеротерапии [166].
Уровень убедительности рекомендаций – А (уровень достоверности доказательств – 1).
Для профилактики алопеции на фоне ХТ пациентам рекомендуется использование систем охлаждения кожи головы (например: аппарат для профилактики алопеции при химиотерапии и др.) [167].
Уровень убедительности рекомендаций – B (уровень достоверности доказательств – 3).
Для восстановления когнитивных функций (объем рабочей памяти, устойчивость внимания), снижения уровня тревоги, улучшения функции дыхания и вариабельности сердечного ритма пациентам рекомендована БОС-терапия (различные методики с биологической обратной связью), 20– 30 сеансов [168].
Уровень убедительности рекомендаций – B (уровень достоверности доказательств – 3).
4.6. Реабилитация при лучевой терапии
Для улучшения функции внешнего дыхания, уменьшения слабости, снижения числа осложнений, улучшения качества жизни пациентам во время проведения ЛТ пациентам рекомендуется заниматься лечебной физкультурой (аэробная нагрузка в сочетании с силовой) [169].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Для профилактики лучевого дерматита пациентам рекомендуется низкоинтенсивная лазеротерапия [170].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Для повышения адаптивности пациентов к новому образу жизни, снижения симптомов тревожных, депрессивных расстройств и повышения совладания со стрессовыми ситуациями вне и после терапевтических сессий рекомендуется проводить краткосрочные психотерапевтические сессии в рамках когнитивно-поведенческой психотерапии (КПТ) длительность 45-60 мин в течение 2 мес [171].
Уровень убедительности рекомендаций – B (уровень достоверности доказательств – 2).
Для адекватного обеспечения нутриентами, стабилизации питательного статуса, а также во избежание перерывов в лучевой терапии, рекомендуется консультации диетолога (прием (осмотр, консультация) врача-диетолога первичный, прием (осмотр, консультация) врача-диетолога повторный) и/или назначение сипинга. При тяжёлом лучевом мукозите рекомендуется проведение энтерального питания через назогастральный зонд или чрескожную эндоскопическую гастростому. Парентеральное питание показано в случае невозможности проведения адекватного перорального или энтерального питания [281].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Пациентам рекомендуется отказ от курения, как от активного, так и от пассивного, c целью профилактики возникновения РЛ. Существует прямо пропорциональная зависимость между количеством сигарет, выкуриваемых за день, и риском возникновения РЛ. Пассивное курение повышает риск развития РЛ на 20-30% [7, 12].
Уровень убедительности рекомендаций – С (уровень достоверности доказательства – 5).
Комментарий: Курение ассоциировано с худшей общей и онкологической выживаемостью. Продолжение табакокурения пациентами после постановки диагноза рака легкого негативно влияет на их общую выживаемость и отрицательно влияет на результаты противоопухолевой терапии. Табакокурение достоверно повышает уровень послеоперационных осложнений и смертности таких пациентов. Табакокурение увеличивает риск осложнений, связанных с лучевой терапией, достоверно снижает ответ на проводимую терапию. Табакокурение, вероятно, изменяет метаболизм и эффективность химио- и таргетной терапии [290].
Рекомендуется пациентам своевременное лечение заболеваний легких (например, хроническая обструктивная болезнь легких), которые могут повышать риск возникновения рака легкого [7, 12].
Уровень убедительности рекомендаций – С (уровень достоверности доказательства – 5).
Рекомендуется использовать современные средства защиты лицам, контактирующим с веществами, обладающими канцерогенным действием: асбестом, хромом, никелем, кадмием, мышьяком, дизельным топливом и прочими с целью первичной профилактики [7, 12].
Уровень убедительности рекомендаций – С (уровень достоверности доказательства – 5).
Рекомендуется соблюдать следующую периодичность наблюдения врачом-онкологом (прием (осмотр, консультация) врача-онколога первичный/повторный) пациентов в удовлетворительном состоянии после радикального лечения РЛ: каждые 3 мес в течение первых 3 лет и каждые 6 мес в течение 4-го и 5-го годов. Применяются следующие методы наблюдения: физикальный осмотр, ультразвуковое исследование органов брюшной полости (комплексное), забрюшинного пространства, лимфатических узлов и рентгенография лёгких или КТ головного мозга с в/в контрастированием, МРТ головного мозга с контрастированием, сцинтиграфия костей всего тела проводятся 1 раз в год. Через 5 лет после операции обследование проходят раз в год [12].
Уровень убедительности рекомендаций – С (уровень достоверности доказательства – 5).
Не рекомендуется проведение ПЭТ-КТ в качестве метода наблюдения пациентов [7, 12].
Уровень убедительности рекомендаций – С (уровень достоверности доказательства – 5).
Пациентам с МРЛ, которым не было выполнено профилактическое облучение головного мозга, рекомендуется проведение МРТ головного мозга каждые 3-4 мес в течение первых 2 лет [12].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Комментарий: задачей наблюдения является раннее выявление прогрессирования заболевания с целью раннего начала ХТ или хирургического удаления резектабельных метастатических очагов, рецидивных опухолей.
5.1 Профилактика и лечение осложнений злокачественных опухолей и противоопухолевой лекарственной терапии
При проведении противоопухолевой лекарственной терапии препаратами с эметогенным побочным действием пациентам рекомендуется проведение профилактики и лечения тошноты и рвоты [1, 2].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Комментарии: Принципы диагностики, профилактики и лечения тошноты и рвоты при проведении противоопухолевой лекарственной терапии изложены в Практических Рекомендациях Российского общества клинической онкологии по профилактике и лечению осложнений злокачественных опухолей и противоопухолевой лекарственной терапии: Владимирова Л.Ю. и соавт. Тошнота и рвота [3]. https://rosoncoweb.ru/standarts/?chapter=nausea_vomiting
У пациентов с метастатическим поражением костей рекомендуется профилактика и лечение костных осложнений [4].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Комментарии: Принципы диагностики, профилактики и лечения костных осложнений изложены в Практических Рекомендациях Российского общества клинической онкологии по профилактике и лечению осложнений злокачественных опухолей и противоопухолевой лекарственной терапии: Багрова С.Г. и соавт. Патология костной ткани [5]. https://rosoncoweb.ru/standarts/?chapter=bone_pathology
Пациентам с факторами риска развития тромбоэмболических осложнений рекомендуется профилактика и лечение венозных тромбоэмболических осложнений [6-8].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Комментарии: Принципы диагностики, профилактики и лечения венозных тромбоэмболических осложнений изложены в Практических Рекомендациях Российского общества клинической онкологии по профилактике и лечению осложнений злокачественных опухолей и противоопухолевой лекарственной терапии: Сомонова О.В. и соавт. Тромбоэмболические осложнения [9]. https://rosoncoweb.ru/standarts/?chapter=thromboembolism
При проведении противоопухолевой лекарственной терапии пациентам рекомендуется профилактика и лечение фебрильной нейтропении и инфекционных осложнений [10-12].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Комментарии: Детальный алгоритм диагностики, профилактики и лечения фебрильной нейтропении и инфекционных осложнений, принципы антибактериальной терапии изложены в Практических Рекомендациях Российского общества клинической онкологии по профилактике и лечению осложнений злокачественных опухолей и противоопухолевой лекарственной терапии: Сакаева Д.Д. и соавт. Практические рекомендации по диагностике и лечению фебрильной нейтропении [13]. https://rosoncoweb.ru/standarts/?chapter=febrile_neutropenia
При проведении противоопухолевой лекарственной терапии пациентам рекомендуется коррекция гепатотоксичности [14, 15].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5).
Комментарии: Принципы диагностики, профилактики и лечения гепатотоксичности изложены в Практических Рекомендациях Российского общества клинической онкологии по профилактике и лечению осложнений злокачественных опухолей и противоопухолевой лекарственной терапии: Ткаченко П.Е. и соавт. Гепатотоксичность [16]. https://rosoncoweb.ru/standarts/?chapter=hepatotoxicity
При проведении пациентам противоопухолевой лекарственной терапии рекомендуется профилактика и лечения кардиоваскулярных осложнений [8, 9].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5).
Комментарии: Принципы диагностики, профилактики и лечения сердечно-сосудистых осложнений при проведении противоопухолевой терапии изложены в Практических Рекомендациях Российского общества по профилактике и лечению осложнений злокачественных опухолей и противоопухолевой лекарственной терапии: Виценя М.В. и соавт. Кардиоваскулярная токсичность [21]. https://rosoncoweb.ru/standarts/?chapter=cardiovascular_toxicity
При проведении противоопухолевой лекарственной терапии пациентам рекомендуется профилактика и лечение дерматологических реакций [8, 9].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5).
Комментарии: Принципы диагностики, профилактики и лечения кожных осложнений изложены в Практических Рекомендациях Российского общества клинической онкологии по профилактике и лечению осложнений злокачественных опухолей и противоопухолевой лекарственной терапии: Королева И. А. и соавт. Дерматологические реакции [23]. https://rosoncoweb.ru/standarts/?chapter=dermatological_reactions
Для поддержания метаболических резервов организма онкологического пациента и повышения его устойчивости к лечению (хирургическому, лекарственному, лучевому) рекомендована нутритивная поддержка. Выбор метода нутритивной поддержки определяется различными видами нарушений питания у пациента. Может быть рекомендована установка назогастральной, назоинтестинальной, чрескожной, эндоскопической, лапароскопической, лапаротомной стомы, эндоскопическое стентирование при опухолевом стенозе, паллиативная лучевая терапия [8, 9].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5).
Комментарии: Принципы проведения нутритивной поддержки представлены в Практических рекомендациях Российского общества клинической онкологии по профилактике и лечению осложнений злокачественных опухолей и противоопухолевой лекарственной терапии: Сытов А.В. и соавт. Нутритивная поддержка [26]. https://rosoncoweb.ru/standarts/?chapter=nutritional_support
При проведении противоопухолевой лекарственной терапии пациентам рекомендуется профилактика и лечение нефротоксичности [8, 9].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Комментарии: Детальный алгоритм диагностики, профилактики и лечения нефротоксичности представлен в Практических рекомендациях Российского общества клинической онкологии по профилактике и лечению осложнений злокачественных опухолей и противоопухолевой лекарственной терапии: Громова Е.Г. и соавт. Нефротоксичность [30]. https://rosoncoweb.ru/standarts/?chapter=nephrotoxicity
При проведении противоопухолевой лекарственной терапии пациентам рекомендуется профилактика и лечение иммуноопосредованных нежелательных явлений [8, 9].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5).
Комментарии: Детальный алгоритм диагностики, профилактики и лечения иммуноопосредованных нежелательных явлений изложен в Практических Рекомендациях Российского общества клинической онкологии по профилактике и лечению осложнений злокачественных опухолей и противоопухолевой лекарственной терапии: Новик А.В., Проценко С.А. и соавт. Иммуноопосредованные нежелательные явления [35]. https://rosoncoweb.ru/standarts/?chapter=immunerelated_adverse_events
При проведении противоопухолевой лекарственной терапии пациентам рекомендуется профилактика и лечение мукозитов [8, 9].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5).
Комментарии: Детальный алгоритм диагностики, профилактики и лечения мукозитов изложен в Практических Рекомендациях Российского общества клинической онкологии по профилактике и лечению осложнений злокачественных опухолей и противоопухолевой лекарственной терапии: Семиглазова Т.Ю. и соавт. Мукозиты [38]. https://rosoncoweb.ru/standarts/?chapter=mucositis
Пациентам рекомендуется лечение анемии, которая возникает как симптом злокачественного новообразования и как нежелательное явление при проведении противоопухолевой лекарственной терапии [8, 9].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5).
Комментарии: Порядок и принципы профилактики и лечения анемии соответствуют принципам, изложенным в клинических рекомендациях «Анемия при злокачественных новообразованиях» (ID: КР624, год утверждения 2024, www.cr.rosminzdrav.ru) и в Практических Рекомендациях Российского общества клинической онкологии по профилактике и лечению осложнений злокачественных опухолей и противоопухолевой лекарственной терапии: Орлова Р.В. и соавт. Анемия [41]. https://rosoncoweb.ru/standarts/?chapter=anemia
При проведении лечения пациентам рекомендуется лечение синдрома анорексии-кахексии [8, 9].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5).
Комментарии: Детальный алгоритм диагностики и лечения синдрома анорексии-кахексии изложен в Практических Рекомендациях Российского общества клинической онкологии по профилактике и лечению осложнений злокачественных опухолей и противоопухолевой лекарственной терапии: Сытов А.В. и соавт. Практические рекомендации по лечению синдрома анорексии-кахексии у онкологических больных [43]. https://rosoncoweb.ru/standarts/?chapter=anorexia-cachexia
При проведении пациентам цикловой противоопухолевой лекарственной терапии с включением непрерывных длительных (свыше 6 часов) инфузий противоопухолевых препаратов (доксорубицина** и т.д.) или при неудовлетворительном состоянии периферических вен рекомендуется использование центрального венозного доступа и инфузионных помп [8, 9].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5).
Комментарии: Выбор варианта центрального доступа определяется запланированной длительностью всего курса лечения, предпочтениями пациента, анатомическими особенностями. При длительных (свыше 3 месяцев) курсах терапии наиболее удобным является имплантация подкожной венозной порт-системы. При меньших сроках альтернативой может служить периферически имплантируемый центральный венозный катетер. Принципы использования центрального венозного доступа изложены в Практических Рекомендациях Российского общества клинической онкологии по профилактике и лечению осложнений злокачественных опухолей и противоопухолевой лекарственной терапии: Исянгулова А.З. и соавт. Центральный венозный доступ [45].https://rosoncoweb.ru/standarts/?chapter=central_venous_access
При проведении противоопухолевой лекарственной терапии пациентам рекомендуется профилактика и лечение экстравазатов противоопухолевых препаратов. При планировании противоопухолевой лекарственной терапии важен выбор сосудистого доступа для профилактики экстравазации противоопухолевых препаратов [8, 9].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Комментарии: Алгоритмы выбора сосудистого доступа, профилактики, диагностики и лечения эксравазации изложены в Практических Рекомендациях Российского общества клинической онкологии по профилактике и лечению осложнений злокачественных опухолей и противоопухолевой лекарственной терапии: Буйденок Ю.В. и соавт. Экстравазация противоопухолевых препаратов [47]. https://rosoncoweb.ru/standarts/?chapter=extravasation_antitumor_drugs
При проведении противоопухолевого лечения пациентам рекомендуется лечение хронического болевого синдрома [8, 9].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5).
Комментарии: Алгоритмы диагностики и лечения хронического болевого синдрома у онкологических больных изложены в Практических Рекомендациях Российского общества клинической онкологии по профилактике и лечению осложнений злокачественных опухолей и противоопухолевой лекарственной терапии: Когония Л.М. и соавт. Хронический болевой синдром [49]. https://rosoncoweb.ru/standarts/?chapter=chronic_pain_syndrome
При проведении противоопухолевой лекарственной терапии пациентам рекомендуется профилактика и лечение инфузионных реакций [8, 9].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Комментарии: Алгоритмы профилактики, диагностики и лечения инфузионных реакций изложены в Практических Рекомендациях Российского общества клинической онкологии по профилактике и лечению осложнений злокачественных опухолей и противоопухолевой лекарственной терапии: Орлова Р.В. и соавт. Инфузионные реакции [51]. https://rosoncoweb.ru/standarts/?chapter=infusion_reactions
При проведении терапии пациентам рекомендуется мониторинг и лечение реактивации/обострения хронических вирусных гепатитов [8, 9].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5).
Комментарии: Принципы мониторинга и лечебной тактики у онкологических пациентов с хроническим вирусным гепатитом изложены в Практических Рекомендациях Российского общества клинической онкологии по профилактике и лечению осложнений злокачественных опухолей и противоопухолевой лекарственной терапии: Феоктистова П.С. и соавт. Хронические вирусные гепатиты [53]. https://rosoncoweb.ru/standarts/?chapter=chronic_viral_hepatitis
При проведении противоопухолевой лекарственной терапии пациентам рекомендуется профилактика и лечение неврологических осложнений [8, 9].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5).
Комментарии:
Принципы диагностики, профилактики и лечения неврологических осложнений противоопухолевой терапии изложены в Практических Рекомендациях Российского общества клинической онкологии по профилактике и лечению осложнений злокачественных опухолей и противоопухолевой лекарственной терапии: Латипова Д.Х. и соавт. Неврологические осложнения [55]. https://rosoncoweb.ru/standarts/?chapter=neurological_complication
При проведении противоопухолевой гормональной терапии пациентам рекомендуется профилактика и лечение гормоноопосредованных побочных явлений [8, 9].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5).
Комментарии: Принципы диагностики, профилактики и лечения гормоноопосредованных побочных явлений изложены в Практических Рекомендациях Российского общества клинической онкологии по профилактике и лечению осложнений злокачественных опухолей и противоопухолевой лекарственной терапии: Стенина М.Б. и соавт. Гормоноопосредованные побочные явления [57]. https://rosoncoweb.ru/standarts/?chapter=hormone-mediated_side_events
При проведении терапии пациентам рекомендуется профилактика и лечение тромбоцитопении, индуцированной противоопухолевой лекарственной терапией [8, 9].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 3).
Комментарии: детальный алгоритм диагностики и лечения тромбоцитопении изложен в Практических Рекомендациях Российского общества клинической онкологии по профилактике и лечению осложнений злокачественных опухолей и противоопухолевой лекарственной терапии: Рыков И.В. и соавт. Тромбоцитопения. https://rosoncoweb.ru/standarts/?chapter=thrombocytopenia
Медицинская помощь, за исключением медицинской помощи в рамках клинической апробации, в соответствии с Федеральным законом от 21.11.2011 № 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации», организуется и оказывается:
1) в соответствии с положением об организации оказания медицинской помощи по видам медицинской помощи, которое утверждается уполномоченным Федеральным органом исполнительной власти;
2) в соответствии с порядками оказания медицинской помощи, утверждаемыми уполномоченным федеральным органом исполнительной власти и обязательными для исполнения на территории Российской Федерации всеми медицинскими организациями
3) на основе настоящих клинических рекомендаций;
4) с учетом стандартов медицинской помощи, утвержденных уполномоченным Федеральным органом исполнительной власти.
Первичная специализированная медико-санитарная помощь оказывается врачом-онкологом и иными врачами-специалистами в центре амбулаторной онкологической помощи, а при его отсутствии в первичном онкологическом кабинете, поликлиническом отделении онкологического диспансера (онкологической больницы).
При подозрении или выявлении у пациента онкологического заболевания врачи-терапевты, врачи-терапевты участковые, врачи общей практики (семейные врачи),
врачи-специалисты, средние медицинские работники в установленном порядке направляют пациента на консультацию в центр амбулаторной онкологической помощи, а при отсутствии в первичный онкологический кабинет, поликлиническое отделение онкологического диспансера (онкологической больницы) для оказания ему первичной специализированной медико-санитарной помощи.
Консультация в центре амбулаторной онкологической помощи либо в первичном онкологическом кабинете, поликлиническом отделении онкологического диспансера (онкологической больницы) не должна превышать срока, установленного в программе государственных гарантий бесплатного оказания гражданам медицинской помощи, утверждаемой Правительством Российской Федерации. Врач-онколог центра амбулаторной онкологической помощи (в случае отсутствия центра амбулаторной онкологической помощи врач-онколог первичного онкологического кабинета или поликлинического отделения онкологического диспансера (онкологической больницы организует взятие биопсийного (операционного) материала, а также организует выполнение иных диагностических исследований, необходимых для установления диагноза, включая распространенность онкологического процесса и стадию заболевания.
В случае невозможности взятия в медицинской организации, в составе которой организован центр амбулаторной онкологической помощи (первичный онкологический кабинет) биопсийного (операционного) материала, проведения иных диагностических исследований пациент направляется врачом-онкологом в онкологический диспансер (онкологическую больницу) или в медицинскую организацию, оказывающую медицинскую помощь пациентам с онкологическими заболеваниями.
Срок выполнения патолого-анатомических исследований, необходимых для гистологической верификации злокачественных новообразований не должен превышать срок, установленный в программе государственных гарантий бесплатного оказания гражданам медицинской помощи, утверждаемой Правительством Российской Федерации.
Сроки проведения диагностических инструментальных и лабораторных исследований в случае подозрения на онкологическое заболевание не должны превышать сроков, установленных в программе государственных гарантий бесплатного оказания гражданам медицинской помощи, утверждаемой Правительством Российской Федерации.
Диагноз онкологического заболевания устанавливается врачом-специалистом на основе результатов диагностических исследований, включающих в том числе проведение цитологической и (или) гистологической верификации диагноза, за исключением случаев, когда взятие биопсийного и (или) пункционного материала не представляется возможным.
Врач-онколог центра амбулаторной онкологической помощи (первичного онкологического кабинета) направляет пациента в онкологический диспансер (онкологическую больницу) или иную медицинскую организацию, оказывающую медицинскую помощь пациентам с онкологическими заболеваниями, в том числе подведомственную федеральному органу исполнительной власти (далее – федеральная медицинская организация), для уточнения диагноза (в случае невозможности установления диагноза, включая распространенность онкологического процесса и стадию заболевания), определения тактики лечения, а также в случае наличия медицинских показаний для оказания специализированной, в том числе высокотехнологичной, медицинской помощи.
В сложных клинических случаях для уточнения диагноза (в случае невозможности установления диагноза, включая распространенность онкологического процесса и стадию заболевания) в целях проведения оценки, интерпретации и описания результатов врач-онколог организует направление:
цифровых изображений, полученных по результатам патоморфологических исследований, в патолого-анатомическое бюро (отделение) четвертой группы (референс-центр) путем информационного взаимодействия, в том числе с применением телемедицинских технологий при дистанционном взаимодействии медицинских работников между собой;
цифровых изображений, полученных по результатам лучевых методов исследований, в дистанционный консультативный центр лучевой диагностики, путем информационного взаимодействия, в том числе с применением телемедицинских технологий при дистанционном взаимодействии медицинских работников между собой;
биопсийного (операционного) материала для повторного проведения патоморфологических, иммуногистохимических, и молекулярно-генетических исследований: в патолого-анатомическое бюро (отделение) четвертой группы (референс-центр), а также в молекулярно-генетические лаборатории для проведения молекулярно-генетических исследований.
Тактика лечения устанавливается консилиумом врачей, включающим врачей-онкологов, врача-радиотерапевта, врача-нейрохирурга (при опухолях нервной системы) медицинской организации, в составе которой имеются отделения хирургических методов лечения злокачественных новообразований, противоопухолевой лекарственной терапии, радиотерапии (далее – онкологический консилиум), в том числе онкологическим консилиумом, проведенным с применением телемедицинских технологий, с привлечением при необходимости других врачей-специалистов.
Диспансерное наблюдение врача-онколога за пациентом с выявленным онкологическим заболеванием устанавливается и осуществляется в соответствии с порядком диспансерного наблюдения за взрослыми с онкологическими заболеваниями.
С целью учета информация о впервые выявленном случае онкологического заболевания направляется в течение 3 рабочих дней врачом-онкологом медицинской организации, в которой установлен соответствующий диагноз, в онкологический диспансер или организацию субъекта Российской Федерации, исполняющую функцию регистрации пациентов с впервые выявленным злокачественным новообразованием, в том числе с применением единой государственной информационной системы в сфере здравоохранения. В случае подтверждения у пациента наличия онкологического заболевания информация об уточненном диагнозе направляется из онкологического диспансера или организации субъекта Российской Федерации, исполняющей функции регистрации пациентов с впервые выявленном злокачественным новообразованием, в медицинскую организацию, осуществляющую диспансерное наблюдение пациента
Специализированная, в том числе высокотехнологичная, медицинская помощь в медицинских организациях, оказывающих медицинскую помощь взрослому населению при онкологических заболеваниях, оказывается по медицинским показаниям, предусмотренным положением об организации оказания специализированной, в том числе высокотехнологичной, медицинской помощи.
Специализированная, за исключением высокотехнологичной, медицинская помощь в медицинских организациях, подведомственных федеральным органам исполнительной власти, оказывается по медицинским показаниям, предусмотренным порядком направления пациентов в медицинские организации и иные организации, подведомственные федеральным органам исполнительной власти, для оказания специализированной (за исключением высокотехнологичной) медицинской помощи, предусмотренного в приложении к положению об организации оказания специализированной, в том числе высокотехнологичной, медицинской помощи. В случае если в реализации Программы принимают участие несколько федеральных медицинских организаций, оказывающих специализированную медицинскую помощь при заболеваниях, состояниях (группе заболеваний, состояний), соответствующих заболеваниям, состояниям (группе заболеваний, состояний) пациента, лечащий врач обязан проинформировать пациента (законного представителя пациента) о возможности выбора федеральной медицинской организации, в том числе о возможных сроках ожидания специализированной медицинской помощи, которые могут превышать сроки ожидания, установленные программой государственных гарантий бесплатного оказания гражданам медицинской помощи.
Сроки ожидания оказания специализированной (за исключением высокотехнологичной) медицинской помощи не должны превышать сроков, установленных в программе государственных гарантий бесплатного оказания гражданам медицинской помощи, утверждаемой Правительством Российской Федерации.
При наличии у пациента с онкологическим заболеванием медицинских показаний для проведения медицинской реабилитации врач-онколог организует ее проведение в соответствии с порядком организации медицинской реабилитации взрослых.
При наличии у пациента с онкологическим заболеванием медицинских показаний к санаторно-курортному лечению врач-онколог организует его в соответствии порядком организации санаторно-курортного лечения.
Паллиативная медицинская помощь пациенту с онкологическими заболеваниями оказывается в соответствии с положением об организации оказания паллиативной медицинской помощи, включая порядок взаимодействия медицинских организаций, организаций социального обслуживания и общественных объединений, иных некоммерческих организаций, осуществляющих свою деятельность в сфере охраны здоровья.
При подозрении и (или) выявлении у пациента онкологического заболевания в ходе оказания ему скорой медицинской помощи его переводят или направляют в медицинские организации, оказывающие медицинскую помощь пациентам с онкологическими заболеваниями, для определения тактики ведения и необходимости применения дополнительно других методов специализированного противоопухолевого лечения.
Показаниями для госпитализации в медицинскую организацию в экстренной или неотложной форме являются:
1) наличие осложнений онкологического заболевания, требующих оказания ему специализированной медицинской помощи в экстренной и неотложной форме;
2) наличие осложнений лечения онкологического заболевания (хирургическое вмешательство, ЛТ, лекарственная терапия и т.д.), требующих оказания ему специализированной медицинской помощи в экстренной и неотложной форме.
Показаниями для госпитализации в медицинскую организацию в плановой форме являются:
1) необходимость выполнения сложных интервенционных диагностических медицинских вмешательств, а также проведение эндоскопических исследований при невозможности выполнить их амбулаторно, требуют последующего наблюдения в условиях круглосуточного или дневного стационара;
2) наличие показаний к специализированному противоопухолевому лечению (хирургическое вмешательство, ЛТ, в том числе контактная, ДЛТ и другие виды ЛТ, лекарственная терапия и др.), требующему наблюдения в условиях круглосуточного или дневного стационара.
Показаниями к выписке пациента из медицинской организации являются:
1) завершение курса лечения или одного из этапов оказания специализированной, в том числе высокотехнологичной, медицинской помощи в условиях круглосуточного или дневного стационара при условии отсутствия осложнений лечения, требующих медикаментозной коррекции и/или медицинских вмешательств в стационарных условиях;
2) отказ пациента или его законного представителя от специализированной, в том числе высокотехнологичной, медицинской помощи в условиях круглосуточного или дневного стационара, установленной консилиумом медицинской организации, оказывающей онкологическую помощь при условии отсутствия осложнений основного заболевания и/или лечения, требующих медикаментозной коррекции и/или медицинских вмешательств в стационарных условиях;
3) в случаях несоблюдения пациентом предписаний или правил внутреннего распорядка лечебно-профилактического учреждения, если это не угрожает жизни пациента и здоровью окружающих;
4) необходимость перевода пациента в другую медицинскую организацию по соответствующему профилю оказания медицинской помощи.
Заключение о целесообразности перевода пациента в профильную медицинскую организацию осуществляется после предварительной консультации по предоставленным медицинским документам и/или предварительного осмотра пациента врачами-специалистами медицинской организации, в которую планируется перевод.
На течение заболевания и эффективность его лечения помимо распространенности опухолевого процесса, морфологической и молекулярно-генетических характеристик опухоли существенное влияние оказывают сопутствующие патологии, адекватность сопроводительной терапии, социальная адаптация пациента, наличие или отсутствие ежедневной физической активности. Рекомендована ежедневная 30-минутная умеренно-интенсивная физическая активность. Отказ от курения улучшает прогноз заболевания [7, 12].














