Кистозный фиброз (муковисцидоз, МВ) — аутосомно-рецессивное моногенное наследственное заболевание, характеризующееся поражением всех экзокринных желёз, а также жизненно важных органов и систем [1,2].
Ген CFTR (МВТР - трансмембранный регулятор проводимости муковисцидоза) был идентифицирован в 1989 г. Ген расположен в середине длинного плеча 7 аутосомы, содержит 27 экзонов и охватывает 250 000 пар нуклеотидов. Он контролирует структуру и функцию одноимённого белка. Последние исследования показали, что МВТР является собственно хлоридным каналом.
Белок МВТР локализуется в апикальной части мембраны эпителиальных клеток, выстилающих выводные протоки желез внешней секреции (потовых, слюнных, желез в бронхах, поджелудочной железе, кишечнике, урогенитальном тракте), он регулирует транспорт электролитов (главным образом хлора) между этими клетками и межклеточной жидкостью. По состоянию на 25 сентября 2024 года на веб-сайте международного проекта CFTR2 (https://cftr2.org) представлены всего 1167 генетических вариантов нуклеотидной последовательности гена CFTR (ГВНП CFTR), из них 1085 клинически значимых (патогенных). Они препятствуют синтезу белка CFTR, его транспорту к апикальной мембране клетки или нарушают его функцию в качестве канала анионов хлора. В зависимости от влияния на функцию белка CFTR все варианты нуклеотидной последовательности гена CFTR подразделяют на 7 основных классов [3,4].
Известно, что один и тот же вариант может вызвать несколько видов нарушения структуры или функции белка, и не для всех вариантов нуклеотидной последовательности гена CFTR определен класс.
Согласно данным национального регистра наиболее часто встречаются следующие мутации: F508del (52,8%), СFTRdele2,3 (6,21%), E92K (3%), 2143delT (2,15%), 3849+10kbC>T (2,02%), W1282X (1,9%), 2184insA (1,85%), 1677delTA (1,81%), N1303K (1,54%), G542X (1,35%), L138ins (1,24%) [5].
Мутации гена CFTR нарушают не только транспорт, но и секрецию ионов хлора. При затруднении их прохождения через клеточную мембрану увеличивается реабсорбция натрия железистыми клетками, нарушается электрический потенциал просвета, что вызывает изменение электролитного состава и дегидратацию секрета желез внешней секреции. В результате выделяемый секрет становится чрезмерно густым и вязким. При этом страдают легкие, желудочно-кишечный тракт, печень, поджелудочная железа, мочеполовая система (табл.1) [1,5].
Таблица 1. Патогенез МВ
Органы и системы |
Патологические процессы |
Конечный результат |
|---|---|---|
Легкие |
Бронхообструкция, снижение толерантности к инфекции, колонизация дыхательных путей Pseudomonas aeruginosa (P. aeruginosa) и другими патологическими микроорганизмами, хроническое воспаление дыхательных путей, бронхоэктазы, деструкция паренхимы легких |
Дыхательная недостаточность, легочная гипертензия, сердечная недостаточность |
Поджелудочная железа |
Обструкция протоков железы, появление кист, недостаточность поджелудочной железы (внутренне - и внешнесекреторная), кишечная мальабсорбция |
Мекониевый илеус Нарушение стула (частый, жирный, зловонный, обильный), снижение нутритивного статуса (у детей – отставание в развитии), авитаминозы, выпадения прямой кишки, сахарный диабет |
Печень |
Холестаз, холелитиаз |
Цирроз печени, синдром портальной гипертензии, гиперспленизм, печеночная недостаточность, желчнокаменная болезнь (ЖКБ) |
Кишечник |
Увеличение вязкости/адгезивности каловых масс |
Кишечная непроходимость СДИО Выпадения прямой кишки |
Околоносовые пазухи |
Обструкция соустий околоносовых пазух, застой слизи в пазухах, колонизация слизистой оболочки полости носа и околоносовых пазух патологической микрофлорой (в том числе P. aeruginosa), формирование полипов в околоносовых пазухах с распространением в полость носа |
Хронический риносинусит, полипы в околоносовых пазухах и полости носа |
Электролитный баланс |
Гипокалиемия, гипонатриемия, гипохлоремия, алкалоз |
Синдром псевдо-Барттера – синдром потери солей |
Репродуктивная система (у мужчин) |
Обструкция и последующая атрезия выносящих протоков яичек. Азооспермия |
Бесплодие |
Прогрессирование легочной и сердечной недостаточности является наиболее частой причиной смерти пациентов (95%).
Спектр микроорганизмов, связанных с инфекциями дыхательных путей у пациентов с МВ продолжает расширяться и исследования микробиома легких у данной категории пациентов демонстрируют сложный синергизм между культивируемыми и некультивируемыми микроорганизмами. Микробиологическая диагностика у пациентов с МВ имеет ряд особенностей, которые необходимо учитывать при организации работы с данной категорией пациентов.
Чаще всего в отделяемом нижних дыхательных путей у пациентов с МВ выявляются S. aureus, P. aeruginosa, B. cepacia complex, S. maltophilia, Achromobacter spp. Более типичные респираторные патогены, такие как H. influenzae, S. pneumoniae, M. catarrhalis также могут играть важную роль в развитии бронхолегочного процесса. У пациентов с МВ может встречается хроническая колонизация микроорганизмами порядка Enterobacterales.
Имеются наблюдения выделения из нижних дыхательных путей пациентов с МВ неферментирующих грамотрицательных бактерий (НГОБ Burkholderia gladioli, Inquilinus spp, Ralstonia spp., Cupriavidus spp., Pandoraea spp.) Данные виды являются близкородственными, имеют генетическое сходство с бактериями рода Burkholderia. Они редко выделяются у пациентов с МВ, однако описаны случаи выделения их при хронической инфекции. Нет достаточного количества исследований, указывающих на возможность передачи штаммов от пациента к пациенту.
Другие микроорганизмы, имеющие этиологическое значение при МВ: нетуберкулезные микобактерии (НТМБ) - Mycobacterium abscessus complex, Mycobacterium avium complex и другие микобактерии, грибы - Aspergillus spp., Scedosporium spp., Trichosporon spp., вирусы - Respiratory syncytial virus, Influenza virus, Adenovirus, Rhinovirus, Coronavirus, Parainfluenza virus, Human metapneumovirus. Возрастает выявляемость нетуберкулезных микобактерий у пациентов старшего возраста. Mycobacterium abscessus complex и Mycobacterium avium complex являются наиболее часто встречающимися [2].
Особенностями хронической инфекции легких у больных муковисцидозом является то, что данная инфекция в 2/3 случаев вызывается не монокультурой, а ассоциацией микроорганизмов. За рубежом эти показатели в два раз ниже — в 35% исследуемых образцов бронхоальвеолярного лаважа (БАЛ) выявляют рост двух микроорганизмов и в 10% случаев ассоциации представлены тремя и более видами микроорганизмов. Наиболее часто встречающейся ассоциацией является сочетание P. aeruginosa и S. aureus [6,7]. В составе микробных ассоциаций выделяли одновременно P.aeruginosa мукоидный и немукоидный фенотипы. Кроме P.aeruginosa, часто выделяли других представителей неферментирующих грамотрицательных микроорганизмов – Burkholderia cepacia complex, Achromobacter spp., S.maltophilia, A.baumanii и др. [8].
При анализе данных микробиологических исследований установлено, что микроорганизмы были выделены у 61,9% детей в возрасте до 1 года, у 92,9% - в возрасте 1-4 года, у 93,8% - в возрасте 5-7 лет и в возрасте 8-14 и 15-18 у 100% детей. Это свидетельствует о том, что колонизация легких больных муковисцидозом микроорганизмами начинается, фактически, с первых дней после рождения и достигает максимума уже к 5 годам жизни. В возрасте до 1 года более чем у 1/3 больных муковисцидозом нижние дыхательные пути еще не обсеменены микроорганизмами, в возрасте 1-4 лет нижние дыхательные пути обсеменены почти у всех больных (92,9%), а к 8-18 годам – у 100% больных. Хроническую стафилококковую, синегнойную или смешанную инфекцию диагностируют у 25% детей уже в возрасте 1-4 года, в возрасте 5-7 лет – у 50% больных, в возрасте 8-14 лет – у 65% и к 18 годам – у 80% больных муковисцидозом [6].
При оценке микробиологического профиля респираторного тракта выявлен рост частоты высева грамотрицательной флоры с увеличением возраста больных.
Наибольшая частота инфицирования S.aureus отмечена в возрастной группе 12-16 лет, где она составила 64,5%, P. aeruginosa в 24-28 лет с частотой 55,0%, в этой же возрастной группе максимальное инфицирование Вurkholderia cepacia complex, которое составило– 22,6%, S. maltophilia в 16-20 лет – 5,6%. Achromobacter spp. достигает своего пика у пациентов старше 36 лет, где ее частота составила 14,3%. MRSA имеет два пика максимальной частоты, в 20-24 года и 32-36 лет, где его частота составила 11,4% и 10,5%, соответственно.
Частота хронического инфицирования дыхательных путей S. aureus составляет 56,0%, P. aeruginosa – 32,1%, Bcc – 6,6%, MRSA- 6,4%, Achromobacter spp.-3,9%, S. maltophilia– 3,4%. В 7,5% случаев дыхательные пути больных хронически инфицированы другой грамоотрицательной флорой, среди которых наиболее часто встречающиеся представители семейства Enterobacteriacaee (Klebsiella spp.: Klebsiella pneumoniae, Klebsiella oxytoca, Raoultella (Klebsiella) ornithinolytica; Escherichia coli), Serratia spp. (семейство Yersiniaceae), Proteus spp. (семейство Morganellaceae A и др.), а также представители неферментирующих грамотрицательных бактерий (НГОБ) (Pseudomonas spp.: P. stutzeri, P. oryzihabitans, P. montelii, P. putida, P. koreensis, P. fluorescens, P. fragi, P. luteola; Аcinetobacter spp.: A. baumanii, A. lwoffii, A. haemolyticus, A. calcoaceticus, A. junii, A. pittii, A. anitratus.). У ряда пациентов встречается микст-инфицирование респираторного тракта различной непсевдомонадной грамотрицательной флорой. Доля пациентов, инфицированных НТМБ составляет 0,9 %.
Наиболее часто встречающимися в респираторных образцах пациентов с муковисцидозом микроорганизмами являются грибы Candida spp., распространенность которых достигает до 80%. Однако, клиническое значение этих видов при муковисцидозе остается неясным.
Другой представитель грибов - Pneumocystis jirovecii был также обнаружен у пациентов с МВ. При этом, отмечается, что ДНК P. jirovecii чаще всего находили в образцах мокроты при легочных обострениях. Распространенность P. jirovecii у пациентов с МВ, которым не делали трансплантацию легких, варьировала: 2,5% во Франции, 7,4% в Германии, 21,5% в Испании и 38,2% в Бразилии. Пневмоцистная пневмония также была зарегистрирована у пациентов с МВ после трансплантации легких. Это обстоятельство возможно требует внедрения профилактических стратегий. Однако из-за нерегулярного скрининга на P. jirovecii истинная распространенность и клиническое значение этого гриба у пациентов с МВ остаются неясными.
Также существуют виды Scedosporium и Rasamsonia, которые могут вызывать инвазивные заболевания у пациентов с МВ после трансплантации легких. Также Exophiala (Wangiella) dermatitidis может быть выделен из респираторных образцов у пациентов с муковисцидозом, и имеются сообщения о его потенциально неблагоприятном влиянии [398].
Другой особенностью микрофлоры при хронической инфекции легких у больных муковисцидозом является различная резистентность к противомикробным препаратам системного действия представителей одного и того же вида возбудителя, персистирующего у больного в легких. Это обусловлено как фенотипической гетерогенностью, которая является результатом адаптации микроорганизма при персистенции под воздействием антибиотикотерапии и/или иммунной системы, так и изменчивостью, связанной с генетическими изменениями, происходящими в бактериях при персистенции – мутациями, приобретением или потерей мобильных генетических элементов, имеющих в своем составе гены резистентности к антибиотикам. Данная особенность имеет как клиническое, так и эпидемиологическое значение и должна рассматриваться как фактор, ограничивающий эффективность антибиотикотерапии, способствующий выживанию бактерий и формированию хронической инфекции. Этот факт является важным для клиницистов и еще раз подтверждает необходимость исследования антибиотикочувствительности выделенных изолятов при назначении антибиотикотерапии и указывает на необходимость применения комбинированной антибиотикотерапии при лечении хронической инфекции у больных МВ [9,10].
Развитию аспергиллеза легких у пациентов с МВ способствуют нарушение мукоцилиарного клиренса и иммунного ответа, а также продолжительная антибактериальная и глюкокортикоидная терапия.
Колонизация дыхательных путей у пациентов с МВ Aspergillus spp.- выявление грибов рода Aspergillus в ≥50% образцов мокроты или в течение ≥6 месяцев в год, отсутствие инструментальных признаков ухудшения легочной функции, а также отсутствие клинических признаков обострения МВ [11,12].
В настоящее время нет убедительных данных о негативном влиянии колонизации Aspergillus spp. дыхательных путей на функцию дыхания пациентов с МВ [11,12,13]. Колонизация дыхательных путей пациентов с МВ грибами Aspergillus spp. не является показанием для назначения системных противогрибковых ЛС.
Наиболее распространенным осложнением, обусловленным Aspergillus spp., у пациентов с МВ является аллергический бронхолегочный аспергиллез (АБЛА). АБЛА характеризуется развитием реакции гиперчувствительности I типа при колонизации дыхательных путей Aspergillus spp., которая без лечения приводит к развитию фиброза легких и необратимой дыхательной недостаточности. У пациентов с МВ инвазивный аспергиллез встречается редко, чаще как осложнение после трансплантации легких на фоне иммуносупрессивной терапии.
Инвазивного поражения тканей легких при АБЛА обычно не происходит, хотя сочетание с ХАЛ выявляют у 10% пациентов. Основные возбудители АБЛА – A. fumigatus и A. niger [14,15].
Хронический аспергиллез легких (ХАЛ) представляет собой медленно прогрессирующий деструктивный процесс в легких, обусловленный грибами Aspergillus spp., в ранее существовавших бронхоэктазах, полостях и пр. Описана генетическая предрасположенность к этому заболеванию, связанная с дефицитом или дисфункцией Th-17 лимфоцитов [16,17].
Многие пациенты с МВ до развития ХАЛ получали ингаляционные или низкие дозы кортикостероидов для системного применения. Кроме того, развитию ХАЛ способствует повышенное содержание конидий Aspergillus spp. в окружающей среде, в том числе в жилых и производственных помещениях. Основные возбудители ХАЛ – A. fumigatus, A.flavus и A.niger. Без лечения ХАЛ приводит к ухудшению качества жизни пациентов с МВ и увеличению летальности.
Частота МВ колеблется среди представителей европеоидов от 1:600 до 1:17000 новорожденных. В РФ частота муковисцидоза составляет по данным ФГБНУ «Медико-генетический научный центр им. академика Н.П. Бочкова» 1:7411 новорожденных [1,5].
Частота носительства одного патогенного варианта в гене CFTR значительно варьирует в различных популяциях. В российской популяции она составляет примерно 1:40 человек [399]. Этот показатель сравним с частотой, наблюдаемой в других европейских популяциях – частота гетерозиготных носителей вариантов гена CFTR среди европейцев составляет около 4% [400], ашкеназских евреев - примерно 2% [401], в азиатских популяциях частота носительства значительно ниже - около 0,2% [402]. Среди коренных американцев частота носительства мутаций в гене CFTR составляет примерно 0,1% [403].
Кистозный фиброз (E84):
E84.0 – Кистозный фиброз с лёгочными проявлениями;
E84.1 – Кистозный фиброз с кишечными проявлениями1;
E84.8 – Кистозный фиброз с другими проявлениями;
E84.9 – Кистозный фиброз неуточнённый2.
1 – Код E84.1 Изолированной кишечной формы нет в современной классификации ВОЗ и Европейской Ассоциации Муковисцидоза. Код E84.1 - кистозный фиброз с кишечными проявлениями не рекомендуется использовать [18,19].
2 – В настоящее время –
1) неопределенный диагноз при положительном неонатальном скрининге на муковисцидоз;
2) у пациентов любого возраста из группы риска по муковисцидозу, которым на основании результатов обследования не удается окончательно исключить или подтвердить диагноз.
Классификация, принятая ВОЗ, Международной Ассоциацией Муковисцидоза, Европейской Ассоциацией Муковисцидоза [1,2,3,4,5,7,8,9]:
o Классический муковисцидоз с панкреатической недостаточностью (смешанная или легочно-кишечная форма заболевания1), PI. E84.8.
o Классический муковисцидоз с ненарушенной функцией поджелудочной железы (преимущественно легочная форма заболевания1), PS. E84.0.
o Неопределенный диагноз при положительном неонатальном скрининге на муковисцидоз. E84.9.
o Заболевания, ассоциированные с геном CFTR (МВТР). Используются коды из соответствующего раздела
изолированная обструктивная азооспермия;
хронический панкреатит;
диссеминированные бронхоэктазы.
В клинической практике используется классификация, представленная в таблице 2 [2].
Таблица 2. Клиническая классификация муковисцидоза (предложена на основе Рабочей классификации муковисцидоза (Рачинский С.В., Капранов Н.И., 2000), рекомендаций ВОЗ и Европейской ассоциации муковисцидоза), опубликовано -https://mukoviscidoz.org/doc/konsensus/CF_consensus_2017.pdf
Форма |
Характеристика бронхолегочных изменений |
Проявления |
Осложнения |
||
|---|---|---|---|---|---|
Клиническая |
Фаза и активность процесса |
Степень ДН2 |
|||
|
Классический муковисцидоз1 Смешанная или легочно-кишечная форма заболевания (муковисцидоз с панкреатической недостаточностью – E84.8) Легочная форма заболевания (муковисцидоз с ненарушенной функцией поджелудочной железы – E84.0) |
Хронический обструктивный бронхит Бронхоэктазы (локализованные и диссеминированные) с указанием локализации Пневмофиброз |
Вне обострения Обострение Тип обострения: Обострение хронического бронхита Пневмония (с указанием локализации) Смешанный тип |
I. ст. II. ст. III. ст. |
Хронический (гнойный, полипозно-гнойный) риносинусит Синдром псевдо- Барттера Азооспермия Рецидивирующий панкреатит |
Абсцессы, ателектазы, пневмо-пиопневмоторакс, кровохаркание, кровотечение (легочное, желудочное), аллергический бронхолегочный аспергиллез (АБЛА), легочная гипертензия, полипоз носа. Мекониевый илеус, эквиваленты мекониевого илеуса, выпадение прямой кишки Цирроз печени (без и с портальной гипер- тензией) ЖКБ Отставание в физическом развитии. Белково-энергетическая недостаточность Нарушение толерантности к углеводам Муковисцидоз-ассоциированный сахарный диабет Снижение минеральной плотности костной ткани Вторичный остеопороз Амилоидоз почек Сиалоаденит Витамин К-дефицитные состояния (геморрагическая болезнь) |
Генотип (мутации гена CFTR (МВТР)) |
Указать согласно базе данных CFTR2. org и Консенсусу по клиническим эффектам генетических вариантов (база данных SeqDBhttp:// seqdb.med-gen.ru/) |
||||
Микробиологический статус (указывается дата первичного высева (выявления) микробного патогена (патогенов) и, если есть, последнего) |
Стафилококковая инфекция. Синегнойная инфекция. Инфекция, вызванная B. cepacia complex Другие инфекции. Микробные ассоциации |
||||
Указать препарат таргетной терапии и дату старта/смены препарата | |||||
|
Другие формы: Неопределенный диагноз при положительном неонатальном скрининге на муковисцидоз3 – E84.9. Заболевания, ассоциированные с геном CFTR (МВТР):4 – изолированная обструктивная азооспермия; – хронический панкреатит; диссеминированные бронхоэктазы |
|||||
Примечания: 1 - Форма из классификации МВ Рачинского С.В., Капранова Н.И. (2000).
2 - Степень дыхательной недостаточности устанавливается согласно «Классификации дыхательной недостаточности» (Национальное руководство по болезням органов дыхания, 2010). Степень тяжести заболевания рекомендуется не указывать исходя из первично-хронического течения, полиорганного поражения и прогредиентного течения.
3 - Положительный неонатальный скрининг или неонатальная гипертрипсиногенемия не являются диагнозом и в классификацию не включены, пациентам с неонатальной гипертрипсиногенемией рекомендуется в 1 год провести повторно потовую пробу. Используется новый диагноз – «неопределенный диагноз при положительном неонатальном скрининге на муковисцидоз».
4 - Код МКБ рекомендуется использовать из соответствующих разделов.
Тяжесть состояния устанавливается согласно Приложению к приказу Министерства труда и социальной защиты Российской Федерации «О классификациях и критериях, используемых при осуществлении медико-социальной экспертизы граждан федеральными государственными учреждениями медико-социальной экспертизы» (с 01 января 2019, см. раздел «Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата»).
В будущем, по мере углубления знаний, эта классификация также потребует пересмотра.
Муковисцидоз может быть заподозрен по следующим признакам (табл. 3,4).
Наличие внутриутробно по данным УЗИ плода - гиперэхогенного кишечника, мекониевый илеус - при рождении.
В периоде новорожденности затяжная неонатальная желтуха, витамин К-зависимые геморрагические состояния, мекониевый илеус.
Мекониевый илеус – это синдром, характеризующийся проявлением низкой обтурационной кишечной непроходимости, без перерыва просвета кишечной трубки. Данное заболевание при муковисцидозе обусловлено механическими причинами - облитерацией просвета плотной мекониальной пробкой.
В мировой общепринятой практике считается, что в 90-95% случаев этиологией мекониевого илеуса является муковисцидоз [20]. Мекониевый илеус диагностируется у 15–20% новорожденных с муковисцидозом. Пациенты с мекониевым илеусом подлежат обязательному обследованию на муковисцидоз [1,21]. По данным регистра пациентов с муковисцидозом РФ, доля пациентов с муковисцидозом, перенесших мекониевый илеус при рождении, в группе детей первого года жизни составила 22,1% пациентов, что отражает его реальную распространенность [22].
Задержка прибавки веса, частый, обильный, с примесью жира и зловонным запахом стул, повышенный аппетит, в возрасте после года эпизоды выпадения прямой кишки, эпизоды задержки стула с клиническими проявлениями частичной или полной кишечной непроходимости (синдром дистальной интестинальной обструкции – СДИО).
С раннего возраста возможны навязчивый коклюшеподобный кашель, часто рецидивирующие респираторные инфекции с явлениями бронхитов, пневмоний, может отмечаться свистящее дыхание и/или «оральная крепитация», одышка, кашель с выделением гнойной мокроты, в том числе вне периодов обострения, влажные разнокалиберные хрипы разной степени локализации в зависимости от распространенности процесса.
В раннем возрасте отмечаются эпизоды проявлений синдрома потери солей (гипокалиемия, гипонатриемия, гипохлоремия) – потеря веса, срыгивания, рвота, вялось, отказ от еды. Вследствие потери электролитов с потовой жидкостью, особенно в условиях усиленного потоотделения (лихорадка, жаркая погода, пребывание в сауне, физические нагрузки), через желудочно-кишечный тракт, а также недостаточного поступления солей с пищей и водой (особенно у детей первого года жизни при отсутствии дотации соли) может развиваться Псевдо-Барттер синдром (ПБС).
Синдром манифестирует преимущественно на первом году жизни у пациентов с муковисцидозом и является жизнеугрожающим состоянием, поэтому рассматривается с точки зрения тяжелого и опасного осложнения МВ, требующего в определенных случаях экстренного вмешательства. ПБС может быть первым симптомом МВ. Клинические проявления: от медленно развивающейся задержки физического развития до острого состояния, протекающего с отказом от еды и питья, вялостью, срыгиваниями и рвотой, признаками дегидратации. Часто ошибочно принимается за острую кишечную инфекцию, патологию почек, адреногенитальный синдром [2].
Соленый привкус кожных покровов при поцелуе.
Деформации грудной клетки.
Формирование признаков хронической гипоксии в виде деформации концевых фаланг и ногтей по типу «барабанных палочек» и «часовых стекол».
Признаки хронического риносинусита, с полипами или без.
Муковисцидоз-ассоциированные заболевания печени (cystic fibrosis-associated liver disease (CFLD) включают в себя такое многообразие нозологий как: билиарный цирроз печени с и без синдрома внутрипеченочной портальной гипертензии, персистирующее повышение уровня печеночных ферментов, фиброз, стеатоз, желчнокаменная болезнь и изолированно лишь ультразвуковые изменения паренхимы печени [23,24].
Встречаемость муковисцидоз-ассоциированной гепатобилиарной патологии во всем мире примерно 37,9%, причем 2,5% летальных исходов отмечается именно по причине декомпенсации заболеваний печени [25]. По Европейскому Регистру пациентов с муковисцидозом за 2017 г. процент пациентов с циррозом печени и портальной гипертензией в Великобритании составляет – 1,51% (149 пациентов от 8344), в России же – 4,42% (136 пациентов от 2291) [5]. Цирроз печени с портальной гипертензией зафиксирован у 4,5% пациентов РФ в 2017 г, без портальной гипертензии – у 2,3%, цирроз печени (о наличии гипертензии не известно) у 0,7% больных и поражение печени без цирроза – у 15,9% пациентов.
У 1,5% пациентов поражение печени является первым клиническим симптомом МВ; именно поэтому в диагностический алгоритм при циррозе печени неясной этиологии рекомендуется включать потовую пробу для исключения МВ [23,24].
Поражение печени, как и многие другие фенотипические проявления МВ, зависит не только и не столько от генетического дефекта и типа мутации CFTR, но от действия генов-модификаторов, находящихся вне локуса CFTR, например, Z аллель гена SERPINA1 (α1-antitrypsin или α1-antiprotease) [2,5] и аллель A VNTR в гене eNOS4 [18], и от факторов окружающей среды, включая ятрогенные.
Клинически при формировании цирроза печени диагностируется увеличение живота за счет гепатоспленомегалии, расширение поверхностных вен на передней брюшной стенке.
Рецидивирующие панкреатиты (как правило, у пациентов с сохранной функцией поджелудочной железы – PS).
С возрастом у пациентов с МВ нередко развивается и эндокринная недостаточность поджелудочной железы (муковисцидоз-ассоциированный сахарный диабет (МАСД), который, как правило, протекает бессимптомно, и может долгое время оставаться не диагностированным. При этом известно, что уже за 2–4 года до манифестации диабета ухудшаются показатели нутритивного статуса и дыхательной функции. Комбинация МВ и диабета оказывает негативное влияние на продолжительность жизни. Так, средняя продолжительность жизни пациентов с МАСД ниже по сравнению с пациентами без диабета, медиана выживаемости у пациентов с МАСД составляет 24 года, по сравнению с 32 годами у пациентов с МВ, но без диабета [26].
У большинства пациентов мужского пола снижена фертильность.
В большинстве случаев фертильность женщин, больных муковисцидозом, сохранена. Однако в определенных случаях возможно бесплодие, обусловленное ановуляторным менструальным циклом и вторичной аменореей, вызванной истощением пациентки.
Наиболее частой причиной снижения фертильности у пациенток с нормальным овуляторным циклом является изменения водного и электролитного состава цервикальной слизи, в связи с большим количеством МВТР в цилиндрическом эпителии шейки матки. В результате цервикальный секрет (отделяемое шейки матки) становится слишком вязким, что снижает способность к оплодотворению [27,28].
Наличие у пациента симптомов, указанных в таблице 3, требует проведения дифференциального диагноза МВ. Необходимо учитывать, что перечни симптомов, представленные в таблице 3, составлены в примерном соответствии каждой из рассматриваемых возрастных групп пациентов с МВ. Любой из указанных симптомов может наблюдаться у детей младшего или старшего возраста.
Таблица 3. Клинические проявления, требующие дифференциального диагноза с МВ [1,2,29].
Возраст |
Симптомы и синдромы |
|---|---|
Грудной |
Рецидивирующие или хронические респираторные симптомы, такие как кашель или одышка Рецидивирующая или хроническая пневмония Отставание в физическом развитии Неоформленный, обильный, маслянистый и зловонный стул Хроническая диарея Выпадение прямой кишки Затяжная неонатальная желтуха Соленый вкус кожи Тепловой удар или дегидратация при жаркой погоде Гипоэлектролитемия и метаболический алкалоз Данные семейного анамнеза о смерти детей на первом году жизни или наличие сибсов со сходными клиническими проявлениями Гипопротеинемия / отеки Мекониевый илеус |
Дошкольный |
Стойкий кашель с или без гнойной мокроты Диагностически неясная рецидивирующая или хроническая одышка Хронический гнойный/полипозно-гнойный синусит Отставание в весе и росте Выпадение прямой кишки Инвагинация Хроническая диарея Симптом «барабанных палочек» Кристаллы соли на коже Гипотоническая дегидратация Гипоэлектролитемия и метаболический алкалоз Гепатомегалия или диагностически неясное нарушение функции печени |
Школьный |
Хронические респираторные симптомы неясной этиологии Pseudomonas aeruginosa в мокроте Хронический синусит Назальный полипоз Бронхоэктазы Симптом «барабанных палочек» Хроническая диарея Синдром дистальной интестинальной обструкции Панкреатит Выпадение прямой кишки Сахарный диабет в сочетании с респираторными симптомами Гепатомегалия Заболевание печени неясной этиологии |
Подростки и взрослые |
Гнойное заболевание легких неясной этиологии Симптом «барабанных палочек» Панкреатит Синдром дистальной интестинальной обструкции Сахарный диабет в сочетании с респираторными симптомами Признаки цирроза печени и портальной гипертензии Отставание в росте Задержка полового развития Инфертильность с азооспермией у лиц мужского пола Снижение фертильности у лиц женского пола |
Таблица 4. Клинические проявления, характерные для муковисцидоза [2,29].
Высокоспецифичные для МВ |
Менее специфичные для МВ |
|---|---|
|
Со стороны системы пищеварения:
|
Со стороны системы пищеварения:
|
|
Со стороны дыхательных путей:
|
Со стороны дыхательных путей:
|
|
Другое:
|
Другое:
|
При МВ нередко встречается остеопороз, который у этих пациентов всегда носит вторичный характер.
К причинам его развития у пациентов с МВ относят: хронический микробно – воспалительный процесс, дефицит витамина D и K; низкое потребление кальция; низкая физическая активность, сахарный диабет на фоне МВ, трансплантация органов и иммуносупрессивная терапия; гипоксия и гиперкапния; дефицит костной массы и нарушение микроархитектоники кости вследствие недостаточного набора пика костной массы в период активного роста и избыточной костной потери у взрослых.
В некоторых работах показана взаимосвязь различных мутаций и/или их комбинаций (F508del и др.) c развитием низкой костной массы [30,31], большинство других авторов не отмечают данной связи.
Рекомендации по формулировке диагноза изложены в клинических рекомендациях по остеопорозу. Согласительная комиссия по европейскому консенсусу решила использовать термин «болезни кости при МВ» (включающий низкую минеральную плотность кости и переломы), а не «остеопороз». Для РФ, учитывая особенности медицинского обеспечения, рекомендуется оставить диагноз – остеопороз [32,33,34].
Частота остеопороза при МВ в детском и подростковом возрасте составляет от 20 до 50% и увеличивается после 18 лет жизни (50 - 75%) [35].
По данным российских исследователей в детском возрасте частота снижения минеральной плотности кости (МПК) составляет от 33 до 65,2% и остеопороза - от 7,7% до 15,6% [36,31].
Во взрослой популяции пациентов с муковисцидозом частота низких показателей МПК составляет 43,6%, остеопороза - 8,4% [32].
Классификация аспергиллеза легких представлена в приложении А3.1.
Аллергический бронхолегочный аспергиллез у пациентов с МВ протекает хронически с периодическими обострениями. Основными клиническими признаками обострения АБЛА являются неконтролируемое течение МВ, приступы удушья, кашель с мокротой, содержащей коричневые или черные включения и слизистые пробки, бронхообструктивный синдром и/или возникновение эозинофильных инфильтратов, боли в грудной клетке, рефрактерное к применению антибактериальных препаратов повышение температуры тела, а также снижение дыхательной функции. При длительном течении АБЛА развивается зависимость от кортикостероидов для системного применения, формируется фиброз легких, приводящий к дыхательной недостаточности [14].
Хронический аспергиллез легких. Продолжительность ХАЛ ≥ 3 мес. Наиболее частые пульмональные симптомы – продуктивный кашель, одышка и кровохарканье, прогрессивное снижение легочной функции, общие – субфебрилитет, общая слабость и снижение массы тела, снижение толерантности к нагрузкам, отсутствие или неполный ответ на полноценный курс антибактериальной терапии широкого спектра действия. ХАЛ часто принимают за обострение МВ, обусловленное бактериальным возбудителем, и назначают неэффективную в этих случаях терапию антибактериальными препаратами резерва [14,16,17].
Прогноз: ХАЛ нередко диагностируют поздно и лечение проводят неадекватно. Без лечения ХАЛ приводит к ухудшению качества жизни пациентов с МВ и увеличению летальности. Летальность при ХАЛ в первые 6 месяцев после диагноза составляет 15 – 30%. Наиболее частая непосредственная причина смерти – легочное кровотечение.
Клинические проявления у носителей вариантов гена CFTR и CFTR ассоциированных заболеваний
Гетерозиготные носители имеют только один патогенный вариант гена CFTR, они экспрессируют вдвое меньше каналов CFTR, чем люди без вариантов в гене CFTR [404].
Исторически считалось, что у носителей одного патогенного варианта функция канала CFTR обеспечивает нормальную работу хлорного канала [405] и в большинстве случаев отсутствуют симптомы заболевания МВ [406].
Однако, оценка состояния здоровья гетерозиготных носителей вариантов гена CFTR показала, что у них уровень хлоридов пота в среднем выше, чем у здоровых людей, но ниже, чем у пациентов с МВ [407]. Они имеют повышенные уровни внутриклеточного кальция, белка в меконии в младенческом возрасте [408], альфа-фетопротеина [409], измененную функцию нейтрофилов и др. Неонатальный скрининг (анализ ИРТ) часто выявляет гетерозиготных носителей, потому что у них могут быть более высокие значения ИРТ, чем у людей без МВ [410].
Носители вариантов CFTR подвергаются повышенному риску некоторых состояний, ассоциированных с МВ, таких как хронический панкреатит, нарушение репродукции, хронический риносинусит и бронхоэктазы [406].
Острый, рецидивирующий и хронический панкреатиты в сочетании с вариантами CFTR могут развиваться на фоне муковисцидоза или в виде CFTR-ассоциированного панкреатита. Бишоп и др. отметили, что 43% и 11% пациентов с идиопатическим рецидивирующим острым или хроническим панкреатитом имеют один или два варианта гена CFTR соответственно [411]. Обструкция протоков поджелудочной железы вследствие дисфункции CFTR считается первичным патогенным фактором, хотя точный механизм панкреатита, связанного с мутациями CFTR, изучен недостаточно. Исследования, проведенные на моделях мышей, показало влиние CFTR на ацинарные клетки поджелудочной железы путем нарушения апикального эндоцитоза за счет уменьшения секреции бикарбоната в протоках и последующего снижения подщелачивания ацинарного просвета. Недавнее исследование также предполагает важную роль нарушения регуляции pH в развитии панкреатита. Сложность изучения формирования панкреатитов при носительстве варинатов гена CFTR обусловлено влиянием большого количества факторов на возможное формирование панкреатита. Помимо влияния гена CFTR, возможны различные факторы окружающей среды (например курение, употребление алкоголя с жирными продуктами) и других факторов [412], рисунок 1.
Мужчины с синдромом врожденной двусторонней аплазии семявыносящих протоков (congenital bilateral aplasia of vas deferens, CBAVD, ОMIM #277180) и обструктивной азооспермией часто являются носителями по крайней мере одного патогенного варианта гена CFTR [413].
Синдром CBAVD является одной из причин обструктивной азооспермии и мужского бесплодия. Данный синдром диагностируют примерно у 1–2% от всех мужчин с бесплодием, а его вероятная частота в европейских популяциях оценивается примерно 1:2000 мужчин [Claustres M. Molecular pathology of the CFTR locus in male infertility // Reprod. Biomed. Online. 2005. V. 10(1). P. 14–41.]. Выявлены этнические особенности по распространенности и спектру патогенных вариантов гена CFTR в различных регионах мира. У мужчин с CBAVD из Азии частота встречаемости муковисцидоз-вызывающих патогенных вариантов и аллеля 5Т несколько ниже, чем в европейских популяциях [414,415,416,417].
CBAVD может возникать как самостоятельное заболевание, так и быть одним из проявлений муковисцидоза у мужчин [418].
В среднем у 80% мужчин с синдромом CBAVD выявляют один или два патогенных варианта в гене CFTR, в большинстве случаев представленные в гетерозиготном состоянии, и редко – в гомозиготном или в компаунд-гетерозиготном состоянии, часто в сочетании с 5Т (IVS8-T5)-аллелем. Данный вариант гена CFTR формирует “мягкий” фенотип, детектируемый у 40–45% пациентов с синдромом CBAVD [419].
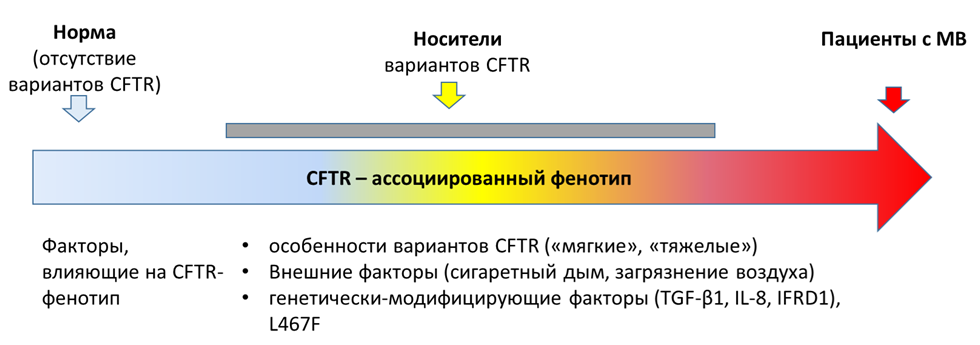 Рисунок 1. Факторы, потенциально модифицирующие фенотипы носителей гена CFTR [420]
Рисунок 1. Факторы, потенциально модифицирующие фенотипы носителей гена CFTR [420]
Как скрининг новорожденных, так и пренатальный скрининг будут все чаще выявлять носителей МВ.
Информированность о том, что человек является носителем патогенных вариантов гена CFTR, дает возможность избежать факторов, влияющих на здоровье носителей.
Например, курение может снижать активность канала CFTR и носители ГВНП CFTR могут подвергаться более высокому риску неблагоприятного влияния табачного дыма [421].
Информация о носительстве вариантов CFTR может помочь объяснить, почему некоторые люди имеют тяжелые легочные инфекции (например, легочный микобактериоз). Дискутируются вопросы о целесообразности использования модуляторов CFTR для лечения тяжелых и сложных респираторных инфекций у носителей ГВНП CFTR, которым в отличие от пациентов с МВ такое лечение может потребоваться только в течение относительно коротких периодов времени для усиления антимикробной терапии [422].
С учетом того, что гетерозиготные носители ГВНП CFTR могут иметь различные патологические состояния, требуется изучение и мониторирование состояния их здоровья.
Носители патогенных вариантов гена CFTR могут быть выявлены:
I. При проведении скринингов:
1. неонатального скрининга на МВ;
2. пренатальной диагностики при желании будущих родителей узнать, являются ли они носителями патогенного варианта гена CFTR;
3. расширенного скрининга носителей (преконцепционный генетический скрининг).
II. В рамках обследовании членов семьи, где уже есть больные МВ.
III. При молекулярно-генетическом обследовании на другие наследственные заболевания.
Кроме того, облигатными носителями вариантов CFTR являются дети и родители пациентов с МВ.
Диагноз МВ подтверждается при наличии одного или более характерных фенотипических проявлений МВ в сочетании с доказательствами нарушения функции МВТР, такими как: выявление клинически значимых мутаций гена МВТР при генотипировании или увеличение уровня хлоридов в секрете потовых желез пациента. Для решения проблем диагностики МВ были разработаны критерии, согласно которым обязательным для МВ является наличие характерного клинического синдрома плюс доказательство какого-либо нарушения функции хлорного канала одним из методов.
В настоящее время существует несколько вариантов диагностических критериев МВ, которыми пользуются специалисты [1,2].
Наиболее распространено использование диагностических критериев, утвержденных Европейскими стандартами и национальным консенсусом (таблица 5) [1,21].
Таблица 5. Диагностические критерии, утвержденные Европейскими стандартами 2014 года, пересмотр 2018 года [21,37] и национальным консенсусом (2016) [2].
Положительный результат потового теста (потовой пробы) |
|---|
и/или |
Две мутации МВТР (CFTR), вызывающие МВ (согласно базе CFTR-2 http://www.cftr2.org) |
и |
Неонатальная гипертрипсиногенемия |
или |
Характерные клинические проявления, такие как диффузные бронхоэктазы, высев из мокроты значимой для МВ патогенной микрофлоры (особенно синегнойной палочки), экзокринная панкреатическая недостаточность, синдром потери солей, обструктивная азооспермия |
Диагностика обтурационной кишечной непроходимости (в т.ч., мекониевого илеуса) в периоде новорожденности
Кишечные проявления муковисцидоза в периоде новорожденности могут сводиться не только к формированию мекониевого илеуса. Также муковисцидоз может быть диагностирован у пациентов с внутриутробной перфорацией тонкой кишки, признаками перенесенного внутриутробного энероколита (внутриутробное формирование спаек, перитонит) и при нарушении проходимости толстой кишки, при нормальном формировании ее нервного аппарата.
Антенатальная – описанные заболевания относятся к поздним фетопатиям, поэтому возможные проявления могут быть визуализированы в III триместре. При наличии у плода по данным УЗИ плода признаков гиперэхогенного кишечника целесообразно направить родителей на ДНК диагностику муковисцидоза – поиск наиболее частых мутаций, а ребенка при рождении – как составляющего группу риска по мекониевому илеусу и кишечной непроходимости.
После рождения – диагностика кишечной непроходимости и осложнений в соответствии с клинической практикой пациентов с мекониевым илеусом, обязательная консультация специалиста по муковисцидозу, проведение потовой пробы, ДНК-диагностики (Молекулярно-генетическое исследование мутаций в гене CFTR (муковисцидоз) в крови/Комплекс исследований для диагностики муковисцидоза). При невозможности проведения потовой пробы – обязательная ДНК-диагностика (Молекулярно-генетическое исследование мутаций в гене CFTR (муковисцидоз) в крови/Комплекс исследований для диагностики муковисцидоза) [21].
Диагностика Псевдо-Барттер синдрома у пациентов с МВ
Псевдо-Барттер синдром диагностируется на основании наличия у ребенка установленного диагноза «Муковисцидоз», характерной клинической картины (см. раздел 1.6 «Клиническая картина») и биохимических изменений: гипонатриемии, гипокалиемии, гипохлоремии, метаболического алкалоза [2].
Диагностика аспергиллеза при муковисцидозе сложна и нередко запаздывает, поскольку многие диагностические критерии пересекаются с типичными проявлениями основного заболевания.
Для постановки диагноза необходимо комплексное специализированное обследование (табл 6,7).
Таблица 6. Диагностические критерии АБЛА согласно консенсусу Фонда МВ (2003) [38].
• ухудшение течения муковисцидоза: кашель с мокротой, содержащей слизистые пробки, одышка, приступы удушья, снижение ФЖЕЛ, ОФВ1, острое или персистирующее ухудшение состояния, не связанное с другими причинами; |
|---|
и |
|
• уровень общего IgЕ> 500 ед./мл; • наличие специфических Aspergillus IgЕ или положительная кожная проба с антигеном Aspergillus; • наличие специфических Aspergillus IgG; • изменения на рентгенограмме или КТ, рефрактерные к «стандартной» терапии [11,39]. |
Таблица 7. Диагностические критерии ХАЛ согласно руководству по диагностике и лечению хронического аспергиллеза (2016) [2].
Ухудшение течения МВ, отсутствие или неполный ответ на 2-4–недельный курс антибактериальной терапии широкого спектра действия |
|---|
и |
наличие КТ признаков хронического аспергиллеза легких, |
|
наличие специфического IgG к Aspergillus в сыворотке крови, выявление мицелия Aspergillus в окрашенных мазках и/или в биопсийном материале, или выделение Aspergillus spp. при посеве биопсийного материала, БАЛ, мокроты [40]. |
Диагностика цирроза печени у пациентов с МВ:
o Повышение аланинаминотрансферазы, аспартатаминотрансферазы и гаммаглютамилтрансферазы, в течение более, чем 6 месяцев при исключении других причин [41,42] (следует учесть, что данные показатели имеют невысокую специфичность у пациентов с кистозным фиброзом (муковисцидозом));
o Пальпаторное увеличение размеров печени и селезенки [42];
o Удлинение протромбинового (тромбопластинового) времени в крови или в плазме [42,89];
o Характерная УЗИ-картина (неоднородная эхогенность паренхимы, тяжистость, закругление печеночного края, прорастание соединительной ткани в ворота печени), выявление избыточной свободной жидкости в брюшной полости как признак асцита [43,44,45];
o Обеднение венозного кровотока и формирование признаков портальной гипертензии по данным УЗДГ;
o Признаки формирования фиброза/цирроза по данным непрямой эластометрии печени с оценкой степени фиброза по морфологической классификации METAVIR (Приложение Г1): 5 стадий фиброза - от 0 до 4, где F0 - отсутствие фиброза, F1 - портальный фиброз (звездчатое расширение портальных трактов) без септ, F2 - портальный фиброз и единичные септы, F3 - портальный фиброз и множественные септы без ЦП, F4 –цирроз печени [46];
o Выявление варикозно-расширенных вен пищевода и желудка при проведении диагностической ЭГДС;
o Тяжесть и степень компенсации МВ-ассоциированного цирроза печени в клинической практике проводится по классификации Чайлд-Пью (Сhild-Pugh)(Приложение Г2) [47,48].
Диагностические критерии муковисцидоз-ассоциированного сахарного диабета (МАСД): гипергликемия натощак (уровень глюкозы плазмы натощак ≥7,0 ммоль/л) или «диабетический» уровень глюкозы крови в ходе ПГТТ (при уровне глюкозы плазмы натощак <7,0 ммоль/л и глюкозы плазмы через 2 часа в ходе ПГТТ ≥11,1 ммоль/л), или постпрандиальная гипергликемия, определяемая непрерывным мониторингом глюкозы (CGM) при отсутствии симптомов [49].
Диагностика остеопороза у пациентов с МВ включает оценку клинической картины, рентгеноденситометрию (раздел 2.4), лабораторные методы исследования.
Диагноз остеопороза при МВ ставится при наличии:
o 1 и более компрессионных переломов тел позвонков, которые не связаны с высокоэнергетической травмой или локальным заболеванием, приводящим к изменению минеральной плотности кости (МПК). При наличии компрессионных переломов позвонков для постановки диагноза остеопороза не требуется, чтобы Z-критерий был ≤ -2 SD.
или
o Клинически значимого анамнеза переломов и МПК по Z-критерию ≤-2 SD (стандартные отклонения). Клинически значимый анамнез переломов ‒ это:
1) 2 и более переломов длинных костей в возрасте до 10 лет;
2) 3 и более переломов длинных костей в любом возрасте до 19 лет [50].
См. раздел 1.6 Клиническая картина.
Ребенку с подозрением на МВ следует провести полное физикальное обследование, т.к. при этом заболевании имеются мультиорганные проявления.
См. раздел 1.6 Клиническая картина.
Тесты для установления диагноза муковисцидоз
Рекомендуется проведение скрининга новорожденных на муковисцидоз (неонатальный скрининг, комплекс исследований для диагностики муковисцидоза), так как раннее выявление и своевременное начало терапии позволяет предупредить развитие тяжелых осложнений, улучшает показатели физического развития, замедляет темпы снижения функции легких, снижает потребность в госпитализации [1,51,52,18,29,2,21,53].
(УУР – B, УДД – 2).
Комментарий: проводится в Российской Федерации у всех новорожденных.
Протокол скрининга в РФ включает 3 обязательных этапа: ИРТ1, ИРТ2, потовая проба (таблица 8). На первом этапе в крови новорожденных (24-48 часов у доношенных, 7-8 день (144-168 часов) у недоношенных) определяется уровень ИРТ. Взятие образцов крови осуществляется в соответствии с Приказом № 274н от 21 апреля 2022 г. "Об утверждении Порядка оказания медицинской помощи пациентам с врожденными и (или) наследственными заболеваниями" (вступил в силу 31.12.2022 г.). При превышении порогового уровня ИРТ проводится ретест на 21-28 день жизни. При положительном ретесте проводится потовая проба. Позитивная потовая проба расценивается как положительный результат скрининга, и пациента направляют в Центр муковисцидоза (либо профильное отделение). Дети с мекониевым илеусом независимо от уровня ИРТ нуждаются в проведении потовой пробы из-за возможного у них ложно отрицательного результата [2,21]. При приеме матерью патогенетической (таргетной) терапии (ивакафтор + лумакафтор**, ивакафтор + тезакафтор + элексакафтор и ивакафтор и т.п.) во время беременности возможно получение ложноотрицательного результата неонатального скрининга у новорожденного c муковисцидозом. В этом случае показано генотипирование (молекулярно-генетического исследования для идентификации мутаций гена МВТР (CFTR) (молекулярно-генетическое исследование мутаций в гене CFTR (муковисцидоз)) и/или проведение потовой пробы новорожденному, если не проводилось исследование амниотической жидкости /ворсин хориона во время беременности (Приложение Б2) .
Оптимальные сроки установки диагноза и начала наблюдения пациента, выявленного по программе неонатального скрининга - первые 2 месяца жизни [2,21].
Обследование и наблюдение новорожденных по программе массового скрининга должно проводиться с соблюдением принципов профилактики перекрестного и внутрибольничного инфицирования, оптимально амбулаторно или в условиях дневного стационара [2].
Таблица 8. Этапы неонатального скрининга в Российской Федерации (Приказ № 274н от 21 апреля 2022 г. "Об утверждении Порядка оказания медицинской помощи пациентам с врожденными и (или) наследственными заболеваниями" (вступил в силу 31.12.2022 г.)).
I этап |
В возрасте 24-48 часов у доношенного (на 7-8 –й день (144-168 часов)– у недоношенного) новорожденного – определение иммунореактивного трипсина (ИРТ) в высушенной капле крови |
|---|---|
II этап |
При положительном результате (cut-off>99,5 центиля) на 21-28-й день повторный тест на ИРТ |
III этап |
При положительном результате – потовая проба |
IV этап |
При пограничном результате потовой пробы – дополнительные методы обследования, включая ДНК-диагностику, определение разности кишечных потенциалов и другие. |
Для диагностики муковисцидоза рекомендуется проведение потовой пробы (исследование уровня хлоридов в поте по методу Гибсона-Кука, или с помощью анализаторов проводимости пота ИВД (для in vitro диагностики), автоматических). Для установления диагноза необходимо получить как минимум 2 положительных результата. Потовая проба может быть проведена ребенку в возрасте 48 часов с весом не менее 2 кг [1,2,21,55,56].
(УУР – В, УДД – 2).
Комментарии: потовая проба является «золотым стандартом» диагностики муковисцидоза, проводится как минимум дважды. В РФ используются 2 методики потового теста.
1) Классический прямой метод определения электролитного состава пота (хлора или натрия) методом пилокарпинового электрофореза по Гибсону и Куку (1959 г.). Норма – до 30 ммоль/л, пограничные значения 30-59 ммоль/л, положительный результат - 60 ммоль/л и выше (при навеске пота не менее 100 мг) [1,2,5,37]. Показатели хлоридов выше 150 ммоль/л должны быть подвергнуты сомнению.
2) Потовая проба путем определения проводимости пота с помощью специальных потовых анализаторов коррелирует с определением уровня хлоридов, позволяет получить адекватный результат при количестве пота в образце – 3-10 мкл. Получил широкое распространение при внедрении массового скрининга новорожденных.
При определении проводимости положительным результатом для муковисцидоза считается показатель: выше 80 ммоль/л; пограничным значением – 50-80 ммоль/л; нормальным – до 50 ммоль/л. Показатели проводимости выше 170 ммоль/л должны быть подвергнуты сомнению.
Время сбора пота не должно превышать 30 минут, минимально допустимое количество пота – 75-100 мг (15 мкл в коллекторе “Macroduct”), скорость потоотделения должна быть не менее 1 г/м2/мин. (для системы “Nanoduct”) [21]. Обязательным является предварительное тщательное очищение кожи пациента [2]. Особого внимания требует подготовка кожи у пациентов, длительно находящихся в стационаре.
Пограничные результаты потовой пробы.
Возможные причины пограничных результатов потовой пробы:
o Индивидуальные особенности у людей без муковисцидоза, особенно у взрослых;
o Неправильная подготовка к пробе;
o Носительство «мягких» мутаций при муковисцидозе [21].
Рекомендации:
o использование разных методов определения хлоридов пота, повторные исследования;
o расширенный ДНК-анализ (секвенирование гена);
o расширенное клинико-лабораторное и инструментальное обследование: Копрологическое исследование и Определение активности панкреатической эластазы-1 в кале, электролиты в биохимическом общетерапевтическом анализе крови (Исследование уровня калия в крови, Исследование уровня хлоридов в крови), посев мокроты/ мазок с задней стенки глотки (Микробиологическое (культуральное) исследование слизи с миндалин и задней стенки глотки на аэробные и факультативно-анаэробные микроорганизмы, Микробиологическое (культуральное) исследование мокроты на аэробные и факультативно-анаэробные микроорганизмы), рентгенография легких, придаточных пазух носа, спермограмма;
o наблюдение в центре муковисцидоза до окончательного принятия решения о диагнозе. Не снимаются с учета, пока диагноз не будет исключен;
o метод определения разности назальных потенциалов или измерение электрического тока в биоптате кишки, отражающие нарушение функции хлорного канала*.
Примечание: * - В качестве дополнительного теста пациентам с подозрением на муковисцидоз, особенно в сомнительных случаях при пограничных значениях потового теста, при невыраженной симптоматике и/или при неполных классических проявлениях болезни может быть рекомендовано проведение исследование с помощью метода определения разности кишечных потенциалов (ОРКП) [1,2,5,37,57].
Согласно стандартным операционным процедурам, для измерения разности кишечных потенциалов используются ректальные биоптаты, полученные при ректороманоскопии. Для проведения исследования необходимо не менее 4 образцов биоптатов. Рекомендуемые референтные значения (контрольные показатели здоровых людей) при использовании метода ОРКП в РФ: плотность тока короткого замыкания (ΔISC) в ответ на введение амилорида (стимуляция натриевых каналов) в контрольной группе составила 8,98±3,42 µA/cm2. Изменение ΔISC в ответ на введение форсколина (стимуляция хлорных каналов) составило 25,78±4,41 µA/cm2. В ответ на введение гистамина ΔISC изменяется в положительную сторону, что отражает вход ионов калия в клетки. При этом плотность тока составила 101,68±10,99 µA/cm2 [58].
Рекомендовано проведение молекулярно-генетического исследования для идентификации мутаций гена МВТР (CFTR) (молекулярно-генетическое исследование мутаций в гене CFTR (муковисцидоз) в крови, комплекс исследований для диагностики муковисцидоза) по показаниям:
1) Новорожденным с положительным ИРТ и положительными или пограничными значениями потовой пробы, мекониевым илеусом;
2) Людям с пограничными значениями потовой пробы (см. Раздел «Диагностика муковисцидоза»);
3) Пациентам с клиническими проявлениями классического или моносимптомного МВ;
4) При CFTR-ассоциированных заболеваниях (панкреатит, врожденное двустороннее отсутствие семявыносящего протока/обструктивная азооспермия);
5) Родственникам пациентов с МВ (для определения статуса носительства по желанию);
6) Женщинам после рождения первого ребенка с муковисцидозом, а также во время последующих беременностей при наличии ребенка с муковисцидозом;
7) Плодам на 10-12-й неделе при подозрении на МВ (при наличии сибса с МВ) или обнаружении гиперэхогенного кишечника при УЗ-обследовании;
8) Донорам гамет и эмбрионов в программах ЭКО (ЭКО-ИКСИ), внутриматочной инсеминации;
9) Супружеским парам с высоким генетическим риском МВ, желающим пройти ЭКО-ПГТ МВ для предотвращения рождения ребенка с МВ (при отсутствии противопоказаний и ограничений) [2,21,59].
(УУР – C, УДД – 5).
Комментарии: клиническую значимость обнаруженных генетических вариантов следует устанавливать с учетом рекомендаций Консенсуса [2], постоянно обновляемых баз данных : [60].
Стратегия молекулярно-генетической диагностики МВ включает несколько этапов.
На первом этапе проводится поиск вариантов, наиболее частых в популяции, к которой принадлежит обследуемый [2].
На втором этапе проводят расширенный поиск более редких вариантов, используя секвенирование по Сэнгеру или высокопроизводительное секвенирование генома (MPS/NGS). Анализ включает исследование всей кодирующей последовательности гена CFTR (27 экзонов), областей экзон-интронных соединений, 5’- и 3’- некодирующих областей (до 200-300 нуклеотидов), а также, желательно, глубоких интронных областей, где расположены варианты с доказанной патогенностью.
Примечание: применение данного метода необходимо при назначении CFTR-модуляторов с целью исключения комплексных аллелей, влияющих на эффективность терапии.
Третий этап. Обычными сканирующими методами, в том числе секвенированием, можно выявить нарушения последовательности гена, незначительные по протяженности: нуклеотидные замены, небольшие делеции/инсерции. Перестройки, охватывающие несколько экзонов/интронов, такими методами не выявляются. Рекомендуется использовать следующие технологии: MLPA – мультиплексную лигазную зондовую амплификацию либо QFMP – количественную флуоресцентную мультиплексную ПЦР [21,29,61].
На следующих этапах может применяться анализ генома при отсутствии вариантов при исследованиях на предыдущих этапах. В отличии от других технологий высокопроизводительного секвенирования при анализе генома можно выявить протяженные делеции/инсерции, инверсии, а также глубокие интронные варианты.
Для уточнение патогенности, положения и зиготности выявленных вариантов, при подготовки к таргетной терапии проводится семейный анализ, который позволяет уточнить положение выявленных вариантов нуклеотидной последовательности – на одной хромосоме в составе комплексного аллеля (цис-положение), на разных хромосомах (транс-положение); зиготность вариантов – гомозиготный – на обеих хромосомах больного выявлены одинаковые мутации или гемизиготный – на одной хромосоме мутация, а на другой – протяженная делеция [423].
Требования к лаборатории, проводящей анализы на патогенные варианты гена CFTR, изложены в Консенсусе [2].
Согласно данным Европейского консенсуса по МВ, проведение расширенного молекулярного исследования гена CFTR позволяет выявить патогенный вариант в 98%. Это может быть связано либо с тем, что использованные методы не позволили проанализировать регионы гена, где располагаются патогенные генетические варианты, либо с явлением однородительской дисомии, либо с фенокопиями МВ [21].
Прочие лабораторные исследования, проводимые при диагностике и в процессе динамического наблюдения
Рекомендовано проведение всем пациентам с МВ общего (клинического) анализа крови развернутого с целью ориентировочной оценки воспалительного процесса, контроля влияния на показатели крови проводимой терапии и в комплексной оценке нутритивного статуса [2,62,63,64].
(УУР – B, УДД – 3).
Комментарии: в среднем необходимая частота проведения исследования – ежеквартально. В рамках общего (клинического) анализа крови необходимо: исследование уровня общего гемоглобина в крови, исследование уровня эритроцитов в крови, исследование уровня лейкоцитов в крови, исследование уровня тромбоцитов в крови, дифференцированный подсчет лейкоцитов (лейкоцитарная формула), просмотр мазка крови для анализа аномалий морфологии эритроцитов, тромбоцитов и лейкоцитов, определение цветового показателя, определение размеров эритроцитов, исследование скорости оседания эритроцитов.
Рекомендовано проведение общего (клинического) анализа мочи всем пациентам с муковисцидозом при первичной диагностике и динамическом наблюдении с целью своевременного выявления поражения почек [65].
(УУР – С, УДД – 5).
Комментарий: кратность исследования – не реже 1-2 раз в год, при необходимости - чаще.
Определение наличия панкреатической недостаточности
Рекомендуется проведение лабораторных тестов для определения степени панкреатической недостаточности всем пациентам с подозрением на муковисцидоз и пациентам с муковисцидозом (определение активности панкреатической эластазы-1 в кале), степени коррекции панкреатической недостаточности – копрологическое исследование с определением нейтрального жира в кале [1,2,21].
(УУР – C, УДД – 5).
Комментарии: у пациентов с сохранной функцией поджелудочной железы определение активности панкреатической эластазы-1 в кале проводится ежегодно.
Средняя частота исследований у пациентов с муковисцидозом приведена в Приложении А3.2.
Микробиологическая диагностика
Рекомендуется всем пациентам с муковисцидозом (или с подозрением на муковисцидоз) микробиологическое исследование мокроты (индуцированной мокроты или трахеального аспирата), или, в случае отсутствия отделения мокроты и у пациентов младшей возрастной группы - орофарингеального мазка и/или жидкости бронхоальвеолярного лаважа для идентификации патогена/-ов и определения чувствительности выделенной микрофлоры (Микробиологическое (культуральное) исследование мокроты на аэробные и факультативно-анаэробные микроорганизмы и/или Микробиологическое (культуральное) исследование мокроты на аэробные и факультативно-анаэробные микроорганизмы с использованием автоматизированного оборудования и/ или Микробиологическое исследование мокроты на облигатные анаэробные микроорганизмы и/или Микробиологическое (культуральное) исследование мокроты на облигатные анаэробные микроорганизмы с использованием автоматизированного оборудования и/или Микробиологическое исследование мокроты на неферментирующие грамотрицательные микроорганизмы методом времяпролетной масс-спектрометрии с матрично-активированной лазерной десорбцией/ионизацией Микробиологическое исследование бронхоальвеолярной лаважной жидкости на неферментирующие грамотрицательные и/или Микробиологическое исследование бронхоальвеолярной лаважной жидкости на неферментирующие грамотрицательные микроорганизмы методом времяпролетной масс-спектрометрии с матрично-активированной лазерной десорбцией/ионизацией и/или Микробиологическое исследование мазка слизистой носоглотки на неферментирующие грамотрицательные микроорганизмы методом времяпролетной масс-спектрометрии с матрично-активированной лазерной десорбцией/ионизацией и/или Определение ДНК неферментирующих грамотрицательных микроорганизмов в мазке слизистой носоглотки методом полимеразной цепной реакции в режиме реального времени и/или Определение ДНК неферментирующих грамотрицательных микроорганизмов в мокроте методом полимеразной цепной реакции в режиме реального времени и/ или Определение ДНК неферментирующих грамотрицательных микроорганизмов в бронхоальвеолярной лаважной жидкости методом полимеразной цепной реакции в режиме реального времени и/или Идентификация культур (колоний) микроорганизмов, выделенных из мокроты методом масс-спектрометрии и/или Микробиологическое (культуральное) исследование лаважной жидкости на аэробные и факультативно-анаэробные микроорганизмы) и/или Идентификация культур (колоний) микроорганизмов, выделенных из мазка слизистой слизистой задней стенки глотки методом масс-спектрометрии и/или Микробиологическое исследование мазка с миндалин и задней стенки глотки на аэробные и факультативно-анаэробные микроорганизмы и/или Микробиологическое (культуральное) исследование мазка с миндалин и задней стенки глотки на аэробные и факультативно-анаэробные микроорганизмы с использованием автоматизированного оборудования и/или Микробиологическое исследование мазка с миндалин и задней стенки глотки на грибы, Определение чувствительности микроорганизмов к антимикробным химиотерапевтическим препаратам [1,2,5,21].
(УУР – C, УДД – 5).
Комментарии: исследование проводится при первичной диагностике и в процессе динамического наблюдения, в том числе, для контроля эффективности терапии, не реже 1 раза в 3 мес., по показаниям - чаще. Также проводится контрольное исследование после курса антимикробной терапии при госпитализации или с целью оценки эффективности проведения эрадикации при первичном высеве P. aeruginosa и другой грамотрицательной антибиотикорезистентной флоры (через 7-10 дней от начала терапии).
При хронической грамотрицательной антибиотикорезистентной флоре рекомендуется направлять на микробиологическое обследование пациентов с МВ в период проведения эрадикационной терапии – ежемесячно с целью оценки эффективности элиминации возбудителей;
Направлять детей до 5 лет на диагностику микробной флоры, полученной с помощью глубокого мазка из зева. Для детей старше 5-6-летнего возраста и взрослых рекомендуется приоритетным считать анализ мокроты. У детей с полипозным синуситом исследование рекомендуется проводить путем получения глубокого мазка при риноскопии;
При наличии непроизвольного отхаркивания у пациентов со стабильным течением болезни рекомендовано направлять пациентов ежегодно для исследования диагностического материала на выявление НТМБ. Для скрининга на микобактериоз нужно использовать посевы и мазки на наличие кислотоустойчивых микроорганизмов, которые берутся из мокроты пациента.
Микробиологическим лабораториям учреждений первичной медико-санитарной помощи при выделении из респираторных образцов быстрорастущих НТМБ, следует направлять штаммы в микробиологическую лабораторию экспертного уровня для определения чувствительности к антимикробным препаратам.
Пациентам, которые не откашливают мокроту, со стабильным течением заболевания, находящимся на таргетной терапии, после ингаляций гипертоническим раствором или маннитолом и кинезитерапии для посева мокроты 1 раз в год следует проводить стимуляцию отделения мокроты при помощи аппарата для помощи удаления выделений из дыхательных путей на основе передачи вибрационного пневматического сигнала частотой 6 Гц и 12 Гц во время выдоха пациента. Данный метод влияет на реологию слизи, способствуя разжижению и мобилизации мокроты, в том числе из дистальных отделов легких.
Основным микробиологическим методом диагностики бронхолегочной инфекции является культуральный метод с посевом респираторных образцов на неселективные, селективные и хромогенные питательные среды.
Целесообразно проведение микробиологического исследования респираторных образцов по рекомендации врача в одной из лабораторий экспертного уровня по МВ не реже 1 раза в год.
Важным является использование селективных сред для выделения микроорганизмов, требующих особые условия культивирования или для выделения их специфических, связанных с МВ морфотипов. Особенно для B. cepacia complex, а также S.aureus в виде фенотипа мелких колоний [66,69].
Для повышения вероятности выделения S.aureus у пациентов с МВ рекомендуется использовать одну из селективных сред – маннитол-солевой агар и желточно-солевой агар или хромогенный агар для S.aureus.
В случае выделения SCVs фенотипа S.aureus следует использовать дополнительные методы идентификации (ПЦР, масс-спектрометрию)
Скрининг на MRSA проводить путем прямого посева биоматериала на плотные питательные среды, с дальнейшим определением чувствительности выделенного S.aureus к цефокситину диско-диффузионным методом или посевом образцов на хромогенные среды для MRSA.
Использование селективных сред (агар МакКонки, агар Эндо, цетримидный агар с цетримидом) может помочь в выделении P.aeruginosa.
Для повышения вероятности обнаружения B.cepacia complex в респираторном образце от пациента с МВ строго рекомендуется использование селективной среды для B.cepacia complex (BCSA или другие полимиксин содержащие среды).
На селективных средах для B.cepacia complex может быть получен рост других НГОБ (B.gladioli, Ralstonia spp., Cupriavidus spp., Pandoraea spp., Inquilinus spp. и др.).
Для всех бактерий B. cepacia complex, идентифицированных фенотипическими методами на тест-системах, провести подтверждающую идентификацию методами молекулярной идентификации (масс-спектрометрии или молекулярно-генетическими методами).
Идентификацию до рода микроорганизмов, относящихся к Achromobacter spp. рекомендуется проводить фенотипическими методами на коммерческих тест-системах. Видовую идентификацию рекомендуется проводить молекулярными методами (с помощью -масс-спектрометрии или молекулярно-генетическими методами).
Идентификацию S.maltophilia рекомендуется проводить фенотипическими методами с использованием коммерческих тест-систем.
На селективных средах для B.cepacia complex при рутинном микробиологическом исследовании может наблюдаться рост быстрорастущих НТМБ (наиболее часто M.abscessus), что требует проведения идентификации молекулярными методами (с помощью масс-спектрометрии или молекулярно-генетическими методами).
Идентификацию H.influenzae следует проводить в соответствии с Рекомендациями «Определение чувствительности микроорганизмов к антимикробным препаратам», 2024 г. https://www.antibiotic.ru/files/334/ocmap2024.pdf, Методическими рекомендациями для микробиологов «Выделение, идентификация и определение чувствительности к антибиотикам Haemophilus influenzae», 2000 года [67,68].
Длительность инкубации первичного посева необходима сроком не менее 7 суток с ежедневным просмотром и изучением всех выросших видов колоний [69].
Идентификация микроорганизмов с использованием коммерческих тест-систем, может потребовать пролонгированного периода инкубации (до 48 часов).
Все микроорганизмы, выделенные из дыхательных путей от пациентов с МВ, должны быть идентифицированы как минимум до рода, микроорганизмы, имеющие клиническое значение – до вида [70].
В случае выделения из образца микроорганизмов, идентификацию которых технически невозможно провести в лаборатории, необходимо сохранение культуры для ее последующей реидентификации с использованием масс-спектрометрии или молекулярно-генетических методов [71].
Определение чувствительности выделенной микрофлоры к антибактериальным препаратам и интерпретацию результатов исследования необходимо проводить в соответствии с актуальной версией рекомендаций по определению чувствительности микроорганизмов к антибактериальным препаратам или новых версий после их вступления в силу [67].
Бактерии, вызывающие хроническую инфекцию при муковисцидозе могут расти в виде смеси колониальных морфотипов одного и того же микроорганизма. Чувствительность различных морфотипов в пределах одного образца может значительно варьировать. Необходимо определение антибиотикорезистентности каждого выделенного морфотипа [67].
Определение чувствительности типичных штаммов S.aureus к противомикробным препаратам может быть выполнено диско-диффузионным методом, методом градиентной диффузии, с использованием тест-систем, основанных на методе определения пограничных концентраций или методами серийных разведений (определение минимальной подавляющей концентрации (МПК)) [67]. Определение чувствительности S.aureus ко всему перечню перечисленных для тестирования противомикробных препаратов следует проводить не чаще 2 раз в год. При всех последующих микробиологических исследованиях при выделении S.aureus следует проводить скрининг резистентности к β-лактамам у выделенного штамма с помощью цефокситина [72].
Определение чувствительности штаммов P.aeruginosa. Для типичных штаммов P.aeruginosa тестирование может быть выполнено как диско-диффузионным методом, так и с использованием тест-систем, созданных на основе последовательных разведений как в варианте пограничных концентраций, так и серийных разведений с определением МПК, а также определение МПК методом градиента [73,74,75]. Определение чувствительности P.aeruginosa следует проводить отдельно для каждого морфотипа с указанием профиля чувствительности по каждому морфотипу [76].
Для ингаляционных форм тобрамицина наряду с определением степени чувствительности P.aeruginosa следует определять значение МПК [77].
Комментарии: испанским советом по стандартизации чувствительности и резистентности к антибиотикам MENSURA (Mese Espanola de Normalizacion de la Suseptibilitad y Resistencia a los Antimicrobianos) в 2005 году пересмотрены и установлены более высокие точки отсечения для ингаляционных форм введения тобрамицина при определении чувствительности P. Aeruginosa: точки для чувствительных штаммов <64мг/л, для устойчивых штаммов >128мг/л, по сравнению со значением ≤4мг/л для чувствительных штаммов и >4 мг/л для устойчивых штаммов при парентеральном введении [78].
Определение чувствительности к колистину проводится методом МПК. МПК колистина следует определять только методом микроразведений в бульоне [67].
Следует учитывать, что критерии для определения категорий активности колистина по отношению к микробу основаны на сывороточной концентрации антибактериального препарата системного действия. В связи с широким применением ингаляционных форм препарата эти критерии теряют свою значимость, поскольку в случае ингаляции локальные концентрации действующих веществ многократно превышают те, которые можно достичь при парентеральном способе введения. В то же время к настоящему времени не определены критерии значения МПК для колистина при ингаляционном его применении. Использование критериев, основанных на сывороточных концентрациях, таким образом, может привести к ошибкам интерпретации результатов исследования чувствительности микроорганизмов для ингаляционных форм антибиотиков [2,77].
Определение чувствительности Burkholderia cepacia complex. По идеологии EUCAST не представляется возможным рекомендовать определение чувствительности бактерий B.cepacia complex для выбора противомикробных препаратов системного действия для терапии инфекций, вызванных представителями этой группы микроорганизмов [67]. В случае необходимости определения чувствительности B.cepacia complex следует использовать методы и критерии, определенные актуальными стандартами CLSI (Clinical and Laboratory Standards Institute, Институт клинических и лабораторных стандартов) [67].
Определение чувствительности Stenotrophomonas maltophilia. При определении чувствительности штаммов S.maltophilia следует руководствоваться актуальной версией рекомендаций по определению чувствительности микроорганизмов к противомикробным препаратам [79].
Определение чувствительности Achromobacter spp. Определение чувствительности штаммов A.xylosoxidans следует проводить в соответствии с Рекомендациями МАКМАХ «Определение чувствительности микроорганизмов к антимикробным препаратам (2024)» и последующих версий [67].
При выдаче заключения по микробиологическому исследованию целесообразно указывать группу выделенных микроорганизмов в соответствии с ранжированием бактерий по их клиническому значению при муковицидозе. В отчете о результате исследования материала от больного пациента с МВ рекомендуется указывать наличие мукоидных и немукоидных фенотипов P.aeruginosa [80].
При интерпретации результатов определения чувствительности микроорганизмов следует указывать стандарт и год издания, по которому проводилось исследование [67,81,82].
При интерпретации результатов определения чувствительности следует использовать пограничные значения EUCAST 10.0 и последующих версий, Российские рекомендации. Определение чувствительности микроорганизмов к антимикробным препаратам. Версия 2024-02. - МАКМАХ, СГМУ: Смоленск, 2024. - 192 с. для оценки результата по одной из трех категорий чувствительности:
Ч - Чувствительный при стандартном режиме дозирования: микроорганизм оценивается как «Чувствительный при стандартном режиме дозирования» в том случае, если уровень активности противомикробного препарата свидетельствует о высокой вероятности эффективности терапии при стандартном режиме дозирования.
У - Чувствительный при увеличенной экспозиции: микроорганизм оценивается как «Чувствительный при увеличенной экспозиции»1, если уровень активности препарата свидетельствует о высокой вероятности эффективности терапии при увеличении экспозиции препарата путем коррекции режима дозирования или благодаря его концентрации в очаге инфекции.
Р - Резистентный: микроорганизм оценивается как «Резистентный» при высокой вероятности терапевтической неудачи даже при увеличенной экспозиции препарата.
1 - Экспозиция отражает зависимость влияния противомикробного препарата на возбудителя в очаге инфекции от пути введения, дозы, интервала дозирования, продолжительности инфузии препарата, а также его распределения и пути выведения.
Кроме этого, следует указывать в заключении, что интерпретация значений минимальной подавляющей концентрации как чувствительный/резистентный осуществляется на основании критериев, рассчитанных для сывороточных концентраций препарата при его внутривенном введении. При других путях применения препарата аналогичное значение минимальной подавляющей концентрации может быть интерпретировано иначе.
В соответствии с приказом Минздрава России 13 октября 2017 г. № 804н от «Об утверждении номенклатуры медицинских услуг» по определению чувствительности выделенной микрофлоры есть несколько услуг: Определение чувствительности микроорганизмов к антимикробным химиотерапевтическим препаратам (в т.ч., Определение чувствительности микроорганизмов к противомикробным химиотерапевтическим препаратам диско-дифузионным методом, Определение чувствительности микроорганизмов к противомикробным химиотерапевтическим препаратам методом градиентной диффузии, Определение чувствительности микроорганизмов к противомикробным химиотерапевтическим препаратам методом разведений, Определение чувствительности микроорганизмов к противомикробным химиотерапевтическим препаратам с использованием автоматических анализаторов, Определение чувствительности микроорганизмов к противомикробным химиотерапевтическим препаратам методом пограничных концентраций).
Пациентам с МВ с подозрением на микобактериоз, вызванный НТМБ необходимо исследование образцов диагностического материала как минимум один раз в год в динамике [1,2,5,21]. Исследование на выявление микобактерий в диагностическом материале следует проводить в специализированных бактериологических лабораториях при противотуберкулезных учреждениях.
Показанием к исследованию диагностического материала на НТМБ служат: отрицательная клиническая и/или рентгенологическая динамика при отсутствии новых патогенов, отсутствие эффекта от проводимой антибактериальной терапии. В качестве диагностического материала используют: мокроту (или индуцированную мокроту), в случаях отсутствия мокроты – смыв с ротоглотки (СРГ), бронхоальвеолярный лаваж (БАЛ).
Для проверки подозрений, что пациент с МВ заражен микобактериями, в качестве диагностического материала используют мокроту или индуцированную мокроту (в исключительных случаях - исследование трахеального аспирата при невозможности получить мокроту/индуцированную мокроту. Следует помнить, что в данном случае эффективность выявления микобактерий очень низкая).
Для исследований на наличие НТМБ не следует использовать трансбронхиальную биопсию (ТББ) (Биопсия легкого трансбронхиальная рентгенохирургическая/ Трансбронхиальная пункция) и взятие орофарингеальных мазков.
У пациентов, выделяющих мокроту в достаточном количестве, для исследования собирают ее утреннюю порцию. Достаточный объем исследуемой порции мокроты составляет 3 - 5 мл, в целях повышения информативности необходимо исследовать мокроту, которую собирают для исследования три дня подряд.
Значимыми критериями микобактериоза у пациентов с МВ являются следующие результаты материала из дыхательных путей: положительный результат на наличие кислотоустойчивых микроорганизмов (КУМ) при микроскопии препаратов с окраской по Цилю-Нильсену или люминесцентными красителями (Микроскопическое исследование мокроты на микобактерии (Mycobacterium spp. (кислотоустойчивую микрофлору)), наличие роста НТМБ на специализированных питательных средах и подтверждение одного и того же вида микобактерий как минимум из двух образцов мокроты (Микробиологическое (культуральное) исследование мокроты на аэробные и факультативно-анаэробные микроорганизмы).
С целью контроля эффективности химиотерапии не реже, чем раз в 1-3 месяца необходимо проводить посев мокроты на выявление НТМБ в диагностическом материале [83,84].
Критерием эффективного лечения является отсутствие роста микобактерий на питательных средах не менее чем в трех последовательно взятых образцах диагностического материала.
После завершения курса химиотерапии микобактериоза необходимо постоянное динамическое наблюдение за состоянием пациента и регулярное, не реже чем раз в 6 месяцев лабораторное обследование на наличие или отсутствие НТМБ в диагностическом материале.
Методы диагностики микобактериоза/туберкулеза.
-
Всем пациентам с подозрением на микобактериоз органов дыхания следует проводить исследование не менее трех образцов мокроты, собранных последовательно с интервалом в сутки.
Исследование диагностического материала проводят по определенному алгоритму. Необходимые лабораторные тесты выполняют параллельно из одной порции диагностического образца.
Посев диагностического материала на питательные среды с обязательной последующей дифференциацией МБТК/НТМБ и определением НТМБ до вида (Микробиологическое (культуральное) исследование мокроты на аэробные и факультативно-анаэробные микроорганизмы).
Комментарий: выделение культуры микробактерий НТМБ осуществляется исключительно в специализирован
Методы визуализации легких
Рекомендуется проведение рентгенографии органов грудной клетки (Рентгенография легких/Рентгенография легких цифровая) пациентам с подозрением на муковисцидоз и пациентам с муковисцидозом с целью определения характера и объема поражения легочной ткани [1,2,21].
(УУР – C, УДД – 5).
Комментарии: рентгенография органов грудной клетки может выявить такие признаки, как деформация и усиление легочного рисунка, пневмофиброз, перибронхиальная инфильтрация, консолидация (ателектазы), бронхоэктазы, буллы, выявить проявления бронхиальной обструкции: локальные участки вздутия легочной ткани, увеличение ретростернального пространства, уплощение диафрагмы, а также кифоз, утолщение бронхиальных стенок, слизистые пробки. Пациентам с муковисцидозом проводится по показаниям, в среднем 1 раз в 2 года (Приложение А3.2).
Данный метод может быть недостаточно информативен для точного описания характера изменений в легких, но имеет меньшую лучевую нагрузку. До настоящего времени в разных центрах, курирующих пациентов с муковисцидозом, в том числе зарубежных, для динамического наблюдения за пациентом чаще используется рентгенография, в ряде центров - компьютерная томография [21].
Рекомендуется проведение компьютерной томографии (КТ) органов грудной полости пациентам с подозрением на муковисцидоз и пациентам с муковисцидозом с целью определения характера и объема поражения легочной ткани [1,2,21].
(УУР – C, УДД – 5).
Комментарий: в настоящее время компьютерная томография органов грудносй полости является основным методом диагностики изменений в легких при МВ.
Компьютерная томография органов грудной полости (КТ) - экспертная методика для детализации изменений. Проводится низкодозная компьютерная томография (НДКТ) – снижение силы тока до 1 мА/кг массы для детей и молодых взрослых весом <50 кг в сочетании с напряжением на трубке 100 кВ. Выполняется на глубине вдоха, при невозможности задержки дыхания, детям до 3-х лет – в условиях седации. 1 раз в 2 года, при обострении – внеочередное исследование. Функциональное КТ-исследование органов грудной полости «на выдохе» для оценки бронхиальной обструкции при невозможности выполнения КИФВД.
- КТ-ангиография органов грудной полости (Компьютерная томография органов грудной полости с внутривенным болюсным контрастированием/ Компьютерная томография грудной полости с внутривенным болюсным контрастированием, мультипланарной и трехмерной реконструкцией) / ангиография легочной артерии и ее ветвей / перфузионная сцинтиграфия легких при подозрении на ТЭЛА, перед трансплантацией легких, при кровохарканьи).
- Компьютерная томография является, в том числе, основным методом диагностики аспергиллеза при МВ. Компьютерная томография легких органов грудной полости может выявить такие признаки, как деформация и усиление легочного рисунка, пневмофиброз, перибронхиальную инфильтрацию, ателектазы, бронхоэктазы, буллы.
- При АБЛА на КТ легких выявляют «летучие» инфильтраты в легких, бронхоэктазы, расширение бронхов из-за скопившейся слизи («симптом перчатки»), так называемые симптомы «кольца» и «трамвайных путей», представляющие собой утолщение стенок периферических бронхов в результате перибронхиальной инфильтрации и фиброза, возможны ателектазы. Основными рентгенологическими признаками ранних стадий АБЛА являются двусторонние инфильтраты, исчезающие после применения кортикостероидов для системного применения; признаки хронического перибронхиального воспаления и мукоидных пробок. Позднее выявляют двусторонние, проксимальные, чаще верхнедолевые бронхоэктазы; фиброз и утолщение плевры. КТ – более чувствительный метод выявления указанных признаков, чем рентгенография.
- У пациентов с ХАЛ на КТ обычно выявляют комплекс бронхоэктазов, окруженный зоной воспаления, иногда содержащих аспергилломы. КТ признак аспергилломы: одиночная полость с содержимым, смещающимся при перемене положения тела (симптом «погремушки»), с характерной прослойкой воздуха (симптом «серпа») [16,38,85,86].
Рекомендуется выполнять контрольную КТ органов грудной полости с целью оценки эффективности таргетной терапии, в среднем, через 12 месяцев с момента старта терапии вне острых респираторных заболеваний во избежание «островоспалительных артефактов. При проведении таргетной терапии отмечается обратное развитие структурных изменений у детей и взрослых [429,430].
(УУР – C, УДД – 5).
Рекомендовано проведение магнитно-резонансной томографии органов грудной клетки пациентам с МВ в качестве уточняющего метода для снижения лучевой нагрузки при многократном контроле воспалительного процесса. До 7 лет – в условиях седации, после – на свободном дыхании [119,120].
(УУР – C, УДД – 5).
Методы визуализации околоносовых пазух
Рекомендуется проведение КТ ОНП (конусно-лучевая или мультиспиральная) или МРТ ОНП при первичной оценке патологического процесса в околоносовых пазухах и при подготовке к каждому ринохирургическому вмешательству [121,122].
(УУР – С, УДД – 4).
Комментарий: КТ ОНП производится в аксиальной плоскости с реконструкцией изображения в коронарной и сагиттальной проекциях. Детям не рекомендуется выполнение КТ ОНП без клинических показаний (с целью динамического наблюдения), т.к. это в значительной мере увеличивает суммарную лучевую нагрузку (в связи с необходимостью периодического выполнения КТ органов грудной полости). Взрослым КТ ОНП проводится 1 раз в 1-2 года или чаще по показаниям. В значительной мере патогномоничными для ХРС при МВ КТ-признаками являются: деминерализация и медиализация крючковидного отростка в сочетании с заполнением верхнечелюстной пазухи плотным содержимым; гипоплазия (вплоть до агенезии) лобных и клиновидных пазух; медиализация («медиальное выбухание») латеральной стенки полости носа; более быстрый рост задних клеток решетчатого лабиринта по сравнению с передними. Должны оцениваться: наличие полипов носа (степень ПН I-III, согласно классификации Johansen LV, 1993), послеоперационные изменения. Рентгенография ОНП не является информативным методом диагностики ХРС при МВ. МРТ околоносовых пазух также не может быть альтернативой КТ, т.к. не позволяет оценить состояние костных структур.
Проводится, в том числе, для оценки эффективности таргетной терапии через год от ее старта.
Рекомендуется выполнение контрольной КТ ОНП с целью оценки эффективности таргетной терапи, в среднем, через 12 месяцев с момента старта терапии вне острых респираторных заболеваний во избежание «островоспалительных артефактов» [431,432].
(УУР – С, УДД – 4).
Комментарии: при дальнейшем наблюдении КТ ОНП должна выполняться в зависимости от наличия клинических показаний.
В настоящий момент накоплен большой клинический опыт и достаточное число публикаций в мире, демонстрирующих выраженный положительный эффект таргетной терапии на течение ХРС в виде значительного улучшения или нормализации пневматизации ОНП [431,433]. Объективная констатация эффекта должна основываться на результатах КТ ОНП с оценкой в баллах по системе Lund-Mackay (Приложение Г3) (или иной балльной оценке) [434] и эндоскопической картине. При этом подобный эффект следует ожидать, прежде всего, на «тройной» терапии препаратом ивакафтор + элексакафтор + тезакафтор и ивакафтор, в то время как на терапии препаратом ивакафтор + лумакафтор** значимого улучшения состояния ОНП обычно не наблюдается [435].
На фоне лечения препаратом ивакафтор + элексакафтор + тезакафтор и ивакафтор отмечается быстрое наступление эффекта (средний срок с момента старта терапии и контрольной КТ ОНП составил 7,6 месяцев [431]) и его стойкость (не менее 180 дней [436]).
Ряд авторов указывают на достоверный параллелизм между степенью улучшения рентгенологической картины ОНП и снижением показателя потовой пробы [431,436], что вероятно может использоваться в роли прогностического критерия.
При этом отмечается неравномерность восстановления пневматизации разных групп ОНП и анатомических зон синоназальной области: более быстрая положительная динамика отмечается в отношении проходимости остиомеатального комплекса и пневматизации верхнечелюстных пазух; наиболее отсроченная – в задних клетках решетчатого лабиринта и клиновидных пазухах. Вероятно, это связано с анатомическими особенностями путей их вентиляции и дренирования [431,432].
Неоднозначными остаются критерии деэскалации терапии ХРС на фоне эффективной таргетной терапии. Полное восстановление воздушности околоносовых пазух (отсутствие какого-либо патологического субстрата в них) и достаточная проходимость естественных и/или послеоперационных соустий, констатированные с помощью КТ, могут служить основанием отмены топической муколитической и глюкокортикостероидной терапии с рекомендацией продолжения ирригационных процедур/гигиены полости носа с учетом изначальной скомпрометированности данной зоны.
В соответствии с Приказом Минздрава России 13 октября 2017 г. № 804н от «Об утверждении номенклатуры медицинских услуг»: компьютерная томография придаточных пазух носа, гортани, спиральная компьютерная томография придаточных пазух носа, магнитно-резонансная томография околоносовых пазух.
Абдоминальная рентгенография
Рекомендовано проведение абдоминальной рентгенографии (Обзорная рентгенография органов брюшной полости) при мекониевом илеусе и синдроме дистальной интестинальной обструкции (СДИО) с целью диагностики непроходимости кишечника [123,124].
(УУР – С, УДД – 5).
Комментарий: обзорная рентгенография органов брюшной полости проводится в вертикальном положении пациента, в прямой проекции.
С той же целью при синдроме дистальной интестинальной обструкции может применяться компьютерная томография органов брюшной полости.
Методы диагностики остеопороза
Общую информацию об оценке МПК у пациентов с МВ см. в Приложении А3.3.
Определение исходной МПК при проведении рентгеноденситометрии назначается детям старше 8 лет. Раньше - при наличии таких факторов риска как:
1) низкий ИМТ (<90% от идеального ИМТ),
2) активность легочного заболевания (ОФВ1 <50% должного),
3) длительная (3 мес. и более) терапия пероральными кортикостероидами для системного применения,
4) задержка полового созревания, гипогонадизм,
5) наличие низкоэнергетических переломов в анамнезе.
Повторные исследования рекомендовано проводить детям и взрослым до 50 лет:
1) приблизительно через 5 лет, если Z-критерий выше -1 SD и пациент клинически стабилен,
2) каждые 2 года, если Z-критерий между -1 и -2 SD,
3) каждый год, если Z-критерий -2 SD и ниже или есть низкоэнергетические переломы в анамнезе или имеются значимые факторы риска остеопороза.
У женщин в постменопаузе и мужчин 50 лет и старше рекомендуется проведение остеоденситометрии приблизительно:
1) каждые 5 лет, если Т-критерий выше -1 SD,
2) каждые 2 года, если Т-критерий между -1 и -2,5 SD,
3) ежегодно, если Т-критерий ≤ -2,5 SD или имеются значимые факторы риска остеопороза.
Рентгеноденситометрия должна быть проведена до назначения антиостеопоротической терапии [2].
Для оценки динамики МПК на фоне лечения остеопороза рекомендовано проводить рентгеноденситометрию (DXA) 1 раз в 6-12 мес. у детей старше 8 лет и 1 раз в 12 мес. у взрослых [35,125,126].
(УУР – С, УДД – 5).
Комментарий: рентгеноденситометрию желательно проводить на одном и том же аппарате (денситометре костном рентгеновском) одним и тем же специалистом.
Рентгенография костей скелета (Рентгенография пораженной части костного скелета) пациентам с МВ для диагностики остеопороза не проводится, применяется при переломах [35].
У детей и подростков с МВ рекомендуется проводить рентгеноденситометрию поясничного отдела позвоночника в передне-задней проекции (от 0 лет) и по программе «все тело» (с 3 лет по показаниям), исключая голову из расчетов костной минеральной плотности с целью своевременного выявления снижения МПК и коррекции выявленных изменений [50].
(УУР – С, УДД – 5).
Комментарии: исследование МПК проксимального отдела бедра у детей и подростков не проводится в связи вариабельностью развития скелета.
У детей с задержкой линейного роста и развития результаты МПК должны анализироваться с учетом абсолютного роста или ростового возраста, или сравниваться с соответствующими педиатрическими базами данных, включающих специфические для возраста, пола и возраста Z-критерии [50,127].
У взрослых пациентов с МВ рекомендуется проводить остеоденситометрическое исследование (рентгеноденситометрию) поясничного отдела позвоночника в передне-задней проекции и с 20 лет - проксимального отдела бедренной кости (анализируется область шейки бедра (Neck) и общий показатель бедра (TotalHip), для заключения выбирается наименьшее значение Z- или Т-критерия) с целью своевременной диагностики нарушения костной минерализации [35,127].
(УУР – С, УДД – 5).
Определение функции внешнего дыхания
Рекомендовано при подозрении на МВ и у пациентов с МВ исследовать функцию внешнего дыхания: спирометрия – в среднем каждые 3 месяца (исследование неспровоцированных дыхательных объемов и потоков, при необходимости – дополнительно исследование дыхательных объемов с применением лекарственных препаратов), бодиплетизмография – по показаниям, в среднем - ежегодно с целью определения и динамического контроля легочной функции, определения обратимости обструкции при ее наличии (при отсутствии возрастных или иных противопоказаний) [1,2,21].
(УУР – C, УДД – 5).
Комментарий: исследование функции внешнего дыхания (спирометрия) возможно у детей с 5-6 лет, в том случае, если пациент может выполнить маневр форсированного выдоха, диагностическая ценность исследования у детей младше 5 лет ниже. Спирометрия позволяет косвенно оценить легочные объемы, бодиплетизмографию проводят для более точной оценки легочных объемов по показаниям.
Наиболее часто у пациентов с МВ выявляются обструктивные и рестриктивные нарушения вентиляции (в зависимости от объема и характера поражения бронхиального дерева).
При исследовании ФВД на ранних стадиях АБЛА обычно выявляют признаки бронхиальной обструкции, по мере прогрессирования заболевания – сочетание обструктивных и рестриктивных нарушений.
В соответствии с Приказом Минздрава России 13 октября 2017 г. № 804н от «Об утверждении номенклатуры медицинских услуг»: исследование неспровоцированных дыхательных объемов и потоков, исследование дыхательных объемов с применением лекарственных препаратов, бодиплетизмография.
Рекомендовано проведение пульсоксиметрии и/или исследование газового состава крови (исследование уровня кислорода крови, исследование уровня углекислого газа в крови) всем пациентам с подозрением на МВ и всем пациентам с МВ при каждой госпитализации, по показаниям (обострение хронического бронхолегочного процесса, наличие дыхательной недостаточности, требующей оксигенотерапии) – чаще [2,128,129].
(УУР – С, УДД – 5).
Ультразвуковые методы исследования
Рекомендовано проведение ультразвукового исследования органов брюшной полости и печени (ультразвуковое исследование органов брюшной полости (комплексное), ультразвуковое исследование печени, ультразвуковое исследование гепатобилиарной зоны) всем пациентам с подозрением на муковисцидоз и пациентам с муковисцидозом, особое внимание уделять структуре поджелудочной железы, определять тип кровотока в печени (допплерография сосудов портальной системы, дуплексное сканирование сосудов печени) с целью выявления изменений, характерных для данного заболевания и их динамики [1,2,21].
(УУР – C, УДД – 5).
Комментарий: наличие линейного кровотока в печени свидетельствует о формировании фиброза. Целесообразно сопоставить с данными фиброэластометрии.
Рекомендовано проведение фиброэластометрии печени (эластометрия печени) всем пациентам с МВ с целью оценки степени выраженности фиброза по шкале METAVIR (Приложение Г1) [2,21,130,508].
(УУР – A, УДД – 1).
Комментарии: фиброэластометрия. печени (эластометрия печени) также целесообразно назначать пациентам с подозрением на МВ при наличии неясного поражения печени.
Рекомендовано дополнительно к проведению эластометрии печени пациентам с МВ определение отношения уровня АСТ к тромбоцитам [APRI]: значение ≥0,545 является пороговым для продвинутых стадий фиброза (F3–F4) с целью более точной диагностики степени цирроза [2,21,130,508].
(УУР – C, УДД – 5).
Комментарии: формула расчета APRI = [(АСТ (МЕ/л) /ВГН АСТ (МЕ/л) )/уровень тромбоцитов в общем (клиническом) анализе крови развернутом (109/л)] × 100.
Рекомендовано всем пациентам мужского пола в возрасте старше 15 лет с муковисцидозом выполнение урологического/андрологического обследования с проведением ультразвукового исследования половых органов (УЗИ органов мошонки, Ультразвуковое исследование предстательной железы трансректальное, Ультразвуковое исследование органов малого таза (комплексное) для выявления структурных и морфологических изменений [98,104,119,131].
(УУР – С, УДД – 4).
Комментарии: при наличии нарушений- повторное обследование 1 раз в год, при отсутствии нарушений- по мере необходимости, но не реже 1 раза в 3 года.
Рекомендовано регулярное периодическое эхокардиографическое исследование (эхокардиография, Эхо-КГ) с допплеровским анализом (измерение градиента давления на легочной артерии) у пациентов с МВ, так как при этой патологии, особенно при распространенном поражении, возможно развитие легочной гипертензии и формирование легочного сердца [2].
(УУР – C, УДД – 5).
Комментарий: средняя частота проведения Эхо-КГ – 1 р./год (представлена в Приложении А3.2).
Электрокардиография
Рекомендовано проведение электрокардиографии пациентам с муковисцидозом при Псевдо-Барттер синдроме с целью контроля влияния электролитных нарушений на сердечную деятельность, перед началом терапии ингибиторами протонного насоса, лекарственной терапией НТМБ, при длительном применении азитромицина** по другим показаниям, на фоне терапии высокими дозами селективных β2-адреномиметиков (2 недели) с целью оценки интервала QT [89,132].
(УУР – C, УДД – 4).
Эндоскопические методы исследования
-
Рекомендовано проведение трахеобронхоскопии пациентам с муковисцидозом:
- в случаях необходимости проведения дополнительного микробиологического исследования жидкости бронхоальвеолярного лаважа (в т. ч. необходимость уточнения микробиологического диагноза у детей, которые не продуцируют мокроту);
- с санационной целью при попытке расправить ателектаз доли легкого в случае неэффективности проведения консервативной терапии;
- при отсутствии ответа на внутривенную противомикробную терапию;
у детей – дополнительно при труднокупируемых свистящих хрипах для исключения сопутствующих заболеваний (например, бронхомаляции)[1,2,16,85,86,133].
(УУР – C, УДД – 5).
Комментарий:
- Трахеобронхоскопия с санационной целью рассматривается в клинических случаях когда стандартная консервативная терапия ателектаза (ингаляции Дорназой альфа**, кортикостероидами системного действия (Преднизолон**)) не эффективна, В такой ситуации при наличии персистирующих локальных зон коллапса/консолидации на рентгенограмме легких можно эндобронхиально вводить #дорназу альфа** в дозе 2,5 мг в 10 мл 0,9% хлорида натрия** [501]. В некоторых случаях эндотрахеально может быть рассмотрено введение противомикробных препаратов системного действия;
- Высокий риск развития трахеобронхита при аспергиллезе требует проведения ранних бронхоскопий с последующим лабораторным исследованием БАЛ. Критерием диагностики аспергиллезного трахеобронхита является выявление при бронхоскопии специфических изменений (эритема, изъязвления, псвдомембранозные изменения);
- Показания для проведения трахеобронхоскопии при кровохарканьи/легочном кровотечении – см. раздел 3.4.
В соответствии с Приказом Минздрава России 13 октября 2017 г. № 804н от «Об утверждении номенклатуры медицинских услуг»: трахеобронхоскопия, видеотрахеобронхоскопия.
Рекомендуется проведение эндоскопии полости носа (эндоскопическая эндоназальная ревизия полости носа, носоглотки) пациентам с МВ по показаниям: при необходимости оценки выраженности хронического риносинусита, степени назального полипоза, уточнения показаний к ринохирургическому лечению, оценки результатов эндоназальных эндоскопических хирургических вмешательств [133,135,136,137].
(УУР – С, УДД – 4).
Комментарий: эндоскопия полости носа выполняется оториноларингологом. Частота исследования определяется индивидуально в зависимости от течения ХРС.
Фиброэзофагогастродуоденоскопию (эзофагогастродуоденоскопию) рекомендуется проводить всем пациентам с МВ с циррозом печени для контроля варикозно расширенных вен пищевода (ВРВП) 1 раз в 6-12 мес., при подозрении на ГЭРБ, эрозивно-язвенные поражения, воспалительные заболевания слизистой пищевода и желудка [2].
(УУР – С, УДД – 5).
Ректороманоскопия с биопсией прямой кишки с помощью видеоэндоскопических технологий рекомендуется по показаниям пациентам с подозрением на МВ или для оценки эффективности таргетной терапии пациентам с МВ для проведения измерения разности кишечных потенциалов [2,138,139].
(УУР – С, УДД – 5).
Инструментальная диагностика мекониевого илеуса
Рекомендовано проведение обзорной рентгенографии грудной и брюшной полости в прямой проекции вертикальном положении пациентам с МВ и подозрением на мекониевый илеус с целью оценки состояния органов брюшной полости [140].
(УУР – С, УДД – 5).
Пациентам с подозрением на мекониевый илеус рекомендуется УЗИ органов брюшной полости (комплексное) для оценки скорости кровотока и индекса резистентности на сосудах брыжейки в различных уровнях, определения наличия и характера свободной жидкости в межпетлевом пространстве, латеральных каналах, малом тазу (ультразвуковое исследование органов брюшной полости (комплексное), ультразвуковая допплерография сосудов брыжейки, ультразвуковое определение жидкости в брюшной полости, ультразвуковое исследование органов мошонки, ультразвуковое исследование органов малого таза (комплексное)) [140].
(УУР – С, УДД – 5).
Комментарий: исследование рекомендуется проводить врачом ультразвуковой диагностики совместно с врачом-детским хирургом.
Рекомендуется проведение рентгеноконтрастных методов исследования при подозрении на мекониевый илеус для установления диагноза, оценки уровня поражения, определения объема контрастного вещества для проведения повторного тугого контрастирования [140].
(УУР – С, УДД – 5).
Комментарии: диагностические методы, применяемые при обследовании: ирригография (ретроградная), интервальная рентгенография для оценки пассажа по желудочно-кишечному тракту (A06.17.002 Рентгеноконтроль прохождения контрастного вещества по желудку, тонкой и ободочной кишке, A06.18.002 Рентгеноконтроль прохождения контраста по толстой кишке).
o У новорожденных детей применяются водорастворимые рентгенконтрастные вещества на основе йода. Контрастное вещество вводится эндопросветно, что минимизирует системное воздействие, но нужно учитывать воздействие на кишечную стенку, поскольку данный раствор гиперосмолярный и может провоцировать дегидратацию и желудочно-кишечные кровотечения. Также водорастворимое контрастное вещество может всасываться в кишечнике, выводится в этом случае оно почками, и мы можем визуализировать на отсроченных снимках контраст в собирательной системе почек. Чтобы минимизировать риск поражения слизистой, рекомендуется разведение физиологическим раствором в соотношении 1:1.
o Введение бариевой взвеси недопустимо у данной группы пациентов, поскольку продвижение бария по ЖКТ требует соответствующей перистальтической активности, которой у новорожденных детей нет. Это может привести к формированию обтурационной кишечной непроходимости бариевыми камнями на фоне всасывания жидкой части контрастной взвеси.
o Ретроградная ирригография с водорастворимым контрастным веществом. Контрастное вещество вводится в толстую кишку через зонд, заведенный в анус на глубину 2-3 см, с контролем заполнения толстой кишки под рентгеноскопией. Объем заполнения толстой кишки 20 мл/кг, для тугого контрастирования возможно увеличение объема до 25 мл/кг. Контраст вводится медленно, контролируется ход толстой кишки, диаметр просвета кишки, характер гаустрации, наличие содержимого внутри просвета кишки. При достижении контрастом купола слепой кишки необходимо оценить его расположение. Далее продолжается введение контрастного вещества, оценивается растяжимость кишки, заброс контраста выше Баугиниевой заслонки, характер подвздошной кишки (диаметр просвета, гаустрация, содержимое), а также возможность попадания контрастного вещества в расширенный отдел тонкой кишки и расстояние от илеоцекального угла до расширенного отдела. Для лучшего продвижения контраста по кишечнику, возможно использовать легкий массаж передней брюшной стенки. По завершении исследования необходимо зафиксировать объем использованного контрастного вещества в медицинской документации для проведения повторного тугого контрастирования в качестве консервативного лечения мекониевого илеуса.
Рекомендовано проведение диагностической лапароскопии пациентам с подозрением на мекониевый илеус для установления причины кишечной непроходимости [123,140].
(УУР – С, УДД – 5).
Комментарий: в настоящий момент в связи с активным развитием лапароскопической техники и анестезиологического пособия новорожденным и недоношенным детям, данный метод является наиболее информативным и наименее травматичным для верификации причин кишечной непроходимости. Если есть возможность, хирургическое лечение можно выполнить лапароскопически или расширить объем лечения до минилапаротомии в зоне интереса, либо, исключив анатомический дефект, поставить показания к консервативному лечению.
Инструментальная диагностика синдрома дистальной интестинальной обструкции
Синдром дистальной интестинальной обструкции – это частный случай низкой обтурационной кишечной непроходимости, возникающий при нарушении кишечного транзита у пациентов с муковисцидозом, старше неонатального возраста. Данное состояние редко встречается в возрасте до 2 лет, в силу особенности диеты и сохранении перистальтической активности кишки. Для развития описываемого синдрома необходимо сочетание нескольких факторов – нарушенная секреция пищеварительных ферментов, пищевой рацион, состоящий из продуктов, приводящих к загустению кишечного химуса (рис, яблоко, груша, банан, хлебобулочные изделия: пшеничный хлеб, макароны, печенье; картофель, чай, желе, мясо, курица или рыба), а также декомпенсация кишки на фоне хронического растяжения кишечной стенки. Заболевание проявляется по типу калового завала, но характерной особенностью является то, что обструкция происходит выше толстой кишки и стандартные консервативные методы разрешения калового завала будут не эффективны.
Понимая вышеописанные факторы, возможно сформировать группы риска, создать систему профилактики, диагностики и лечения.
Рекомендовано проведение обзорной рентгенографии органов брюшной полости в прямой проекции вертикальном положении пациентам с МВ и клиникой низкой обтурационной кишечной непроходимости с целью оценки состояния органов брюшной полости [141,142,143].
(УУР – С, УДД – 5).
Комментарии: при описании рентгенограммы брюшной полости следует обратить внимание также на состояние диафрагмы.
Пациентам с подозрением на синдром дистальной интестинальной обструкции рекомендуется УЗИ органов брюшной полости комплексное, ультразвуковое исследование органов малого таза (комплексное), ультразвуковое определение жидкости в брюшной полости (в т.ч., с определением наличия свободной жидкости в межпетлевом пространстве латеральных каналах, малом тазу), ультразвуковое исследование органов мошонки для оценки характера содержимого кишечника, преимущественно в правых отделах брюшной полости) [141,142].
(УУР – С, УДД – 5).
Комментарий: исследование рекомендуется проводить врачом ультразвуковой диагностики совместно с врачом-детским хирургом. Проводится также прием (осмотр, консультация) врача-детского хирурга. Ультразвук может не обеспечить адекватной визуализации причины формирования обструкции, тогда в принятии хирургического решения необходимо руководствоваться клинической картиной и данным рентгенографии.
Рекомендуется проведение рентгеноконтрастных методов исследования при подозрении на синдром дистальной интестинальной обструкции для установления диагноза, оценки уровня поражения [141,143].
(УУР – С, УДД – 5).
Комментарии: диагностические методы, применяемые при обследовании: ирригография (ретроградная), интервальная рентгенография для оценки пассажа по желудочно-кишечному тракту (А06.17.002 Рентгеноконтроль прохождения контрастного вещества по желудку, тонкой и ободочной кишке, А06.18.002 Рентгеноконтроль прохождения контраста по толстой кишке).
o У детей с муковисцидозом и синдромом дистальной интестинальной обструкции целесообразно применение водорастворимых рентгенконтрастных средств, содержащих йод. Контрастное средство вводится эндопросветно, что минимизирует системное воздействие, но нужно учитывать воздействие на кишечную стенку. Также водорастворимое контрастное средство может всасываться в кишечнике, выводится в этом случае оно почками, и мы можем визуализировать на отсроченных снимках контрастное средство в собирательной системе почек. Чтобы минимизировать риск поражения слизистой, рекомендуется разведение раствором натрия хлорида** 0,9% в соотношении 1:1.
o Введение бария сульфата** допустимо у данной группы пациентов, но не желательно поскольку продвижение бария по ЖКТ может быть нарушено, вследствие декомпенсированного состояния перистальтической активности. Это может привести к формированию обтурационной кишечной непроходимости бариевыми камнями на фоне всасывания жидкой части контрастного средства.
Ретроградная ирригография с водорастворимым контрастным средством. Контрастное средство вводится в толстую кишку через зонд, заведенный в анус на глубину 2-3 см, с контролем заполнения толстой кишки под рентгеноскопией. Объем заполнения толстой кишки 20 мл/кг, для тугого контрастирования возможно увеличение объема до 25 мл/кг. Контраст вводится медленно, контролируется ход толстой кишки, диаметр просвета кишки, характер гаустрации, наличие содержимого внутри просвета кишки. При достижении контрастом купола слепой кишки необходимо оценить его расположение. Далее продолжается введение контрастного средства, оценивается растяжимость кишки, заброс контраста выше Баугиниевой заслонки, характер подвздошной кишки (диаметр просвета, гаустрация, содержимое), а также возможность попадания контрастного средства в расширенный отдел тонкой кишки и расстояние от илеоцекального угла до расширенного отдела. Для лучшего продвижения контраста по кишечнику, возможно использовать легкий массаж передней брюшной стенки.
Рекомендовано рассмотреть проведение диагностической лапароскопии пациентам с подозрением на синдром дистальной интестинальной обструкции без анамнеза оперативных вмешательств на брюшной полости (при отсутствии спаек) для верификации причины кишечной непроходимости и для обеспечения визуализации места обструкции при применении минилапоротомного доступа при интестинотомии [143,144,145].
(УУР – С, УДД – 4).
Исследование слуха
Рекомендуется проведение тональной пороговой аудиометрии при субъективном снижении слуха и/или появлении ушного шума; пациентам, получающим регулярные или длительные курсы терапии аминогликозидами (системными); при уже выявленной сенсоневральной тугоухости в связи с риском развития сенсоневральной тугоухости на фоне применения системной антибактериальной терапии препаратами аминогликозидного ряда, обладающими ототоксичностью [2,21,146,147,148].
(УУР – С, УДД – 5).
Комментарий: тональная пороговая аудиометрия должна выполняться:
а) при субъективном снижении слуха и/или появлении ушного шума;
б) при проведении регулярных или длительных курсов терапии аминогликозидами (системными) (при старте и ежегодно);
в) при уже выявленной сенсоневральной тугоухости не реже 1 раза в год. Для детей младше 4-7 лет (в зависимости от способности к кооперации во время субъективного исследования слуха) альтернативными объективными методами являются регистрация вызванной отоакустической эмиссии и/или регистрация коротколатентных слуховых вызванных потенциалов, ASSR-тест.
Инструментальная оценка оценка состава тела
Рекомендовано селективное (при возможности) Определение процентного соотношения воды, мышечной и жировой ткани с помощью биоимпедансметра в комплексной оценке нутритивного статуса у пациентов с МВ [424].
(УУР – С, УДД – 5).
Комментарий: метод является неинвазивным и простым методом, который можно рассматривать для оценки состава тела у пациентов с МВ, проводиться при диагностике и в процессе динамического наблюдения (частота определяется индивидуально).
Предпочтительным является использование специальных уравнений прогнозирования или использование необработанных значений для сопротивления и реактивного сопротивления.
При невозможности использования определения процентного соотношения воды, мышечной и жировой ткани с помощью биоимпедансметра – следует применять оценку окружности плеча (см. рекомендации по недостаточности питания) [424].
Дифференциальный диагноз
Наиболее частые нозологические формы для дифференциального диагноза при МВ:
o врожденные аномалии бронхиального дерева (Компьютерная томография органов грудной полости, трахеобронхоскопия);
o туберкулезная инфекция (прием (осмотр, консультация) врача-фтизиатра, внутрикожная проба с туберкулезным аллергеном при необходимости – Исследование уровня интерферона-гамма на антигены Mycobacterium tuberculosis complex в крови);
o иммунодефицитное состояние (необходим прием (осмотр, консультация) врача-иммунолога (аллерголога-иммунолога), определение уровней иммуноглобулинов основных классов (G, M, A, Е) (Исследование уровня иммуноглобулинов в крови), а также, по показаниям, иные обследования для подтверждения/исключения иммунодефицитного состояния;
o первичная цилиарная дискинезия (ПЦД) – респираторные симптомы, сходные с муковисцидозом, при отсутствии частого обильного стула с примесью жира и зловонным запахом, «соленого» привкуса кожных покровов могут наблюдаться у пациентов с первичной цилиарной дискинезией. Характерные клинические проявления: хронический бронхит, бронхоэктазы (у части пациентов), хронический синусит, хронический отит (триада Картагенера у половины пациентов первичной цилиарной дискинезией сопровождаются сходными клиническими проявлениями и обратным расположением внутренних органов), отсутствие движения или неадекватный паттерн движения ресничек мерцательного эпителия (при патолого-анатомическом исследовании биопсийного (операционного) материала тканей трахеи и бронхов (световая микроскопия/ высокоскоростной видео-микроскопический анализ) и/или патология строения ресничек (при патолого-анатомическом исследовании биопсийного (операционного) материала тканей нижних дыхательных путей с применением электронно-микроскопических методов (слизистой оболочки носа и/или бронха), генетическое исследование – секвенирование экзома или генома), как скрининг-метод может быть использовано определение уровня оксида азота в выдыхаемом назальном воздухе (у большинства пациентов с первичной цилиарной дискинезией – снижен, см. КР по оказанию медицинской помощи детям с первичной цилиарной дискинезией).
Дифференциальная диагностика мекониевого илеуса:
Болезнь Гиршпрунга, нейроинтестинальная дисплазия;
Внутриутробная инфекция, внутриутробный некротизирующий энтероколит новорожденного;
Внутриутробный перитонит, адгезивный перитонит;
Поражения нервного аппарата толстой кишки [149].
Консультации специалистов
Рекомендуется в ведении пациентов с муковисцидозом использовать мультидисциплинарный подход в виду того, что заболевание характеризуется поражением многих органов и систем, требует комплексной терапии, что диктует необходимость совместного ведения пациента специалистами разных профилей [2,21].
(УУР – С, УДД – 5).
Комментарии: пациентов с МВ наблюдает врач-пульмонолог (и/или, в детской практике, врач-педиатр), иногда – врач-инфекционист, а также врач-генетик, необходимы приемы (осмотры, консультации):
-
врача-гастроэнтеролога (или врача-диетолога) для исключения гиперацидного состояния и его коррекции при отсутствии эффекта от ферментозаместительной терапии и (по показаниям) при других патологических проявлениях со стороны желудочно-кишечного тракта,
врача-диетолога – для подбора диеты и ферментной терапии,
врача-оториноларинголога при обострении хронического синусита, диагностики или динамического наблюдения назального полипоза,
врача- сурдолога-оториноларинголога – при необходимости контроля слуховой функции у пациентов, получающих препараты, обладающие ототоксичностью,
врача-эндокринолога/врача-детского эндокринолога - при задержке роста, полового развития и нарушенииях углеводного обмена,
врача по лечебной физкультуре (или врача по медицинской реабилитации, или врача–физиотерапевта или специалиста с высшим (немедицинским) образованием (инструктор–методист по лечебной физкультуре; или специалиста со средним профессиональным (медицинским) образованием (инструктор по лечебной физкультуре, медицинская сестра по массажу, медицинская сестра по физиотерапии) - для обучения ингаляционной терапии, кинезитерапии, использованию дыхательных тренажеров,
врача–кардиолога (врача- детского кардиолога) при наличии легочной гипертензии (легочного сердца),
врача-уролога, врача-уролога-андролога детского, врача-акушера-гинеколога по поводу репродуктивной функции,
клинического фармаколога для решения сложных вопросов по терапии и предотвращению/лечению нежелательных явлений лекарственной терапии, консультации врача-фтизиатра при диагностике и терапии легочного микобактериоза,
врача-торакального хирурга/врача-хирурга/врача-детского хирурга, врача-анестезиолога-реаниматолога, при возникновении хирургической патологии,
врача-хирурга/врача-детского хирурга (со специализацией по трансплантологии) при наличии цирроза печени, показаний для трансплантации легких и постановки в лист ожидания трансплантации,
врача-офтальмолога при таргетной терапии,
врача-психиатра при таргетной терапии и при подозрении на депрессию, в т.ч., после выявления риска развития депрессии на основе анкетирования
и других специалистов по клинической необходимости.
Рекомендован пациентам мужского пола в возрасте с 15 лет прием (осмотр, консультация) врача-уролога/врача-уролога-андролога детского для оценки состояния репродуктивной системы и определения тактики дальнейшего наблюдения [98,104].
(УУР – С, УДД – 5).
Комментарии: алгоритм обследования и тактика решения вопроса репродукции у мужчин с МВ представлена в Приложении Б1.
Консультирование в процессе динамического наблюдения осуществляется по мере необходимости.
Рекомендовано пациентам мужского пола с муковисцидозом при гипоплазии тестикул, гипогонадизме – наблюдение и обследование у врача-эндокринолога или врача-уролога/ детского уролога-андролога (Прием (осмотр, консультация) врача-эндокринолога первичный и Прием (осмотр, консультация) врача-эндокринолога повторный/Прием (осмотр, консультация) врача-детского эндокринолога первичный и Прием (осмотр, консультация) врача-детского эндокринолога повторный, Прием (осмотр, консультация) врача-уролога первичный и Прием (осмотр, консультация) врача-уролога повторный/Прием (осмотр, консультация) врача-детского уролога-андролога первичный и Прием (осмотр, консультация) врача-детского уролога-андролога повторный ) для выявления признаков эндокринных, андрологических нарушений и решения вопроса о необходимости гормональной коррекции [98,99,104].
(УУР – С, УДД – 5).
Рекомендуются первичные консультации врачей и иных специалистов из медицинской организации или ее структурного подразделения, оказывающего паллиативную специализированную медицинскую помощь детям с кистозным фиброзом (муковисцидозом) (Прием (осмотр, консультация) врача по паллиативной медицинской помощи первичный/ Прием (осмотр, консультация) врача по паллиативной медицинской помощи повторный и др.), при наличии показаний, для определения объема необходимой паллиативной медицинской помощи [437].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Комментарии: консультация относительно паллиативной медицинской помощи может проводиться на всех этапах ведения пациента с муковисцидозом: во время принятия ключевых терапевтических решений, при возникновении жизнеугрожающих состояний, а также в терминальной фазе заболевания.
Рекомендуются повторные консультации врачей и иных специалистов из медицинской организации или ее структурного подразделения, оказывающего паллиативную специализированную медицинскую помощь детям с кистозным фиброзом (муковисцидозом) (Прием (осмотр, консультация) врача по паллиативной медицинской помощи первичный/ Прием (осмотр, консультация) врача по паллиативной медицинской помощи повторный и др.), при наличии показаний, для определения объема необходимой паллиативной медицинской помощи и оценки ее эффективности [437].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Цели лечения:
o Обеспечивать максимально высокое качество жизни пациента;
o Предупреждать и лечить обострения хронического инфекционно-воспалительного процесса в бронхолёгочной системе;
o Предупреждать и лечить обострения инфекционно-воспалительного процесса в околоносовых пазухах (ОНП) для уменьшения степени нисходящей контаминации бронхолегочной системы;
o Обеспечить физическое развитие пациента согласно возрастным нормам (достижение оказателей физического развития в границе 25-75 перцентиль после коррекции нутритивного статуса, рекомендуемая цель - 50 перцентиль);
o Обеспечить профилактику осложнений;
o Лечение осложнений (псевдо-Барттер синдром, мекониевый илеус, СДИО, МАСД (муковисцидоз-ассоциированный сахарный диабет) цирроз печени без\с синдромом портальной гипертензии, гиперспленизмом, ЖКБ (желчнокаменная болезнь), полипозный риносинусит, БЭН (белково-энергетическая недостаточность), кровохаркание, кровотечения легочные, кровотечения из ВРВП (варикозно расширенных вен пищевода) и верхней трети желудка.
Обязательные составляющие лечения:
o Диетотерапия;
o Заместительная терапия недостаточности экзокринной функции поджелудочной железы;
o Муколитическая терапия;
o Дренирование бронхиального дерева и лечебная физкультура;
o Антибактериальная терапия;
o Витаминотерапия;
o Терапия осложнений [1,2,5].
3.1 Консервативное лечение
3.1.1 Муколитическая терапия
Рекомендовано всем пациентам с МВ (за исключением имеющих медицинские противопоказания) проведение активной муколитической терапии с целью уменьшения вязкости мокроты и облегчения ее эвакуации [1,2,5,21].
(УУР – C, УДД – 5).
Комментарии: выбор лекарственных средств определяется индивидуально.
Выбор пути введения: предпочтение отдается ингаляционному введению муколитиков (АТХ Муколитические препараты).
Оценка эффективности лечения: клинически (оценка суточного количества мокроты, изменений ее консистенции, оценка степени дыхательной недостаточности).
Оценка безопасности лечения: клинически (специальных стандартизованных методик оценки безопасности этих лекарственных средств не существует, подбор осуществляется в присутствии врача-пульмонолога или врача-педиатра/врача-терапевта, специализирующегося на оказании медицинской помощи пациентам с муковисцидозом).
Дополнительные замечания: все способы разжижения мокроты необходимо комбинировать с удалением ее из дыхательных путей, используя методы кинезитерапии. Перед сеансом кинезитерапии желательно, а при наличии бронхообструкции – обязательно, перед ингаляциями муколитиков провести ингаляции бронхолитиков.
В клинической практике для муколитической терапии используются:
o Дорназа альфа** - разрывает водородные связи молекул ДНК, которые являются основной составляющей гнойной мокроты, и является базисной муколитической терапией, обеспечивает эффект в течение суток. Применяется ингаляционно в дозе 2,5 мг в сутки; при необходимости (распространенные бронхоэктазы- 5 мг в сутки (по 2,5 мг х 2 раза в день через небулайзер); хронический полипозный синусит - 5 мг в сутки (2,5 мг – через небулайзер, 2,5 мг - с использованием универсальной ингаляционной системы с функцией пульсирующей подачи аэрозоля по 1,25мг=1,25мл в каждый носовой ход) [1,2,21,150].
o 3% или 6 % или 7% гипертонический раствор натрия хлорида** с 0,01% и 0,1% натрием гиалуронатом (зарегистрирован как медицинское изделие - раствор для ингаляционной терапии с органическими веществами) применяется ингаляционно через небулайзер по 5 мл 2 раза в день, улучшает клиренс дыхательных путей и является базисной муколитической терапией с быстрым муколитическим эффектом [1,2,21,151,37,152,153,154,155,156,157,158,159,160,161], также может применяться 3% гипертонический раствор натрия хлорида**, особенно у детей младшего возраста [152].
o Маннитол** в форме порошка для ингаляций улучшает клиренс дыхательных путей, способствует гидратации слизи [2,21,162].
Маннитол** применяется в дозе 400 мг дважды в день через специальный ингалятор. Перед назначением маннитола** пациент должен пройти тест на бронхиальную гиперреактивность при назначении начальной дозы в соответствии с инструкцией к препарату. Противопоказан детям до 6 лет. Повышает комплаентность подростков [163].
Маннитол** и 3%, 6%, 7% гипертонический раствор натрия хлорида** с 0,001% и 0,1% натрием гиалуронатом являются муколитиками быстрого действия и сочетаются с дорназой альфа**.
Муколитическая терапия подбирается пациентам индивидуально специалистом, имеющим опыт ведения пациентов с муковисцидозом, амбулаторно на приеме врача или в стационаре при наличии показаний к госпитализации.
Согласно данным регистра пациентов с муковисцидозом в 2021 году [5] дорназу альфа** в РФ в виде воспроизведенного препарата получали 95% пациентов. Переносимость препаратов дорназы альфа** сопоставима [165,438,439,440,441].
По данным европейского регистра 2021 г. медиана назначения дорназы альфа** у пациентов 6 и старше лет 86,2%, назначение у детей младше 3 лет – в среднем 43,6%, у детей 3-5 лет – 69,2%, что свидетельствует о взаимозаменяемости муколитических средств, в частности, при нежелательных побочных реакциях (при замене дорназы альфа** используются 3%, 6%, 7% р-р натрия хлорида** с 0,01% и 0,1% натрия гиалуронатом или маннитол**) [166].
Показаниями к отмене дорназы альфа** для нижних дыхательных путей являются:
- наличие комплекса показателей на фоне таргетной терапии: нормализация функции хлорного CFTR канала при отсутствии грамотрицательной флоры, легочного микобактериоза, MRSA, бронхоэктазов и наличии нормальных показателей функции внешнего дыхания (Исследование неспровоцированных дыхательных объемов и потоков (спирометрия) с динамическим наблюдение в последующем
- нежелательные реакции , при этом дорназу альфа** заменяют на 3%, 6%, 7% р-р натрия хлорида** с 0,01% и 0,1% натрия гиалуронатом или маннитол**).
Основанием служат данные регистров разных стран, где дорназа альфа используется с меньшей частотой [442,443].
Показаниями к отмене дорназы альфа** с использованием универсальной ингаляционной системы с функцией пульсирующей подачи аэрозоля через носвые канюли на фоне таргетной терапии являются:
- отсутствие патологических изменений по данным спиральной компьютерной томографии придаточных пазух носа (КТ ОНП) через год от старта терапии при условии организации динамического наблюдения со стороны врача-оториноларинголога в последующем [167].
3.1.2 Бронхолитическая терапия
Рекомендовано назначение ингаляционной бронхолитической терапии пациентам с МВ при наличии обратимой или частично обратимой бронхиальной обструкции (прирост уровня ОФВ1 после ингаляции препарата для лечения обструктивных заболеваний дыхательных путей (бронхолитика) >15%) с целью улучшения эвакуации мокроты, перед применением ингаляцией противомикробных препаратов системного действия (ингаляционных), гипертонического раствора натрия хлорида**, перед кинезитерапией (Дыхательные упражнения дренирующие) [1,2,5,21].
(УУР – C, УДД – 5).
Комментарий: противопоказанием является индивидуальная непереносимость.
Рекомендуется пациентам с МВ в качестве бронхолитической терапии назначить бронхолитический препарат из групп: селективные β2-адреномиметики или адренергические средства в комбинации с антихолинергическими или антихолинергические средства либо другой препарат для лечения обструктивных заболеваний дыхательных путей по индивидуальным показаниям в режиме «по требованию» [1,2,21,164,168,169,170].
(УУР – B, УДД – 2).
Комментарий: в режиме «по требованию» используется селективный бета-2-адреномиметик сальбутамол** в монотерапии или в сочетании с ипратропия бромидом** или фиксированная комбинация фенотерол + ипратропия бромид** или тиотропия бромид** либо другой препарат для лечения обструктивных заболеваний дыхательных путей по индивидуальным показаниям.
Использование дозированных аэрозольных ингаляторов обязательно со спейсером, при назначении ингаляционных бронхолитиков (препаратов для лечения обструктивных заболеваний дыхательных путей) (селективный бета-2-адреномиметик сальбутамол** в монотерапии или в сочетании с М-холинергническими препаратами (ипратропия бромид**) или фиксированная комбинация фенотерол + ипратропия бромид** или препараты пролонгированного действия (тиотропия бромид**) либо другого препарата для лечения обструктивных заболеваний дыхательных путей по индивидуальным показаниям) пациентам с тяжелой бронхообструкцией (ОФВ1 <30% от должного) ингаляции должны проводиться при помощи небулайзера.
Выбор пути введения препарата для лечения обструктивных заболеваний дыхательных путей: предпочтение отдается ингаляционному пути введения.
Оценка эффективности лечения: клинически (симптомы бронхообструкции) и по данным спирометрии.
Оценка безопасности лечения: клинически и по результатам объективного осмотра (число сердечных сокращений, сердечный ритм).
Применение препаратов вне зарегистрированных в инструкции лекарственного средства показаний осуществляется по решению врачебной комиссии, с разрешения Локального этического комитета медицинской организации (при наличии), с условием подписанного информированного согласия родителей (законного представителя) и ребенка в возрасте старше 15 лет.
3.1.3 Антибактериальная терапия (АБТ)
3.1.3.1 Общие принципы антибактериальной терапии
Рекомендована антибактериальная терапия (плановые курсы АБП в виде ингаляций через небулайзер или совместно с таблетированными формами, или внутривенно) всем пациентам с легочными проявлениями МВ, у которых отмечается обострение МВ (включая обострения на фоне острой респираторной инфекции) или выявляются новые патогенные возбудители респираторной инфекции в количестве более 105 колониеобразующих единиц при плановом микробиологическом исследовании (Микробиологическое (культуральное) исследование мокроты на аэробные и факультативно-анаэробные микроорганизмы, Определение чувствительности к антибактериальным препаратам микроорганизмов, выделенных из мокроты, Определение чувствительности к противогрибковым препаратам грибов, выделенных из мокроты) с целью эрадикации причиннозначимых микроорганизмов [2,5,21,171,172,173,174].
(УУР – В, УДД – 2).
Комментарий: для грамотрицательной микрофлоры (P. aeruginosa, В. cepacia complex, Stenotrophomonas maltophilia, Achromobacter spp), MRSA, нетуберкулезных микобактерий или при их хроническом высеве значение имеет любое количество колоний, определенное по результатам микробиологического исследования.
При проведении антибактериальной терапии (АБТ) пациентам с муковисцидозом рекомендовано ориентироваться на чувствительность выделенного из бронхолегочной системы микроорганизма (Pseudomonas aeruginosa, MRSA, Burkholderia cepacia complex, Stenotrophomonas maltophilia, Staphylococcus aureus и Haemophilus infuenzae и др.) к антибактериальным препаратам с целью повышения эффективности лечения [2].
(УУР – C, УДД – 5).
Комментарии: лабораторное определение чувствительности микроорганизма к антибиотикам (Определение чувствительности микроорганизмов к антимикробным химиотерапевтическим препаратам) не всегда полностью совпадает с клиническим ответом на проводимую терапию [2,5,21,172,173,174].
При выборе противомикробного препарата системного действия целесообразно учесть эффективность ранее проводимых курсов антибактериальной терапии [2].
Пациентам с МВ назначают максимальные возрастные дозы препаратов или дозы, рекомендуемые для пациентов с МВ. В связи с тяжестью заболевания, необходимостью максимальных дозировок антимикробных препаратов и дефицитом лекарственных форм для ингаляционного применения в мировой клинической практике традиционно применяются off-label (вне инструкции) противомикробные препараты системного действия (инъекционные) в виде ингаляций [89,175,176,177,178,179,180,181,182,183].
o Противопоказания: определяются индивидуально и зависят от индивидуальной непереносимости (в том числе аллергии), характера сопутствующих заболеваний (главным образом заболевания печени и почек) и возраста пациента.
o Выбор лекарственных средств определяется: видом возбудителя, выявленного у пациента; чувствительностью возбудителя (in vitro) к данному АБП; фазой заболевания (обострения – ремиссия); продолжительностью инфекционного процесса (хроническая инфекция – впервые выявленный возбудитель); эффективностью терапии предшествующего обострения легочной инфекции (данные о природной резистентности основных патогенов, характерных для пациентов с МВ представлен в Приложении А3.4).
o Выбор пути введения определяется: видом возбудителя, выявленного у пациента; фазой заболевания (обострение – ремиссия); продолжительностью инфекционного процесса (хроническая инфекция – впервые выявленный возбудитель); местом оказания медицинской помощи (амбулаторная – стационарная); эффективностью предшествующей антибактериальной терапии. Внутривенное введение антибиотиков начинается в стационаре с курсом лечения 14-21 день. Введение осуществляется через периферический венозный катетер (катетер периферический) или через порт-систему (порт инфузионный/инъекционный, имплантируемый***), которые устанавливаются согласно методическим руководствам «Венозный доступ, 2019 (https://msestra.ru/download/file.php?id=4763) с использованием необходимых лекарственных средств. Порт-системы устанавливаются согласно Распоряжению Правительства Российской Федерации от 31.12.2018 г.№ 3053-р «Об утверждении перечня медицинских изделий, имплантируемых в организм человека при оказании медицинской помощи в рамках программы государственных гарантий бесплатного оказания гражданам медицинской помощи, а также перечня медицинских изделий, отпускаемых по рецептам на медицинские изделия при предоставлении набора социальных услуг». По показаниям до постановки, в процессе использования и после снятия порт-системы (порта инфузионного/инъекционного, имплантируемого***) может проводиться дуплексное сканирование артерий верхних конечностей, дуплексное сканирование вен верхних конечностей Лечение может проводиться в стационаре и в амбулаторных условиях. Внутримышечный путь введения при муковисцидозе применяться не должен в связи с необходимостью длительных частых курсов терапии, так как при МВ имеются особенности в фармакокинетике АМГ, β-лактамных антибиотиков, выражающиеся в увеличении объема распределения на килограмм массы тела и снижении периода полувыведения. Увеличение системного клиренса за счет ускорения метаболизма в печени и увеличение почечного клиренса определяют необходимость применения высоких доз антибиотиков с более частым их введением [2,21,176,184,185,186,187].
o Безопасность: в связи с применением у пациентов с муковисцидозом высоких доз, длительных курсов и комбинаций антибактериальных препаратов, одновременной терапии лекарственными препаратами разных групп, а также в связи с возможным нарушением функции печени, следует осуществлять соответствующие контролирующие мероприятия (клинические, лабораторные, инструментальные) для мониторирования возможных нежелательных эффектов лекарственных препаратов, их предупреждения и, при необходимости, терапии [2,189].
При острой респираторной инфекции пациентам с муковисцидозом рекомендовано назначение антибактериальной терапии в домашних условиях согласно профилю чувствительности выделенной респираторной микрофлоры в сязи с активацией хронического воспалительного процесса на фоне присоединения острой респираторной инфекции [2,21,89].
(УУР – С, УДД – 5).
Оценка эффективности АБТ: клинически (лихорадка, респираторные симптомы), по данным лабораторных методов обследования (лейкоцитоз, уровень С-реактивного белка, по показаниям - прокальцитонина (исследование уровня прокальцитонина в крови)) и по данным микробиологического исследования (микробиологическое (культуральное) исследование слизи с миндалин и задней стенки глотки на аэробные и факультативно-анаэробные микроорганизмы, микробиологическое (культуральное) исследование мокроты на аэробные и факультативно-анаэробные микроорганизмы, Микробиологическое (культуральное) исследование лаважной жидкости на аэробные и факультативно-анаэробные микроорганизмы, Определение чувствительности к антимикробным препаратам микроорганизмов, выделенных из бронхоальвеолярной лаважной жидкости, Определение чувствительности к противогрибковым препаратам грибов, выделенных из бронхоальвеолярной лаважной жидкости, Определение чувствительности к антибактериальным препаратам микроорганизмов, выделенных из мокроты, Определение чувствительности к противогрибковым препаратам грибов, выделенных из мокроты) (эрадикация возбудителя, персистирование, суперинфекция, снижение выделения возбудителя <104 колониеобразующих единиц или отрицательный результат посева и т.д.).
Оценка безопасности лечения: зависит от применяемого лекарственного средства (ЛС) и проводится с учетом возможных нежелательных явлений.
Дополнительные замечания:
1. При назначении АБП следует использовать комбинации ЛС с различным механизмом действия (например, Бета-лактамные антибактериальные препараты, пенициллины/Другие бета-лактамные антибактериальные препаратыв комбинации с аминогликозидами). При выделении в мокроте пациента одновременно двух микроорганизмов выбор АБП зависит от свойств более резистентного возбудителя.
2. Одновременное назначение препаратов для ингаляционного и внутривенного путей введения одной фармакологической группы не рекомендуется. Возможно назначение ингаляционной и внутривенной АБТ одновременно по решению консилиума специалистов и с учетом фармакологической группы препаратов.
3. Применение АБП в виде ингаляций через небулайзер:
- может проводиться как в стационаре, так и в домашних условиях;
- для решения вопроса о назначении ингаляционной терапии следует провести спирометрию до первой ингаляции противомикробного препарата системного действия (ингаляционно) и через несколько минут после ингаляции (для выявления возможного бронхоспазма (при отсутствии возрастных и/или иных противопоказаний)) (см. раздел «Бронхолитическая терапия») - перед ингаляцией АБП необходимо провести ингаляцию бронхолитика (препарата для лечения обструктивных заболеваний дыхательных путей). Симпатомиметики для ингаляционного применения, например, сальбутамол** 2,5 мг через небулайзер (или дозированный аэрозольный ингалятор по 200 – 400 мкг с использованием спейсера) за 15-30 минут до ингаляции антибиотика в монотерапии или в сочетании с ипратропия бромидом** или фиксированная комбинация фенотерол + ипратропия бромид** или тиотропия бромид**) или другие препараты для лечения обструктивных заболеваний дыхательных путей, муколититические препараты, а также дренаж (дыхательные упражнения дренирующие);
- при ингаляции АБП в домашних условиях желательно использовать небулайзер, оснащенный фильтром для выдыхаемого воздуха;
- при ингаляции АБП предпочтительнее применять мундштук, по сравнению с маской. Следует рекомендовать пациентам переходить на применение мундштука в максимально ранние сроки, как правило, с 3-х летнего возраста [190]. Вдыхание препарата лучше осуществлять через рот, применение носовых зажимов во время ингаляции увеличивает эффективность лечения;
- при проведении ингаляций в условиях медицинской организации и амбулаторно пациенты с МВ, должны пользоваться индивидуальным небулайзером с возможностью замены каждые 3 месяца комплекта распылителя и трубки воздуховода и фильтра;
- оптимальной для пациента с МВ является ингаляционная система с низкопоточным компрессором (уровень потока сжатого воздуха до 6 л/мин.), с производительностью 0,15 мл-0,25 мл/мин., снабженная системой контроля инспираторного потока и системой клапанов вдоха и выдоха, позволяющей сократить потери медикамента в окружающую среду, обеспечивающий максимальную эффективность терапии, приспособленный к химической и термической дезинфекции и к автоклавированию;
- для введения медикамента в ОНП применяется ингаляционная система с функцией пульсирующей подачи аэрозоля;
- в качестве мобильного устройства возможно использование мэш-небулайзера - ингаляционного прибора, состоящего из блока управления и аэрозольного модуля, включающего в себя резервуар для медикамента, аэрозольную головку, спейсер\накопитель, оснащенный системой клапанов вдоха и выдоха и мундштуком. Скорость распыления в диапазоне 0,3-0,7 мл\мин., с нераспыляемым (остаточным) объемом не более 0,5 мл. Все части аэрозольного модуля должны подлежать термической дезинфекции. Для пациента с МВ важно производить замену компонентов мэш-небулайзера каждые 3 месяца [191].
4. Применение АБП внутрь используется для терапии обострений МВ (включая обострения на фоне ОРИ) в домашних условиях или для профилактического лечения пациентов, хронически инфицированных P. aeruginosa, В. cepacia comрlex, MRSA, Achromobacter spp., НТМБ.
5. Применение АБП внутривенно показано:
- при тяжелых обострениях МВ (лечение в условиях медицинской организации) (не менее, чем двумя препаратами);
- в тех случаях, когда применение АБП внутрь и ингаляционно оказалось неэффективным;
- для плановой терапии пациентов, инфицированных P. aeruginosa, В. cepacia comрlex, MRSA, Achromobacter spp., нетуберкулезными микобактериями;
- при ухудшении течения заболевания и появлении новых симптомов у пациентов, получающих АБП внутрь.
6. Организация внутривенной терапии в амбулаторных условиях способствует повышению комплаентности, профилактике обострений. Пребывание в больнице отягощается риском перекрестного и суперинфицирования резистентными к противомикробным препаратам системного действия штаммами микроорганизмов, стрессом, пропуском школьных занятий. Кроме того, пребывание пациента в стационаре значительно дороже, чем амбулаторное лечение. Катетеризация вен давно стала рутинной медицинской процедурой в мире для обеспечения различных видов внутривенной терапии. Проведение внутривенной терапии через периферический венозный катетер (катетер периферический) или порт-систему (порт инфузионный/инъекционный, имплантируемый***) является практически безопасным, если соблюдаются основные условия: метод должен стать постоянным и привычным в практике, должен быть обеспечен безупречный уход за катетером. Катетер устанавливается в условиях дневного стационара или выездной бригадой на дому [2,192,193,194,195].
Профиль пациента, которому может проводиться внутривенная антибактериальная терапия в домашних условиях
1. Опыт ранее проводимой внутривенной антибактериальной терапии в условиях стационара.
2. Пациент, нуждающийся в проведении планового курса антибактериальной терапии, или имеющий обострение хронического бронхолегочного процесса, не требующий круглосуточного наблюдения медицинским специалистом, в том числе пациенты с тяжелым течением заболевания в стабильном состоянии, получающие на дому кислородотерапию (обеспечены концентратором кислорода, аппаратурой для неинвазивной вентиляции легких).
3. Положительное отношение пациента и членов семьи к проведению внутривенной антибактериальной терапии, отсутствие неврологических и психогенных нарушений, которые могут препятствовать безопасному проведению лечения в домашних условиях.
Условия, необходимые для начала терапии в домашних условиях:
1. Удовлетворительные санитарные условия проживания семьи.
2. Способность пациента или его родственников к обучению правилам ухода за катетером/порт-системой, прохождение обучения практическим навыкам.
3. Комплаентность семьи по выполнению рекомендации врача за предыдущий период наблюдения.
4. Предварительный осмотр специалистом по муковисцидозу в условиях медицинского учреждения, первое введение антибактериального препарата/препаратов в ЛПУ (стационар одного дня, дневной стационар), оценка переносимости терапии, за исключением случаев, когда уже имеется опыт применения конкретного лекарственного препарата.
5. Подписание информированного согласия пациентом/законными представителями
(подробная информация – в методических рекомендациях «Организация внутривенной терапии пациентам с муковисцидозом в амбулаторных условиях».
3.1.3.2 Антибактериальная терапия при высеве метициллинчувствительного Staphylococcus aureus (MSSA) и Haemophilus influenzae
Рекомендовано при выборе антибактериальных препаратов системного действия для терапии пациентов с муковисцидозом с высевом Staphylococcus aureus и Haemophilus influenzae применять ЛС в соответствии с чувствительностью с целью эрадикации причиннозначимого возбудителя (препараты, дозировки и кратность введения, представлены в таблицах 10,11) [2].
(УУР – C, УДД – 5).
Таблица 10. Антибактериальные препараты, применяемые у пациентов с муковисцидозом, при высеве из мокроты/ бронхиального секрета Staphylococcus aureus (MSSA)
Антибактериальный препарат |
Суточные дозы для детей |
Суточные дозы для взрослых |
Способ введения |
Кратность введения |
|---|---|---|---|---|
Амоксициллин + [Клавулановая кислота1]** (суспензия для приема внутрь – противопоказана детям до 3 месяцев, таблетки диспергируемые противопоказаны детям по 2 лет, таблетки, покрытые пленочной оболочкой противопоказаны детям до 12 лет и с массой тела менее 40 кг) |
60-90 мг/кг (расчет по амоксициллину)
|
1,5-2 г (расчет по амоксициллину)
|
Внутрь |
2-32 |
90-120 мг/кг |
3,6-4,8 г |
В/в |
3-4 |
|
Оксациллин** |
200-300 мг/кг |
4-12 г |
В/в |
4-6 |
Цефалексин** (капсулы 250 мг противопоказаны детям до 10 лет, таблетки 250 мг – противопоказаны детям до 7 лет) |
25-50-100 мг/кг |
2-4 г |
Внутрь |
3-4 |
Цефазолин** |
100-150 мг/кг |
4-6 г |
В/в |
2-3 |
|
Цефуроксим** (суспензия для приема внутрь – противопоказана детям до 3 мес., таблетки – противопоказаны детям до 3 лет) |
20 -30 мг/кг |
0,5 – 1 г |
Внутрь |
2 |
150-200 мг/кг |
3–9 г |
В/в |
3-4 |
|
|
Цефтриаксон** |
50-80 мг/кг |
4 г |
В/в |
1-2 |
|
Цефепим** (противопоказан детям до 2 мес. жизни) |
100–150 мг/кг |
4-6 г |
В/в |
2-3 |
|
Азитромицин** (таблетки 125 мг – противопоказаны до 3 лет, суспензия для приема внутрь – противопоказана детям до 6 мес.) |
>6 мес.-10 мг/кг |
500 мг |
Внутрь |
1 Курс 7-10 дней |
|
Кларитромицин** (таблетки – противопоказаны детям до 12 лет) |
15 мг/кг |
1 г |
Внутрь |
2 |
|
Джозамицин** (противопоказание - при массе тела более 10 кг) |
40–50 мг/кг |
1-3 г |
Внутрь |
2-3 |
|
Клиндамицин** (р-р для в/в и в/м введения противопоказан детям до 3 лет, капсулы противопоказаны детям до 8 лет с массой тела до 25 кг) |
20-40 мг/кг |
1,8-2,4 г |
Внутрь |
3-4 |
Детям старше 3х лет 40 мг/кг |
2,4-2,7 г |
В/в |
3-4 |
|
|
Доксициклин** (противопоказан детям до 8 лет) |
Детям с массой тела менее 45 кг в первый день лечения 4 мг/кг, в последующие дни - 2-4 мг/кг. Детям с массой тела более 45 кг - как взрослым |
1 день-200 мг затем 100 мг один раз в сутки |
Внутрь |
1- 2 |
|
Ко-тримоксазол [Сульфаметоксазол + Триметоприм]** (суспензия для приема внутрь – противопоказана детям до 6 недель, таблетки противопоказаны детям до 3 лет, раствор для инфузий противопоказан детям до 3 лет) |
6-10 мг/кг по триметоприму при тяжелой инфекции возможно увеличение дозы на 50% |
320 мг по триметоприму |
Внутрь В/в |
2 |
Тиамфеникола глицинат ацетилцистеинат |
250 мг (в первые 2-3 дня лечения доза может быть увеличена в 2 раза) |
500 мг (в первые 2-3 дня лечения доза может быть увеличена в 2 раза) |
Ингаляции |
2 |
Примечание: 1 - При расчёте дозы Амоксициллин + [Клавулановая кислота]** следует ограничивать количество клавулановой кислоты до ≤ 10 мг/кг/сут во избежание побочных эффектов со стороны ЖКТ и подбирать формы с меньшим относительным содержанием клавулановой кислоты [513,514].
2- в возрасте с 2 до 5 лет назначается 3 раза в день [196,197,198,199].
Таблица 11. Антибактериальные препараты, применяемые у пациентов с муковисцидозом, при высеве из мокроты/бронхиального секрета Haemophilus influenzae
Антибиотик |
Суточные дозы для детей |
Суточные дозы для взрослых |
Способ введения |
Кратность введения |
|---|---|---|---|---|
|
Амоксициллин**
|
60-90 мг/кг |
1,5-2 г |
Внутрь |
2-31 |
|
Амоксициллин + [Клавулановая кислота2]** (суспензия для приема внутрь – противопоказана детям до 3 месяцев, таблетки диспергируемые противопоказаны детям по 2 лет, таблетки, покрытые пленочной оболочкой противопоказаны детям до 12 лет и с массой тела менее 40 кг) |
60-90 мг/кг (расчет по амоксициллину) |
1,5-2 г (расчет по амоксициллину) |
Внутрь |
2-3 |
90-120 мг/кг |
3,6-4,8 |
В/в |
3-4 |
|
|
Цефуроксим** (суспензия для приема внутрь – противопоказана детям до 3 мес., таблетки – противопоказаны детям до 3 лет) |
20 -30 мг/кг |
0,5 – 1 г |
Внутрь |
2 |
150- 200 мг/кг |
3–9 г |
В/в |
3-4 |
|
|
Цефиксим (суспензия для приема внутрь – противопоказана детям до 6 месяцев, таблетки диспергируемые противопоказаны детям с массой тела до 25 кг, таблетки, покрытые пленочной оболочкой и капсулы противопоказаны детям до 12 лет) |
8 мг/кг |
400 мг |
Внутрь |
1-2 |
|
Цефтриаксон**
|
50-80 мг/кг |
4 г |
В/в |
1-2 |
|
Цефотаксим**
|
100-150 мг/кг |
2-8 г |
В/в |
2-4 |
|
Цефепим** (противопоказан детям до 2 мес. жизни) |
Дети с массой тела˂40 кг 100–150 мг/кг; Детям с массой тела ˃40 кг – 4-6 г– |
4-6 г |
В/в |
2-3 |
|
Доксициклин** (противопоказан детям до 8 лет)
|
Дети с массой тела до 45 кг в первый день - 4 мг/кг, в последующие дни - 2-4 мг/кг. Детям с массой тела более 45 кг - как взрослым |
1 день-200 мг затем 100 мг один раз в сутки |
Внутрь |
1- 2 |
Тиамфеникола глицинат ацетилцистеинат |
500 -1000 мг |
1000 мг |
Ингаляции |
2 |
Примечание: 1- в возрасте с 2 до 5 лет назначается 3 раза в день [196,197,198,199].
2 - При расчёте дозы Амоксициллин+[Клавулановая кислота]** следует ограничивать количество клавулановой кислоты до ≤ 10 мг/кг/сут во избежание побочных эффектов со стороны ЖКТ и подбирать формы с меньшим относительным содержанием клавулановой кислоты [513,514].
3.1.3.3 Антибактериальная терапия при MRSA (метициллинрезистентный стафилококк) - инфекции
При первичном высеве MRSA у стабильных пациентов (вне обострения хронического воспалительного процесса) в качестве первой линии терапии при отсутствии противопоказаний рекомендуется назначение двух антибактериальных препаратов per os в течение 14-21 дня, чаще это комбинация рифампицина** с ко-тримоксазолом [Сульфаметоксазол + Триметоприм]** или фузидовой кислотой (табл.12) [2,21,133].
(УУР – C, УДД – 5).
Комментарии:
o у пациентов старше 12 лет рифампицин** может сочетаться с доксициклином** (#миноциклином) для приёма per os (табл.12). Допускается монотерапия доксициклином** или Сульфаметоксазолом + Триметоприм** (табл.12) [6, 7]. Необходимо помнить о гепатотоксичности препаратов.
o Возможной альтернативой является использование #ванкомицина** в форме для инъекционного применения ингаляционно (применение вне зарегистрированных в инструкции лекарственного средства показаний осуществляется по решению врачебной комиссии, с разрешения Локального этического комитета медицинской организации (при наличии), с условием подписанного информированного согласия родителей (законного представителя) и пациента в возрасте старше 15 лет) в течение 3-4 недель [175,176,181,182,183,200,201] (табл. 12).
o С учетом знаний о местах возможной колонизации MRSA, параллельно, одновременно с началом эрадикационной терапии, необходима обработка кожи, полости носа и ротоглотки антисептиками, а также дезинфекция окружающей среды:
1) эндоназально мупироцин 2% 2 раза в день + обработка кожи водным раствором хлоргексидина** 0,5% в течение 5 дней;
3) полоскание полости рта 0,5% водным раствором хлоргексидина** в течение 2-х недель;
4) генеральная уборка жилого помещения;
5) ежедневная смена нательного белья в течение 5 дней;
6) стирка постельных принадлежностей, белья, полотенец в режиме высокой температуры еженедельно в течение всего периода лечения;
7) после инициации лечения необходима смена зубных щеток, расчесок, шариковых дезодорантов, губной помады;
8) все члены семьи, а также домашние животные должны быть обследованы и, в случае идентификации MRSA, санированы.
При первичном высеве MRSA у нестабильных пациентов (при обострении хронического воспалительного процесса), рекомендуется проведение внутривенной или пероральной терапии в течение 2-х недель линезолидом** или тейкопланином, прочими антибактериальными препаратами системного действия, активными в отношении MRSA (табл.12) [2,176,200,201,202].
(УУР – C, УДД – 5).
Комментарии: у пациентов с частыми обострениями при хроническом инфицировании MRSA возможно использование ингаляций #ванкомицина** в форме для инъекционного применения в непрерывном или курсовом режиме (табл.12) [200,201]. При первом высеве MRSA на фоне проводимой таргетной терапии в качестве препарата первой динии следует использовать линезолид внутрь в течение 14 дней [133].
Таблица 12. Антибактериальные препараты системного действия, применяемые у пациентов с муковисцидозом, при высеве из мокроты/бронхиального секрета метициллинрезистентного Staphylococcus aureus (MRSA)1.
Антибактериальный препарат |
Суточная доза для Детей |
Суточная доза для взрослых |
Способ Введения |
Кратность введения |
|---|
Пациентам с МВ рекомендуется проведение индивидуально подобранных реабилитационных мероприятий, нацеленных на поддержание легочной функции.
Способов первичной профилактики МВ – не существует. В качестве мер вторичной профилактики этого заболевания выступают:
1) дородовая диагностика и
2) неонатальная диагностика МВ.
Рекомендуется всем пациентам с муковисцидозом, планирующим деторождение, прием (осмотр, консультация) врача-генетика и молекулярно-генетическое обследование супруги/супруга на носительство мутаций гена CFTR (Молекулярно-генетическое исследование мутаций в гене CFTR (муковисцидоз) в крови). В случае обнаружения патогенных вариантов рекомендуется преимплантационное генетическое тестирование (ПГТ-М) на МВ (Преимплантационная генетическая диагностика эмбриона) [2,101,130,355].
(УУР – C, УДД – 5).
Профилактика Псевдо-Барттер синдрома
Рекомендованы следующие меры для профилактики Псевдо-Барттер синдрома:
o Своевременная диагностика муковисцидоза;
o Информирование родителей о симптомах ПБС;
o Контроль уровня электролитов крови особенно у детей раннего возраста;
o Профилактическое назначение натрия из расчета 1-2 ммоль/кг/сут. в виде поваренной соли (1/5-1/6 чайной ложки примерно соответствует 15 ммоль NaCl), солевых растворов, предназначенных для пероральной регидратации [2].
(УУР – C, УДД – 5).
Вакцинация
Известно, что дети с муковисцидозом являются группой риска по развитию инфекционных заболеваний и носительства таких микроорганизмов, как S. aureus, H. influenzae, S. pneumoniae, мукоидных и немукоидных форм P. aeruginosa и Burkholderia cepacia complex. Высока распространенность среди этих детей сопутствующей хронической патологии, усугубляющей тяжесть течения инфекции и предрасполагающей к возникновению различных осложнений. Профилактика инфекций у пациентов с МВ должна осуществляться не эпизодически, а путем планомерного выполнения мероприятий, предупреждающих распространение инфекции, а также мер, повышающих общую и специфическую сопротивляемость организма. Эффективным средством в предупреждении инфекционной заболеваемости является вакцинопрофилактика.
Рекомендовано проведение вакцинации согласно национальному календарю прививок и календарю профилактических прививок по эпидемическим показаниям. Вакцинировать детей рекомендуется в фазу ремиссии, на фоне стабильного соматического состояния и проводимой терапии [365,366,367,368].
(УУР – C, УДД – 5).
Комментарий: противопоказания: индивидуальная непереносимость.
- Пациенты с хроническим гепатитом, в т.ч. с начинающимся циррозом печени могут быть вакцинированы в периоде ремиссии или низкой активности заболевания на фоне выраженного снижения уровня трансаминаз до максимально достижимых величин [367].
- Терапия кортикостероидами для системного применения приводит к выраженной иммуносупрессии лишь при использовании высоких доз (преднизолон** ≥2 мг/кг/сут. или 20 мг/сут. для ребенка весом >10 кг) в течение 14 дней и более. Таким детям убитые вакцины вводятся в обычные сроки, живые вакцины вводят не ранее, чем через 1 месяц от окончания лечения. Как живые, так и инактивированные вакцины вводят в обычном порядке лицам, получающим стероидные препараты: кратковременно (до 1 недели) любые дозы; курсами длительностью до 2 недель низкие или средние (до 1 мг/кг преднизолона**) дозы; длительно поддерживающие дозы (например, 5-10 мг преднизолона** через день); в качестве заместительной терапии низкие (физиологические) дозы; местно: накожно, ингаляционно, в виде глазных капель, внутрь сустава [367].
- Пациентам, которым планируется проведение трансплантации органов (печень, легкие), следует провести вакцинацию до проведения операции, в связи с дальнейшим применением цитостатической терапии по общепринятым при трансплантации органов рекомендациям [365,367,369].
При возможности, следует при ревакцинации против дифтерии и столбняка дополнительно защищать пациентов с МВ от коклюша - использовать вакцину для профилактики дифтерии (с уменьшенным содержанием антигена), коклюша (с уменьшенным содержанием антигена, бесклеточной) и столбняка, адсорбированную**. Коклюшная инфекция может выступать триггером обострения и утяжеления состояния пациентов с МВ [506], кроме того, есть сообщения, что вакцинация и ревакцинация против коклюша оказывает протективное действие против инфекции, вызванной Bordetella bronchiseptica, риску которой особо подвержены пациенты с МВ, имеющие домашних животных [507].
Рекомендована вакцинация пациентов с МВ против пневмококковой инфекции с целью предотвращения инфекций, вызванных S.pneumoniae [365,367,369,370,371,372,373,374,375].
(УУР – C, УДД – 5).
Комментарий: для вакцинации детей до 2 лет используется Пневмококковая конъюгированная вакцина (ПКВ – 13). Схема зависит от возраста начала иммунизации. Вакцинация проводится согласно инструкции к препарату.
У детей старше 2 лет, возможно применение Пневмококковой полисахаридной вакцины (ППВ – 23) однократно, с повторным введением через 3-5 лет.
Вакцинация взрослых проводится при отсутствии иммунизации против пневмококковой инфекции ПКВ – 13, затем через 12 месяцев вводится ППВ – 23 с ревакцинацией через 4-5 лет. При уже имеющейся прежней вакцинации против пневмококковой инфекции вводится ППВ – 23, однократно, с ревакцинацией через 4-5 лет [372].
Рекомендована вакцинация против гриппа с целью предотвращения сезонного гриппа и, соответственно, обострения хронического воспалительного процесса в легких и ОНП у пациентов с МВ [369,374,376,377,378].
(УУР – C, УДД – 5).
Комментарий: вакцинация против гриппа всех возрастных групп проводится 3 и 4 валентными инактивированными вакцинами 1 раз в год, осенью, до начала эпидемии гриппа. Детям дошкольного возраста, которые первый раз начали вакцинироваться против гриппа, необходимо введение двух доз по 0,25 мл с интервалом 4 недели.
При этом в настоящее время недостаточно рандомизированных исследований, доказывающих эффективность вакцинации против гриппа, что связано с небольшим количеством проведенных исследований и низким их качеством. Есть необходимость в проведении исследований более высокого качества [378].
Рекомендована вакцинация против гемофильной инфекции типа b с целью предотвращения инфекций, вызванных H. influenzae [369,375,379,380,381].
(УУР – C, УДД – 5).
Комментарий: проводится моновакцинами или в составе комбинированных вакцин. Принимая во внимание важное клиническое значение инфекций, вызванных гемофильной палочкой типа b, вакцинация пациентов с МВ должна быть начата в максимально ранние сроки, предусмотренные национальным календарем прививок (с трехмесячного возраста), трехкратно с интервалом в 1,5 месяца; ревакцинация проводится через 12 месяцев после третьей прививки. При начале вакцинации в 6–12 месяцев жизни достаточно двух инъекций с интервалом 1–2 месяца и ревакцинации через 12 месяцев после второй дозы. После года вакцинируют однократно.
Рекомендована вакцинация против ветряной оспы с целью предотвращения данного заболевания и его осложнений [365,382].
(УУР – C, УДД – 5).
Комментарий: вакцинация детей осуществляется с 12-ти месяцев жизни согласно инструкции по применению препарата. Также показано проведение экстренной профилактики ветряной оспы контактных детей, не привитых в течение первых 72- 96 часов после контакта с заболевшим ветряной оспой.
Особое значение инфекция Varicella zoster имеет у пациентов после проведения трансплантации и получающих препараты группы кортикостероиды для системного применения, кроме того, описаны повреждения легких на фоне заболевания ветряной оспой в популяции взрослых людей.
Рекомендована вакцинация против менингококковой инфекции с целью предотвращения менингитов и его осложнений [383].
(УУР – C, УДД – 5).
Комментарий: допускается проведение полисахаридными и конъюгированными вакцинами у всех возрастных групп, зарегистрированными на территории РФ. Следует иметь в виду, что применение полисахаридных вакцин у детей до 2 лет может быть неэффективным. При наличии прежней вакцинации детей полисахаридной вакциной следует провести ревакцинацию конъюгированной вакциной через 12 месяцев. Вакцинация проводится согласно инструкции по применению препарата.
Рекомендована вакцинация против гепатита А и гепатита В с целью предотвращения данных заболеваний, учитывая наличие поражений печени в рамках основной патологии [365].
(УУР – C, УДД – 5).
Комментарий: вакцинация проводится согласно инструкции по применению препарата.
Рекомендована вакцинация против ротавирусной инфекции с профилактической целью [384].
(УУР – C, УДД – 5).
Комментарий: вакцинация проводится согласно инструкции по применению препарата.
Рекомендовано селективное по индивидуальным показаниям проведение пассивной иммунизации против респираторно-синцитиальной вирусной инфекции (РС) с целью предупреждения тяжелых форм острых бронхиолитов у детей с МВ [384,385,499].
(УУР – B, УДД – 2).
Комментарий: применяется детям первого года жизни. Ранее рекомендовалось применение препарата Паливизумаб** ― гуманизированные моноклональные антитела к белку слияния (белок F) РС – вируса, 1 раз в месяц перед началом эпидемического подъема РС-вирусной заболеваемости, который начинается в ноябре и продолжается до апреля (4−5 введений за эпидемический сезон). В настоящее время, в связи с отсутствием четкой сезонности РС-вирусной инфекции, преимущественным считается внесезонный подход с учетом эпидемиологического мониторинга (в дозе 15 мг/кг; курс – 5 инъекций с интервалом в один месяц вне зависимости от сезона) [386,387].
Рекомендована вакцинация против коронавирусной инфекции нового типа (COVID-19) взрослым пациентам с муковисцидозом с целью профилактики данной инфекции, предупреждения тяжелого течения и осложнений [389].
(УУР – С, УДД – 5).
Комментарий: проводится по эпидемиологическим показаниям. Противопоказания - согласно Инструкциям к соответствующим препаратам. Пациентам после трансплантации легких и/или печени может потребоваться бустерная доза для достижения необходимого эффекта [390].
Профилактика аспергиллеза
Рекомендовано принимать меры по минимизации вероятности инфицировани Aspergillus spp., в связи с тем, что данный патоген распространен повсеместно, постоянно присутствуют в воздухе внешней среды и внутри помещений, а полностью исключить контакт пациента с микромицетами невозможно. Цель вмешательства – предупреждение АБЛА и ХАЛ [2].
(УУР – C, УДД – 5).
Комментарии: пациенты с МВ не должны находиться в жилых и больничных помещениях, пораженных плесенью. Необходимо следить за соблюдением температурно-влажностного режима в помещениях, не допускать протечек, аварий, затоплений подвалов и т.п. В случае появления признаков плесени в помещениях необходимо перевести пациентов с МВ в другое помещение. Для ликвидации последствий появления плесени в зданиях необходимо выявить и устранить причину появления сырости в здании, провести просушку и обработку очагов биоповреждений строительными биоцидами, активными против грибов.
В квартирах пациентов с МВ, а также больничных помещениях и поликлиниках, не должно быть цветов в горшках, зимних садов и пр. В связи с тем, что большое количество спор грибов присутствует на частичках пыли, необходимо избегать контакта пациентов с МВ с пылью, тщательно проводить влажную уборку помещений.
Пациентам с МВ следует избегать мест с большой концентрацией спор грибов в окружающей среде – парки, сады, леса, места скопления разлагающихся органических веществ (компостные массы, гниющая древесина, трава), зернохранилища, строительные площадки, помещения с текущим ремонтом, не следует работать в таких сферах, как садоводство, земледелие, строительство, пребывать в специализированных помещениях (конюшни, курятники и т. д.).
Пациенты с МВ не должны использовать в пищу подгнившие или заплесневелые овощи, ягоды, фрукты, так как в процессе контакта возможна инспирация спор микромицетов, обсеменение кожи и одежды пациента.
При нарушении правил эксплуатации Aspergillus spp. могут поражать системы вентиляции, поэтому следует своевременно обслуживать и осуществлять замену фильтров кондиционеров.
Динамическое наблюдение носителей ГВНП CFTR
Рекомендовано при выявлении носителей патогенных вариантов CFTR их дальнейшее динамическое наблюдение в медицинских организациях, где оказывается помощь пациентам с МВ с проведением регулярного обследования и, при необходимости, лечения (табл. 35) [500].
(УУР – C, УДД – 5).
Комментарии:
Таблица 35. Рекомендации по наблюдению носителей вариантов гена CFTR [500]
Носитель |
Наблюдение |
Кратность обследований |
|---|---|---|
одного патогенного варианта гена CFTR, ассоциированного с панкреатитами1 |
- Определение активности амилазы в крови - Определение активности липазы в сыворотке крови - Ультразвуковое исследование органов брюшной полости (комплексное) - Прием (осмотр, консультация) врача-генетика первичный/ Прием (осмотр, консультация) врача-генетика повторный - Прием (осмотр, консультация) врача-гастроэнтеролога первичный/ Прием (осмотр, консультация) врача-гастроэнтеролога повторный - Обследование партнера при планировании беременности/семьи (Молекулярно-генетическое (панель на частые мутации, покрывающая не менее 98%)) |
1 раз в год, по показаниям - чаще |
одного патогенного варианта гена CFTR, ассоциированного с бесплодием у лиц мужского пола1 |
- Консультация репродуктолога - Прием (осмотр, консультация) врача-генетика первичный/ Прием (осмотр, консультация) врача-генетика повторный - Прием (осмотр, консультация) врача-уролога/прием (осмотр, консультация врача-детского уролога-андролога - Обследование партнера при планировании беременности/семьи (Молекулярно-генетическое (панель на частые мутации, покрывающая не менее 98%)) |
в возрасте 15 лет или ранее при достижении репродуктивного возраста |
|
одного патогенного варианта гена CFTR 2, 3 |
- Консультация врача-генетика - Обследование партнера при планировании беременности/семьи (Молекулярно-генетическое (панель на частые мутации, покрывающая не менее 98%)) |
при достижении репродуктивного возраста |
|
1 Согласно базе данных OMIM https://www.omim.org/ 2 Cогласно базе данных CFTR2 https://cftr2.org/ 3 Согласно базе CFTR France https://cftr.iurc.montp.inserm.fr | ||
Рекомендовано избегать табакокурения носителям патогенных вариантов гена CFTR вследствие того, что табачный дым снижает активность канала CFTR и носители МВ могут подвергаться более высокому риску его неблагоприятного влияния [421].
Комментарии: информированность о данном состоянии дает возможность избежать неблагоприятных факторов, влияющих на здоровье носителей.
Рекомендовано избегать избыточного употребления алкоголя носителям патогенных вариантов гена CFTR с целью профилактики панкреатита [421].
Комментарии: информированность о данном состоянии дает возможность избежать неблагоприятных факторов, влияющих на здоровье носителей.
Пациентам с МВ, в зависимости от необходимости, может быть оказана медицинская помощь любого вида, условия, формы, предусмотренных законодательством Российской Федерации.
При оказании медицинской помощи пациентам с муковисцидозом необходимо использовать мультидисциплинарный подход, что обусловлено как тяжестью состояния, так и поражением различных органов и систем (Приложение А3.2).
Ведение пациентов с МВ предпочтительно проводить в специализированных центрах (кабинетах или отделениях муковисцидоза). Следует использовать стационарозамещающие технологии.
Динамическое наблюдение в амбулаторно-поликлинических условиях при оказании первичной медико-санитарной помощи осуществляет врач-педиатр участковый (врач-педиатр, или врач-пульмонолог, или врач общей практики, врач-детский хирург/врач-хирург (по показаниям, в т.ч., например, после мекониевого илеуса) которые прошли соответствующий тематический курс в рамках программ непрерывного медицинского образования, а также имеют опыт ведения пациентов с данной нозологией; приемы (осмотры, консультации) врачей-специалистов – по показаниям) с частотой, определяемой тяжестью состояния пациента и имеющимися осложнениями болезни (1 раз в 1-3 месяца или по показаниям). Впервые диагностированные дети или пациенты с тяжелыми формами заболевания должны наблюдаться чаще (ежемесячно), пациенты с легким течением МВ могут наблюдаться реже (каждые 3-6 мес.).
Наблюдение за пациентом и контроль состояния необходимо осуществлять регулярно в условиях дневного стационара. Госпиализация проводится по показаниям (Приложение А3.9) в круглосуточный стационар (в пульмонологическое, инфекционное или иное отделение, в штате которого есть специалисты, имеющие опыт ведения пациентов с данной нозологией). Пациента госпитализируют в индивидуальную палату с учетом подтвержденного ранее микробиологического пейзажа (особенно для Р. aeruginosa, В. cepacia comрlex, MRSA, Stenotrophomonas maltophilia, Achromobacter spp., нетуберкулезных микобактерий, хронический аспергиллеза), при возможности – индивидуальный бокс. В зависимости от состояния пациента срок госпитализации может составить от 4 до 21 дня.
Пациенты с МВ, нуждающиеся в стационарном лечении в рамках первичной специализированной медико-санитарной помощи, направляются по медицинским показаниям в пульмонологическое, инфекционное или иное отделение (по показаниям, условия – указаны выше) медицинской организации врачом скорой медицинской помощи, врачом-педиатром участковым, врачом-пульмонологом или иным специалистом амбулаторно-поликлинического звена.
Пациентов с муковисцидозом, нуждающихся в оказании специализированной медицинской помощи, в том числе высокотехнологичной, в стационарных условиях, по медицинским показаниям направляют в соответствующее отделение медицинской организации врач-пульмонолог или врач-педиатр.
Маршрутизация пациента детского возраста во взрослую сеть – во взрослый центр МВ, осуществляется к 18 годам.
Пациенты с муковисцидозом получают:
- в рамках первичной медико-санитарной помощи – плановую и неотложную амбулаторно-поликлиническую и первичную специализированную помощь (соответствующего профиля, по показаниям и в зависимости от тяжести состояния, а также скорую медицинскую помощь);
- в рамках специализированной медицинской помощи – специализированную, в том числе высокотехнологичную медицинскую помощь, в соответствующих условиях дневного или круглосуточного стационара.
При направлении в отделение (центр или кабинет) муковисцидоза, врачом-педиатром участковым или врачом другой специальности предоставляется выписка из амбулаторной карты (истории болезни) с указанием предварительного (или заключительного) диагноза, сопутствующих заболеваний, а также имеющихся результатов лабораторных и функциональных исследований.
Правила профилактики перекрестной инфекции при муковисцидозе [2,364]
1. Организация оказания помощи пациентам. Профилактика инфекции.
Общие меры профилактики
Меры по изоляции биологических жидкостей (мокрота, кровь) пациента с МВ.
Дезинфекция оборудования или предметов, которые могут быть загрязнены жидкостями и выделениями.
-
Строгое соблюдение мер предосторожности медицинскими работниками при контакте с пациентами с МВ:
– использование одноразовых медицинских перчаток, обработка фонендоскопа, пульсоксиметра и т.д.;
– использование одноразовых пеленок для осмотра;
– использование одноразовых халатов при работе с пациентами, требующими соблюдения мер контактной изоляции (B. cepacia complex, MRSA, мультирезистентная P. aeruginosa, Achromobacter spp., НТМБ), и во время кинезитерапии;
– использование одноразовых антибактериальных фильтров при спирометрии.
Контакты между пациентами с МВ должны быть сведены к минимуму.
-
Гигиена рук медицинских работников:
1. Мытье и дезинфекция рук проводится:
– после снятия перчаток,
– до и после контакта с пациентом,
– после контакта со:
– слизистыми пациента,
– мокротой пациента,
– предметами, загрязненными мокротой пациента,
– дыхательным оборудованием, которым пользовался пациент.
Использование спиртовых антисептиков (в виде салфеток, в диспенсерах) в кабинетах и в общем коридоре.
Медицинские работники, непосредственно контактирующие с пациентами, не должны использовать накладные ногти.
Использование перчаток необходимо при: контакте с пациентами, требующими изоляции, контакте с мокротой или кровью пациента.
Использование одноразовых халатов, масок, защитных очков: при контакте с больными, требующими изоляции, при контакте с мокротой пациента (при дренаже, аспирации, осмотре пациента с приступообразным кашлем) или при контакте с кровью.
-
Гигиена рук пациентов:
– обработка спиртовыми антисептиками (в нескольких клинических исследованиях показано, что обработка спиртовыми антисептиками удаляет бактерии с рук эффективнее, чем мытье рук с антисептическим мылом). Если есть видимое загрязнение, то используют мыло и антисептик,
– после пульсоксиметрии,
– после контакта с медицинским оборудованием,
– после проведения кинезитерапии,
– после посещения санузла,
– после приема врачом.
Предметы (платки, салфетки, маски, баночки и др.), загрязненные мокротой пациента, должны утилизироваться согласно СанПиН 3.3686-21.
Дезинфекция в амбулаторных условиях
Оборудование:
Спирометры – внутренние механизмы аппарата не стерилизуются, не дезинфицируются. Обработка турбины или датчика производится в соответствии с инструкцией изготовителя, обязательно использование одноразовых антибактериальных фильтров, предпочтительны одноразовые загубники или стерилизация многоразовых. У пациентов, подлежащих мерам контактной изоляции, спирометрия должна проводиться на отдельном аппарате. Категория А
Пульсоксиметры – обработка рук спиртовым антисептиком после использования.
Кинезитерапевтическое оборудование, мячи, манжета тонометра обрабатываются дезинфицирующими средствами.
Небулайзеры и дыхательные тренажеры должны быть только индивидуального использования.
Твердые поверхности (плановые текущие уборки, а также уборка после окончания приема пациента).
Обработка фонендоскопа после каждого осмотра пациента.
Выявление источника, путей и факторов передачи
Врачам-бактериологам и врачам-эпидемиологам:
при первичном выявлении у пациента с МВ Burkholderia cepacia complex (Всс), Achromobacter spp., мультирезистеного клона P. aeruginosa и метициллин-резистентных Staphylococcus aureus (MRSA), а также при выявлении нового генотипа необходимо проводить эпидемиологическое расследование с целью выявления источника инфекции, факторов передачи, а также контактировавших пациентов с МВ;
при выявлении источников и факторов передачи инфекции требуется провести дополнительные действия, например, изоляцию госпитализированного пациента с МВ, т.е. источника инфекции, внеплановую профилактическую дезинфекцию больницы, а также микробиологическое обследование контактировавших пациентов;
для выявления источника инфекции и факторов передачи необходимо собрать эпидемиологический анамнез и провести внутривидовое типирование выделенных микроорганизмов. При этом исходить из предположения, что штаммы Burkholderia cepacia complex, Achromobacter spp., P. aeruginosa и MRSA, выделенные от источника инфекции, с объектов внешней среды, являющихся факторами передачи, и от обследуемого пациента с МВ, должны быть идентичными по фенотипическим и генотипическим свойствам;
бактерии Burkholderia cepacia complex и Achromobacter spp. типировать молекулярно-генетическими методами, так как типирование по фенотипическим свойствам имеет низкую дискриминационную способность. Для оперативного анализа и выявления источника использовать быстрые методы, основанные на ПЦР или другие методы типирования;
генетическое типирование на данном этапе могут выполнять лаборатории стационаров, использующие в своей практике метод ПЦР;
при невозможности внутривидового типирования в лаборатории стационара для генотипирования направлять изоляты бактерий в специализированные лаборатории, имеющие оборудование для молекулярного типирования;
-
в специализированную лабораторию следует направлять:
- все изоляты (Burkholderia cepacia complex, Achromobacter spp., мультирезистентные P. aeruginosa и MRSA), впервые выделенные от каждого пациента,
по крайней мере, по одному изоляту Burkholderia cepacia complex, Achromobacter spp., мультирезистентного P. aeruginosa и MRSA в год от каждого пациента,
любой изолят, подозрительный на возможную связь со вспышкой или трансмиссией между пациентами,
грамотрицательные колистинрезистентные микроорганизмы, которые не были идентифицированы окончательно после рутинного анализа или при сомнительных результатах;
доставка изолятов должна осуществляться максимально быстро с соблюдением мер биологической безопасности, применяемых при упаковке и транспортировке штаммов микроорганизмов согласно санитарным правилам СанПиН 3.3686-21. Штаммы должны сопровождаться направлением, содержащим информацию о пациенте, о предполагаемых источниках и факторах риска колонизации данным микроорганизмом;
на основании данных типирования рекомендуется осуществлять слежение за динамикой распространения среди пациентов МВ клонов, имеющих эпидемическое значение, а также оценить циркуляцию международных эпидемических клонов.
Мониторинг антибиотикочувствительности
Кроме подтверждение принадлежности штаммов к Burkholderia cepacia complex и Achromobacter spp. с помощью MALDI-TOF или молекулярно-генетическим методом и внутривидового типирования в референс-лаборатории должно проводиться также определение антибиотикочувствительности и мониторинг антибиотикорезистентности, молекулярно-генетический мониторинг за популяцией возбудителя - секвенирование возбудителей, исследование микроэволюционных процессов, слежение за изменчивостью возбудителей, а также необходимо создание и ведение баз данных возбудителей.
В таблице 36 приведены антимикробные препараты, резистентность к которым основных возбудителей хронической инфекции легких у пациентов с МВ является клинически и эпидемиологически значимой и подлежит мониторингу.
Таблица 36. Антимикробные препараты системного действия, резистентность к которым подлежит мониторингу.
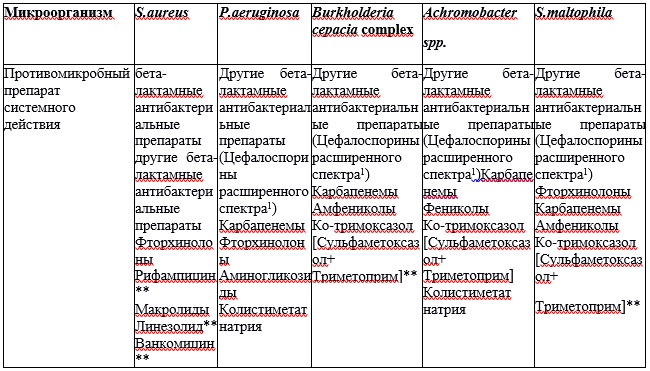
1 – цефотаксим**, цефтриаксон**, цефоперазон, цефоперазон+[Сульбактам]**, цефтазидим**, цефдиторен, цефиксим, цефтибутен, цефепим**, цефпиром и др.
Молекулярно-генетический мониторинг позволит выявить возникновение новых эпидемических клонов; возникновение новых клонов с высокой вирулентностью в результате горизонтального переноса генов или межвидовой рекомбинации; новых антибиотикорезистентных клонов, изменения антигенных свойств. Это поможет сделать эпидемическое прогнозирование и обосновать своевременное вмешательство в ход эпидемического процесса.
На основе полученных данных проводится эпидемиологическая диагностика с определением типа эпидемического процесса по ведущему пути передачи и эпидемическое прогнозирование. Данные эпидемиологического мониторинга могут быть использованы в качестве основы при разработке научно обоснованных эффективных мер по борьбе с распространением Burkholderia cepacia complex, Achromobacter spp., мультирезистентных P. aeruginosa и MRSA, микобактерий и грибов среди пациентов с МВ и в популяции в целом. При этом, в случае с МВ, как и при других хронических инфекциях, результаты проводимых мероприятий будут заметны через многие годы.
Организация амбулаторной и стационарной помощи
Прием пациентов с МВ не должен осуществляться в поликлиниках, где находятся одновременно другие пациенты с МВ. Работа амбулаторного центра и стационара регулируется Постановлением Главного государственного санитарного врача РФ от 28 января 2021 г. № 4 "Об утверждении санитарных правил и норм СанПиН 3.3686-21 "Санитарно-эпидемиологические требования по профилактике инфекционных болезней и рекомендациями European Cystic Fibrosis Society.
Пациенты должны быть разделены на потоки в зависимости от микрофлоры дыхательного тракта. Пациенты не должны контактировать в зонах ожидания, как, например, в регистратуре, палатах, отделениях аптеки и рентгенологии. Во время пребывания в стационаре пациенты не должны пользоваться одной комнатой, ванной или туалетом. Пациент с микробиологическим высевом из мокроты бактерий Burkholderia cepacia complex, метициллин-резистентных Staphylococcus aureus, Achromobacter spp., нетуберкулезных микобактерий должен приниматься на амбулаторном приеме в отдельном боксе с отдельным входом, не заходя в центр муковисцидоза (или в МО).
Пациенты с муковисцидозом должны обеспечиваться одноразовыми лицевыми масками, бахилами. Пациенты с муковисцидозом при нахождении в одном помещении должны держаться на расстоянии не менее 2 м друг от друга и соблюдать все меры профилактики. После приема каждого пациента проводится обработка поверхностей мебели, приборов и дверных ручек.
Пациенты обеспечиваются одноразовыми масками, бахилами.
Врачи должны быть обеспечены одноразовыми халатами, масками, перчатками, должен быть обеспечен доступ к средствам дезинфекции рук и приборов.
Правила ожидания приема врача в поликлинике
Все пациенты с муковисцидозом, ожидая начала приема, обязаны находиться в лицевой маске.
Гигиена рук (обработка дезинфицирующим раствором из бесконтактных диспенсеров в зоне ожидания, использование антибактериальных гелей или спиртовых салфеток для индивидуального использования).
Сплевывание мокроты должно осуществляться пациентом в бумажный платок или салфетку, баночку (одноразовый стакан) с крышкой. Категорически запрещается эвакуация мокроты в раковину, душевую кабину или унитаз.
Пациенты в зоне ожидания должны находиться друг от друга на расстоянии не менее 2 метров.
Не рекомендуется использовать предметы, которые нельзя обработать после посещения Центра муковисицидоза (мягкие игрушки и пр.).
Не рекомендуется принимать пищу, находясь в общей зоне ожидания приема (допускается кормление грудью).
В центре муковисцидоза правила поведения пациентов должны быть размещены на доске объявлений, на сайте организации (www.mukoviscidoz.org) и доступны для ознакомления.
Правила нахождения пациентов с МВ в стационаре
Перед госпитализацией пациенты с муковисцидозом сдают микробиологический анализ мокроты (не ранее чем за 1 месяц). Пациенты размещаются в одноместные палаты (боксы) согласно микрофлоре дыхательного тракта.
Госпитализация пациентов с Burkholderia cepacia complex осуществляется в лечебные учреждения, имеющие специализированные боксы для данной инфекции. Пациенты, инфицированные Burkholderia cepacia complex, Achromobacter spp., нетуберкулезными микобактериями или устойчивыми к ванкомицину энтерококками, должны размещаться в отдельной палате/боксе с душем и туалетом, желательно с отдельным входом. Госпитализация пациентов с резистентной флорой ведется в приемном отделении для инфекционных пациентов; пациенты проходят в палаты (боксы) через отдельный вход.
Пациенты с муковисцидозом, инфицированные иной флорой, размещаются в одноместной палате с душем и туалетом или с другими пациентами, не страдающими муковисцидозом и с низким риском инфицирования.
Боксы для пациентов со стафилококковой и синегнойной инфекцией желательно размещать при планировании отделения в противоположных концах коридора или на разных этажах.
Все пациенты c муковисцидозом после трансплантации должны находиться в одноместной палате.
Для пациентов с муковисцидозом с Burkholderia cepacia complex и Achromobacter spp., нетуберкулезными микобактериями или устойчивыми к ванкомицину энтерококками, должно быть отдельное медицинское оборудование для каждого пациента (индивидуальный спирометр, фонендоскоп, пульсоксиметр, глюкометр, тонометр и т.д.).
Посещение диагностических процедур пациентов муковисцидозом должно планироваться согласно микрофлоре дыхательного тракта.
Дезинфекция помещений, оборудования и т.д. проводится согласно СанПиН 3.3686-21
Пациенты с МВ, которые дома спят в одной комнате, могут в стационаре находиться в одной палате.
Пациентов обучают кашлять в бумажный платок, в салфетку или одноразовый стакан с крышкой, которые затем утилизируют.
Салфетки, испачканные мокротой, пациенты должны утилизировать в закрытые контейнеры, открывающиеся без касания рук.
В стационарных условиях пациенты с МВ используют только индивидуальное оборудование (дыхательные тренажеры, аппараты для кинезитерапии, ингаляторы), которое приносят с собой из дома.
Обрабатывать руки перед выходом из палаты.
Избегать контактов с другими пациентами с МВ.
В общих помещениях держаться от других пациентов на расстоянии не менее 2 метров.
Использовать лицевую маску.
Диагностические службы (кабинет рентген-диагностики, УЗИ и др.) должны быть осведомлены о правилах изоляции пациентов с МВ.
Правила поведения в стационаре должны быть выданы родителям и ребенку/пациенту при госпитализации и размещены сайте медицинской организации.
Инженерный путь решения инфекционного контроля при планировке отделения, вентиляции.
Планирование отделения проводится согласно СанПиН 3.3686-21.
План бокса для пациентов со стафилококковой и синегнойной инфекцией: вход из коридора отделения, при возможности - тамбур на входе с раковиной; санитарный узел с раковиной и желательно душем; палата.
План бокса для пациентов с B. cepacia complex и Achromobacter spp: для медицинского персонала рекомендуется планировать вход из коридора отделения в шлюз на входе из отделения, тамбур при наличии нескольких палат с раковиной; санитарный узел в каждой палате с раковиной; палата(ы), для пациентов и родственников вход с улицы.
Правила и методы обработки и смены ингаляторов, небулайзеров и дыхательных тренажеров (при индивидуальном использовании и в стационаре)
! Неполная дезинфекция способствует росту бактерий, и тем самым увеличивает риск инфицирования.
Небулайзер и использованные принадлежности должны быть тщательно очищены после каждого применения. Дезинфекция должна проводиться не реже одного раза в день.
Подготовка к очистке
Отсоедините трубку от небулайзера;
Разберите небулайзер на составные части;
При использовании мундштука с клапаном осторожно вытащить синий клапан выдоха из гнезда в наконечнике. Клапан должен оставаться присоединенным к мундштуку.
Уход за соединительной трубкой
Подключить соединительную трубку к компрессору;
Включить компрессор;
-
Оставить компрессор в работающем состоянии до тех пор, пока конденсат, образовавшийся в трубке, не будет удален воздухом, проходящим через трубку;
- при загрязнении и изменении цвета пластмассы трубку-воздуховод следует заменить.
Очистка
Поместить все детали небулайзера в теплую водопроводную воду с небольшим количеством жидкости для мытья посуды не менее чем на 5 мин.;
Тщательно промыть все детали в проточной воде;
Для удаления лишней воды встряхнуть детали.
Дезинфекция
После очистки проводится дезинфекция составных частей небулайзера и использованных принадлежностей (кроме соединительных трубок). Эффективная дезинфекция возможна только если небулайзер был тщательно очищен.
При использовании маски с резиновыми лентами: резиновые ленты могут подвергаться только очистке (стирке), так как при действии высоких температур, используемых при дезинфекции, они могут быть повреждены.
Дезинфекция кипячением
Поместить все детали в кипящую воду не менее чем на 5 минут. Используется чистая кастрюля и свежая вода с пониженным содержанием кальция.
Пластик может расплавиться, если он вступит в контакт с горячим дном кастрюли. Поэтому следует убедиться, что в кастрюле достаточно воды.
Дезинфекция с помощью стандартного термического дезинфектора для детских бутылочек (не для микроволновой печи)
Для эффективной дезинфекции используется дезинфектор с рабочим циклом не менее 6 минут. Во время дезинфекции, чтобы определить продолжительность процедуры дезинфекции и количество воды, необходимое для этого, необходимо следовать инструкции по эксплуатации дезинфектора, который используется.
Неполная дезинфекция способствует росту бактерий, и тем самым увеличивает риск инфицирования. Дезинфекция не завершена, если была прекращена до автоматического выключения дезинфектора, или минимальное время дезинфекции, указанное в инструкции по эксплуатации дезинфектора не истекло. Дезинфектор должен содержаться в чистоте, и его работоспособность следует регулярно контролировать.
Дезинфекция с помощью микроволнового дезинфектора
Микроволновые дезинфекторы обеспечивают эффективную дезинфекцию компонентов изделия в стандартной коммерческой микроволновой печи.
Составные части небулайзеров, содержащие металлические компоненты не является устойчивыми к воздействию микроволн, и, следовательно, они не должны дезинфицироваться в микроволновой печи.
Поместить компоненты изделия в дезинфектор, оставив достаточное пространство между ними, чтобы пар мог надежно проникнуть ко всем поверхностям.
Условия дезинфекции в микроволновой печи:
Мощность в ваттах Время дезинфекции Время охлаждения
850–950 4 мин. 2 мин.
600–850 6 мин. 2 мин.
Информация о количестве воды, необходимой для процесса дезинфекции, включена в инструкции по эксплуатации дезинфектора и микроволновой печи.
Компоненты изделия не должны подвергаться воздействию микроволнового излучения, если они не находятся в микроволновом дезинфекторе. Если компоненты изделия подвергаются нагреву в микроволновой печи без защиты дезинфектора, отдельные детали могут быть повреждены.
Нельзя для дезинфекции использовать функцию гриля, так как это тоже может привести к повреждению обрабатываемых частей небулайзера.
Дезинфекция не считается завершенной должным образом, если не соблюдено указанное минимальное время дезинфекции, а также требуемая выходная мощность микроволновой печи. Дезинфектор также должен быть чистым. Регулярно проверяйте работоспособность микроволнового дезинфектора. Для дезинфекции используется только вода, никогда не используются химические вещества.
Химическая очистка с дезинфекцией
Очистка и дезинфекция могут быть проведены в рамках одного цикла при помощи химических веществ. С этой целью используется средство дезинфицирующее, содержащее дидецилметилполиэтоксиаммония пропионат 17.5%. Для обеспечения безопасности при обращении с химическими веществами следуйте инструкции по эксплуатации дезинфицирующего средства, в частности прилагаемой инструкции по технике безопасности.
Приготовьте 2% раствор средства дезинфицирующего, содержащего дидецилметилполиэтоксиаммония пропионат 17.5% путем смешивания 10 мл концентрата с 500 мл водопроводной воды.
Поместить все детали в приготовленный раствор и оставьте их там на 5 мин.
Если значительно превысить период применения, то пластмассовые детали могут иметь запах дезинфицирующего средства.
Тщательно вымыть все детали в проточной (свежевскипяченной или дистиллированной) воде (остатки дезинфицирующего средства могут вызывать аллергические реакции или раздражение слизистой оболочки).
-Утилизировать использованный раствор (разбавленный раствор можно вылить в канализацию).
Визуальный контроль
Требуется осмотреть все компоненты изделия после каждой чистки и дезинфекции. Замените неисправные, деформированные или сильно обесцвеченные части.
Влажная среда может способствовать росту бактерий. Поэтому следует удалить все части устройства из кастрюли или дезинфектора после окончания дезинфекции. Необходимо высушить все детали. Риск инфицирования снижается, когда детали полностью высушены.
Сушка и хранение
Поместить все детали на сухую, чистую и впитывающую поверхность для просушки.
Завернуть небулайзер в чистую салфетку без ворса (например, в чистое кухонное полотенце) и держите его в сухом, защищенном от пыли месте.
Не следует оставлять небулайзер для хранения в ванной комнате.
Стерилизация в условиях стационара
При нахождении пациента в стационаре небулайзер и принадлежности могут подвергаться автоклавированию каждые 3-4 дня. Метод стерилизации может быть применен для изделий, которые прошли очистку и дезинфекцию.
Подготовка и процедура автоклавирования
Упакуйте все отдельные детали в систему со стерильным барьером согласно DIN EN 11607 (например, в бумажно-пленочную упаковку).
Максимальная температура и время стерилизации: 121 °C, по меньшей мере, в течение 20 мин. или 132 °C / 134 °C, по меньшей мере в течение 3 мин.
Хранение
Стерильный небулайзер может храниться в бумажном пакете до 3 суток, в биксе – до 7 суток.
Не следует подвергать стерилизации взрослую и детскую мягкие маски без стабилизатора маски, так как это может привести к потере формы под воздействием высоких температур.
Содержание и очистка компрессора
Очистку разрешается проводить только в том случае, если устройство выключено и сетевая вилка вынута из розетки.
Существует опасность повреждения устройства из-за проникновения жидкостей.
Запрещается распылять жидкость на компрессор или сетевой кабель.
Для очистки наружной поверхности компрессора следует использовать чистую влажную (смоченную дезинфекционным средством) салфетку.
Замена фильтра
При стандартных условиях эксплуатации фильтр компрессора требуется заменять через каждые 200 часов работы, но не реже одного раза в год.
Следует регулярно проверять фильтр (после каждой 10-й процедуры). Если он загрязнен (имеет серый или коричневый оттенок) или засорен, его необходимо заменить. Если фильтр стал влажным, его также требуется заменить новым.
Очищать фильтр и использовать его повторно запрещается!
Хранить компрессор и принадлежности следует в сухом месте, защищенном от продолжительного действия прямых солнечных лучей. Не рекомендуется хранить компрессор на балконе, в автомобиле, в запыленных и влажных помещениях.
Сроки использования небулайзера и компрессора.
Быстро изнашиваемые комплектующие, такие как небулайзер, мундштук или маска, трубка-воздуховод и фильтр к компрессору подлежат регулярной замене, не реже одного раза в год, а в случае сильного загрязнения, деформации или поломки - немедленно.
При колонизации антибиотикорезистентной микробной флорой смену небулайзера рекомендуется производить после каждого курса ингаляционной антибактериальной терапии или 1 раз в 2-3 мес. В остальных случаях не реже 2 раз в год.
Компрессор должен быть ежегодно протестирован специалистами технической поддержки.
Ожидаемый средний срок службы компрессора ингаляционной системы определяется согласно эксплуатационной документации.
Дыхательные тренажеры используются и обрабатываются аналогично. Дыхательные тренажеры без возможности их дезинфекции не должны использоваться более 1 месяца.
Организация обучения и досуга пациентов с муковисцидозом
ДДУ, школы, и другие образовательные учреждения
В одной школе могут учиться несколько пациентов с МВ, но они не должны обучаться в одном классе. Категория А.
Пациенты с МВ не должны находиться в одном помещении (столовая, физкультурный зал) одновременно. Категория В.
Если они находятся в одном помещении, должны держаться на расстоянии не менее 2 м друг от друга и соблюдать все меры профилактики. Категория В.
Учителя и медицинские работники должны быть информированы о правилах поведения детей в школе.
Школы для родителей и другие мероприятия, посвященные МВ
Организация школ для пациентов, совместного отдыха и мероприятий, проведение праздников для пациентов с МВ недопустимы! Школы проводятся для родителей, родственников и их попечителей. Для пациентов возможны школы в системе он-лайн, в виде вебинаров. Пациенты с МВ должны избегать прямого контакта. Необходимо разрабатывать образовательные программы по МВ, не требующие прямого контакта между пациентами: видеозаписи, видеоконференции, образовательные порталы в Интернете [110,23].
Строительство, ремонт, садоводческие работы
Пациенты с МВ должны избегать мест, где проводятся строительство, ремонт и садоводческие работы, чтобы избежать контакта со спорами Aspergillus spp. Пациентам с МВ не следует работать на приусадебных участках с использованием компоста и пр.
Организация санаторно-курортного лечения
Организация спортивных лагерей, летних школ, совместного отдыха для пациентов с МВ недопустима!
При организации санаторно-курортного лечения требования предъявляются аналогично, как при госпитализации (см. Организация амбулаторной и стационарной помощи). При организации санаторно–курортного лечения в один заезд должны быть направлены пациенты с однотипной микрофлорой. Следует размещать пациентов на отдельных этажах или в разных корпусах, не допускать их контакта при выполнении диагностических и лечебных процедур, в столовой и игровых комнатах.
МВ — хроническое неизлечимое заболевание, поэтому пациенты нуждаются в активном диспансерном наблюдении и непрерывном лечении. У одних пациентов, несмотря на своевременную диагностику и адекватную терапию, поражение бронхолёгочной системы быстро прогрессирует, у других - динамика изменений более благоприятна. Многие пациенты доживают до взрослого и даже зрелого возраста.













