Хронический болевой синдром (ХБС) у взрослых пациентов, нуждающихся в паллиативной медицинской помощиКод: 400 • Редакция: 2
Боль – это не только симптом большинства заболеваний, но и сложный психофизиологический феномен, в который вовлечены механизмы регуляции и формирования эмоций, моторные, гуморальные и гемодинамические проявления, формирующие болевой синдром. Международная ассоциация по изучению боли (IASP) дала в 2020 г. следующее определение понятию боли: «Боль — неприятное сенсорное и эмоциональное переживание, связанное с действительным или возможным повреждением тканей, или схожее с таковым переживанием» [1]. Хроническая боль определяется как боль, которая сохраняется дольше, чем обычно необходимо для заживления повреждения, иначе говоря (в т.ч. для случаев отсутствия явных признаков фактического повреждения тканей) сохраняется / возобновляется в течение трех и более месяцев [55]. Однако, согласно современным представлениям, хроническая боль имеет важные отличия от острой (сигнальной) боли не только по продолжительности.
Хронический болевой синдром фактически является самостоятельным заболеванием. Он не выполняет защитной функции и не несет никакой биологической целесообразности. Напротив, хроническая боль ведёт к дезадаптации, к ненормальному восприятию болевых и неболевых импульсов и сопровождается различными нарушениями функций ЦНС. Клиническая картина зависит от локализации очага поражения, конституции больного, его психики и индивидуального порога болевой чувствительности, предшествующего болевого опыта [2, 3].
Основной причиной возникновения хронического болевого синдрома является длительно существующая постоянная боль, которая вызывает дисбаланс в работе периферической и центральной нервной системы. Нейрональные рецепторы и волокна в этом случае подвергаются постоянной активизации, что приводит к возрастающей стимуляции центральной нервной системы (спинного и головного мозга) болевыми раздражителями. Одна из основных причин хронической боли – появление комплексов гиперреактивных нейронов на различных уровнях ЦНС. Их патологическая активность обусловлена поломкой механизмов нейронального торможения, повышенной возбудимостью нейронов и активацией неактивных синапсов, что объединяет эти нейроны в единый очаг возбуждения с самоподдерживающейся эктопической активностью. Эта активность приводит к функциональным, структурным и адаптивным (нейропластическим) изменениям в головном и спинном мозге, из-за чего боль продолжается, даже когда ее причина устранена [4, 5].
Боль, вызванная злокачественным опухолевым процессом, имеет свою специфику. Опухолевые клетки быстро растут, сдавливая прилежащие здоровые ткани, которые чувствительны к механическим воздействиям (висцеральные боли), либо прорастают или сдавливают периферические и центральные структуры нервной системы (например, нейропатические боли). В процессе развития и роста опухоль выделяет специфические алгогены: эндотелин, простагландины и фактор некроза опухолей-альфа (TNF-α), которые возбуждают или повышают восприимчивость периферических рецепторов и нервных волокон к сенсорным раздражителям. Опухоли выделяют ионы водорода Н+, что приводит к местному ацидозу, сопровождающемуся сходным эффектом. Протеолитические ферменты, вырабатываемые опухолевыми клетками, постоянно возбуждают и дестабилизируют сенсорную симпатическую иннервацию, что приводит к нейропатической боли. Боль, вызванная метастазами опухоли, возникает в результате прямого опухолевого повреждения С-афферентов сенсорных нейронов, иннервирующих костный мозг, а также из-за нарушения баланса между активностью остеокластов и остеобластов. Кости теряют прочность, подвержены остеолизу, патологическим переломам и микропереломам, в результате механическая деформация периоста становится основным источником боли [6].
Ноцицептивная соматическая боль возникает в результате повреждения ткани или воздействия на него болезненного агента, в том числе опухоли с последующей активизацией болевых рецепторов (ноцицепторов) в костях, коже, подкожной клетчатке, в мышцах и мягких тканях, и пр. Эта боль хорошо локализована, может быть приходящей или постоянной, имеет различные описательные характеристики: тупая или острая, давящая, пульсирующая, дергающая, сверлящая, грызущая, распирающая и пр. [7].
Ноцицептивная висцеральная боль возникает при повреждении симпатически иннервируемых органов (при поражении поджелудочной железы, стенок желудка и кишечника, растяжении капсулы печени и пр.). Эта боль плохо локализована, имеет разлитой характер (тупая с приступами обострения, сжимающая, схваткообразная, тянущая, изнуряющая и пр.) [7].
Нейропатическая боль является результатом повреждения нервной системы на периферическом или центральном уровне, или патологического процесса в соматосенсорной системе. Зачастую она сопровождает тяжелые ноцицептивные болевые синдромы, но иногда встречается, как самостоятельный вид боли, например, после хирургического лечения, или при проведении химиотерапии, а также в результате сдавления нерва опухолью, при вирусном повреждении нерва, при тяжелых формах диабета [6, 7].
Нейропатическую боль несложно распознать:
• пациент описывает свою боль как необычную: жгучую, стреляющую, “как будто бьет током”, или как иные странные ощущения;
• участок кожи рядом с местом локализации боли может быть либо лишенным чувствительности, либо слишком чувствительным, настолько, что даже легкое прикосновение ткани оказывается болезненным [7, 8, 9].
Ноципластическая (дисфункциональная) боль – боль, возникающая при отсутствии активации ноцицепторов и видимого органического повреждения, в том числе со стороны нервной системы. Главное отличие дисфункционального типа боли от ноцицептивной и нейропатической в том, что при традиционном обследовании не удается выявить причину боли или органические заболевания, которые могли бы объяснить ее происхождение. К типичным примерам такой боли относятся фибромиалгия, головная боль напряжения и психогенные боли (соматоформное болевое расстройство) [10].
Хроническая / персистирующая боль может быть результатом следующих заболеваний:
1) хронические заболевания (опухолевые процессы, сердечно-сосудистые, неврологические, эндокринные, психиатрические, ревматоидные и др.);
2) заболевания, опасные для жизни (могут провоцировать одновременно острую и хроническую боль, например, злокачественные новообразования, ВИЧ/СПИД).
Оценка частоты распространенности боли при различных заболеваниях отражена в рекомендациях ВОЗ [11]:
• Онкологические заболевания: 35–96%;
• Сердечно-сосудистые заболевания: 41–77%;
• Почечная недостаточность: 47–50%;
• Хронические обструктивные болезни легких: 34–77%;
• ВИЧ/СПИД: 63–80%;
• Цирроз печени: 67%;
• Рассеянный склероз: 43%;
• Болезнь Паркинсона: 82%;
• Болезнь Альцгеймера и другие деменции: 47%;
• Ревматоидный артрит 89%;
• Сахарный диабет 64%;
• Мультирезистентный туберкулез 90%.
Онкологические пациенты составляют около 1/3 от всего контингента взрослых паллиативных пациентов [56]. При этом боль является одним из основных симптомов, причиняющих страдания при ЗНО. Несмотря на выдающиеся успехи, достигнутые в диагностике и терапии опухолей, по прогнозам экспертов ВОЗ в ближайшем будущем заболеваемость и смертность от онкологических заболеваний будет увеличиваться, соответственно будет расти число пациентов с болевым синдромом, обусловленным опухолевым процессом.
В России на учете состоит около 4 млн пациентов (в 2020 году - 3 973 295 человек) с установленным диагнозом ЗНО, из них ежегодно умирает около 300 тыс. и выявляется более 560 тыс. новых случаев заболевания [57]. На начальных стадиях опухолевого процесса 35–50% больных жалуются на боль, при прогрессировании ЗНО их число увеличивается до 75%, а в терминальной стадии – до 95–100%. Таким образом, число онкологических больных, нуждающихся в обезболивающей терапии, значительно превышает число умерших от ЗНО и только в нашей стране составляет более 430 тыс. пациентов [7].
Боль, не классифицированная в других рубриках (R52):
R52.1 – постоянная некупирующаяся боль;
R52.2 – другая постоянная боль.
Боль является проявлением или симптомом какого-либо заболевания или состояния, поэтому при оформлении медицинской документации используется код по МКБ-10, соответствующий основному заболеванию, который может быть дополнен кодами, свидетельствующими о существовании у пациента боли. Это важно при дифференциальной диагностике сложных случаев, когда установить причину боли сразу не удается.
Паллиативная помощь (Z51.5).
Согласно Распоряжению Правительства РФ от 16 мая 2022 г. N 1180-р “О перечне заболеваний или состояний (групп заболеваний или состояний), при которых допускается применение лекарственного препарата в соответствии с показателями (характеристиками) лекарственного препарата, не указанными в инструкции по его применению”, при оказании паллиативной помощи (Z51.5) допускается назначение лекарственных препаратов офф-лейбл.
Наиболее часто используемые классификации боли:
● По патофизиологическому механизму: ноцицептивная – соматическая (поверхностная/глубокая) или висцеральная; нейропатическая – периферическая или центральная; ноципластическая (дисфункциональная).
● По временному фактору: острая или хроническая, однако такое деление условно и не является необходимым для принятия решения о лечебной стратегии, т.к. симптомы и причины двух этих видов могут перекрываться, а патофизиологические факторы могут не зависеть от длительности. Допустимо использовать термин «персистирующая» боль. Отдельно выделяют прорывную боль.
● По этиологии: онкологическая или неонкологическая боль (не имеет значимого влияния на тактику терапии при запущенных, неизлечимых и прогрессирующих заболеваниях).
● По анатомической локализации: например, головная боль, боль в спине, мышечно-фасциальная, ревматическая, скелетная, неврологическая, сосудистая; однако деление по локализации/функции не всегда учитывает механизм боли и не предлагает стратегии для лечения боли [12].
Хронический болевой синдром вызывает ряд патологических реакций: выброс катехоламинов, как следствие: расширение зрачков, тахикардию, артериальную гипертензию, тахипноэ, повышает тонус скелетных мышц и вызывает их судорожную активность. Все эти вегетативные реакции со временем ведут к дезадаптации организма: нарушают ночной сон, резко снижают аппетит, вызывают депрессию и психосоматические расстройства, способствуют развитию нутритивной недостаточности и, как следствие, синдрома системной воспалительной реакции. Все эти факторы вызывают угнетение функции иммунитета, дисбаланс нейро-эндокрино-иммунных взаимодействий, которые усугубляют прогрессирование основного патологического процесса, являющегося причиной боли. Длительно существующая боль является одним из самых мощных неприятных ощущений человека, снижающих качество жизни вплоть до суицидальных последствий.
Критериями диагностики хронического болевого синдрома у взрослого пациента, нуждающегося в паллиативной медицинской помощи, следует считать:
• наличие жалоб пациента на боль;
• количество баллов по шкалам оценки боли, свидетельствующее о наличии боли;
• продолжительность боли на протяжении большинства дней в течение не менее 3 месяцев;
• наличие связанного с болью значимого эмоционального дистресса и/или нарушений функциональной активности (повседневной, социальной, трудовой).
Любое восприятие боли субъективно, поэтому не существует метода для объективного ее измерения. Сбор анамнеза хронического болевого синдрома должен включать следующие важные моменты (см. Приложение А3. Примерная форма опросного листа для первичной оценки боли):
1) число и локализацию очагов боли;
2) длительность предшествующего болевого анамнеза;
3) эффективность предшествующей терапии боли;
4) применяемые анальгетики;
5) влияние боли на физическую активность;
6) влияние боли на продолжительность ночного сна;
7) влияние боли на возможность приема пищи и прочее.
Рекомендуется для оценки интенсивности боли и эффективности лечения при каждом посещении или осмотре больного применять специальные шкалы, регистрировать локализацию болевых ощущений, время появления боли, характер и тип боли, длительность болевого синдрома (при движении и в покое) [2, 10, 12, 69, 113].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: боль необходимо регулярно оценивать. Цель оценки боли – понимание, что испытывает пациент, и установление влияющих на нее факторов (усиливающих и облегчающих). Рутинно используют субъективные методы оценки боли с помощью шкал: это делает сам пациент или врач, медсестра или при отсутствии контакта с пациентом, лицо, осуществляющее уход. В процессе оценки проводят идентификацию типа боли (ноцицептивная, нейропатическая, ноципластическая (дисфункциональная), смешанная), ее интенсивность (слабая, умеренная, сильная) и продолжительность (острая или хроническая); устанавливают локализацию и определяют эффективность лечения. При любом виде боли нужно понять причину и лечить ее, если это возможно.
Оценка боли проводится врачом или медицинской сестрой при каждом визите и осмотре больного раздельно при движении и в состоянии покоя, что должно быть зафиксировано в медицинской документации (см. Приложение А3. Примерная форма дневника оценки боли).
Интенсивность боли оценивается по различным шкалам, наиболее часто используемые из них: нумерологическая оценочная шкала (НОШ, синоним: числовая рейтинговая шкала), имеющая цифровую градуировку, соответствующую баллам от 0 до 10, и визуально-аналоговая шкала (ВАШ), представляющая собой отрезок 10 см без градуировки и отражающая силу боли в миллиметрах от 0 до 100 мм (рис. 1, см. Приложение Г1. Визуальная аналоговая шкала, Приложение Г2. Нумерологическая оценочная шкала (числовая рейтинговая шкала и Приложение Г3. Шкала лиц Wong-Baker). Больному предлагается отметить свое восприятие боли за последние 24 часа на шкале (от минимальной до нестерпимой), что позволяет количественно выразить оценку в миллиметрах по ВАШ или в баллах по НОШ [14].
Сопоставив полученные сведения с клинической картиной и данными инструментальных методов обследования, определяется степень интенсивности боли согласно следующей градации [14, 58]:
o боли нет: 0-4 мм по ВАШ или 0 баллов по НОШ;
o боль слабая: 5-44 мм по ВАШ или 1-3 балла по НОШ;
o боль умеренная: 45-74 мм по ВАШ или 4-6 баллов по НОШ;
o боль сильная: 75-100 мм по ВАШ или 7-10 баллов по НОШ.
Уменьшение интенсивности боли по НОШ на 2 балла или 30% считается клинически значимым, изменения больше, чем на 3 балла по НОШ или на 50% по ВАШ – существенными; результаты лечения интерпретируют в зависимости от природы болевого синдрома, но обычно изменение более 20 мм считают существенным [58].
Оценка боли у лиц с когнитивными нарушениями основана на схожих принципах оценки боли у детей. Основой являются поведенческие реакции и возможность отвлечь или утешить, причем степень выраженности проявлений оценивается в динамике. Крайне важным является холистический (целостный) подход к купированию целого ряда симптомов, которые могут быть связаны между собой или выражаться в различных формах (например, когда боль проявляется в виде ажитации). В связи с этим, все изменения в поведении пациента следует расценивать как возможное проявление боли при спутанности сознания:
Для определения причины дискомфорта (например, боль, ощущение холода) при тяжелой форме когнитивных расстройств необходимо учитывать мнение нескольких лиц, осуществляющих уход за пациентом.
Для скрининга и мониторинга состояния пациентов с умеренной и тяжелой формами когнитивных расстройств, в литературе описаны различные инструменты оценки боли у пациентов с когнитивными нарушениями, но до настоящего времени они не прошли языковую адаптацию и валидацию в РФ.
Дополнительно следует учитывать и оценивать такие компоненты боли как психологические и физические страдания (тягостные симптомы, способные усилить ощущение боли) и психосоциальные расстройства [15, 16].
Визуально-аналоговая шкала

Нумерологическая оценочная шкала
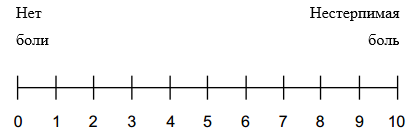
Шкала лиц Wong-Baker
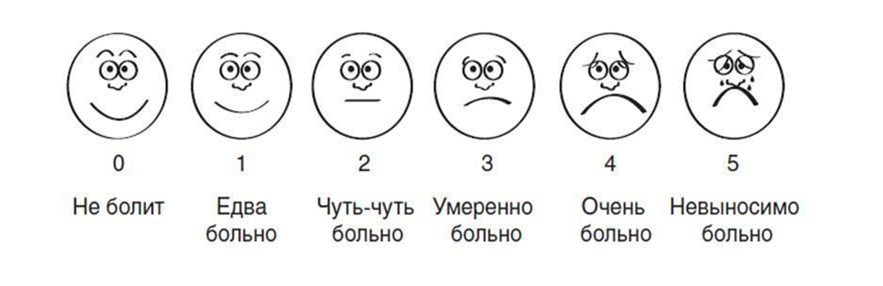
Рисунок 1 – Шкалы для оценки интенсивности боли
Для выявления нейропатической боли следует использовать скрининговый опросник (см. Приложение Г4. Диагностический опросник нейропатической боли DN4) [59, 60], предназначенный для врачей лечебных специальностей, не являющихся неврологами. Опросник дает возможность выявить наличие нейропатической боли с достоверностью более 80%. Наличие нейропатической боли у пациента высоко вероятно, если сумма баллов по опроснику DN4 составляет ≥4.
У паллиативных пациентов часто выявляется два вида боли одновременно: нейропатическая и ноцицептивная (смешанный тип боли).
Лабораторные исследования не дают значимых диагностических сведений о интенсивности, локализации и виде болевого синдрома.
Не рекомендуется для выбора и проведения обезболивающей терапии у пациентов, получающих паллиативную медицинскую помощь, использовать инструментальные методы обследования, поскольку они не подтверждают и не опровергают наличие боли [61,62,63].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии. Инструментальные методы обследования: рентгенография, ультразвуковое исследование (УЗИ), магнитно-резонансная томография (МРТ), компьютерная томография (КТ), позитронная эмиссионная томография совмещенная с компьютерной томографией (ПЭТ-КТ) и др. являются вспомогательными. Они позволяют определить характер, локализацию и выраженность патологического процесса, который является источником боли [62,63,64]. В выборе тактики терапии боли данные методы не имеют значения, поскольку паллиативное лечение направлено на повышение качества жизни у пациентов с неизлечимыми заболеваниями, где возможности терапии основного заболевания исчерпаны.
Целью обследования пациента с любым болевым синдромом, является уточнение характера боли, а также определение заболевания, являющегося источником боли.
Важно выявление нескольких источников, как основного, так и дополнительных при их наличии, а также уточнение локализации болевых ощущений [62,63,64].
При любой острой или хронической боли необходимо оценить качественные и количественные её характеристики: интенсивность, описание болевых и сенсорных ощущений пациентом, а также насколько боль неприятна и непереносима.
Помимо этого, следует уточнять факторы, приводящие к усилению и ослаблению боли, оценивать длительность болевого синдрома, флуктуации боли и сенсорных нарушений во времени.
При осмотре пациента также необходимо оценивать наличие признаков болевого поведения, «катастрофизации» боли, присутствие коморбидных болей или существующих независимо эмоционально-аффективных расстройств, обусловленных болью нарушений сна, степень социальной дезадаптации [65,66,67].
Необходимо помнить, что небольшая деструкция способна вызывать сильную боль и, напротив, распространенный патологический процесс может протекать без боли.
3.1 Консервативная терапия
Принципы терапии онкологической боли впервые были провозглашены ВОЗ в 1986 г. [68]. Впоследствии они распространились на терапию боли неонкологического генеза и, таким образом, они могут быть использованы для оказания паллиативной помощи пациентам, нуждающимся в обезболивании, независимо от причины болевого синдрома. Однако сам алгоритм терапии в виде «3-ступенчатой лестницы обезболивания» (рис. 2) в третьем пересмотре рекомендаций ВОЗ от 2018 г предлагается рассматривать в большей степени как обучающий инструмент [69]. Еще ранее, в 2012 г., исследовательский отдел EAПП провел научную оценку рекомендаций ВОЗ в части использования опиоидов на основе современных методов доказательной медицины по системе GRADE и опубликовал свои рекомендации, где были пересмотрены и уточнены некоторые положения фармакотерапии онкологической боли [15, 16]. В частности, сделан акцент на том, что пациент с тяжелым болевым синдромом сразу может нуждаться в сильных опиоидных анальгетиках (группа N02A, за исключением трамадола**, в т.ч. в комбинациях), и в этом случае не требуется последовательно идти от первой ступени «лестницы» к третьей.
Таким образом, выбор терапии хронического болевого синдрома должен определяться интенсивностью и патогенетической характеристикой боли. Терапия опиоидами остается основным методом лечения боли при оказании паллиативной медицинской помощи онкологическим и неонкологическим больным.

Рисунок 2 – «Лестница обезболивания» Всемирной организации здравоохранения [68].
3.1.1 Общие принципы терапии хронической боли при оказании паллиативной медицинской помощи
Рекомендуется использовать в качестве стартовой терапии хронической боли парацетамол**, НПВП, опиоид, как по-отдельности, так и в комбинации, в зависимости от клинической оценки и интенсивности болевого синдрома, с целью достижения быстрого, эффективного и безопасного обезболивания [69,70].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5)
Комментарии: Начинать обезболивающую терапию следует с анальгетика, сила и доза которого соответствуют интенсивности боли, оцененной пациентом по валидированной ВАШ или НОШ. Таким образом, слабые анальгетики (парацетамол**, НПВП) не должны назначаться в виде единственной терапии пациенту, страдающему от боли умеренной или сильной интенсивности. С учетом интенсивности боли такому пациенту может изначально потребоваться назначение опиоида (например, морфина** перорально) или комбинации опиоида с парацетамолом** / НПВП. На основании доступных рандомизированных исследований с участием опиоид-наивных пациентов невозможно определить предпочтительный тип анальгетика для стартовой терапии [69]. Вместе с тем, частота побочных эффектов между слабыми и сильными анальгетиками различается незначительно (при этом они отличаются по характеру).
Рекомендуется использовать для поддерживающей терапии хронической боли любой опиоид в корректной дозе (в виде монотерапии или в комбинации с парацетамолом** / НПВП), на основании клинической оценки и интенсивности болевого синдрома, с целью достижения устойчивого, эффективного и безопасного обезболивания [69,70].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5)
Комментарии: Корректной дозой опиоида считается доза, обеспечивающая снижение боли у пациента до приемлемого уровня (интенсивность боли менее 40% по ВАШ или менее 4 баллов по НОШ). Ответ на опиоидные препараты может отличаться у разных пациентов, и зависит как от особенностей пациента, так и от применяемого препарата. Опиоид, эффективный у одного пациента, может не оказать достаточного эффекта у другого пациента в той же самой дозе. Аналогичным образом различается переносимость препаратов. Выбор опиоида, его дозировка и схема применения должны основываться на фармакокинетических параметрах конкретного препарата, с учетом противопоказаний и побочных эффектов, а также состояния и сопутствующих заболеваний пациента.
Рекомендуется обезболивающий препарат вводить неинвазивно, следует ограничить использование инъекций [15, 17, 18, 19].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии: лекарственные препараты должны вводиться наиболее эффективным, удобным и, в то же время, наименее болезненным способом. Исследовательский отдел EAПП рекомендует пероральный путь введения препаратов, как предпочтительный, если есть возможность применения обезболивающих средств «через рот» [15]. Трансдермальный способ введения препаратов возможен в случае умеренной и сильной боли постоянного и длительного характера (например, при опухолях ЖКТ), с учетом клинической картины заболевания и пожеланий пациента. Из парентеральных путей введения основным является подкожный, а при необходимости достижения быстрого контроля боли – внутривенный. Внутримышечный способ не применяется для постоянного обезболивания. Спинальное (эпидуральное и интратекальное) введение опиоидов (в частности, морфина** и #фентанила**) [150, 151] и/или анестетиков (бупивакаина**) [152] используется у некоторых пациентов при наличии интенсивных болей, а также при плохом ответе на рутинную системную терапию опиоидами или в связи с плохо переносимыми нежелательными реакциями высоких доз опиоидов. Спинальный путь введения опиоидов относится к категории офф-лейбл применения, но позволяет в ряде случаев рефрактерной боли добиться успешного результата [153, 154]. Дозы опиоидов при интратекальном введении меньше, чем при пероральном и эпидуральном введении, в среднем в 300 раз и 24 раза соответственно [70]. В частности, интратекальное введение морфина** наиболее часто ограничивается дозой 1-4 мг, а #фентанила** (при Z51.1) – от 5 до 25 мкг [155].
Рекомендуется обезболивающий препарат вводить регулярно через определенные интервалы времени с учетом периода полувыведения или «по часам» [15, 18, 20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии: анальгетики следует назначать регулярно по схеме, не дожидаясь усиления боли, с учетом длительности действия препарата и индивидуальных особенностей пациента.
Рекомендуется применять обезболивающий препарат, увеличивая дозировку «по восходящей» [15, 18, 20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии: дозы анальгетиков подбираются, начиная от высоких доз слабых препаратов к низким дозам сильных анальгетиков в соответствии с интенсивностью боли. Переход на более сильный анальгетик определяется усилением боли, плохим ответом на применяемую обезболивающую терапию и нежелательными реакциями на лекарственные препараты у конкретного пациента. При этом пациенту с сильным болевым синдромом может изначально требоваться сильный опиоид, применение которого необходимо начинать с малых доз и достигать минимальной эффективной дозировки у конкретного пациента путем титрования дозы.
Рекомендуется обезболивающий препарат применять «индивидуально» – с учетом индивидуальных реакций организма конкретного пациента и с учетом особенностей его физического состояния [15, 18, 20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии: эффективное обезболивание достигается путем подбора анальгетика и его адекватной дозы (титрование дозы препарата), обеспечивающей обезболивание до приема следующей дозы. Не существует единой дозы и комбинации лекарственных препаратов универсальных для всех. Кроме того, ранее эффективные доза и/или препарат/ы у одного и того же больного в определенный момент могут стать неэффективны из-за прогрессирования основного заболевания, нарушения всасывания, развития толерантности (при использовании опиоидов) и др. причин, что является основанием для пересмотра и коррекции схемы обезболивания.
Рекомендуется обезболивающий препарат применять «с вниманием к деталям» [15, 18, 20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии: необходимо регулярно производить оценку эффективности терапии, проводить терапию, возникающих побочных эффектов. Рекомендуется пациенту вести ежедневный индивидуальный дневник (см. Приложение А3. Примерная форма дневника оценки боли).
3.1.2 Терапия боли слабой интенсивности
Интенсивность боли оценивается пациентом, как слабая, в пределах от 5 до 44 мм по ВАШ или 1-3 балла по НОШ.
Рекомендуется для фармакотерапии боли слабой интенсивности использовать неопиоидные анальгетики / НПВП, при необходимости дополнительно назначать адъювантные анальгетики [21, 22, 71,72,73,74].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии: боль слабой интенсивности может поддаваться терапии неопиоидными анальгетиками парацетамолом** и метамизолом натрия, а также НПВП. Имеющиеся данные не позволяют выделить наиболее эффективный препарат из группы неопиоидных анальгетиков / НПВП. Различные НПВП, парацетамол** и метамизол натрия исследовались у онкологических пациентов с болевым синдромом умеренной и сильной интенсивности, и продемонстрировали примерно схожую активность, за исключением парацетамола**. Вместе с тем, до настоящего времени не получено убедительных доказательств «за» или «против» применения неопиоидных анальгетиков / НПВП для лечения боли слабой интенсивности, в т.ч. у пациентов с прогрессирующими заболеваниями неонкологической природы. Метамизол натрия и кеторолак** не могут рассматриваться в качестве основных средств для лечения хронической боли, поскольку непрерывный курс терапии данными препаратами ограничен пятью днями (а кеторолака** в инъекциях только двумя днями) согласно инструкциям по их применению.
Эффективность неопиоидного анальгетика центрального действия нефопама, выпускаемого только в форме раствора для инфузий и внутримышечного введения, оценивалась у пациентов с хроническим болевым синдромом лишь в отдельных исследованиях. По всей видимости, его собственная анальгетическая активность в рекомендуемом диапазоне суточных доз не имеет клинического значения, тем не менее, на фоне его применения отмечена тенденция к уменьшению потребности в опиоидах (опиоид-сберегающий эффект) [75]. Кроме того, согласно инструкции по применению, нефопам показан к применению при остром болевом синдроме.
Применение неопиоидных анальгетиков/НПВП при необходимости сопровождается адъювантной и симптоматической терапией: противоэпилептическими средствами, антидепрессантами, спазмолитиками (A03A и A03B), миорелаксантами центрального действия, анксиолитиками, снотворными и седативными средствами (в т.ч. бензодиазепиноподобными средствами), глюкокортикостероидами, бисфосфонатами (МО5ВА, бифосфонаты) и др. препаратами [23] (см. Приложение А3. Адъювантные анальгетики и средства для симптоматической терапии). Цель применения таких препаратов – повысить эффективность обезболивающей терапии с учетом специфики патогенеза болевого синдрома у пациента, избегая при этом эскалации дозы основного анальгетика или перехода на более сильный препарат, тем более, неоправданного. В частности, антидепрессанты и противоэпилептические средства рекомендованы в качестве средств первой линии терапии нейропатической боли [60, 94] (см. раздел 3.1.9). Анксиолитики необходимы для снятия ажитации, связанной с болевым синдромом; седативные и снотворные препараты - для лечения нарушений сна, в т.ч. расстройств засыпания, связанных с болевым синдромом [148, 149]. Спазмолитики (A03A и A03B) потенцируют эффект анальгетиков при спастических болях и коликах; миорелаксанты центрального действия - для терапии болезненных спазмов скелетной мускулатуры (крампи); глюкокортикоиды эффективны при компрессии нервов и спинного мозга, а также в случаях выраженного перитуморального отека при прогрессирующих злокачественных новообразованиях [113, 147]. Бисфосфонаты рекомендуется использовать для уменьшения боли, связанной с метастатическим поражением костей, если исчерпаны стандартные методы терапии [156].
Рекомендуется учитывать специфические нежелательные эффекты НПВП и оценивать факторы риска развития осложнений терапии у конкретного пациента [76,77,78].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
Комментарии: к класс-специфическим нежелательным реакциям НПВП относятся: гепатотоксичность, нефротоксичность, а также риски со стороны сердечно-сосудистой системы (в виде дестабилизации артериальной гипертензии, декомпенсации хронической сердечной недостаточности и возникновения тромбоза артерий) и желудочно-кишечного тракта (НПВП-ассоциированная диспепсия, гастропатия и энтеропатия, осложняющиеся в т.ч. перфорацией и кровотечением ЖКТ). Риск развития нежелательных гастроинтестинальных и кардиоваскулярных реакций различается при использовании разных НПВП. Прием селективных ингибиторов ЦОГ-2 (M01AH коксибов) по сравнению с неселективными НПВП ассоциируется с меньшим риском поражения желудочно-кишечного тракта; к наиболее гастротоксичным НПВП относятся индометацин, напроксен и кеторолак** [78]. Наименьший риск кардиоваскулярных катастроф среди НПВП (кроме ацетилсалициловой кислоты**) в нескольких метаанализах показан лишь для напроксена, однако все НПВП способны с одинаковой вероятностью ухудшать течение хронической сердечной недостаточности [79,80]. Таким образом, при выборе препарата НПВП следует принимать во внимание факторы риска развития нежелательных реакций у конкретного пациента (см. Приложение А3. Факторы риска развития осложнений, связанных с приемом НПВП (для общей популяции) и рекомендации по назначению терапии. При этом необходимо иметь в виду вероятность повышенного риска развития типичных осложнений НПВП у пациентов паллиативного профиля, страдающих анорексией, кахексией, белковой недостаточностью, перенесших курсы химио- и/или лучевой терапии и т.д., поскольку репаративные возможности организма у таких пациентов существенно снижены [76]. Выбирая НПВП, можно ориентироваться на тот препарат, который был эффективен и хорошо переносим пациентом в прошлом. Тем не менее, в целях безопасности следует по возможности применять любой НПВП максимально коротким курсом в наименьшей эффективной дозе. Целесообразно использовать для профилактики поражения верхних отделов ЖКТ ингибиторы протонового насоса, которые, однако, не снижают, а по некоторым данным даже повышают риск повреждения слизистой оболочки тонкой кишки (НПВП-ассоциированной энтеропатии) [81,82,83], или блокаторы H2-гистаминовых рецепторов. Для некоторых пациентов опиоиды могут представлять более безопасную и эффективную альтернативу НПВП [76].
3.1.3 Терапия боли умеренной интенсивности
Интенсивность боли оценивается пациентом, как умеренная, в пределах от 45 мм до 74 мм по ВАШ или 4-6 баллов по НОШ, или если адекватный ее контроль не достигается регулярным приемом парацетамола, НПВП и адъювантных анальгетиков. Перечень опиоидов для терапии хронической боли умеренной интенсивности представлен в Таблице 1.
Таблица 1 – Опиоиды для терапии умеренной боли при оказании паллиативной медицинской помощи в Российской Федерации
№ |
Препарат |
Лекарственная форма |
Разовая доза |
Суточная доза |
|---|---|---|---|---|
1. |
Трамадол** |
Капсулы, таблетки, таблетки, покрытые пленочной оболочкой, таблетки с пролонгированным высвобождением, покрытые пленочной оболочкой, суппозитории ректальные, раствор для инъекций |
50 мг или 100 мг |
≤ 400 мг |
2. |
Парацетамол + трамадол
|
Таблетки, покрытые пленочной оболочкой |
37,5 мг/325 мг |
≤ 300 мг/2600 мг |
3. |
Пропионилфенилэтоксиэтилпиперидин** |
Таблетки защечные |
10 мг или 20мг |
≤ 40 мг |
4. |
Морфин** |
Таблетки и капсулы продленного действия; таблетки, покрытые пленочной оболочкой; раствор для приема внутрь |
5 мг или 10 мг |
≤ 30 мг |
5. |
Налоксон + оксикодон** |
Таблетки продленного действия |
5 мг/2,5 мг или 10 мг/5 мг |
≤ 20 мг/10 мг |
6. |
Фентанил** |
Трансдермальная терапевтическая система(пластырь трансдермальный) |
12,5 мкг/ч - 1 пластырь на 3 суток |
нет |
7. |
#Бупренорфин + налоксон1 |
Таблетки сублингвальные |
0,2 мг/0,2 мг |
0,4 мг/0,4 мг |
8. |
Тапентадол** |
Таблетки пролонгированного действия, покрытые пленочной оболочкой; таблетки, покрытые пленочной оболочкой |
50 мг |
100 мг |
1 #Бупренорфин + налоксон применяется при Z51.5 [7, 171, 174, 179].
В качестве адъювантных анальгетиков могут дополнительно применяться неопиоидные анальгетики / НПВП, противоэпилептические средства, антидепрессанты, анксиолитики, снотворные и седативные средства (в т.ч. бензодиазепиноподобные средства), антигистаминные средства системного действия, глюкокортикоиды, спазмолитики (A03A и A03B), миорелаксанты, бисфосфонаты (МО5ВА, бифосфонаты) и пр. (см выше раздел 3.1.2.). Дополнительно целесообразно назначить терапию, уменьшающую побочные эффекты применяемых препаратов: ингибиторы протонового насоса, слабительные средства, противорвотные препараты, блокаторы H2-гистаминовых рецепторов и др. (см. Приложение А3. Адъювантные анальгетики и средства для симптоматической терапии).
Рекомендуется для фармакотерапии боли умеренной интенсивности использовать слабые опиоиды (трамадол**), при необходимости дополнительно назначать неопиоидные и адъювантные анальгетики [13, 22].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: регулярное использование слабого опиоида трамадола** обеспечивает достижение эффективного обезболивания без выраженных нежелательных побочных эффектов в течение суток. Для терапии умеренной боли трамадол применяется в суточной дозе до 400 мг (у лиц старше 75 лет — до 300 мг/сут) [51] (Таблица 1).
Рекомендуется при умеренно выраженной боли в качестве альтернативы трамадолу, применять препараты сильных опиоидов в низких дозах (морфин**, налоксон+оксикодон**, фентанил**, бупренорфин**, тапентадол**) [15,17].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: ЕАПП внесла изменения в перечень препаратов 2-й ступени «лестницы обезболивания», где наряду со слабыми опиоидами рекомендовано, как альтернативу, применять сильные опиоиды в низких дозах (Рис. 1). С учетом зарегистрированных в России препаратов, можно использовать: препараты морфина**, налоксона + оксикодона**, тапентадола**, фентанила** в форме пластыря трансдермального (ТТС).
Рекомендуется для терапии умеренной боли применять лекарственный препарат пропионилфенилэтоксиэтилпиперидин** в защечных таблетках 20-40 мг/сут [24, 25, 26].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Комментарии: Российский препарат пропионилфенилэтоксиэтилпиперидин является синтетическим опиоидным агонистом, по силе действия сопоставим с тримеперидином. Хорошо всасывается через слизистую оболочку полости рта, применяется в виде подъязычных (защечных) таблеток. (Таблица 1).
Рекомендуется в качестве альтернативы пероральным опиоидам, применять трансдермальную форму фентанила** [15, 31, 32].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: для пациентов, которым невозможно по объективным причинам назначить пероральные формы пролонгированных опиоидов (за исключением пациентов с выраженной кахексией, потливостью, гипертермией или изменениями кожных покровов), оба препарата являются эффективным неинвазивным средством транспорта опиоидов в системный кровоток.
Рекомендуется в случае невозможности применения пероральных форм препаратов и использования ТТС назначать парентеральное введение морфина** [15, 22, 33].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: парентеральное введение морфина** при умеренной боли осуществляется дробно по 3-5 мг 2-4 раза в сутки, суммарно до 10 мг/сут, возможно использование продленной подкожной или внутривенной инфузии [53]. С учетом зарегистрированных в РФ инвазивных форм сильных опиоидов, возможно использование комбинированного препарата, содержащего Кодеин + Морфин + Носкапин + Папаверин+ Тебаин, в форме раствора для подкожного введения, с учетом индивидуальной переносимости компонентов. Тримеперидин** в таблетках и растворе для парентерального введения в терапии хронической боли применять не рекомендуется ввиду риска нейротоксических эффектов склонного к кумуляции метаболита нормеперидина, в особенности у ослабленных пациентов.
3.1.4 Терапия боли сильной интенсивности
Интенсивность боли оценивается пациентом, как сильная, в пределах от 75 мм до 100 мм по ВАШ или 7-10 баллов по НОШ, или если адекватный ее контроль не достигается регулярным приемом слабых опиоидов или низких доз сильных опиоидов (Таблица 1) в сочетании с адъювантными анальгетиками.
Рекомендуется для фармакотерапии сильной боли использовать сильные опиоиды, при необходимости дополнительно назначать неопиоидные анальгетики / НПВП и адъювантные анальгетики (Таблица 2 и см. Приложение А3. Адъювантные анальгетики и средства для симптоматической терапии). [15, 23, 84].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Таблица 2 – Опиоидные анальгетики в неинвазивных лекарственных формах для терапии сильной боли при оказании паллиативной медицинской помощи в Российской Федерации
№ |
Препарат |
Лекарственная форма |
Максимальная суточная доза |
|---|---|---|---|
1. |
Пропионилфенил- этоксиэтилпиперидин** |
Таблетки защечные |
250 мг |
2. |
Морфин** |
Таблетки и капсулы продленного действия; таблетки, покрытые пленочной оболочкой; раствор для приема внутрь |
Нет |
3. |
Налоксон + оксикодон** |
Таблетки продленного действия |
160 мг/ 80 мг |
4. |
Фентанил** |
Трансдермальная терапевтическая система (пластырь трансдермальный) |
Нет |
5 |
#Бупренорфин + налоксон1 |
Таблетки сублингвальные |
≤ 1,6 мг/1,6 мг |
6. |
Тапентадол** |
Таблетки пролонгированного действия, покрытые пленочной оболочкой; таблетки, покрытые пленочной оболочкой |
500 мг2 |
1#Бупренорфин + налоксон применяется при Z51.5 [7, 171 ,174, 179];
2Максимальная доза тапентадола в таблетках, покрытых пленочной оболочкой, составляет 700 мг в первые сутки, в последующие дни – 600 мг в сутки.
Комментарии: к сильным опиоидам, зарегистрированным в РФ для терапии хронического болевого синдрома, относятся морфин**, налоксон +оксикодон** , фентанил**, бупренорфин** и тапентадол** и пропионилфенилэтоксиэтилпиперидин** (см. Приложение А3. Перечень зарегистрированных препаратов опиоидов в инъекционных лекарственных формах, Перечень зарегистрированных препаратов опиоидов в неинвазивных лекарственных формах, Краткая характеристика препаратов опиоидов в неинвазивных лекарственных формах). Пролонгированными формами сильных опиоидов являются: морфин** в капсулах и в таблетках, комбинированный препарат налоксон + оксикодон** в таблетках, тапентадол** в таблетках, ТТС фентанила** (Таблица 2).
У пациентов, без нарушения функции глотания и явлений умеренной и выраженной почечной и печеночной недостаточности, с учетом его пожелания, терапию сильной боли начинают с таблетированных форм лекарственных препаратов (морфин**, налоксон +оксикодон**, тапентадол**) [15, 50] (см. Приложение А3. Определение степени печеночной недостаточности и Определение степени нарушения почечной функции). У пациентов с нарушением глотания можно использовать раствор морфина для перорального приема, а также содержимое капсул морфина пролонгированного действия, где морфин представлен в виде микрогранул с замедленным высвобождением, в т.ч. через назогастральный зонд или гастростому. В случае если по объективным причинам прием пероральных форм невозможен, включая случаи отказа пациента от приема лекарств через рот, наличия тошноты или рвоты, непереносимости препаратов морфина или налоксон +оксикодон**, или тапентадола**, терапию начинают с ТТС фентанила**. Имеющиеся данные свидетельствуют об отсутствии значимых различий в анальгетической эффективности между сильными опиоидами, назначаемыми перорально, – морфином** и препаратом налоксон+оксикодон**, и позволяют дать лишь частично обоснованные рекомендации по использованию любого из этих двух препаратов в качестве препарата выбора.
Рекомендуется использовать трансдермальные опиоиды, как альтернативу пероральным препаратам при нарушении функции глотания, тошноте и рвоте, почечной и печеночной недостаточности, отказе пациента от пероральных форм, в случае наличия у пациента сильной боли постоянного характера, когда произведен подбор адекватной обезболивающей суточной дозы опиоидами короткого действия [15].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: трансдермальные опиоиды, имеют показания к назначению у пациентов с сильной персистирующей болью и расстройством функции глотания и при невозможности назначить препараты трансмукозально (защечно или под язык); например, при мукозитах, язвенном или опухолевом поражении слизистой полости рта.
Трансдермальные опиоиды являются средством выбора у пациентов с сохраненной функцией глотания, если сильная боль носит постоянный/персистирующий характер. Согласно анализу, проведенных рандомизированных исследований не было выявлено никаких достоверных различий в эффективности между трансдермальными и пероральными опиоидами, но было отмечено превосходство первых в отношении риска развития запора и предпочтений пациентов. Это свидетельствует о том, что в ряде случаев трансдермальные опиоиды являются удобными и эффективными обезболивающими средствами у пациентов, ранее не получавших сильные опиоиды [15]. Исключениями являются пациенты с выраженной кахексией, повышенным потоотделением, нарушением целостности кожных покровов, высокой температурой тела. В этих ситуациях необходимо оценить целесообразность использования трансдермальных опиоидов и более тщательно контролировать эффективность и безопасность препарата; может потребоваться снижение дозы.
Рекомендуется с осторожностью применять опиоиды у пациентов с печеночной и почечной недостаточностью [15, 29, 34, 35].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: морфин** метаболизируется в печени с образованием активных метаболитов, которые выводятся преимущественно почками – 85%, с желчью – 10%. Из-за особенностей элиминации следует снижать дозу морфина** у пациентов с нарушением кишечного пассажа (при запорах), тяжелых нарушениях функции почек и печени. Фентанил**, в отличие от морфина**, имеет неактивные метаболиты, в связи с чем, является преимущественным препаратом выбора для пациентов со средней и тяжелой степенью нарушения функции почек и печени. Тапентадол** противопоказан пациентам с тяжелой почечной или тяжелой печеночной недостаточностью. (см Приложение А3. Определение степени печеночной недостаточности и Определение степени нарушения почечной функции).
Рекомендуется назначать морфин** парентерально пациентам, которым невозможно по различным причинам обеспечить адекватное обезболивание неинвазивными опиоидами [14, 15, 22, 30].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: имеющиеся данные позволяют дать четко обоснованные рекомендации о том, что подкожный путь введения является простым и эффективным в качестве альтернативного метода у пациентов, неспособных принимать опиоиды пероральным или трансдермальным способами. Внутривенные инфузии применяются в том случае, когда подкожное введение препарата противопоказано (при выраженных периферических отеках, нарушении свертывания крови, нарушении периферического кровообращения и необходимости введения больших объемов и высоких доз препарата) и при необходимости быстрого достижения обезболивания. В отдельных случаях применяется методика постоянной контролируемой анальгезии для подкожных и внутривенных инфузий опиоидов. При переходе с перорального применения морфина** на его подкожное и внутривенное введение, следует учитывать, что относительная анальгезирующая активность одинакова для обоих способов введения и находится в пределах от 3:1 до 2:1 (неинвазивный: инвазивный).
Не рекомендуется использовать тримеперидин** (таблетки, раствор для инъекций) для длительной терапии боли [37].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 2)
Комментарии: тримеперидин** подвергается биотрансформации с образованием нейротоксичного Н-деметилированного метаболита – нормеперидина, который стимулирует ЦНС (возможны тремор, подергивания мышц, гиперрефлексия, судороги). Метаболит имеет длительный период полувыведения (15–20 ч), поэтому может наблюдаться кумулятивный эффект, что особенно часто возникает у онкологических больных, о чем предупреждает ВОЗ, ЕАПП, IASP, рекомендуя сократить время терапии тримеперидином** до 3–5 дней. Ввиду кратковременности эффекта введенной внутримышечно дозы тримеперидина** (в среднем 4 ч) основным показанием к его применению является, острая боль (сильной и средней интенсивности): послеоперационная боль, травмы, ожоги, болевые синдромы в клинике внутренних болезней (нестабильная стенокардия, инфаркт миокарда и др.). При энтеральном применении эффективность тримеперидина** снижается в 2–3 раза, поэтому таблетки тримеперидина** не нашли широкого применения и в лечении острой боли.
3.1.5 Титрование дозы сильного опиоида
Рекомендуется при подборе необходимой дозы базового обезболивания с применением препаратов в пролонгированных формах проводить ее титрование препаратами короткого действия [15, 28, 36].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3).
Комментарии: для подбора дозы сильного опиоида следует использовать препараты в лекарственных формах с немедленным высвобождением вещества. Для этих целей используют морфин** в форме таблеток, покрытых пленочной оболочкой по 5 и 10 мг, раствора для перорального приема или (при невозможности применения неинвазивных форм) раствора для подкожного или внутривенного введения. Анальгетический эффект пероральных форм морфина** с немедленным высвобождением вещества начинается через 30 мин после приема и продолжается около 4-6 ч. После приема первой дозы препарата необходимо определить длительность его действия и, как только боль возобновилась, дать следующую дозу морфина** и продолжать его прием по такому же принципу (при ослаблении эффекта предыдущей дозы). Для пожилых и/или кахектичных пациентов рекомендуется начинать терапию пероральным морфином** с дозы 2,5 - 5 мг. По прошествии суток следует рассчитать необходимую кратность приема перорального морфина** на ближайшие сутки и расписать пациенту схему терапии «по часам». Максимальную эффективность назначенной дозы перорального морфина** следует оценивать через 60-90 мин после приема. Если эффект неудовлетворителен (боль сохраняется), то следует назначить дополнительную дозу морфина** к основной схеме приема, не изменяя плановое время введения следующей дозы. Итоговую эффективную суточную дозу морфина** оценивают путем простого суммирования всех примененных за сутки доз. Если в течение 2-3 дней подобранная суточная доза адекватно контролирует боль, можно перевести пациента на пролонгированные формы морфина** (таблетки или капсулы) или на другие сильные опиоиды в эквивалентной дозе, подобрав нужную разовую дозировку препарата с учетом кратности его введения. Если доза морфина** короткого действия недостаточна, следует продолжить ее постепенное повышение каждый раз не более чем на 30-50% от суточной дозы до достижения полноценного контроля боли или появления трудно контролируемых нежелательных реакций [28, 52]. В последнем случае следует рассмотреть вопрос об изменении лечения (отмене морфина** и использовании другого опиоида, либо уменьшении дозы морфина** и добавлении других препаратов, использование нефармакологических методов и т. д.).
Подбор дозы сильного опиоида у пациентов, которые не могут глотать, можно проводить парентеральным введением морфина** (от 2,5 до 5 мг) с учетом возраста пациента и тяжести состояния.
Почечная недостаточность может привести к накоплению активных метаболитов морфина**, поэтому при ее наличии, следует избегать его назначения и использовать иные опиоиды (например, бупренорфин** или фентанил**). Однако, в отдельных случаях, при наличии легкой или средней степени нарушения функции почек, возможно применение препаратов морфина** в меньших дозах, увеличивая интервалы между приемами (до 6-8 ч.), или применяя последующие дозы только в случае необходимости [52].
Для титрования дозы тапентадола** можно использовать его лекарственную форму с немедленным высвобождением – таблетки, покрытые пленочной оболочкой по 50 мг каждые 4-6 часов; причем при отсутствии эффекта, вторая доза препарата может быть принята через 1 ч после приема начальной дозы.
Для титрования дозы препарата налоксон + оксикодон** используются таблетки пролонгированного действия в дозировке 5 мг/2,5 мг каждые 12 ч; такая схема может быть затруднительна в случае усиления боли в течение интервала дозирования, для купирования которой потребуется применение быстродействующего сильного опиоида (например, морфина**).
3.1.6 Смена (ротация) опиоида
Рекомендуется при переходе с одного опиоида на другой, осуществляемом из-за недостаточного обезболивания и/или трудно контролируемых побочных эффектов или иным причинам, использовать нач
Кроме перечисленных методов терапии боли, всем пациентам и их близким необходимо оказывать психологическую помощь и поддержку. Правильно выстроенная коммуникативная работа с пациентами значительно улучшает психологический статус больного, нивелирует тревожность, уменьшает страхи и способствует снижению интенсивности боли [17, 18].
Организация лечения хронического болевого синдрома осуществляется в соответствии с действующими нормативными правовыми актами, устанавливающими порядок назначения лекарственных препаратов и оформления назначения лечения в медицинской документации пациента и в рецептурных бланках.
В рамках оказания паллиативной первичной доврачебной и врачебной медицинской помощи лечение хронического болевого синдрома, в том числе с назначением лекарственных препаратов, содержащих наркотические средства и психотропные вещества списков II и III Перечня, осуществляется фельдшерами, при условии возложения на них функций лечащего врача и иными медицинскими работниками со средним медицинским образованием фельдшерских здравпунктов, фельдшерско-акушерских пунктов, врачебных амбулаторий, иных медицинских организаций (их структурных подразделений), оказывающих первичную доврачебную медико-санитарную помощь, врачами-терапевтами, врачами терапевтами-участковыми, врачами общей практики (семейными врачами), врачами-специалистами медицинских организаций, оказывающих первичную медико-санитарную помощь, первичную специализированную медицинскую помощь [127].
Лечение хронического болевого синдрома в рамках оказания паллиативной специализированной медицинской помощи, в том числе с назначением лекарственных препаратов, содержащих наркотические средства и психотропные вещества списков II и III Перечня, осуществляется врачами-специалистами, занимающими должность врача по паллиативной медицинской помощи, иными врачами-специалистами, медицинскими работниками со средним профессиональным образованием кабинетов паллиативной медицинской помощи взрослым, отделений выездной патронажной паллиативной медицинской помощи взрослым, отделений паллиативной медицинской помощи взрослым, хосписов для взрослых, отделений сестринского ухода для взрослых, домов (больниц) сестринского ухода для взрослых, дневных стационаров паллиативной медицинской помощи взрослым, респираторных центров для взрослых [127].
При оказании первичной доврачебной и врачебной паллиативной медицинской помощи и паллиативной специализированной медицинской помощи в амбулаторных условиях назначение лекарственных препаратов, в том числе содержащих наркотические средства и психотропные вещества списков II и III Перечня, осуществляется медицинским работником самостоятельно, исходя из тяжести и характера заболевания пациента. Сведения о назначенном лекарственном препарате (наименование лекарственного препарата, дозировка, способ введения и применения, режим дозирования, продолжительность лечения и обоснование назначения лекарственного препарата) вносятся медицинским работником в медицинскую документацию пациента. Медицинский работник оформляет назначение лекарственных препаратов, в том числе содержащих наркотические средства и психотропные вещества списков II и III Перечня, на рецептурном бланке, оформленном на бумажном носителе за своей подписью, и (или) с согласия пациента или его законного представителя на рецептурном бланке в форме электронного документа с использованием усиленной квалифицированной электронной подписи медицинского работника [128].
Назначение лекарственных препаратов по решению врачебной комиссии при оказании первичной доврачебной и врачебной паллиативной медицинской помощи и паллиативной специализированной медицинской помощи в амбулаторных условиях производится в случаях первичного назначения пациенту лекарственных препаратов, содержащих наркотические средства и психотропные вещества списков II и III Перечня (в случае принятия руководителем медицинской организации решения о необходимости согласования назначения таких лекарственных препаратов с врачебной комиссией) [128].
Пациентам с хроническим болевым синдромом любого генеза повторное назначение лекарственных препаратов, содержащих наркотические средства и психотропные вещества списков II и III Перечня, производится медицинским работником самостоятельно [128].
Количество назначенных лекарственных препаратов, включенных в перечень препаратов, подлежащих предметно-количественному учету, при оказании пациентам паллиативной медицинской помощи, может быть увеличено с учетом клинических рекомендаций не более чем в 2 раза по сравнению с количеством наркотических средств или психотропных веществ, которое может быть выписано в одном рецепте [128].
В случаях необходимости оформления рецепта на наркотический (психотропный) лекарственный препарат на дому в рамках оказания паллиативной медицинской помощи допускается предварительное заверение рецепта штампом медицинской организации, печатью медицинской организации либо структурного подразделения медицинской организации "Для рецептов", которая проставляется лицом, уполномоченным руководителем медицинской организации, с указанием фамилии, имени, отчества (последнее - при наличии) и проставлением его личной подписи. Факт оформления рецепта на дому может быть дополнительно подтвержден фото- и (или) видеоматериалами [128].
При оказании скорой медицинской помощи лекарственные препараты, в том числе содержащие наркотические средства и психотропные вещества списков II и III Перечня, назначаются медицинским работником выездной бригады скорой медицинской помощи, медицинским работником медицинской организации при наличии у пациента, признанного нуждающимся в паллиативной медицинской помощи, болевого синдрома, не купируемого имеющимися анальгетиками [129].
При оказании пациенту паллиативной медицинской помощи в стационарных условиях назначение лекарственных препаратов, в том числе содержащих наркотические средства и психотропные вещества списков II и III Перечня, производится медицинским работником единолично, без оформления рецепта [128].
Согласование назначения лекарственных препаратов с заведующим отделением или ответственным дежурным врачом либо другим лицом, уполномоченным приказом главного врача медицинской организации, а также, при наличии, с врачом - клиническим фармакологом необходимо в случаях назначения лекарственных препаратов, в том числе содержащих наркотические средства и психотропные вещества списков II и III Перечня, не входящих в перечень жизненно необходимых и важнейших лекарственных препаратов.
В указанных случаях назначение лекарственных препаратов фиксируется в медицинской документации пациента и заверяется подписью медицинского работника и заведующего отделением (ответственного дежурного врача или другого уполномоченного лица) [128].
По решению врачебной комиссии пациентам при оказании им паллиативной медицинской помощи в стационарных условиях назначаются лекарственные препараты, не включенные в перечень жизненно необходимых и важнейших лекарственных препаратов, в случае их замены из-за индивидуальной непереносимости, по жизненным показаниям.
Решение врачебной комиссии фиксируется в медицинской документации пациента и журнале врачебной комиссии [128].
Медицинский работник медицинской организации (ее структурного подразделения), расположенной в сельском населенном пункте, осуществляет назначение лекарственных препаратов, в том числе содержащих наркотические средства и психотропные вещества списков II и III Перечня, единолично [128].
При выписке пациента из медицинской организации, в которой ему оказывалась паллиативная медицинская помощь в стационарных условиях, данному пациенту по решению руководителя медицинской организации назначаются с оформлением рецепта в форме электронного документа и (или) на бумажном носителе (за исключением оформления рецептов на лекарственные препараты, подлежащие отпуску бесплатно или со скидкой) либо выдаются (пациенту или его законному представителю) одновременно с выпиской из истории болезни лекарственные препараты, в том числе содержащие наркотические средства и психотропные вещества списков II и III Перечня, сильнодействующие лекарственные препараты, на срок приема пациентом до 5 дней [128].
Необходимо осуществлять систематический контроль за соблюдением правил следования алгоритмам диагностики и лечения ХБС, алгоритмам и требованиям оформления медицинской документации. Уполномоченным приказом руководителя медицинской организации лицам проводить ежемесячно выборочный контроль и анализ не менее 10 медицинских карт стационарного (амбулаторного) больного с ХБС, с последующим оформлением итогового заключения по экспертизе оцениваемых случаев.
При наличии показаний больные с ХБС госпитализируются в структурные подразделения медицинских организаций, оказывающие паллиативную специализированную медицинскую помощь в стационарных условиях.
Показаниями для госпитализации больных с ХБС в отделение паллиативной медицинской помощи взрослым являются:
- выраженный болевой синдром, не поддающийся лечению в амбулаторных условиях, в том числе на дому или в стационарных организациях социального обслуживания;
- подбор схемы обезболивающей терапии для продолжения лечения на дому.
Показаниями для госпитализации больных с ХБС в хоспис для взрослых являются:
- выраженный болевой синдром в терминальной стадии заболевания преимущественно у пациентов с онкологическими заболеваниями, не поддающийся лечению в амбулаторных условиях, в том числе на дому или в стационарных организациях социального обслуживания;
- необходимость подбора схемы терапии для продолжения лечения на дому [127].
Показаниями для выписки больных с ХБС из отделения паллиативной медицинской помощи взрослым и хосписа для взрослых являются:
- достижение адекватного обезболивания;
- подбор оптимальной схемы обезболивающей терапии с точки зрения эффективности и переносимости.
Информация отсутствует













