Синдром слабости синусового узла (СССУ) – состояние, обусловленное снижением функциональной способности синусового узла выполнять функцию основного водителя ритма и\или обеспечивать регулярное проведение импульсов к предсердиям, что предопределяет появление выраженной брадикардии и сопутствующих эктопических аритмий.
СССУ в большинстве случаев у детей развивается в отсутствие органической патологии сердечно-сосудистой системы. Нарушения ритмовождения в детском возрасте могут быть обусловлены различными факторами: вегетативным дисбалансом с преобладанием парасимпатических влияний, медикаментозным воздействием, воспалительным поражением миокарда, нарушением обмена, аутоиммунным поражением антителами к проводящей системе сердца [1, 2, 3, 4]. По этиологическим факторам выявляют:
СССУ органической природы (при миокардитах, кардиомиопатиях, амилоидозе, саркоидозе, коллагенозах, врожденных пороках сердца и сосудов, питающих синоатриальную зону, ишемической болезни сердца, опухолях сердца, гормонально-обменных кардиотоксических нарушениях и т.д., обусловливающих замещение функционирующих синоатриальных клеток соединительной тканью).
Регуляторные (вагусные) дисфункции синусового узла (вегетативная дисфункция с преобладанием парасимпатических влияний на сердце гипоксического характера, при спортивном перенапряжении, повышении внутричерепного давления, отеке мозга, висцеровагальные рефлексы при патологии глотки, мочеполовой и пищеварительной системы).
СССУ как следствие токсических влияний (бета-адреноблокаторов, селективных блокаторов кальциевых каналов с преимущественным действием на сосуды, сердечных гликозидов, антидепрессантов, снотворных и седативных средств, отравления карбофосом и антихолинэстеразными средствами и др.).
Нарушение функции синусового узла (СУ) у детей после хирургических операций на сердце (коррекция врожденных пороков сердца - транспозиции магистральных сосудов, дефекта межпредсердной перегородки и др.).
Аутоиммунные нарушения функции СУ.
Генетически детерминированное нарушение функции СУ.
Идиопатические (причина не установлена).
В первых пяти случаях имеет место так называемый, вторичный СССУ, устранение которого находится в прямой зависимости от эффективности терапии основного заболевания. В случаях, когда не удается обнаружить кого-либо заболевания, способного привести к нарушению функции СУ, принято говорить о идиопатическом варианте.
Среди патогенетических механизмов в развитии идиопатического СССУ обсуждается значение вегетативной нервной системы, дегенеративных изменений, апоптоза, а также роль воспалительного поражения миокарда. Значение недостаточности симпатических влияний на сердце в патогенезе прогрессирующего нарушения функции синусового узла у детей доказано, при этом в формировании нарушений вегетативной регуляции сердца важная роль принадлежит гипоксическим поражениям в перинатальном периоде [5]. В экспериментальных работах создана модель развития СССУ, в которой прогрессивное нарастание выраженности электрокардиографических изменений ассоциировалось с ослаблением влияний центральной нервной системы на ритмогенез [6].
Активно дискутируется вопрос о роли аутоиммунных механизмов в развитии и прогрессировании СССУ. Уровень антикардиальных аутоантител к СУ и атриовентрикулярному (АВ) узлу [7, 8] может быть одним из факторов в патогенезе развития нарушений сердечного ритма. Показана значимость аутоиммунных процессов в развитии фибрилляции предсердий, которая часто регистрируется у пациентов с СССУ [9]. В литературе имеются работы, описывающие устойчивую связь морфологических признаков миокардита по данным биопсии с уровнями аутоантител у пациентов с аритмиями, а иммунная активность коррелирует с выраженностью нарушений ритма [10, 11]. Для изучения аутоиммунного генеза воспалительных явлений в миокарде может быть применено выявление циркулирующих аутоантител как неселективных - к миокарду, так и селективных к белкам кардиомиоцитов актину и миозину, антифибрилляторные, антисарколемные, к мускариновым и адренорецепторам. Повышение титров антикардиальных антител у больных наряду с вегетативной дисфункцией может являться одним из звеньев патогенеза СССУ у детей [12].
К настоящему моменту описано большое количество вариантов и полиморфизмов в генах, ассоциированных с развитием СССУ - SCN5A, HCN4, MYH6, ANK2, TRPM4, NKX2-5, TBX3 и др. [13-17]. Генетические механизмы развития синусовой брадикардии и СССУ можно разделить на нарушения функции ионных каналов, межклеточных соединений, внутриклеточных белков миозина, анкирина, генов-регуляторов и др. [18]. Наличие мутаций может предрасположить к развитию дисфункции СУ или привести к повышенной чувствительности клеток СУ к препаратам.
Распространенность СССУ оценить сложно из-за невозможности учета бессимптомных случаев и трудностей диагностики патологической брадикардии в популяционных исследованиях. Частота выявления СССУ растет с возрастом, но в группе старше 50 лет она составляет всего 5/3000 (0,17%). В детской популяции СССУ составляет до 30% всех аритмий [5]. На долю СССУ приходится около половины всех имплантаций электрокардиостимуляторов (ЭКС), но число имплантаций неадекватно оценивает частоту симптоматичных случаев СССУ. В хирургических клиниках с СССУ связывают около 10% всех нарушений сердечного ритма [19]. Распространенность электрокардиографических (ЭКГ) феноменов, являющихся частью симптомокомплекса СССУ, достигает 0,84% среди детей с заболеваниями сердечно-сосудистой системы [20]. Среди практически здоровых детей признаки дисфункции СУ на стандартной ЭКГ выявляются у 2% детей [5]. Синусовая брадикардия является самой частой (до 85%) разновидностью брадиаритмий у детей [21]. По данным популяционного ЭКГ-скрининга детей России распространенность миграции ритма составляет 1,9%, выскальзывающих и замещающих наджелудочковых ритмов – 0,7%, а синоатриальной блокады - 0,3% [22].
Холтеровское мониторирование ритма (ХМ) выявляет значительно более высокую распространенность ЭКГ феноменов, входящих в симптомокомплекс СССУ у практически здоровых детей. При проведении ХМ признаки дисфункции синусового узла встречаются в 2,7% случаев [5]. Одиночные узловые сокращения в ночное время регистрируются у 13% детей [23], а узловые ритмы у 19% новорожденных и 45% детей более старщего возраста [24, 25]. Среди детей с брадиаритмиями синоатриальные блокады отмечены в 50% случаев [21].
I49.5 — Синдром слабости синусового узла
У детей выделены 4 устойчивых клинико-электрокардиографических варианта нарушения функции СУ (таблица 1): первый с минимальными проявлениями в виде синусовой брадикардии и миграции ритма; второй - замещающие ритмы, остановки СУ, синоатриальные блокады на фоне более выраженной депрессии основного ритма; третий (синдром тахи-брадикардии) – сочетание синусовой брадикардии с суправентрикулярной гетеротопной тахикардией и четвертый – кардионейропатию с ригидной выраженной брадикардией, множеством замещающих ритмов, асистолиями и нарушением реполяризации миокарда [5, 26].
Каждый из вариантов в достаточно высоком проценте случаев характеризуется присоединением нарушений атриовентрикулярного (АВ) проведения. Имеет место стадийность формирования нарушений функции СУ у детей: от первого ко второму (или третьему, в зависимости от наличия электрофизиологических условий для развития тахиаритмий) и четвертому вариантам.
Таблица 1. Клинико-электрокардиографические варианты синдрома слабости синусового узла у детей
Нарушения функции синусового узла |
Нарушение функции нижележащих уровней проводящей системы сердца |
|---|---|
I вариант. Синусовая брадикардия с ЧСС на 20% ниже возрастной нормы, миграция водителя ритма. Паузы ритма при ХМ до 1500 мс. Адекватное учащение ЧСС при физической нагрузке |
Замедление атриовентрикулярного проведения до АВ блокады I степени. Альтернация АВ проведения |
II вариант. Синоатриальная блокада, остановка синусового узла, выскальзывающие сокращения и ускоренные ритмы. Паузы ритма при ХМ от 1500 мс до 2000 мс. Неадекватный прирост ЧСС при нагрузке |
Атриовентрикулярная диссоциация, атриовентрикулярная блокада II-III степени |
III вариант. Синдром тахи-брадикардии. Паузы ритма при ХМ от 1500 мс до 2000 мс |
Атриовентрикулярная диссоциация, атриовентрикулярная блокада II-III степени |
IV вариант. Ригидная синусовая брадикардия с ЧСС менее 40 уд/мин, эктопические ритмы с единичными синусовыми комплексами, мерцание-трепетание предсердий. Отсутствие восстановления устойчивого синусового ритма и адекватного его учащения при физической нагрузке. Паузы ритма при ХМ более 2000 мс |
Нарушения атриовентрикулярного и внутрижелудочкового проведения. Вторичное удлинение интервала QT. Нарушение процесса реполяризации (депрессия сегмента ST, снижение амплитуды T в левых грудных отведениях) |
Клинические проявления СССУ у детей не являются специфическими, часто могут отсутствовать. Чаще всего дети жалуются на головокружения, плохую переносимость физических нагрузок, одышку при нагрузке, утомляемость и эпизоды слабости. Наиболее угрожающими проявлениями СССУ являются аритмогенные обморочные состояния и внезапная сердечная смерть [27], однако слабая корреляция длительности пауз ритма и клинической симптоматики у детей не позволяет зачастую прогнозировать внезапную смерть.
Синкопальные состояния (приступы Морганьи-Адамса-Стокса) - нарушение сознания вследствие ишемии головного мозга при внезапном уменьшении сердечного выброса, обусловленном остро возникшим нарушением сердечного ритма и проводимости (арест/остановка синусового узла, полная АВ-блокада и т.д.). У пациентов появляется внезапная резкая слабость и головокружение, потеря сознания, бледность, липкий холодный пот, могут быть отмечены тонические и клонические судороги, непроизвольные мочеиспускание и дефекация. Аритмогенные синкопальные состояния требуют дифференциального диагноза с рефлекторными синкопальными состояниями и эпилептическим приступом [28, 29]. У детей с начальными проявлениями СССУ могут отмечаться рефлекторные обморочные состояния, развивающиеся в результате резкого падения общего периферического сосудистого сопротивления или артериального давления (АД), а аритмогенные обмороки наблюдаются чаще у детей с IV и III вариантами заболевания [12].
Критерии установления диагноза/состояния:
Диагноз СССУ рекомендовано устанавливать в соответствии с классификацией, представленной в разделе 1.5. на основании документированного подтверждения любым из инструментальных методов исследования (ЭКГ и/или ХМ) в сочетании\без с клинической симптоматикой [5, 12, 26, 30-32].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 4)
Принципы формулировки диагноза.
В диагнозе указывается основное состояние – СССУ, вариант заболевания (см. классификацию в 1.5): синусовая брадикардия, остановка синусового узла, синдром тахи-брадикардии.
Примеры формулировки диагноза:
Синдром слабости синусового узла (брадикардия, остановки синусового узла, выскальзывающие наджелудочковые сокращения, паузы ритма до 1850 мс).
Синдром слабости синусового узла (синдром тахи-брадикардии: узловая тахикардия, брадикардия, остановки синусового узла, паузы ритма до 2000 мс).
-
Рекомендуется при сборе анамнеза у всех пациентов с подозреваемым или установленным СССУ:
установить наличие патогномоничных для нарушения мозговой перфузии жалоб;
уточнить характер синкопальных и пресинкопальных состояний: возраст появления, наличие патологии перинатального периода, связь с перенесенными острыми заболеваниями и наличием хронических, провоцирующими факторами, приемом лекарственных препаратов; наличие ауры, субъективных ощущений предобморока, судорог и непроизвольного мочеиспускания во время синкопе, результаты измерения частоты сердцебиения и измерения артериального давления на периферических артериях во время обморока, продолжительность синкопе и способы купирования;
оценить наличие и степень выраженности брадикардии, нарушений сердечного ритма на ретроспективных ЭКГ пациента;
провести анализ ЭКГ родственников на предмет наличия наследственной брадикардии, нарушений сердечного ритма [5, 12, 26, 30, 31].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 4)
Рекомендовано пациентам с подозреваемым или установленным СССУ при проведении стандартного клинического осмотра провести оценку физического развития - измерение роста и массы тела, полового соответствия возрасту, определение функционального состояния органов и систем – термометрия общая, измерение частоты дыхания, измерение частоты сердцебиения, аритмий при аускультации сердца, измерение артериального давления на периферических артериях, а также выявление признаков сердечной недостаточности и стигм дисэмбриогенеза [30, 32, 33].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 5)
Комментарий: При длительно существующей брадикардии может наблюдаться бледность кожных покровов. Брадикардия может определяться при пальпации пульса на периферических артериях, но наиболее информативным является аускультация сердца, когда выслушиваются редкие сердечные тоны.
Специфической лабораторной диагностики СССУ не существует. У пациентов с брадиаритмиями рекомендованы лабораторные исследования, основанные на клиническом подозрении на потенциальную основную причину СССУ.
Рекомендуется пациентам с подозреваемым или установленным СССУ проведение общего (клинического) анализа крови, общего (клинического) анализа мочи, анализа крови биохимического общетерапевтического, исследование уровня калия, натрия, общего и ионизированного кальция в крови, определение активности лактатдегидрогеназы, аспартатаминотрансферазы, аланинаминотрансферазы и креатинкиназы в крови, исследование уровня/активности изоферментов креатинкиназы в крови, исследование уровня тропонинов I,Т в крови для исключения воспалительного генеза заболевания [2, 3, 32, 34-35].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 5)
Рекомендуется пациентам с подозреваемым или установленным СССУ определить уровень тиреотропного гормона (ТТГ) в крови, уровень свободного тироксина (СТ4) сыворотки крови, содержание антител к тиреоидной пероксидазе в крови для исключения вторичного генеза заболевания [2, 3, 30, 32, 36].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 5)
Рекомендуется пациентам с подозреваемым или установленным СССУ проведение иммунологического исследования для определения уровня специфических селективных или неселективных аутоантител к антигенам проводящей системы сердца, кардиомиоцитам (антифибриллярные, антисарколеммные), гладкой мускулатуре и эндотелию сосудистой стенки, мускариновым и адренорецепторам, определение содержания антинуклеарных антител к Sm-антигену для исключения или подтверждения аутоиммунных причин заболевания [7, 12].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 5)
Комментарий: Повышение титров антикардиальных антител у больных с высокими степенями поражения синусового узла может являться одним из звеньев патогенеза СССУ у детей, хотя убедительных доказательств этому факту нет, или свидетельствовать о течении аутоиммунного миокардита (в том случае если имеются другие признаки миокардита).
Рекомендуется другие методы диагностики, направленные на выявление потенциальной причины развития у пациентов с установленным диагнозом СССУ с подозрением на воспалительный генез для исключения или подтверждения данной причины [2, 3, 21, 32].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 5)
Комментарий: Исследования проводятся с целью выявления бактериальной или вирусной инфекции, которая может быть источником развития воспалительного процесса в миокарде. Также может быть проведено определение антистрептолизина-О в сыворотке крови, исследование микробиоценоза кишечника (дисбактериоз), микробиологическое (культуральное) исследование слизи с миндалин, задней стенки глотки на аэробные и факультативно-анаэробные микроорганизмы. Выявление циркулирующей инфекции может свидетельствовать о вторичном (воспалительном) генезе брадиаритмии и требовать антибактериальной или другой специфической терапии.
Рекомендуется регистрация ЭКГ в 12 отведениях у пациентов с подозреваемым или установленным СССУ для регистрации ЧСС, источника ритма и нарушений ритма и проводимости [1, 21, 27-29, 32, 37].
Уровень убедительности рекомендаций – УУР B (уровень достоверности доказательств – УДД 3)
Комментарий: ЭКГ рекомендуется как основной метод диагностики СССУ. ЭКГ критерии синусовой брадикардии по данным стандартной ЭКГ представлены в табл. 2. Более информативно Холтеровское мониторирование сердечного ритма, позволяющее выявить нарушения и признаки, с высокой вероятностью указывающие на риск развития каналопатий и других врожденных нарушений ритма и проводимости. Регистрация ЭКГ покоя обязательна перед выполнением таких исследований, как ХМ сердечного ритма, ЭКГ с физической нагрузкой и др.
Таблица 2. Минимально допустимые значения ЧСС по данным ЭКГ покоя у здоровых детей в возрасте от 0 до 18 лет [22]
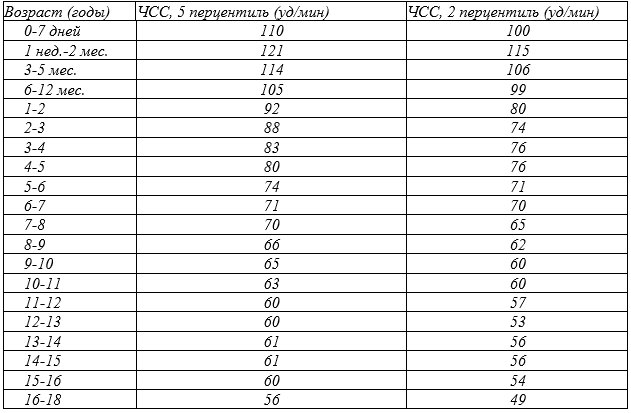
Брадикардией в различных возрастных группах традиционно считается снижение ЧСС на стандартной ЭКГ ниже 5 перцентиля возрастного распределения ЧСС. Более оправдано считать критерием брадикардии снижение ниже 2 перцентиля, которое у детей ассоциируется с высоким риском развития СССУ и появлением синкопальных состояний [12].
Пациентам с подозреваемым или установленным СССУ рекомендуется проведение Холтеровское мониторирования сердечного ритма (ХМ) с целью регистрации ЧСС и аритмий, диагностики метаболических изменений в миокарде, оценки вариабельности ритма и вегетативных влияний на сердечный ритм, а также выявления маркеров риска жизнеугрожающих состояний и оценки эффективности лечения [1, 21, 27-29, 38].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 5)
Комментарий:. Существует несколько видов амбулаторного мониторирования ЭКГ. Холтеровское мониторирование позволяет проводить наблюдение за ритмом сердца на протяжении 24–48 часов, имеются варианты регистрирующих ЭКГ устройств с длительностью записи до 7 суток. Другой разновидностью является запись ЭКГ в момент события (обморока, приступа сердцебиения) с помощью портативных регистраторов, объединяемых под общим названием «амбулаторные событийные регистраторы».
Важная роль в ранней диагностике и прогнозировании СССУ принадлежит оценке допустимых значений минимальной ЧСС при ХМ (табл. 3). Степень снижения средней ЧСС в дневное и ночное время позволяет дифференцировать патологическую и физиологическую брадикардию. Для физиологической брадикардии характерно снижение ЧСС в ночное время, в то время как средняя дневная и средняя суточная ЧСС остаются в пределах нормы.
Таблица 3. Минимально допустимые значения ЧСС по данным ХМ у здоровых детей 0-16 лет [24, 25, 39-42].
Возраст |
Мин. ЧСС в ночное время (уд/мин) |
Мин. ЧСС в дневное время (уд/мин) |
|---|---|---|
Дети 0-1 мес. |
69-70 |
80 |
1 мес.- 1 год |
65-69 |
80 |
1 - 6 лет |
60 |
- |
7 – 10 лет |
45 |
- |
10-11 лет |
40-45 |
- |
12-16 лет |
40 |
- |
У детей с выраженными брадиаритмиями паузы ритма при проведении ХМ, как правило, превышают допустимые значения, что является важным диагностическим и прогностическим критерием. Также как и ЧСС, продолжительность пауз ритма по данным ХМ оценивается с учетом возраста ребенка (табл. 4).
Таблица 4. Максимальная допустимая продолжительность пауз ритма по данным ХМ у здоровых детей 0-16 лет [24, 40, 41]
Возраст |
Максимальная продолжительность пауз ритма (мс) |
|---|---|
Дети до 1 года |
1100 |
1-3 года |
1200 |
3-10 лет |
1300 |
10-16 лет |
1500 |
> 16 лет |
1750 |
> 18 лет |
2020 |
На ЭКГ детей с СССУ, помимо синусовой брадикардии, могут быть зарегистрированы различные наджелудочковые тахиаритмии (наджелудочковые тахикардии, фибрилляция предсердий, одиночная или парная экстрасистолия).
Миграция водителя ритма, замещающие сокращения и/или ритмы из АВ соединения возникают как результат ослабления пейсмекерной функции синусового узла и являются вторичными. Среди других нарушений ритма и проводимости при СССУ встречается ускоренный суправентрикулярный ритм. Эпизоды суправентрикулярного ритма у детей требуют исключения синдрома слабости синусового узла по типу тахи-брадикардии.
Синоатриальная блокада проявляется прогрессивным нарастанием блокады синоатриального проведения, тогда как функция образования импульса в синусовом узле не изменяется. Синоатриальная блокада различается по степени тяжести. Первая степень характеризуется замедлением проведения возбуждения внутри синусового узла и на стандартной ЭКГ не регистрируется. Вторая степень может быть с периодикой Венкебаха или без нее - при этом некоторые из импульсов блокируются и не проводятся на предсердия. Третья степень характеризуется нарушением проведения импульсов нормальной генерации к миокарду правого предсердия. Характерно появление при этом выскальзывающих заместительных сокращений из нижележащих центров автоматизма.
Остановка СУ (синус-арест) - потеря синусовым узлом способности генерации импульсов в пейсмекерных клетках синусового узла. В отличие от синоатриальной блокады, при этом развивается пауза ритма, превышающая предшествующий R-R интервал более чем в 2 раза и не кратная ему.
Рекомендуется применение имплантируемого кардиомонитора для долговременной регистрации электрической активности проводящей системы сердца пациентам с установленным или подозреваемым СССУ для установления корреляции между частотой сердечных сокращений или нарушениями проводимости с симптомами [27-29, 38].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 5)
Комментарий: Имплантируемый кардиомонитор для долговременной регистрации электрической активности проводящей системы сердца (ИКМ) способен фиксировать фрагменты записи на протяжении до 3 лет [27, 38], однако, у педиатрического контингента в настоящее время эта методика применяется недостаточно, несмотря на неплохую эффективность до 56% у пациентов с синкопальными состояниями в анамнезе для регистрации ЧСС в момент появления клинической симптоматики [43]. Диагностическая ценность применения ИКМ для выявления нарушения ритма как причины синкопе значительно выше, чем однократного 24- часового ХМ. Несмотря на отсутствие признаков нарушения функции синусового узла по данным ХМ вне приступа, во время обморока может развиться критическая брадикардия или асистолия. «Золотым стандартом» диагностики синкопальных состояний как аритмогенного, так и нейрокардиогенного характера, остается регистрация ЭКГ в момент развития типичных жалоб, в том числе в провоцирующей ситуации. При необходимости зарегистрировать ЭКГ в момент жалоб следует ориентироваться на частоту развития клинических симптомов, предположительно связанных с брадикардиями или нарушениями проводимости [38]. В случае ежедневных или еженедельных приступов следует отдать предпочтение проведению однократного или многократного Холтеровского мониторирования сердечного ритма, госпитальному мониторированию или телеметрической регистрации ЭКГ. При ежемесячных приступах потери сознания можно рассматривать многократное проведение Холтеровского мониторирования сердечного ритма, телеметрическую регистрацию или применение других устройств регистрации ЭКГ [44, 45]. Если приступы развиваются с частотой 1 раз в мес или реже предпочтительно использование ИКМ.
Пациентам с установленным или подозреваемым СССУ рекомендуется проведение трансторакальной эхокардиографии (ЭхоКГ) для исключения органической патологии сердца, оценки морфометрических показателей, выявления признаков аритмогенной кардиомиопатии [1, 21, 28, 29, 46].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 5)
Комментарии: Под аритмогенной кардиомиопатией подразумевают вторичную обратимую дисфункцию миокарда, проявляющуюся дилатацией всех полостей, начиная с предсердных камер, с последующим снижением сократительной способности миокарда желудочков, возникновением относительной митральной регургитации и развитием застойной сердечной недостаточности, которая развивается в результате существующей брадикардии. Максимальную диагностическую значимость ЭхоКГ демонстрирует у пациентов с органическими заболеваниями сердца [47].
У отдельных пациентов с СССУ для расширенной визуализации рекомендована чреспищеводная эхокардиография, магнитно-резонансная томография сердца и магистральных сосудов или других исследований для исключения наличия структурного заболевания [21, 28, 29].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 5)
У симптомных пациентов с подозрением на СССУ внутрисердечное электрофизиологическое исследование (ЭФИ) для оценки функции СУ рекомендовано для установки диагноза, если диагноз остается неопределенным после проведения неинвазивного обследования [21, 48].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 5)
У пациентов, которым проводят ЭФИ по другим показаниям, рекомендуется оценка функции СУ узла для установки диагноза СССУ [21, 28, 49].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 5)
У пациентов с подозрением на диагноз СССУ рекомендуется проведение чреспищеводной электрокардиостимуляции (ЧПЭС) в качестве альтернативы инвазивному ЭФИ для оценки функции СУ и установки диагноза СССУ, если диагноз остается неопределенным после проведения неинвазивного обследования [21, 48, 50].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 5)
Комментарий: ЧПЭС – малоинвазивное исследование, позволяющее оценить функцию синусового узла. Возможность электрической стимуляции сердца через пищевод определяется его анатомической близостью в средней трети к левому предсердию. Проба оценивает время восстановления функции синусового узла (ВВФСУ) – время от последнего электростимула до первого синусового зубца Р в мс, корригированное время восстановления функции синусового узла (КВВФСУ) – разницу между продолжительностью ВВФСУ и интервалом R-R собственного ритма в мс. В случае, если показатели ВВФСУ и КВВФСУ превышают нормальные значения, то это свидетельствует о снижении автоматической активности СУ. Нормативные значения электрофизиологических показателей функции СУ в различных возрастных категориях детей представлены в табл.5
Таблица 5. Нормативные значения электрофизиологических показателей функции синусового узла [48]
Возраст\показатель |
ВВФСУ (мс) |
КВВФСУ (мс) |
|---|---|---|
Дети до 7 лет |
1220 |
460 |
Дети 7-10 лет |
1240 |
480 |
Дети 11-14 лет |
1300 |
490 |
Дети 15-17 лет |
1400 |
520 |
Наличие нормальных значений параметров чреспищеводной электростимуляции, даже с дополнительным устранением вегетативных влияний (проведение денервации лекарственными препаратами) не позволяет исключить наличие дисфункции синусового узла. Таким образом, ЧПЭС не имеет достаточной прогностической ценности и может быть применена в сложных случаях как дополнительный метод диагностики.
У пациентов с установленным диагнозом СССУ с подозрением на наследственную природу СССУ для исключения или подтверждения данной причины рекомендуется консультация врача-генетика [16, 17, 46, 51].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 5)
Комментарий: Консультация врача-генетика определит необходимость, сроки и методику проведения у пациента молекулярно-генетического анализа для выявления мутаций и полиморфизмом генов, ассоциированных с развитием СССУ, а также при необходимости проведение каскадного скрининга родственников. [13-17, 46, 51, 52]. При проведении молекулярно-генетического анализа может быть применен комплекс исследований пробанда с валидацией одной или нескольких мутации, выявленных методом высокопроизводительного секвенирования, методом секвенирования по Сэнгеру у членов ядерной семьи. Родственники первой степени родства пациентов с выявленными мутациями в генах, ассоциированных с развитием СССУ, также могут быть направлены на генетическое консультирование и тестирование на наличие специфичных мутаций с целью выявления аналогичных заболеваний [16, 17, 46, 51, 52].
Дифференциальная диагностика
Для дифференциальной диагностики СССУ и вегетативных дисфункций синусового узла применяются дополнительные пробы.
Пациентам с установленным или подозреваемым СССУ рекомендуется проводить электрокардиографию с физической нагрузкой для оценки ответа СУ на нагрузки или для выявления клинических симптомов брадиаритмии, провоцируемых физической нагрузкой [5, 21, 26, 31, 32, 33, 49].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 4)
Комментарий: В норме при проведении минимальной физической нагрузки (10-15 приседаний) ЧСС увеличивается на 10-15% от исходных значений [33]. Избыточная реакция ЧСС при исключении других причин свидетельствует о наличии синдрома постуральной тахикардии. Недостаточный прирост ЧСС при физической нагрузке – признак хронотропной недостаточности, или некомпетентности, типичный маркер СССУ. Прирост ЧСС менее 10% от исходных значений при проведении пробы с минимальной физической нагрузкой свидетельствует о наличии СССУ и наряду с появлением нарушений сердечного ритма и нарушений процессов реполяризации является прогностически неблагоприятным фактором [5].
К методикам выполнения динамических физических нагрузок относятся велоэргометрия с использованием велоэргометра, тредмил-тест (беговая дорожка) и др. В педиатрии чаще применяется наиболее физиологичный тест с однократной физической нагрузкой меняющейся интенсивности - тредмил-тест. Самым распространенным является протокол Bruce с базовой ступенью, разминкой и периодом восстановления. Возможно также применение протоколов с постоянной нагрузкой или тест с 6-минутной ходьбой при снижении толерантности к физической нагрузке [53]. Максимальная диагностическая значимость тестов с динамическими физическими нагрузками отмечается у пациентов с обморочными состояниями во время нагрузки или сразу после нее [53, 54]. Значения максимальной ЧСС при проведении теста с физической нагрузкой вычисляется по формуле 208 - 0.7 x возраст в годах [55]. Прирост ЧСС при проведении стресс-теста достигает в норме 70-85% от исходных значений ЧСС [53]. У взрослых пациентов для диагностики хронотропной несостоятельности определяется хронотропный индекс, вычисляемый как отношение разности между пиковой ЧСС на максимуме нагрузки и ЧСС покоя (хронотропный ответ) к разности между предсказанной по возрасту максимальной ЧСС (формуле 220 – возраст (имп/ мин), и ЧСС покоя (хронотропный резерв, в норме ≥80%) [56]. Как правило, максимальная ЧСС сердечного ритма в ответ нагрузку у здоровых детей и подростков достигает 170-180 в минуту. Недостаточным считается прирост ЧСС при проведении пробы с физической нагрузкой менее 170 уд/мин. Однако, у пациентов с СССУ при проведении дозированной физической нагрузки ЧСС возрастает максимально до 120 в минуту, с III-IV вариантами СССУ – до 100-110 уд/мин. [12, 31]. Если синусовая брадикардия связана с повышением активности парасимпатической системы, то прирост ЧСС более выражен. Критерием наличия СССУ при проведении пробы с дозированной физической нагрузкой у детей может быть снижение ЧСС ниже исхода при ее прекращении, а также недостаточный прирост ЧСС при проведении пробы [12, 31]. При проведении пробы с дозированной физической нагрузкой для пациентов с СССУ также характерно появление на 1-3 минуте восстановительного периода аритмий, не регистрируемых в исходе (ускоренных эктопических ритмов, тахи-брадикардии).
Пациентам с установленным или подозреваемым СССУ рекомендуется проведение ортостатической пробы для исключения возможного рефлекторного генеза синкопе [5, 12, 31, 33].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 4)
Комментарий: Нормальная реакция определяется отсутствием жалоб, повышением ЧСС на 20-40% от исходной, кратковременным подъемом АД на 5-10 мм.рт.ст при вставании и возвращением к исходным значениям через 1-3 минуты при горизонтальном положении, а также снижением пульсового давления в процессе выполнения пробы не более чем на 50% [33]. Патологические варианты активной клиноортостатической пробы - гиперсимпатикотонический и тахикардитический, характеризующие избыточное, асимпатикотонический и гипердиастолический – недостаточное, астеносимпатический и симпатоастенический – смешанное вегетативное обеспечение. У детей с СССУ и синкопальными состониями чаще отмечается недостаточное вегетативное обеспечение (преимущественно гипердиастолическое) при проведении активной клиноортостатической пробы, что является дополнительным подтверждением значимости вегетативных влияний в патогенезе синкопе у детей с СССУ [12, 31].
Пациентам с СССУ и синкопальными состояниями неясного генеза рекомендована пассивная длительная ортостатическая проба (тилт-тест) после исключения кардиальных причин обмороков для исключения возможного рефлекторного генеза синкопе [28, 29, 57, 58].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 4)
Комментарий: Для проведения длительной ортостатической пробы (тилт-теста) используют специализированный поворотный стол, который позволяет переводить пациента из горизонтального в вертикальное положение, постоянно регистрируя ЧСС и АД. У пациентов детского возраста пассивная длительная ортостатическая проба применяется ограниченно из-за невысокой чувствительности [57-60], однако, выявлены следующие особенности проведения пробы: угол поворота стола должен составлять 60 º, а оптимальная длительность пробы не должна превышать 30 минут у детей до 12 лет, и 40 минут - у детей старше 12 лет [57, 58].
Пациентам с установленным или подозреваемым СССУ рекомендовано проведение пробы с лекарственным препаратом группы Алкалоиды белладонны, третичные амины #Атропином** для устранения парасимпатических влияний на ритм сердца и исключения вегетативных дисфункций СУ [5, 26, 31-33].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 4)
Комментарий: Внутривенно вводится 0,1% раствор #Атропина** в дозе 0,02 мг\кг. Через 1, 3 и 5 минут после введения проводится оценка ритма и прироста ЧСС по сравнению с исходом, а затем контроль возврата ЧСС к исходу. В норме после введения #Атропина** должен наблюдаться устойчивый синусовый ритм с ЧСС, соответствуюшей возрасту, а относительный прирост ЧСС должен составлять не менее 30% [26, 33]. При недостаточном приросте ЧСС после введения препарата у больного диагностируется СССУ.
Лечение целесообразно разделить на коррекцию острых состояний и плановое лечение брадиаритмии. При острых состояниях проводится медикаментозная терапия и временная электрокардиостимуляция сердца. При хронических состояниях — постоянная электрокардиостимуляция сердца.
Пациентам с установленным СССУ рекомендована оценка состояния и лечение обратимых причин [38].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 5)
Комментарий: В разделе 1.2 представлены причины развития вторичного СССУ, лечение которого зависит от терапии основного заболевания, вызвавшего синдром.
3.1 Консервативное лечение
Пациентам с СССУ с симптомами или гемодинамически нестабильным состоянием с целью увеличения ЧСС и устранения симптомов рекомендовано введение препарата группы Алкалоиды белладонны, третичные амины #Aтропина** [32, 50, 61-64].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 5)
Комментарий: Препарат группы Алкалоиды белладонны, третичные амины #Aтропин** вводится в дозе 0,01-0,02 мг/кг внутривенно, минимальная доза 0,1 мг; максимальная однократная доза 0,5 мг для детей и 1 мг для подростков. Доза может быть введена повторно через 5 минут до максимальной общей дозы 1 мг у детей и 2 мг у подростков [32, 50, 61-64].
Пациентам с СССУ и симптомами или гемодинамически нестабильным состоянием с целью увеличения ЧСС и устранения симптомов рекомендовано введение Адренергического и дофаминергического средства #Эпинефрина** [32, 50, 61-64].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 5)
Комментарий: Адренергическое и дофаминергическое средство #Эпинефрин** вводится внутримышечно или внутривенно или внутрисердечно в дозе 10 мкг/кг (0,01 мг/кг) для первой и последующих доз. При необходимости можно повторять каждые 3-5 мин, но максимальная доза 1 мг. Возможен расчет по возрасту при применении 0,1% раствора в дозе 0,05 мг х год жизни [32, 50, 61-64].
Критические ситуации при развитии головокружений, синкопальных состояний, обусловленных брадикардией или асистолией, купируются применением препаратов группы Алкалоиды белладонны, третичные амины и Адренергические и дофаминергические средства. В табл.6 перечислены международные названия препаратов, коды АТХ, дозировки и пути введения лекарственных препаратов, применяемых для купирования острых ситуаций у пациентов с СССУ. Однако, группы Алкалоиды белладонны, третичные амины и Адренергические и дофаминергические средства не могут постоянно применяться, так как угнетают собственную активность синусового узла и повышают потребность миокарда в кислороде, вызывают такие побочные эффекты как гипотензия и желудочковые аритмии. В приложении А3.2 кроме дозировок и схем применения также представлены механизмы, побочные эффекты и межлекарственные взаимодействия препаратов, используемых при неотложной терапии детей с CCCУ.
Таблица 6. Лекарственные препараты, используемые для купирования острых ситуаций у пациентов с СССУ
Международное непатентованное название препарата |
Код АТХ |
Доза и пути введения препарата |
|---|---|---|
#Atropine** (Атропин) |
A03BA01 |
В экстренных случаях внутривенно 0,1% раствор в дозе 0,01-0,02 мг/кг. Максимальная доза 0,5 мг у детей и 1 мг у подростков. Доза может быть введена повторно через 5 минут до максимальной общей дозы 1 мг у детей и 2 мг у подростков
|
#Epinephrinum** (Эпинефрин) |
CO1CA24 |
В экстренных случаях внутримышечно, внутривенно, внутрисердечно 0,1% раствор в дозе 0,01 мг/кг (0.1 мл/кг) или 1% раствор в дозе 0,1 мг/кг (0.1 мл/кг). Возможен расчет по возрасту – 0,1% раствор в дозе 0,05мг х год жизни. Максимальная доза 1 мг. |
Пациентам с СССУ и симптомами или гемодинамически нестабильным состоянием рефрактерным к медикаментозной терапии рекомендовано проведение чрескожной наружной или трансвенозной электрокардиостимуляции [50, 63, 65-66].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 4)
Комментарий: Пациентам с СССУ и вегетативными дисфункциями может быть рекомендовано назначение комплекса стимулирующей терапии с широким спектром действия для устранения избыточных вегетативных влияний:
Ноотропное средство #Пирацетам** (N06BX030) по 0,2-0,4 г 2-3 раза в день (0,4-1,2 г в день) в течение 2-6 мес., повторный курс через 3-6 мес. [31, 33], или по 20-50 мг/кг/сут. в 2-3 приема в течение 1-2 мес. [67].
Ноотропное средство #Гопантеновая кислота (N06BX) по 250 - 500 мг 1-2 раза в день (75-300 г в сутки) в течение 1-3 мес., повторный курс через 3-6 мес. [31] или по 0, 25-1 3 раза в день в течение 1-2 мес. [67].
Другие психостимуляторы и ноотропные препараты #Аминофенилмасляная кислота (N06BX22) с 0,25-0,5 г/сутки до 0,05-0.3 г 3 раза в день в течение 4-6 нед. [31, 33] или по 0,15-1 г/сут в 3 приема в течение 1-2 мес. [67].
Другие психостимуляторы и ноотропные препараты и #Церебролизин** (N06BX) по 1-2 мл внутримышечно в течение 15-20 дней через день [31].
Антиоксидантное средство #Полидигидроксифенилентиосульфонат натрия (N07XX) по 1 капсуле (250 мг) 3 раза в день в течение 2 мес. [68].
Антиоксидантное средство #Этилметилгидроксипиридина сукцинат (N07XX) по 2-4 мг/кг/сутки, не более 4 мл в вену капельно на 100 мл 0,9% раствора натрий хлорида в течение 10 дней [67].
Общетонизирующие препараты #Элеутерококка колючего корневищ и корней экстракт (A13A) и #Женьшеня настоящего корней настойка (A13A) по 1-2 капле на год жизни утром и днем в течение 10 дней в течение 1 мес. через 1 мес. [31].
При наличии метаболических изменений в виде нарушений процессов реполяризации применяются другие препараты для лечения заболеваний сердца #Убидекаренон (C01EB09) по 3 капли 2 раза в день у детей до года, у детей 1-5 лет по 5 капель 2-3 раза в день, у детей 5-10 лет по 8 капель 2-3 раза в день, у детей старше 10 лет 10-15 капель 2-3 раза в день в течение 1 мес. или по 0,5 мл 1-2 раза в день в течение 1 мес. [69, 70].
В результате длительного применения (до 6 мес.) курса этих препаратов (не более 4-х одновременно) стимулируются окислительно-восстановительные процессы, повышается устойчивость мозга к гипоксии, происходит стабилизация клеточных мембран. Стимуляция симпатического отдела вегетативной нервной системы тормозит прогрессирование синдрома и в большом количестве случаев на ранних этапах СССУ сопровождается восстановлением нормального ритмовождения, что особенно важно для детей раннего возраста, интервенционное лечение которых имеет определенные трудности.
При высокой представленности заместительного гетеротопного ритма с высокой ЧСС и присоединении аритмогенной дисфункции миокарда у детей с синдромом тахи-брадикардии может потребоваться проведение антиаритмической терапии под контролем ЭКГ и ХМ. Антиаритмическая терапия противопоказана детям с обмороками в анамнезе, выраженным угнетением синусового узла, большого количества выраженных пауз ритма, наличии нарушения АВ-проведения.
3.2 Хирургическое лечение
Хирургическое лечение включает электрокардиостимуляцию, которая проводится с помощью Электрокардиостимулятора имплантируемого двухкамерного, частотно-адаптивного***, Электрокардиостимулятора имплантируемого однокамерного, частотно-адаптивного*** (имплантируемого ЭКС***)
ИЗОЛИРОВАННЫЙ СИНДРОМ СЛАБОСТИ СИНУСОВОГО УЗЛА
Постоянная электрокардистимуляция рекомендована детям с СССУ и симптомной брадикардией относительно возрастных норм – I класс показаний [27, 38, 46, 71-75].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 4)
Постоянная электрокардиостимуляция рекомендована детям с симптомным СССУ и брадикардией, вызванной медикаментозными препаратами при отсутствии альтернативных методов лечения – IIa класс показаний [38, 46, 75, 76].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 4)
Постоянная электрокардиостимуляция рекомендована детям с СССУ и симптомами, связанными с хронотропной недостаточностью – IIa [38, 75, 78, 79].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 4)
Постоянная электрокардиостимуляция рекомендована детям с СССУ и симптомами, вероятно связанными с несоответствующей возрасту брадикардией или длительными паузами после тщательного обследования IIb класс показаний [38, 75].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 4)
СИНДРОМ СЛАБОСТИ СИНУСОВОГО УЗЛА В СОЧЕТАНИИ С ВРОЖДЕННЫМ ПОРОКОМ СЕРДЦА
Постоянная электрокардиостимуляция рекомендована детям с врожденным пороком сердца, СССУ и рецидивирующей предсердной тахикардией, когда хирургическое или медикаментозное лечение неэффективно или неприемлемо - IIa класс показаний [38, 46, 68, 75, 80-82].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 4)
Постоянная электрокардиостимуляция рекомендована детям с СССУ и врожденным пороком сердца с нарушением гемодинамики из-за брадикардии или потери АВ синхронности - IIa класс показаний [38, 46, 80, 83-85].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 4)
Постоянная электрокардиостимуляция рекомендована детям с врожденным пороком сердца, СССУ и симптомами, связанными с паузами или брадикардией - IIa класс показаний [38, 75, 80, 86].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 4)
Постоянная электрокардиостимуляция рекомендована детям с врожденным пороком сердца, СССУ и асимптомной синусовой брадикардией с ЧСС в покое 40 в мин. или паузами ритма более 3 сек – IIb класс показаний [27, 38, 71, 75, 84, 87].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 4)
Комментарий: Постоянная электрокардиостимуляция является наиболее эффективным методом коррекции проявлений СССУ. Решение о необходимости и сроках постоянной электрокардиостимуляции, а также о выборе метода и режима стимуляции принимается индивидуально, большое значение имеет возраст ребенка. При наличии потенциально обратимых причин СССУ нет необходимости в постоянной электрокардиостимуляции. При наличии показаний решается вопрос о выборе режима стимуляции. У пациентов с СССУ без признаков нарушения проводимости в АВ узле следует избегать изолированной однокамерной стимуляции желудочков. При наличии минимальных изменений атриовентрикулярного проведения у детей с СССУ необходимо применять стимуляцию обеих камер - предсердия и желудочка. Использование функций и алгоритмов стимуляции, которые позволяют задействовать собственную АВ проводимость, будет снижать количество желудочковой стимуляции у пациентов с электродами в предсердии и желудочке [85].
Одна из наиболее актуальных проблем при имплантации устройств у детей - необходимость пожизненной стимуляции. Повторные замены устройств и возрастание количества проблем с электродами требуют как можно более длительного сохранения возможности венозного доступа. У новорожденных и маленьких детей более предпочтительнее эпикардиальный доступ [88]. Эндокардиальная имплантация электродов допустима по достижении ребёнком массы тела равной 15 кг [89-93]. При массе тела от 15 до 19 кг имплантируется имплантируемый электрокардиостимулятор однокамерный, частотно-адаптивный***. При массе тела 20 кг и более применяется имплантируемый электрокардиостимулятор двухкамерный, частотно-адаптивный***. Наличие внутрисердечных шунтов может увеличивать риск системной эмболии после эндокардиальной имплантации и требует их закрытия до или во время операции, если это возможно, в противном случае должен быть рассмотрен эпикардиальный доступ. Эпикардиальный доступ также необходим у пациентов с ВПС при отсутствии венозного доступа, особенно у пациентов с одним желудочком. Пациентам, которым планируется эпикардиальный доступ, рекомендуется имплантировать электрод в апикальную позицию левого желудочка, при эндокардиальном доступе предпочтительным местом имплантации электрода является межжелудочковая перегородка или проводящая система сердца.
Пациентам с СССУ, имеющим показания к имплантации имплантируемого ЭКС***, должна проводиться психологическая реабилитация до и после хирургического лечения. Специальной реабилитации пациенты после имплантации имплантируемого ЭКС*** и заживления раны не требуют. В отдельных случаях предполагается щадящий режим физической активности с ограничением движений конечности большой амплитуды на стороне имплантации в течение 1 месяца.
Для своевременного выявления детей с пограничной брадикардией, а также группы риска по формированию синдрома и ранней диагностики начальных стадий СССУ требуется проведение регулярного обследования.
У пациентов с брадикардией с ЧСС на ЭКГ менее 5 перцентиля относительно возрастных норм рекомендован осмотр врача-детского кардиолога, контроль ЧСС при регистрации ЭКГ 1 раз в год в течение не менее 5 лет [12, 43].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 5)
При выявлении брадикардии с ЧСС менее 2 перцентиля относительно возрастных норм при регистрации ЭКГ рекомендован осмотр врача-детского кардиолога, контроль ЧСС по данным ЭКГ 1 раз в 3 мес. [12, 43].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 5)
Детям с установленным I вариантом СССУ рекомендовано наблюдение у врача-детского кардиолога 1 раз в год, с установленными II-IV вариантами СССУ – 2 раза в год [12, 43].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 5)
Комментарии: С целью профилактики постмиокардитических брадиаритмий необходима профилактика инфекционных заболеваний у беременных и детей, своевременное назначение адекватной терапии у пациентов при развитии инфекционного заболевания.
При отсутствии прогрессирования СССУ рекомендуется ежегодный мониторинг факторов риска при регистрации ЭКГ и ХМ с контролем значений минимальной ЧСС, пауз ритма, сопутствующих нарушений ритма и проводимости, а также гемодинамических показателей по данным ЭхоКГ. В случае нарастания степени брадикардии, максимальной продолжительности пауз ритма, ухудшении гемодинамических показателей необходим контроль 1 раз в 3-6 мес. с определением показаний для электрокардиостимуляции. При наличии таковых пациент госпитализируется в кардиохирургическую клинику, имеющую опыт имплантации имплантируемого ЭКС***.
Детям после имплантации имплантируемого ЭКС*** по поводу СССУ рекомендовано наблюдение у врача-детского кардиолога и при необходимости тестирование имплантируемого ЭКС*** через 6 мес., затем не реже 1 раза в год [27, 38, 71, 94, 95].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 5)
Детям после имплантации имплантируемого ЭКС*** по поводу СССУ для регистрации ЧСС, источника ритма и нарушений ритма и проводимости, оценки его функционирования рекомендована регистрация ЭКГ не реже 1 раза в год [38].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 5)
Детям после имплантации имплантируемого ЭКС*** по поводу СССУ для оценки сократительной функции, выявления десинхронии сокращения полостей и состояния электродов рекомендовано выполнение ЭхоКГ не реже 1 раза в год [38, 96].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 5)
Детям после имплантации имплантируемого ЭКС*** по поводу СССУ для оценки состояния и расположения электродов рекомендуется прицельная рентгенография органов грудной клетки в двух проекциях каждые 1-3 года в зависимости от роста темпов роста ребёнка и клинической ситуации [38].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 5)
Комментарии: В комплекс регулярного обследования пациента после имплантации имплантируемого ЭКС*** входит: оценка его параметров, регистрация ЭКГ, ЭхоКГ, прицельная рентгенография органов грудной клетки в двух проекциях, Холтеровское мониторирование сердечного ритма и ЭКГ с физической нагрузкой также могут быть проведены в зависимости от особенностей течения СССУ у конкретного пациента. Сроки наблюдения и объём необходимого обследования могут варьировать в зависимости от причины развития и особенностей течения СССУ у конкретного пациента.
Вакцинация детям с СССУ проводится при отсутствии прогрессирования функции синусового узла. Проведение профилактических прививок противопоказано детям с аутоиммунными формами СССУ или постмиокардитического генеза в острой фазе заболевания. У больных с послеоперационным СССУ вакцинация проводится не ранее чем через 6 мес. после коррекции врожденного порока сердца. Предпочтение при вакцинации пациентов с СССУ отдается инактивированным вакцинам. Наличие имплантируемого ЭКС*** у пациента не является противопоказанием к вакцинации.
Занятия спортом
Спортсменам с бессимптомным течением СССУ и без ограничивающего структурного заболевания сердца или других аритмий рекомендовано участие во всех соревновательных видах спорта [97].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 5)
Спортсменам с СССУ и симптомами не рекомендуется занятия спортом на время обследования на предмет наличия структурных заболеваний и лечения [97].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 5)
Пациентам с СССУ после имплантации имплантируемого ЭКС*** рекомендуются занятия спортом при условии отсутствия ограничивающего структурного заболевания сердца, других аритмий или симптомов [97].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 5)
Пациентам с СССУ, полностью зависящим от имплантируемого ЭКС***, не рекомендуется заниматься видами спорта, в которых существует риск столкновения, которое может привести к повреждению имплантируемого ЭКС*** [97].
Уровень убедительности рекомендаций – УУР С (уровень достоверности доказательств – УДД 5)
Пациенты могут иметь дополнительные ограничения, связанные с заболеваниями, ставшими причиной развития вторичного СССУ.
Показания для госпитализации в медицинскую организацию:
1) Ухудшение состояния пациента с установленным диагнозом или подозрением на СССУ, появление жалоб на обмороки, головокружения, слабость;
2) Нарастание степени брадикардии, продолжительности пауз ритма относительно возрастной нормы на ЭКГ у пациента с установленным диагнозом или подозрением на СССУ;
3) Необходимость оценки состояния пациента и мониторинга факторов риска у пациента с установленным диагнозом СССУ;
4) Необходимость коррекции терапии у пациента с установленным диагнозом СССУ;
5) Необходимость плановой имплантации/замены имплантируемого ЭКС*** у пациента с установленным диагнозом СССУ;
6) Необходимость плановой или экстренной оценки и коррекции функции имплантируемого ЭКС*** у пациента с установленным диагнозом СССУ.
Комментарии: Госпитализация осуществляется в специализированное детское кардиологическое отделение медицинских организаций III уровня. При обмороке или остановке кровообращения экстренные лечебные мероприятия должны быть начаты бригадой скорой медицинской помощи. Госпитализация пациента должна быть осуществлена в лечебное учреждение, которое имеет возможность оказания реаниматологической помощи. Оптимальна госпитализация в стационар, располагающий возможностями и опытом установки временной и постоянной электрокардиостимуляции.
Показания к выписке пациента из медицинской организации:
1) Исчезновение симптомов, улучшение состояния пациента у пациента с установленным диагнозом или подозрением на СССУ;
2) Отсутствие нарастания степени брадикардии, продолжительности пауз ритма или нормализация частотных параметров и пауз ритма на ЭКГ у пациента с установленным диагнозом или подозрением на СССУ;
3) Успешная оценка состояния пациента и проведение мониторинга факторов риска у пациента с установленным диагнозом СССУ;
4) Успешная коррекция терапии у пациента с установленным диагнозом СССУ;
5) Успешная оценка и коррекция функции имплантируемого ЭКС*** у пациента с установленным диагнозом СССУ.
Исходы и прогноз
Начальным этапом формирования СССУ является синусовая брадикардия. Устойчивое (более 3-х лет) снижение ЧСС менее 2 перцентиля на стандартной ЭКГ ассоциируется с развитием прогрессирующего нарушения функции синусового узла у детей [5, 12]. Своевременное выявление пограничной брадикардии и адекватная возрасту оценка значений ЧСС может предупредить дальнейшее развитие генерализованного дегенеративного процесса всей проводящей системы сердца, когда на фоне отсутствия лечения отмечается прогрессирование синдрома в виде появления жалоб, изменений на ЭКГ, ухудшения показателей гемодинамики, присоединения нарушений атриовентрикулярного и внутрижелудочкового проведения [3, 5, 12]. Для определения прогноза заболевания у детей следует проводить комплексную оценку клинико-электрофизиологических показателей, хотя наличие клинической симптоматики имеет в ряде случаев большую ценность в сравнении с электрофизиологическими показателями функции синусового узла. Принципы оценки эффективности лечения детей с СССУ отличаются от таковых при других нарушениях ритма. Стабильная клиническая и электрокардиографическая картина при отсутствии положительной динамики может быть расценена как приостановление дальнейшего развития патологического процесса. Наиболее неблагоприятными в плане возникновения жизнеугрожаемых событий являются случаи СССУ с многоуровневым поражением проводящей системы сердца, с дебютом синкопальных состояний в дошкольном возрасте, с семейными и врожденными проявлениями СССУ.













