Идиопатический легочный фиброз (ИЛФ) – особая форма хронической прогрессирующей фиброзирующей интерстициальной пневмонии неизвестной этиологии, которая возникает преимущественно у людей старшего возраста, поражает только легкие и связана с гистологическим и/или компьютерно-томографическим (КТ) паттерном обычной интерстициальной пневмонии (ОИП) [1,2,3]. Гистологический паттерн ОИП включает наличие фибробластических фокусов, интерстициального хронического воспаления, фиброза преимущественно в зонах бронхиоло-альвеолярных переходов, в подплевральных/парасептальных зонах с формированием «сот». Паттерн ОИП при высокоразрешающей КТ (ВРКТ) органов грудной клетки включает распространенные двухсторонние ретикулярные изменения, признаки «сотового легкого» и/или тракционных бронхоэктазов с преобладанием изменений в кортикальных и базальных отделах легких.
Этиология ИЛФ неизвестна, однако определены некоторые факторы риска, связанные с ИЛФ [4,5]:
- курение. Это один из наиболее частых факторов риска, для которых доказана достоверная связь с ИЛФ. Значимость данного фактора риска возрастает у пациентов с анамнезом курения более 20 пачек-лет [6];
- внешнесредовые ингаляционные воздействия, не связанные с курением. Повышенный риск развития ИЛФ ассоциируется с широким спектром неорганических и органических пылей, в частности, с металлической (ОШ 2,44; 95% ДИ 1,74 - 3,40), древесной (ОШ 1,94; 95% ДИ 1,34 - 2,81) и каменной пылью (ОШ 1,97; 95% ДИ 1,09 - 3,55). В качестве потенциального фактора риска рассматривается ингаляционное воздействие органической пыли (растительная или животная) в сельском хозяйстве или в быту (ОШ 1,65; 95% ДИ 1,20 - 2,26) [7];
- гастроэзофагеальный рефлюкс (ГЭР). Взаимосвязь между ГЭР и ИЛФ окончательно не доказана [8];
- метаболические (эндокринные) расстройства. Метаболические (эндокринные) расстройства (сахарный диабет, гипотиреоз) встречаются значительно чаще среди больных ИЛФ и рассматриваются как независимый фактор риска для этого заболевания [9,10];
- генетические факторы. Около 5% всей популяции больных ИЛФ имеют семейный легочный фиброз (среди кровных родственников). Наиболее часто (у 34% больных с семейным легочным фиброзом и у 38% пациентов с ИЛФ) встречается мутация MUC5B [11]; реже (в 25% случаев ИЛФ и в 15% случаев семейного легочного фиброза) мутации генов, связанных с теломеразой (TERT, TERC, DKC1, TINF2, RTEL1, PARN) и вызывающие укорочение теломерных участков; в 3%, в основном при семейном легочном фиброзе, - мутации в генах сурфактантных протеинов C (SP-C) и A2 (SP-A2) [12-16].
В основе патогенеза ИЛФ лежат повторные микроповреждения альвеолярного эпителия с нарушением механизмов его регенерации. Это приводит к патологической реэпителизации, пролиферации фибробластов и синтезу избыточного количества экстрацеллюлярного матрикса. В результате нормальная легочная паренхима постепенно замещается фиброзной тканью [6].
Считается, что в последние годы число больных ИЛФ увеличилось. Однако показатели заболеваемости и распространенности ИЛФ в исследованиях разных авторов существенно отличаются, что можно объяснить отсутствием четких и общепринятых диагностических критериев, как рентгенологических, так и морфологических, отличиями в дизайнах исследований (разные определения ИЛФ, разный возрастной состав пациентов) и др. Заболеваемость ИЛФ зависит от возраста: болезнь возникает чаще в шестом и седьмом десятилетиях жизни. Большинство заболевших являются курильщиками или экс-курильщиками; мужчины болеют несколько чаще, чем женщины [17,18]. По данным разных авторов, заболеваемость ИЛФ составляет от 6,8 до 63 случаев на 100 000 населения в зависимости от используемого определения ИЛФ [19-21].
Согласно предварительным данным, полученным по результатам регистра ИЛФ в Российской Федерации, распространенность ИЛФ в Российской Федерации составляет около 8 - 12 случаев на 100 000 населения, а заболеваемость ИЛФ – 4 - 7 случаев на 100 000 населения [22].
Другие интерстициальные легочные болезни (J84):
Другие интерстициальные легочные болезни с упоминанием о фиброзе (J84.1)
Клиническая классификация ИЛФ отсутствует. По сочетанию специфических компьютерно-томографических и морфологических паттернов можно выделить:
- подтвержденный ИЛФ (наличие паттерна типичной ОИП у больного старше 60 лет при отсутствии клинически значимых внешнесредовых и лекарственных воздействий и отсутствии системных заболеваний соединительной ткани; соответствующее сочетание ВРКТ- и морфологического паттернов (Прил. Д)) [23];
- вероятный ИЛФ (соответствующее сочетание ВРКТ- и морфологического паттернов (см. Прил. Д)) [23];
- комбинация легочного фиброза с эмфиземой.
Пример формулировки диагноза:
а. Интерстициальное заболевание легких: идиопатический легочный фиброз. Хроническая гипоксемическая дыхательная недостаточность.
б. Интерстициальное заболевание легких: идиопатический легочный фиброз (комбинация легочного фиброза с эмфиземой). Буллезная эмфизема верхних отделов обоих легких. Хроническая гипоксемическая дыхательная недостаточность.
Начало заболевания приходится, как правило, на возраст старше 50 лет [18], у больных с семейным анамнезом ИЛФ заболевание может начинаться в более молодом возрасте [24].
Основными клиническими проявлениями ИЛФ являются одышка, снижение толерантности к нагрузке и хронический кашель и такие неспецифические симптомы как слабость, снижение аппетита, потеря веса. Гипертермия, периферическая лимфаденопатия, артриты, миалгии, «свистящее» дыхание, кровохарканье, болевой синдром в грудной клетке и поражение левых камер сердца не характерны для ИЛФ [23,25].
В отсутствие обострений естественное течение болезни характеризуется постепенным нарастанием симптомов в течение нескольких лет до развития тяжелых нарушений функции дыхания и присоединения осложнений [26].
Наиболее частой причиной смерти при ИЛФ (60%) является прогрессирующая дыхательная недостаточность, а также ишемическая болезнь сердца (ИБС), тромбоэмболия легочной артерии (ТЭЛА) и рак легкого [27]. Медиана выживаемости от момента постановки диагноза ИЛФ составляет от 2 до 3 лет [1], а от момента появления первых симптомов ИЛФ и/или изменений по КТ - 6 лет [28]. Вместе с тем, у больных с сохранной легочной функцией этот показатель может быть выше.
У 5-15% пациентов с ИЛФ в течение года развивается острое ухудшение клинического состояния – обострения ИЛФ [6]. Основными признаками обострения ИЛФ являются беспричинное нарастание одышки в течение 1 мес, усиление кашля и продукции мокроты, документированная гипоксемия (ухудшение или тяжелое нарушение газообмена), свежие альвеолярные инфильтраты на рентгенограмме легких и отсутствие других причин ухудшения, таких как экстра-паренхиматозные причины (пневмоторакс, плевральный выпот, ТЭЛА) или сердечная недостаточность с объемной перегрузкой сердца [26, 29-31]. Прогноз обострения ИЛФ, как правило, неблагоприятный, летальность во время госпитализации достигает 65%, а в течение 6 месяцев от начала развития обострения - > 90% [26].
Клиническое подозрение на ИЛФ у больного с хронической одышкой при физической нагрузке, кашлем, двухсторонней инспираторной крепитацией в базальных отделах легких и/или утолщением дистальных фаланг пальцев рук по типу "барабанных палочек", не имеющих очевидной причины, должно возникать в следующей ситуации: возраст старше 60 лет; отсутствие клинически значимых внешнесредовых или лекарственных воздействий; отсутствие признаков системных заболеваний соединительной ткани (СЗСТ) [17].
Критерии установления диагноза/состояния:
1) жалобы на одышку при отсутствии очевидных причин, клинически значимых внешнесредовых или лекарственных воздействий; отсутствие признаков СЗСТ;
2) двухсторонней инспираторной крепитацией в базальных отделах легких при аускультации;
4) выявление паттерна обычной интерстициальной пневмонии (ОИП) при ВРКТ органов грудной клетки и/или при патолого-анатомическом исследовании биоптатов легочной ткани.
- При выявлении ИЗЛ рекомендуется тщательный сбор анамнеза приема лекарственных препаратов и воздействия факторов окружающей среды дома, на рабочем месте и в других местах, часто посещаемых пациентом, для исключения потенциальных причин ИЗЛ [23].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: Клиническое подозрение на ИЛФ у больного с хронической одышкой при физической нагрузке, кашлем, двухсторонней инспираторной крепитацией в базальных отделах легких и/или утолщением дистальных фаланг пальцев рук по типу "барабанных палочек", не имеющих очевидной причины, должно возникать в следующей ситуации: возраст старше 60 лет; отсутствие клинически значимых внешнесредовых или лекарственных воздействий; отсутствие признаков системных заболеваний соединительной ткани (СЗСТ) [17].
- Для оценки одышки при повседневных физических нагрузках у пациентов с ИЛФ рекомендуется использовать шкалу mMRC (Прил. Г) [32].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 4)
- Для оценки тяжести и прогноза ИЛФ рекомендуется использовать шкалу GAP (Прил. Г2) [33].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 4)
У 40% пациентов с ИЛФ при первичном осмотре выявляются изменения дистальных фаланг по типу «барабанных палочек» и ногтевых пластин пальцев рук по типу «часовых стекол» различной выраженности. Выявляемая при аускультации двусторонняя крепитация в конце вдоха (хруст «липучки», или хрипы «velcro») в базальных отделах также характерна для пациентов с ИЛФ и тесно коррелирует с наличием паттерна обычной интерстициальной пневмонии (ОИП) при ВРКТ органов грудной клетки [34].
- У всех пациентов с ИЛФ рекомендуется оценивать состояние дистальных фаланг и ногтевых пластин пальцев рук для исключения изменения по типу «барабанных палочек» и «часовых стекол».
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: Выявление изменения дистальных фаланг по типу «барабанных палочек» и ногтевых пластин пальцев рук по типу «часовых стекол» при первичном осмотре больного с ИЛФ свидетельствует о развернутой стадии болезни и ассоциируется с плохим прогнозом [1].
- Всем пациентам с клиническим подозрением на ИЛФ рекомендуется проводить аускультацию легких для выявления двусторонней крепитации [34].
Уровень убедительности рекомендаций В (уровень достоверности доказательств 2)
- Для исключения ИЗЛ, связанных с СЗСТ (ИЗЛ-СЗСТ), всем больным с клиническим подозрением на ИЛФ рекомендуется выполнять исследование скорости оседания эритроцитов (СОЭ), исследование уровня С-реактивного белка (СРБ) в крови, определение содержания антинуклеарных антител (АНА) в крови (методом иммунофлюоресценции), определение содержания ревматоидного фактора (РФ) в крови, определение содержания антинуклеарных антител к Sm-антигену и определение содержания антител к циклическому цитрулиновому пептиду (анти-CCP) в крови [23].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: У больных с подозрением на ИЛФ и симптомами СЗСТ требуется более детальное исследование сывороточных маркеров СЗСТ:
- при подозрении на миозит: определение активности креатинкиназы в крови, исследование уровня миоглобина в крови, определение активности альдолазы в крови, определение содержания антицентромерных антител в крови и др.;
- при подозрении на системную склеродермию: определение содержания антител к Scl-70 / топоизомеразе-1 в крови, определение содержания антицентромерных антител в крови;
- при подозрении на синдром Шегрена: определение содержания антител к SSA / Ro и SSB / La в крови;
- при подозрении на васкулит: определение маркеров ANCA-ассоциированных васкулитов: PR3 (c-ANCA), МПО (p-ANCA).
Выявление СЗСТ у больного с интерстициальными изменениями в легких исключает диагноз ИЛФ [1].
- Всем больным ИЛФ рекомендуется регулярно выполнять пульсоксиметрию (SpO2) в покое и при физической нагрузке (при выполнении теста с 6-минутной ходьбой (6-МТ)) для выявления десатурации [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: Выявление десатурации ниже 88 % является показанием к назначению кислородотерапии.
2.4.1. Рентгенологическая диагностика
- Больным с подозрением на ИЛФ не рекомендуется проведение обзорной рентгенографии органов грудной клетки в связи с ее низкой информативностью [37]. Уровень убедительности рекомендаций С (уровень достоверности доказательств 3)
- Всем больным с клиническим подозрением на ИЛФ рекомендуется проведение ВРКТ органов грудной клетки для подтверждения диагноза ИЛФ [23].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
- КТ органов грудной клетки с внутривенным контрастированием рекомендуется больным с ИЗЛ только для исключения тромбоэмболии легочной артерии [23].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: Технические требования к ВРКТ органов грудной клетки у больных ИЛФ:
- тонкие томографические срезы (≤1 мм) [38];
- алгоритм высокого пространственного разрешения [39];
- изображения должны быть получены на максимально глубоком вдохе;
- спиральное (объемное) сканирование;
- при сомнительных результатах сканирования в положении на спине рекомендовано выполнение сканирования в положении на животе для устранения «гравитационного эффекта» [40] и экспираторной КТ для выявления «воздушных ловушек» [41];
Изменения на ВРКТ органов грудной клетки отражают морфологические изменения в легких, которые при ИЛФ представляют собой паттерн ОИП.
Основными признаками ОИП при ВРКТ органов грудной клетки являются:
- преобладание изменений в кортикальных и базальных отделах легких;
- диффузные двухсторонние ретикулярные изменения;
- мелкие субплевральные воздушные кисты («сотовое легкое») и/или
- периферические тракционные бронхо- или бронхиолоэктазы [42] (Рис. 1-3).
«Матовое стекло» может присутствовать на фоне ретикулярных изменений и «сотового легкого», но не должно превалировать над другими изменениями. Такое "матовое стекло" является признаком фиброза [43].
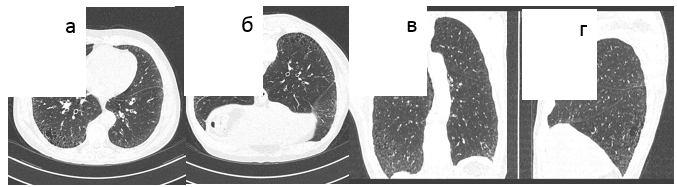
Рис. 1. Обычная интерстициальная пневмония, типичная ВРКТ-картина. а) аксиальный срез, б) фронтальная реформация, в) сагиттальная реформация, д) аксиальный срез в положении на животе. Кортикальное распределение изменений с нарастанием их от верхушек к диафрагме, "сотовое легкое", ретикулярные изменения, отсутствие "матового стекла". Исследование в положении на животе подтверждает отсутствие "матового стекла".
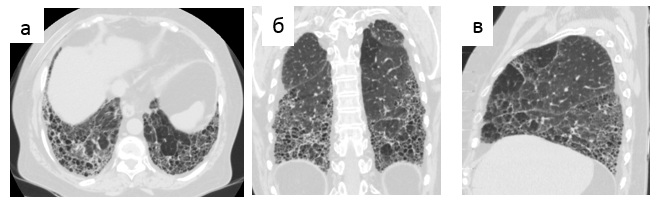
Рис. 2. Обычная интерстициальная пневмония, типичная картина. Сотовое легкое на аксиальном срезе (а), при реформации во фронтальной (б) и сагиттальной (в) плоскостях.
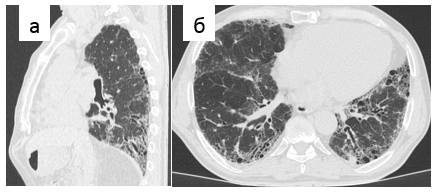
Рис. 3. Обычная интерстициальная пневмония, типичная картина. Тракционные бронхоэктазы в кортикальных отделах легких на реформации в косой плоскости (а) и аксиальном срезе (б)
Выделяют несколько паттернов ОИП по данным ВРКТ органов грудной клетки (Табл. 1).
Таблица 1. Компьютерно-томографические диагностические категории ОИП
|
Типичная ОИП |
Вероятная ОИП |
Сомнительная ОИП |
ВРКТ-картина, не соответствующая ОИП |
|
|
Распределение |
Преобладание в базальных отделах (реже диффузно) и субплеврально; распределение обычно гетерогенное |
Преобладание в базальных и субплевральных отделах; распределение обычно гетерогенное |
Вариабельное или диффузное |
Преобладание в верхних и средних отделах; перибронховаскулярные изменения с интактностью субплевральных отделов |
|
Признаки |
«Сотовое легкое»; ретикулярные изменения с периферическими тракционными бронхо- и бронхиолоэктазами*; отсутствие признаков, позволяющих заподозрить альтернативный диагноз |
Ретикулярные изменения с периферическими тракционными бронхо- и бронхиолоэктазами; отсутствует «сотовое легкое»; отсутствие признаков, позволяющих заподозрить альтернативный диагноз |
Фиброз без каких-либо особенностей, позволяющих заподозрить ОИП |
Любые из перечисленных: преобладание консолидации, распространенное «матовое стекло» (без признаков обострения ИЛФ), распространенная мозаичность с четко очерченными «воздушными ловушками» на выдохе, множественные очаги или кисты |
Примечание: * - могут присутствовать слабо выраженное «матовое стекло», ретикулярные изменения, оссификация.
- При ВРКТ-паттерне типичной ОИП и клинических данных, соответствующих ИЛФ, не рекомендуется выполнение биопсии легкого (хирургической, трансбронхиальной или криобиопсии) и бронхоальвеолярного лаважа (БАЛ) для подтверждения диагноза [23].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: В соответствующей клинической ситуации специфичность паттерна типичной ОИП для диагностики ИЛФ при ВРКТ органов грудной клетки достигает 94–100%, что позволяет поставить диагноз ИЛФ без инвазивных диагностических вмешательств [44,45].
- Больным с клиническим подозрением на ИЛФ и выявлением паттернов вероятной ОИП, сомнительной ОИП или альтернативного диагноза при ВРКТ органов грудной клетки рекомендуется выполнение хирургической биопсии легкого для подтверждения диагноза [23].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: ВРКТ-паттерны вероятной или сомнительной ОИП менее специфичны для ИЛФ и поэтому требуют хирургической биопсии легкого с целью более точной оценки прогноза и выбора более специфичной терапии [23,46].
В настоящее время опубликовано недостаточно доказательных данных для разработки рекомендаций за или против использования других видов биопсии легкого (трансбронхиальной биопсии (ТББЛ) или криобиопсии) у больных с клиническим подозрением на ИЛФ и паттерном вероятной ОИП, сомнительной ОИП или альтернативного диагноза на ВРКТ органов грудной клетки [23].
- Больным с клиническим подозрением на ИЛФ и выявлением паттернов вероятной ОИП, сомнительной ОИП или альтернативного диагноза на ВРКТ органов грудной клетки рекомендуется цитологический анализ бронхоальвеолярного лаважа для дифференциальной диагностики с другими ИЗЛ [23].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: Клеточный состав БАЛ может помочь в дифференциальной диагностике ИЛФ с другими фиброзирующими ИЗЛ. Так, при ИЛФ процентное содержание нейтрофилов в БАЛ выше, чем при гиперчувствительном пневмоните, НСИП и эозинофильной пневмонии; процентное содержание эозинофилов ниже, чем при эозинофильной пневмонии, процентное содержание лимфоцитов ниже, чем при НСИП, саркоидозе, криптогенной организующейся пневмонии (КОП) и лимфоцитарной интерстициальной пневмонии (ЛИП; соотношение CD4 / CD в БАЛ при ИЛФ ниже, чем при саркоидозе, и выше, чем при НСИП [23].
- При одновременном выявлении на ВРКТ органов грудной клетки паттерна ОИП и эмфиземы рекомендуется указывать в диагнозе комбинацию легочного фиброза с эмфиземой (КЛФЭ) в связи с особым течением такого фенотипа ИЛФ [23].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: Клинической особенностью синдрома КЛФЭ является наличие выраженной одышки при нередко нормальных спирографических показателях [1], а также большая распространенность и тяжесть ЛГ, существенно ухудшающая прогноз заболевания [47].
- Больных с клиническим подозрением на ИЛФ, паттерном ОИП и признаками плевропаренхиматозного фиброэластоза (ППФЭ) на ВРКТ органов грудной клетки после многопрофильного обсуждения рекомендуется расценивать как больных с ИЛФ в связи со сходным клиническим течением и прогнозом этих заболеваний [23].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: ППФЭ – прогрессирующее фиброзирующее ИЗЛ неизвестной этиологии. Для ППФЭ типичны неравномерное утолщение плевры и наличие участков субплевральной консолидации легочной паренхимы в верхних и средних отделах легких на ВРКТ органов грудной клетки.
2.4.2. Морфологическая диагностика
Основой морфологической диагностики ИЛФ является выявление морфологического паттерна ОИП.
- Морфологический диагноз ОИП рекомендуется выставлять больным с ИЗЛ при выявлении в биоптатах легочной ткани гетерогенных изменений архитектоники легких за счет участков плотного фиброза, часто с формированием «сотовых» структур, в сочетании с участками менее пораженной (или сохранной) паренхимы и при отсутствии признаков альтернативного заболевания легких [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: Эти патогистологические изменения обычно наиболее выражены в субплевральных и парасептальных зонах (Рис. 4). Интерстициальное воспаление обычно выражено умеренно, в виде очаговых инфильтратов, состоящих из лимфоцитов и плазматических клеток. В зонах фиброза могут встречаться так называемые фибробластические фокусы, состоящие из пролиферирующих фибробластов и миофибробластов (Рис. 5). «Сотовые» структуры представляют собой кистозные полости с фиброзной стенкой, обычно выстланные бронхиолярным эпителием, которые могут содержать слизь и клетки воспаления (Рис. 6).
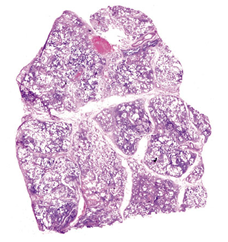
Рис. 4. Обычная интерстициальная пневмония: участки фиброза в подплевральных и парасептальных зонах
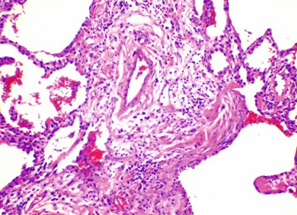
Рис. 5. Обычная интерстициальная пневмония: миофибробластический фокус в месте перехода респираторной бронхиолы в альвеолы
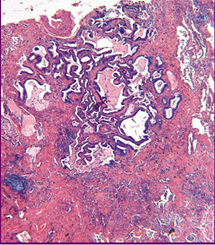
Рис. 6. Обычная интерстициальная пневмония: "сотовые" структуры
Выделены несколько гистологических паттернов ОИП (Табл. 2) [23].
Таблица 2. Гистологические паттерны и признаки ОИП
|
Типичная ОИП |
Вероятная ОИП |
Сомнительная ОИП |
Альтернативный диагноз |
|
Плотный фиброз с нарушениями архитектоники легочной ткани («сотовое легкое») |
Присутствуют некоторые признаки типичной ОИП, но их выраженность не позволяет говорить о типичной ОИП / ИЛФ И |
Фиброз с нарушениями архитектоники или без них, с признаками паттерна ОИП или вторичной ОИП, вызванной другим фибротическим заболеванием легких* |
Признаки других ИИП (например, отсутствие фибробластических фокусов или рыхлый фиброз) во всех биоптатах |
|
Преимущественно субплевральное и парасептальное распределение фиброза |
отсутствие признаков альтернативного заболевания |
Гистологические признаки других заболеваний (гиперчувствительный пневмонит, лангергансоклеточный гистиоцитоз, саркоидоз, лимфангиолейомиоматоз) |
|
|
Очаговый фиброз |
ИЛИ |
Некоторые признаки типичной ОИП, но при этом имеются признаки альтернативного заболевания# |
|
|
Фибробластические фокусы |
наличие только «сотового легкого» |
||
|
Отсутствие признаков альтернативного заболевания |
Примечания: * - Гранулемы, гиалиновые мембраны (отличающиеся от таковых при обострении ИЛФ), выраженное перибронхиальное распределение изменений, участки интерстициального воспаления, не связанные с фиброзом, выраженный хронический фиброз плевры, организующаяся пневмония.
# - Воспалительные клеточные инфильтраты вне зон «сотового легкого», выраженная лимфоидная гиперплазия, в том числе с вторичными герминативными центрами, четкое перибронхиальное распределение изменений, в том числе с распространенной перибронхиолярной метаплазией.
2.4.3. Функциональная диагностика
Легочные функциональные тесты у больных с ИЛФ обычно выявляют рестриктивные вентиляционные нарушения с уменьшением легочных объемов и снижением DLCO [48].
- Всем пациентам с ИЛФ рекомендуется выполнять исследование неспровоцированных дыхательных объемов и потоков для уточнения характера и выраженности нарушений легочной вентиляции, а также мониторирования скорости прогрессирования ИЛФ [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: Значение форсированной жизненной емкости легких (ФЖЕЛ) для прогноза летальности в период постановки диагноза ИЛФ окончательно не установлено, однако снижение ФЖЕЛ в абсолютных значениях на >10% в течение 12 мес. в процессе наблюдения за больным свидетельствует о прогрессировании заболевания и является суррогатным маркером риска летальности [1].
- Всем пациентам с ИЛФ рекомендуется измерение диффузионной способности легких по монооксиду углерода (DLco) для выявления нарушений газообменной функции легких [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: Величина DLCO <40 % от должного значения в период постановки ИЛФ является достоверным фактором риска смерти [35]. Снижение DLco в абсолютных значениях на >15% (наряду со снижением ФЖЕЛ или без такового) в течение 12 мес в процессе наблюдения за больным при отсутствии альтернативных причин свидетельствует о прогрессировании заболевания и является суррогатным маркером риска летальности [1]. На ранних стадиях ИЛФ может быть выявлено изолированное снижение DLCO при нормальных легочных объемах. Прогрессирующее изолированное снижение DLсо при мониторировании течения заболевания требует исключения патологии легочных сосудов, в первую очередь, легочной гипертензии [49].
- Всем пациентам с ИЛФ рекомендуется выполнять тест с 6-минутной ходьбой (6-МТ) для объективной оценки их функционального состояния, потребности в кислородотерапии, определении прогноза, а также оценки эффективности легочной реабилитации [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: Прогностическое значение имеют несколько параметров 6-МТ: пройденное расстояние, десатурация < 88% и скорость восстановления пульса по окончании теста [50-52]. 6-МТ позволяет прогнозировать летальность больных ИЛФ, ожидающих трансплантацию легких [53,54]. 6-МТ не показан больным, у которых ходьба лимитирована другими причинами (например, патологией опорно-двигательного аппарата), и больным с поздними стадиями ИЛФ [55].
- Многопрофильное обсуждение (МПО) рекомендуется проводить для всех пациентов с подозрением на ИЛФ с целью подтверждения диагноза ИЛФ и обсуждения тактики лечения [17,24].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: МПО необходимо всем больным с фибротическими ИЗЛ для установления диагноза, определения потребности в биопсии легкого и других диагностических мероприятиях, а также выбора оптимальной терапии. В состав многопрофильной группы специалистов должны обязательно входить врач-пульмонолог, врач-рентгенолог и врач-патологоанатом с опытом диагностики ИЗЛ, также возможно участие врача-ревматолога, врача-профпатолога, в отдельных случаях – врача-генетика. Обсуждение может проводиться с помощью телемедицинской коммуникации [24].
3.1. Консервативное лечение
3.1.1. Медикаментозное лечение
В настоящее время монотерапия ГКС не рекомендуется для лечения ИЛФ [56-60].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: По данным ретроспективных исследований, монотерапия ГКС не влияет на выживаемость больных ИЛФ [56,57]. Длительная терапия ГКС может сопровождаться серьезными побочными эффектами [58,59,60].
- В настоящее время терапия противоопухолевыми препаратами (цитостатиками), как в виде монотерапии, так и в комбинации с ГКС, не рекомендуется для лечения ИЛФ [2].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: В настоящее время нет убедительных доказательств об улучшении выживаемости больных ИЛФ, получавших противоопухолевые препараты (цитостатики) (аналоги азотистого иприта: циклофосфамид** (Код АТХ: L01AA01), другие иммунодепрессанты: азатиоприн** (Код АТХ: L04AX01)) как в виде монотерапии, так и при комбинации с ГКС [1]. Терапия противоопухолевыми препаратами (цитостатиками) может сопровождаться развитием серьезных побочных эффектов.
- Монотерапию ацетилцистеином** (Код АТХ: R05CB01) не рекомендуется назначать всем больным ИЛФ в рутинном порядке [2,61].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: Монотерапия ацетилцистеином** достоверно не улучшала ни один из значимых для больного показателей, включая выживаемость [62,63]. Терапия ацетилцистеином** может быть эффективной у пациентов ИЛФ с определенными генетическими полиморфизмами (например, TT генотипом TOLLIP), а также у больных интерстициальной пневмонией с аутоиммунными проявлениями (при наличии КТ- или гистологического паттерна ОИП и положительных АНА) [64].
- Комбинированная терапия ацетилцистеином**, азатиоприном** и преднизолоном** (Код АТХ: H02AB06) («тройная комбинация») не рекомендуется для лечения ИЛФ [2].
Уровень убедительности рекомендаций С; уровень достоверности доказательств 5.
Комментарии: Комбинированная терапия пероральным ацетилцистеином**, азатиоприном** и преднизолоном** («тройная комбинация») не оказывает значимого влияния на функциональные показатели, летальность и частоту обострений ИЛФ [65,66].
- Амбризентан** (Код АТХ: C02KX02) не рекомендуется для лечения ИЛФ независимо от наличия или отсутствия у них ЛГ [2].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: Если пациент с ИЛФ и ЛГ принимает амбризентан**, лечение должно быть прекращено в связи с прогрессирующим снижением легочной функции на фоне терапии амбризентаном** у больных ИЛФ [67]
- Силденафил (Код АТХ: G04BE03), бозентан** (Код АТХ: C02KX01) и мацитентан** (Код АТХ: C02KX04) не рекомендуются для лечения ИЛФ [2].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: Силденафил, бозентан** и мацитентан** не рекомендуется применять для лечения ИЛФ в связи с отсутствием положительных клинических результатов и высокой частотой серьезных побочных эффектов [2]. Силденафил может использоваться у больных ИЛФ по другим показаниям, таким как легочная гипертензия или другие варианты дисфункции правого желудочка [2]. Бозентан** и мацитентан** не оказывают положительного влияния на легочную гемодинамику у больных ИЛФ даже при наличии ЛГ [2].
- Варфарин** (Код АТХ: B01AA03) не рекомендуется для лечения ИЛФ [2].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: Применение перорального варфарина** для лечения ИЛФ связано с повышением риска летального исхода [68] При наличии у больного ИЛФ показаний к антикоагулянтной терапии, например, тромбоза глубоких вен голени, мерцательной аритмии, варфарин может использоваться в качестве антикоагулянта в соответствии с существующими клиническими рекомендациями для лечения этих заболеваний. Данная рекомендация не распространяется на применение других антикоагулянтов, назначаемых по другим показаниям [2].
- Ингибиторы протонного насоса рекомендуются в лечении больных ИЛФ при наличии клинически значимого ГЭР [69, 70].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: В ряде исследований установлено, что добавление к терапии ИЛФ ингибиторов протонного насоса повышает ФЖЕЛ, снижает частоту обострений [69] и улучшает выживаемость больных ИЛФ [70]. Больные, получающие пирфенидон** (Код АТХ: L04AX05), не должны лечиться омепразолом** (Код АТХ: A02BC01) ввиду нежелательного лекарственного взаимодействия, в то время как другие ингибиторы протонного насоса могут использоваться одновременно с пирфенидоном** [70].
- Всем больным ИЛФ рекомендуется лечение противоопухолевыми препаратами и другими иммунодепрессантами (антифибротическими препаратами) – нинтеданибом** или пирфенидоном** [71].
Уровень убедительности рекомендаций В (уровень достоверности доказательств 1)
Комментарии: В настоящее время клиническая эффективность в лечении ИЛФ доказана только для двух препаратов, зарегистрированных в Российской Федерации: нинтеданиба** (Код АТХ: L01XE31) и пирфенидона** (Код АТХ: L04AX05).
Терапия нинтеданибом** или пирфенидоном** позволяет затормозить скорость снижения ФЖЕЛ, уменьшить риск обострений ИЛФ и риск летального исхода [72,73]. Показана сходная эффективность нинтеданиба** и пирфенидона** у больных с разной тяжестью функциональных нарушений [77,84]. Поскольку целью лечения является замедление прогрессирования заболевания, длительность лечения не определена [69].
В клинических исследованиях 2-3 фазы, препарат нинтеданиб** показал снижение частоты обострений на 47% [77], средняя выживаемость у пациентов, получавших нинтеданиб** на основе распределения Вейбула, составила 11,6 (95% ДИ 9,6 - 14,1) лет [72]. В исследованиях третьей фазы нинтеданиб** был исследован у пациентов с ВРКТ-паттерном вероятной ОИП без хирургической биопсии лёгкого, с ФЖЕЛ >90% должн., с нормальными значениями соотношения ОФВ1/ФЖЕЛ, а также у пациентов старше 80 лет [83].
Рекомендации по использованию разных групп лекарственных средств в терапии ИЛФ суммированы в таблице 4.
Таблица 4. Рекомендации по фармакологической терапии ИЛФ
|
Не назначать |
Терапия не рекомендована |
Терапия возможна |
Терапия рекомендована |
|
Азатиоприн** + преднизолон** + Ацетилцистеин** («тройная комбинация») Варфарин** Амбризентан** |
ГКС Цитостатики Бозентан** Мацитентан** Силденафил ацетилцистеин** |
Антирефлюксная терапия |
Нинтеданиб** Пирфенидон** |
- Ведение больных ИЛФ с хроническим кашлем рекомендуется осуществлять по принципам, принятым для ведения других больных с хроническим кашлем [85].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
- У больных ИЛФ с хроническим кашлем ингибиторы протонного насоса рекомендуется назначать только при наличии ГЭР [85].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
- Больным с хроническим кашлем, рефрактерным к стандартной терапии и нарушающим повседневную активность больного, при неэффективности других методов лечения рекомендуется назначение опиоидных анальгетиков в рамках паллиативной помощи [84].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: При назначении опиоидных анальгетиков требуется тщательная оценка эффективности и побочных эффектов через 1 неделю лечения и затем ежемесячно в период их использования [85].
Методы терапии обострения ИЛФ с доказанной эффективностью, включая глюкокортикостероидные лекарственные средства, отсутствуют. В связи с этим настоящее время невозможно предоставить специфические рекомендации о дозах, пути введения и длительности терапии ГКС либо другими лекарственными препаратами при обострении ИЛФ [69].
3.1.2. Немедикаментозное лечение
Длительная кислородотерапия (ДКТ)
- Пациентам с ИЛФ и клинически значимой гипоксемией в покое (при SрO2 менее 88% в покое при дыхании комнатным воздухом) рекомендуется проведение ДКТ [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: Косвенные доказательства о пользе ДКТ при ИЛФ основаны на данных, полученных для больных хронической обструктивной болезнью легких (ХОБЛ). Аналогично больным с ХОБЛ, при назначении ДКТ больным ИЛФ ее длительность должна составлять не менее 15-17 часов в сутки, включая период ночного сна [86,87].
Неинвазивная вентиляция легких
- Применение неинвазивной вентиляции легких (НВЛ) с положительным давлением на вдохе рекомендуется у пациентов с ИЛФ и гиперкапнией во время стационарной легочной реабилитации [69], а также у больных с острой дыхательной недостаточностью (ОДН) на фоне обострения ИЛФ [88].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: НВЛ с положительным давлением на вдохе во время ночного сна у больных с ИЗЛ, включая ИЛФ, и гиперкапнией улучшала переносимость физической нагрузки и качество жизни [89].
Положительный эффект в виде снижения летальности от ОДН и риска интубации был достигнут у небольшого числа (44 - 45%) больных, хотя отсутствие НВЛ не влияло на прогноз умерших больных [88].
Искусственная вентиляция легких (ИВЛ)
- Большинству больных ИЛФ не рекомендуется проведение ИВЛ за исключением случаев, когда планируется проведение трансплантации легких [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: Опубликовано несколько небольших исследований ИВЛ у больных с ИЛФ и дыхательной недостаточностью, во всех получена высокая внутрибольничная летальность [90-92], хотя исследования несли риск систематических ошибок.
3.2. Хирургическое лечение
Трансплантация легких
- Пациентам с ИЛФ при наличии соответствующих показаний (Табл. 5) рекомендуется проведение трансплантации легких [93].
Уровень убедительности рекомендаций С; уровень достоверности доказательств 4.
Комментарии: В отдельных исследованиях показано снижение риска летального исхода в течение 5 лет после трансплантации у больных ИЛФ [93], однако точные данные о наиболее оптимальном времени трансплантации при этом заболевании отсутствуют [69]. В систематическом обзоре 54 исследований показана более хорошая выживаемость после трансплантации обоих легких по сравнению с трансплантацией одного легкого, однако эти результаты могут быть связаны с особенностями отбора больных для одно- либо двусторонней трансплантации легких [93].
Таблица 5. Показания к трансплантации легких при ИЛФ [69].
|
Морфологический или КТ-паттерн ОИП плюс один из признаков: • DLCO ниже 40% от должных величин • Снижение ФЖЕЛ на 10% и более в течение 6 мес наблюдения • Снижение SpO2 ниже 88% во время 6-MT. • «Сотовое легкое» на ВРКТ (> 2 баллов по шкале фиброза). |
- Всем пациентам с ИЛФ рекомендуется проводить легочную реабилитацию, объем которой определяется тяжестью состояния больного [94].
Уровень убедительности рекомендаций В (уровень достоверности доказательств 2)
Комментарии: Легочная реабилитация больных с ИЛФ должна включать аэробные тренировки скелетной и дыхательной мускулатуры, образование больных, коррекцию нутритивного статуса и психологическую помощь. Эти меры могут уменьшить одышку, улучшить переносимость повседневных физических нагрузок и качество жизни независимо от тяжести функциональных нарушений [94].
Наблюдение за больными ИЛФ необходимо для активного выявления случаев прогрессирующего течения заболевания, для оценки динамики симптомов и выявления осложнений терапии [1].
- Всем пациентам с ИЛФ рекомендуется измерять ФЖЕЛ и DLCO для мониторирования течения заболевания в повседневной врачебной практике с интервалом в 3 – 6 мес [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: В нескольких когортных клинических исследованиях подтверждено, что снижение абсолютных значений ФЖЕЛ на 10% (с одновременным снижением DLCO или без) либо снижение абсолютных значений DLCO на 15% (с одновременным снижением ФЖЕЛ или без) является суррогатным маркером летальности и, при отсутствии других объяснений, маркером прогрессирования заболевания [35,95]. Прогрессирование болезни также может отражать меньшее (на 5-10%), но неуклонное снижение ФЖЕЛ [96].
- При каждом посещении больного ИЛФ рекомендуется оценивать оксигенацию в покое с помощью пульсоксиметра [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: Оксигенация с помощью пульсоксиметра должна оцениваться в покое и при физической нагрузке у всех больных вне зависимости от симптомов, для выявления потребности в кислородотерапии. Такие измерения следует выполнять исходно и через каждые 3–6 мес. наблюдения.
- При быстром ухудшении респираторных симптомов следует исключить обострение ИЛФ и другие возможные причины, например ТЭЛА, пневмоторакс, респираторную инфекцию, аспирацию [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: У больных ИЛФ могут развиваться такие сопутствующие состояния, как ЛГ, ТЭЛА, рак легкого, ИБС, которые влияют на выживаемость. Однако роль рутинного скрининга для диагностики этих состояний и заболеваний у больных ИЛФ (например, ежегодная ВРКТ для ранней диагностики рака легкого) не изучена.
Плановое ведение больного с ИЛФ осуществляется в условиях первичной специализированной (амбулаторной) медицинской помощи.
Показания для госпитализации в медицинскую организацию:
1) плановая госпитализация в стационар осуществляется для подтверждения диагноза ИЛФ (выполнение хирургической биопсии легкого);
2) экстренная госпитализация в стационар осуществляется при обострении ИЛФ (нарастание одышки, ухудшение оксигенации) либо при развитии осложнений ИЛФ (ТЭЛА, острая инфекция нижних дыхательных путей).
Показания к выписке пациента из медицинской организации:
1) стабилизация клинического состояния;
2) сатурация крови кислородом не ниже 93% в покое при дыхании комнатным воздухом или на фоне кислородотерапии.
В силу возраста - 60 лет и старше – у больных ИЛФ часто имеются многочисленные сопутствующие заболевания, осложняющие течение и лечение ИЛФ и негативно влияющие на прогноз.
Рак легкого
У 12-14% больных ИЛФ развивается периферический рак легкого, чаще аденокарцинома, плоскоклеточный и мелкоклеточный рак [97,98]. Эти заболевания имеют общие факторы риска и патогенетические механизмы. Однако в силу невысокой частоты такого сочетания доказательная информация по лечению ИЛФ в сочетании с раком легкого отсутствует. В то же время сочетание ИЛФ с раком легкого значительно повышает риск летального исхода по сравнению с больными ИЛФ без рака легкого [99].
Легочная гипертензия
ЛГ - повышение срДЛА ≥ 25 мм рт.ст. по данным катетеризации правых камер сердца - наиболее частое осложнение ИЛФ (20 - 84 %, по данным разных авторов). Формирование ЛГ ведет к усилению одышки, снижению физических резервов пациента, повышает риск летального исхода [1].
- Большинству больных ИЛФ с ЛГ не рекомендуется назначение специфических препаратов для лечения ЛГ, однако у отдельных больных такая терапия может улучшить легочную гемодинамику и переносимость физической нагрузки [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: В целом, наиболее обоснованным методом терапии ЛГ при заболеваниях легких остается длительная кислородотерапия в домашних условиях. У больных с тяжелой ЛГ (срДЛА > 35 мм рт.ст.), подтвержденной при катетеризации правых отделов сердца, возможна пробная терапия силденафилом, который может улучшить легочную гемодинамику и переносимость физической нагрузки без ухудшения оксигенации [100-102]. Также есть отдельные данные о положительных эффектах ингаляционного илопроста (Код АТХ: B01AC11) [103] и бозентана [104]. Необходимы специальные клинические исследования по терапии ЛГ у больных ИЛФ.
Гастроэзофагеальный рефлюкс
ГЭР сопровождается микроаспирацией желудочного содержимого и может рассматриваться как триггер альвеолярного повреждения и фактор, ухудшающий течение ИЛФ, однако нередко протекает бессимптомно.
- Большинству больных ИЛФ с бессимптомным ГЭР рекомендуется медикаментозное лечение ГЭР, хотя у отдельных больных оно нецелесообразно [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств5)
- Больным ИЛФ с ГЭР рекомендованы модификация образа жизни (прием малых порций пищи, подъем головного конца кровати), а при клинически значимом ГЭР, не контролируемом медикаментозной терапией, и объективном подтверждении тяжелого кислого рефлюкса рекомендуется фундопликация [105].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: Опубликованы доказательства того, что медикаментозное или хирургическое лечение ГЭР позволяет стабилизировать функцию легких и замедлить прогрессирование ИЛФ [105-108]. Фундопликация желудка по Ниссену, которая уменьшает как кислотный рефлюкс, так и некислотный рефлюкс и микроаспирацию, улучшает выживаемость пациентов ИЛФ [109]. Модификация образа жизни (прием малых порций пищи, подъем головного конца кровати и др.) являются оправданными рекомендациями для пациентов ИЛФ с симптомами ГЭР [105].
Обструктивное апноэ сна (ОАС)
У 20 – 68% больных ИЛФ встречается ОАС, определяемое как увеличение индекса апноэ-гипопноэ > 15 эпизодов в час [110]. Сопряженная с ОАС гиповентиляция усугубляет гипоксемию и ЛГ [111].
- Всем больным ИЛФ рекомендуется проводить скрининг ночной десатурации с последующей диагностикой ОАС [111].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
- Больным ИЛФ с ночной десатурацией рекомендуется назначение кислородотерапии во время ночного сна в качестве паллиативного лечения [110].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: Диагностика ОАС у больных ИЛФ сложна, так как дневная сонливость и слабость характерны для обоих состояний. В то же время ночная десатурация встречается при ИЛФ достаточно часто. По результатам единичных исследований, СРАР-терапия у больных ИЛФ улучшает качество жизни, однако не влияет на летальность. [111].














