Дегенеративно дистрофические заболевания позвоночника (дегенеративно-дистрофические изменения позвоночника) – мультифакториальное, хроническое, рецидивирующее заболевание. Первично изменения появляются в пульпозном ядре межпозвонкового диска, распространяются на фиброзное кольцо, затем на другие элементы позвоночного двигательного сегмента (ПДС), проявляющееся в определенных условиях полиморфными (рефлекторными, компрессионными, компрессионно-рефлекторными и рефлекторно-компрессионными) неврологическими синдромами [1].
Дегенеративный стеноз позвоночного канала – это патологическое сужение центрального позвоночного канала, латерального кармана или межпозвонкового отверстия за счёт вторжения костных, хрящевых или мягкотканных структур, проявляющееся клиническими симптомами компрессии и ишемии нервных корешков и (или) спинного мозга.
Дегенеративный спондилолистез – переднее смещение вышележащего позвонка по отношению к нижележащему, формирующееся за счёт дегенеративных изменений элементов ПДС [1].
Дисфункция крестцово-подвздошного сустава (сочленения) – это состояние, характеризующееся изменением подвижности в данном суставе, с его блокированием или микро-нестабильностью, что ведет к сопутствующим неадекватным, стрессовым нагрузкам на окружающие ткани (капсулу, связки, мышцы, кости).
Сакроилеит – это воспалительный процесс в крестцово-подвздошном суставе (сочленении), который может быть как самостоятельным заболеванием, так и симптомом других болезней инфекционного или аутоиммунного характера.
Спондилоартроз – это поражение дугоотростчатых суставов (ДС), которое развивается в той же последовательности морфологических изменений, как при остеоартрозе периферических суставов. Спондилоартроз сопутствует пожилому возрасту в 85-90% случаев [1].
До настоящего времени нет точных данных об этиологии дегенеративных заболеваний позвоночника. Существует лишь ряд теорий, рассматривающих в качестве причин развития дегенеративных поражений позвоночника различные факторы: инволютивные, дизонтогенетические, механические, иммунные, гормональные, дисметаболические, сосудистые, инфекционные, функциональные и наследственные.
Наиболее распространенной является инволютивная теория, согласно которой происходит локальное преждевременное старение хряща и кости в результате предшествовавших повреждений – механических, воспалительных и т.п. [2]. Согласно этой теории, развитие инволютивных дегенеративных изменений в позвоночнике предопределено генетически, а возникновение дегенерации как болезни, с соответствующими клиническими проявлениями, обусловлено влиянием различных эндогенных и экзогенных факторов.
Если причину дегенеративно-дистрофических изменений удается установить не всегда, то его патогенез достаточно хорошо исследован. Хотя и в данном разделе изучения дегенеративно-дистрофических изменений имеются дискуссионные моменты.
Дегенерация межпозвонкового диска развивается, когда катаболизм протеинов матрикса начинает преобладать над процессом их синтеза. Важнейшим пусковым моментом для этого может быть нарушение условий питания диска. Межпозвонковый диск – одна из самых аваскулярных тканей в организме человека. По мере роста МПД его васкуляризация снижается, поэтому снижается и поступление питательных веществ в ткани. Это уменьшает способность клеток диска синтезировать новый матрикс, ограничивает их пролиферативный потенциал, что приводит к снижению их плотности в диске с возрастом. Результаты гистологических исследований показывают, что причина начала инволютивных и/или дегенеративных изменений межпозвонковых дисков – нарушение питания на фоне исчезновения кровеносных сосудов в замыкательных пластинках позвонков [1].
На молекулярном уровне дегенерация диска проявляется уменьшением диффузии питательных веществ и продуктов катаболизма, снижением жизнеспособности клеток, накоплением фрагментов клеток (вследствие апоптоза) и дегенерированных макромолекул матрикса, уменьшением синтеза протеогликанов, повреждением нормального коллагенового каркаса [3].
Данные изменения являются причиной дегидратации (из-за снижения концентрации хондроитинсульфатов). При этом пульпозное ядро теряет гидростатические свойства, т.е. утрачивает способность распределять вертикальные нагрузки равномерно по всему объему и перестает предохранять фиброзное кольцо от несвойственных его природе сил компрессии. Фиброзное кольцо становится объектом постоянных механических воздействий, вследствие чего в нем развиваются патологические изменения: дезорганизация нормальной слоистой структуры в результате повреждения коллагенового матрикса, что приводит к возникновению трещин и разрывов фиброзного кольца. При развитии таких изменения межпозвонковый диск становится уязвимым для разрушающего воздействия биомеханических влияний, возникающих в условиях нагрузок и усилий человека при его нормальной активности. В результате уменьшения давления в диске напряженность волокон фиброзного кольца уменьшается, нарушаются фиксационные свойства диска, появляется патологическая подвижность в ПДС. Таким образом, идеология данного представления о патогенезе дегенеративно-дистрофических изменений заключается в том, что патологическая подвижность является следствием, а не причиной дегенерации диска.
Еще одним моментом в патогенезе дегенеративных изменений МПД – врастание в фиброзное кольцо межпозвонкового диска нервов и кровеносных сосудов, что является важной особенностью структурно разрушенных дисков [3].
Врастание внутрь возникает ввиду потери гидростатического давления, которое свойственно внутренним областям неповрежденных дисков. Снижение содержания протеогликанов в дегенерированных дисках также облегчает врастание нервов и капилляров [4].
Однако наличие сосудов и нервных волокон не могут влиять на регенераторные способности клетки, так как архитектоника, в которой они нормально функционировали, и ультраструктурные взаимодействия утрачены.
Спондилоартроз чаще бывает вторичным относительно дегенеративно-дистрофических изменений межпозвонкового диска. Снижение высоты измененного диска и (или) патологическая подвижность позвонков неминуемо ведут к перегрузке ПДС, функциональной недостаточности, а затем и дистрофическому поражению суставных отростков. Первичный спондилоартроз бывает значительно реже. Обычно он связан с травмой или значительной хронической перегрузкой суставов позвоночника. Как при артрозе других суставов, при спондилоартрозе возникает субхондральный склероз, некротизация суставных хрящей, неровность суставных поверхностей, а затем и краевые костные разрастания этих отростков для увеличения площади опоры на неполноценные суставные хрящи. Перерастяжение и дистрофия капсульно-связочного аппарата ведут к патологической подвижности позвонков. Нередко формируются защитные костные выступы на суставных отростках, резко ограничивающие подвижность в суставе. Патологическая импульсация из пораженных суставов формирует местные, отраженные и другие более сложные рефлекторно-болевые синдромы, которые в литературе чаще фигурируют как фасеточный синдром.
Костные разрастания суставных отростков могут оказывать динамическое, а затем и стойкое компрессирующее воздействие на прилежащие нервно-сосудистые образования, появляются компрессионные синдромы спондилоартроза. Часто их ошибочно принимают за клинические проявления дегенеративно-дистрофических изменений позвоночника, что может привести к неэффективному хирургическому лечению, если после удаления компримирующего фактора в виде грыжи диска, сохраняется сдавление костными разрастаниями суставных отростков. Спондилоартроз редко бывает изолированным процессом. При жалобах «на боли в спине» он, как правило, диагностируется в сочетании с другой патологией.
Среди этиологических факторов боли в КПС можно выделить внутрисуставные и внесуставные факторы. Внутрисуставные факторы включают: артрит или сакроилеит при системных заболеваниях и инфекции, а таже артроз КПС. К внесуставным факторам относят: переломы, повреждения связок и энтезопатии в области КПС, беременность, состояния после стабилизирующих операций на поясничном отделе позвоночника [5].
Дегенеративные поражения позвоночника и связанные с ними боли и неврологические проявления относятся к одной из важнейших проблем современной медицины. Это обусловлено стабильно высоким количеством больных трудоспособного возраста, зачастую неудовлетворительными результатами консервативной терапии, частыми рецидивами болевого синдрома после хирургического лечения. Боли в спине ограничивают жизнедеятельность, снижают качество жизни пациентов, изменяют психику и поведение людей [6]. Более чем у половины пациентов, страдающих дегенеративно-дистрофическими изменениями позвоночника, имеются признаки хронического эмоционального напряжения.
Частота встречаемости проявлений дегенеративно-дистрофических изменений межпозвонковых дисков растет в геометрической прогрессии в связи с демографическими изменениями, увеличением среднего возраста населения. Доля дегенеративно-дистрофических изменений позвоночника, поражающего людей наиболее активной социальной группы, составляет от 20% до 80% случаев временной нетрудоспособности [7].
В структуре заболеваемости взрослого населения нашей страны дегенеративно-дистрофические изменения составляют 48–52%, занимая первое место по числу дней нетрудоспособности [8].
Временная утрата трудоспособности, обусловленная некомпрессионными синдромами дегенеративно-дистрофических изменений, составляет 40% неврологических заболеваний. В общей структуре инвалидности от заболеваний костно-суставной системы дегенеративные заболевания позвоночника составляют 20,4% и занимают первое место (41,1%) среди причин первичной инвалидности [7].
Показатель инвалидизации при дегенеративных заболеваниях позвоночника равен 0,4 на 10000 жителей. В структуре заболеваемости периферической нервной системы вертеброгенная патология является ведущей, а основное место в ней (77–81%) занимает дегенеративно-дистрофические изменения позвоночника [9].
Среди инвалидов с заболеваниями периферической нервной системы в 80% случаев наблюдаются вертеброгенные поражения.
Пациенты с клинически значимыми проявлениями дегенеративно-дистрофических изменений позвоночника составляют 51,2 на 1000 населения. Компрессионные и некомпрессионные формы дегенеративно-дистрофических изменений начинают диагностироваться с 15-19 лет (2,6 случая на 1000 населения данной возрастной категории), а уже к 30 годам клинические проявления дегенеративно-дистрофических изменений диагностируются у 1,1% населения, к 59 годам – у 82,5% населения [10].
По данным разных исследователей, несмотря на большие возможности консервативной терапии, в хирургическом лечении дегенеративно-дистрофических изменений позвоночника нуждаются от 5% до 33% больных [10].
Выраженное поражение ДС обнаружено авторами у 80 % 20-30-летних людей и до 100 % — у лиц более старшего возраста.
Спондилоартроз сопутствует не только пожилому возрасту (85-90% случаев), но проявляется и у молодых пациентов 25-30 лет. Как причины возникновения спондилартроза можно рассматривать:
травмы позвоночника с подвывихом в суставах позвоночника;
постоянные повышенные нагрузки на позвоночник, приводящие к неправильному распределению нагрузки на его отделы (сидячая работа, профессиональное занятие спортом, плоскостопие, работа с тяжестями);
врожденные аномалии позвоночника, нестабильность позвонков, спондилолистез, спондилолиз;
дегенеративно-дистрофические изменения позвоночника.
Дисфункция КПС выявляется у 15-30% пациентов с неспецифической болью в нижней части спины [11].
M19.8 - Другой уточненный артроз
M41.5 – Вторичный сколиоз
M42.1 - Остеохондроз позвоночника у взрослых
M42.9 - Остеохондроз позвоночника неуточненный
M43.1 - Спондилолистез
M46.1 - Сакроилеит, не классифицированный в других рубриках
M47.0 - Спондилез
M47.1 - Другие спондилезы с миелопатией
M47.2 - Другие спондилезы с радикулопатией
M48.0 - Спинальный стеноз
M50.0 - Поражение межпозвоночного диска шейного отдела с миелопатией
M50.1 - Поражение межпозвоночного диска шейного отдела с радикулопатией
M50.3 - Другая дегенерация межпозвоночного диска шейного отдела
M50.8 - Другие поражения межпозвоночного диска шейного отдела
M50.9 - Поражение межпозвоночного диска шейного отдела неуточненное
M51.0 - Поражения межпозвоночных дисков поясничного и других отделов с миелопатией
M51.1 - Поражения межпозвоночных дисков поясничного и других отделов с радикулопатией
M51.2 - Другое уточненное смещение межпозвоночного диска
M51.3 - Другая уточненная дегенерации межпозвоночного диска
M53.0 - Шейно-черепной синдром
M53.1 - Шейно-плечевой синдром
M53.2 - Спинальная нестабильность
M54.2 - Цервикалгия
M54.3 - Ишиас
M54.4 - Люмбаго с ишиасом
M54.5 - Боль внизу спины
M54.6 - Боль в грудном отделе позвоночника
M54.8 - Другая дорсалгия
M54.9 - Дорсалгия неуточненная
M96.4 - Постхирургический лордоз
M96.8 - Другие поражения костно-мышечной системы после медицинских процедур
M96.9 - Поражение костно-мышечной системы после медицинских процедур неуточненное
M99.5 - Межпозвонковый дисковый стеноз неврального канала
M99.6 - Костный и подвывиховый стеноз межпозвоночных отверстий
M99.7 - Соединительнотканный и дисковый стеноз межпозвоночных отверстий
S33.6 - Растяжение и перенапряжение капсульно-связочного аппарата крестцово-подвздошного сустава
Клинико-патогенетическая классификация А.И. Осна отражает четыре последовательные стадии дегенеративно-дистрофического поражения [12]:
Стадия внутридискового патологического процесса («хондроза»), создающая патологическую импульсацию из пораженного диска. В этот период происходит внутридисковое перемещение пульпозного ядра. Студенистое ядро через трещины в фиброзном кольце проникает в его богато иннервированные наружные волокна. В результате происходит раздражение нервных окончаний и развиваются болевые ощущения, формирующие рефлекторные синдромы дегенеративно-дистрофических изменений.
Стадия нестабильности или утраты фиксационной способности пораженного диска, динамическое смещение вышележащего позвонка по отношению к нижележащему (в связи с растрескиванием не только пульпозного ядра, но и элементов фиброзного кольца). В этот период могут формироваться синдром нестабильности, рефлекторные и даже некоторые компрессионные синдромы.
Стадия формирования грыж межпозвонковых дисков в связи с нарушением целостности фиброзного кольца (протрузии или пролапса), которые могут сдавливать прилежащие сосудисто-нервные образования, в том числе корешок спинномозгового нерва.
Стадия фиброза межпозвонкового диска и формирования краевых костно-хрящевых разрастаний тел позвонков является преимущественно саногенной, т.к. возникают неподвижность, компенсаторное увеличение площади опоры позвонков на неполноценные диски. В ряде случаев эти костные разрастания, как и грыжи дисков, могут сдавливать прилежащие нервно-сосудистые образования.
Классификация L. Armstrong (1952) также соотносит изменения в ПДС с клиническими проявлениями дегенеративно-дистрофических изменений позвоночника [1].
I стадия. Начальные дистрофические изменения в студенистом ядре и задней части фиброзного кольца, которое набухает, выпячивается по направлению к позвоночному каналу, раздражая рецепторы задней продольной связки твердой мозговой оболочки; при этом появляются боли в спине.
II стадия. Смещенное пульпозное ядро располагается в выпятившейся части фиброзного кольца, через дефект которого выпадает грыжа диска; клинически – появляются корешковые симптомы и, нередко, грубые антальгические компоненты вертебрального синдрома.
III стадия. Прогрессирует дегенерация пролабированного диска, как подсвязочно, так и в эпидуральном пространстве за пределами перфорированной задней продольной связки. Начинается рассасывание или обызвествление частей диска, его фиброз. В области разрыва задней продольной связки могут образоваться костные разрастания («остеофиты»). Выпадение секвестров часто вызывает рубцово-спаечный асептический эпидурит. Непосредственное давление на корешок уменьшается, течение болезни приобретает хронический характер.
Классификация дегенеративных изменений межпозвонкового диска по Pfirrmann C.W. с соавт. (2001) [13]. Стадия дегенерации межпозвонкового диска оценивается на Т2-взешенном изображении МРТ сканов (табл. 1)
Таблица 1. Классификация дегенеративных изменений межпозвонкового диска по Pfirrmann с соавт. (2001).
Стадия |
Структура межпозвонкового диска |
Интенсивность сигнала |
Четкость разделения фиброзного кольца и пульпозного ядра |
Высота межпозвонкового диска |
|---|---|---|---|---|
I |
гомогенная |
гиперинтенсивный (белый) |
четкая граница |
нормальная |
II |
негомогенная |
гиперинтенсивный (белый) |
четкая граница |
нормальная |
III |
негомогенная |
промежуточный (серый) |
нечеткая |
нормальная или слегка уменьшенная |
IV |
негомогенная |
промежуточный (серый) |
отсутствует граница |
нормальная или умеренно уменьшенная |
V |
негомогенная |
гипоинтенсивный (черный) |
отсутствует граница |
резко снижена |
1.5.1 Классификация грыж межпозвонковых дисков
Классификация Северо-Американской Ассоциации Вертебрологов (2014 г) [14]:
протрузия - выстояние ткани диска за пределы лимба тел позвонков, при котором основание грыжевого выпячивания больше продольного размера выпячивания;
экструзия - выстояние ткани диска за пределы лимба тел позвонков, при котором основание грыжевого выпячивания меньше продольного размера выпячивания;
секвестр - полное отделение от диска сместившегося фрагмента.
Возможно дополнительное классифицирование грыжи межпозвонковых дисков для уточнения ее локализации, смещения, плотности и т.д.
1.5.2 Классификации стеноза позвоночного канала
Классификация H. Verbiest [15]
I. По этиологии: врожденный и стеноз развития
II. а. Чистый абсолютный стеноз (сагиттальный диаметр ПК равен 10мм и менее)
b. Чистый относительный стеноз (сагиттальный диаметр ПК 10-12мм)
c. Смешанный стеноз
1) Cтеноз производимый костными стенками позвоночного канала:
A. врожденный стеноз
B. стеноз развития в результате врожденных ошибок роста
C. идиопатический стеноз развития
D. приобретенный стеноз
E. рецидивирующий стеноз
2) Cтеноз, производимый некостными компонентами стенок позвоночного канала:
A. Гипертрофия с (или без) кальцификацией задней продольной или желтой связки, или их обеих.
B. Массивная центральная грыжа диска или массивное подсвязочное распространение секвестрированного материала диска
Классификации стеноза позвоночного канала Arnoldi [16]
I. Врожденный
a. Идиопатический
b. Ахондропластический
II. Приобретенный
a. Дегенеративный стеноз
i. Центрального отдела позвоночного канала
ii. Периферического отдела позвоночного канала
iii. Дегенеративный спондилолистез.
b. Комбинированный (любые комбинации врожденного/
приобретенного стеноза, дегенеративного стеноза и грыжи диска)
c. Спондилолистез со спондилолизом
d. Ятрогенный
i. Постляминэктомический
ii. После переднего и заднего спондилодеза
iii. После хемонуклеолиза диска
e. Поздние посттравматические изменения позвоночника
f. Прочие виды стеноза: болезнь
i. Педжета
ii. Флюороз.
С практической точки зрения удобна анатомическая классификация стенозов, в соответствии с которой выделяют следующие его формы: центральный стеноз, латеральный стеноз, стеноз межпозвонкового канала (фораминальный стеноз) и сочетанный стеноз. Латеральные стенозы детально описаны и классифицированы Lee et al [17]. Зона входа в межпозвонковое отверстие является латеральным рецессусом, и причинами радикулярной компрессии здесь являются гипертрофия верхнего суставного отростка, врожденные особенности развития дугоотростчатых суставов и остеофиты края тела позвонка. Средняя зона ограничена спереди задней поверхностью тела позвонка, медиальные отделы этой зоны открыты в сторону центрального канала. Основными причинами стенозов в средней зоне являются остеофиты тел позвонков или в месте прикрепления желтой связки, а также гипертрофия жёлтой связки. В 41,7% случаев имеется так называемая интрафораминальная связка, изменения которой могут быть причиной компрессии спинномозгового корешка. Зона выхода из межпозвонкового отверстия ограничена спереди нижележащим межпозвонковым диском, сзади – наружными отделами дугоотростчатых суставов. Причинами компрессии в этой зоне служат гипертрофические изменения и сублюксация дугоотростчатых суставов, остеофиты верхнего края межпозвонкового диска.
Классификация стенозов позвоночного канала по данным МРТ С. Sсhizas (2010) [18] (рис. 1):
Класс А: Ликвор видим в пределах дурального мешка, но его распределение неоднородно. Выявляются корешки, есть эпидуральный жир. Данная группа подразделяется на подгруппы А1 до А4: A1 – корешки лежат дорсально и занимают менее половины дурального пространства; A2 – корешки лежат дорсально в контакте с твердой мозговой оболочкой, но в форме подковы; A3 – корешки лежат дорсально и занимают более половины площади дурального мешка; А4 – корешки лежат в центре и занимают большую часть площади дурального мешка.
Класс B: определяется концентрация нервных корешков, нет уровня цереброспинальной жидкости, корешки равномерно распределены в срезе и различимы, есть эпидуральный жир.
Класс С: подразумевает наличие концентрации нервных корешков, цереброспинальная жидкость не видна, определяется эпидуральный жир.
Класс D: полный стеноз канала, нет уровня цереброспинальной жидкости, цереброспинальная жидкость не видна, нет эпидурального жира.
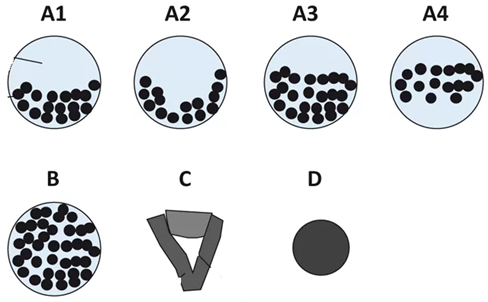
Рисунок 1. Классификация поясничного спинального стеноза по С. Sсhizas.
1.5.3 Классификация дегенеративного спондилолистеза (табл. 2)
Таблица 2. Классификация O. Gille (2017).
Тип |
Описание |
Параметры |
Подтип |
Описание подтипа |
|---|---|---|---|---|
Тип 1 |
LL адаптирован к PI (гармоничный позвоночника) |
PI-LL<10° |
1A |
Сохраненный сегментарный лордоз (SL) |
1B |
Изменённый SL с сохранённым LL |
|||
Тип 2 |
Компенсированный дисбаланс |
PI-LL>10° |
2А |
Сохранённый глобальный баланс без тазовой компенсации (Pelvic tilt PT < 25°) |
2B |
Сохранённый глобальный баланс с тазовой компенсацией (PT > 25°) |
|||
Тип 3 |
Изменённый глобальный баланс (SVA > 40 мм) |
SVA > 40 мм |
3 |
1.5.4 Классификация дегенеративного сколиоза и нарушений сагиттального баланса
Классификация Aebi [19]
Тип 1: первичный дегенеративный сколиоз («de novo scoliosis»)
Тип 2: идиопатический ювенильный сколиоз грудного и (или) поясничного отдела позвоночника с прогрессированием деформации в основных дугах в течение «взрослой» жизни
без выраженных вторичных дегенеративных изменений
с выраженными вторичными дегенеративными изменениями
Тип 3: вторичные сколиозы взрослых
вследствие разной длины нижних конечностей, косого таза, пояснично-крестцовых аномалий, идиопатического, нейромышечного или врожденного сколиоза, травмы или ятрогении
вследствие метаболических нарушений кости (остеопороз)
Классификация, учитывающая тип дуги и 3 сагиттальных параметра: PI – pelvic incidence; LL – поясничный лордоз; PT – наклон таза; SVA – сагиттальная вертикальная ось (рис. 2).
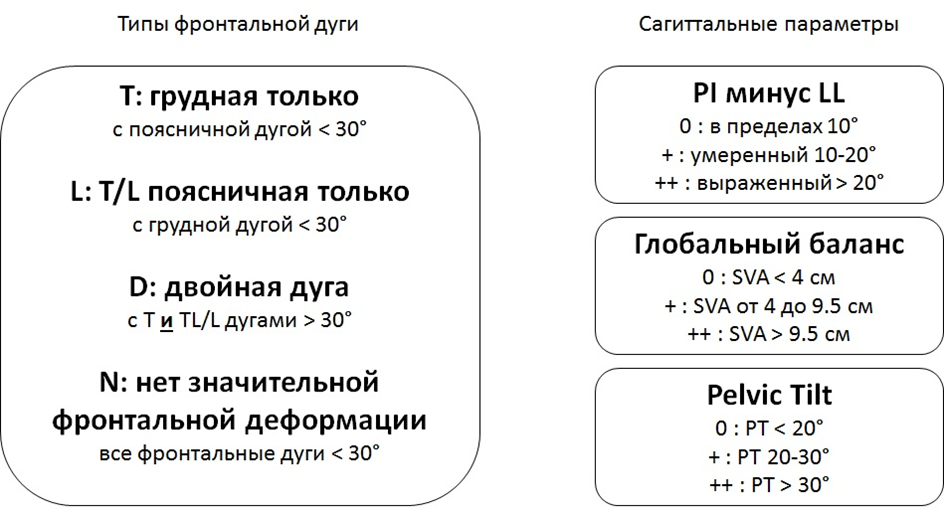
Рисунок 2. Классификация SRS-Schwab [20].
Критерии классификации сколиоза у взрослых в зависимости от тактики хирургического лечения (табл. 3).
Таблица 3. Классификация P. Berjano и C. Lamartina (2013) [21].
Тип деформаций |
Критерии |
Хирургическая стратегия |
|---|---|---|
Тип I: локализованное сдавление нерва при сколиозе у взрослых |
Спинальный стеноз на 1-2 уровне и Два диска, находящиеся между верхним уровнем фиксации и вершиной дуги и Отсутствие серьезной дегенерации или нестабильности (включая латеролистез) выше уровнем и Без сагиттального дисбаланса |
Адресная декомпрессия или адресная декомпрессия и фиксация, если нестабильность уже существует или появится после операции |
Тип II: ограниченная патология диска внутри дуги |
Симптомные диски внутри дуги (например, изменения Модик 1 типа в некоторых дисках, латеролистез на одном или двух дисках, вакуум феномен в дисках с коллапсом) и Чаще без сагиттального дисбаланса (Lumbar lordosis > Pelvic Incidence) и Фронтальный дисбаланс < 4 см и Непрогрессирующая дуга и Дуга менее < 30° и В идеале симптомные диски вокруг (выше и ниже) вершины поясничной дуги |
Необходимо рассмотреть вариант только переднего XLIF (когда коррекция не требуется или небольшая) или XLIF плюс задняя фиксация для коррекции сагиттального баланса или для восстановления фронтального баланса после переднего вмешательства |
Тип III: тяжелая фронтальная деформация |
Боль во всей дуге или Прогрессирующая дуга или Более тяжелая дуга >30° или Фронтальная деформация с умеренным сагиттальным дисбалансом или с сагиттальной компенсацией |
Фиксация всей дуги (при наличии деформации во фронтальной и сагиттальной плоскостях): XLIF на всех уровнях или на более ригидном сегменте плюс задняя фиксация В итоге задняя коррекция фронтального дисбаланса, если он присутствует после XLIF Если диски в нейтральных зонах дуги сохранены и подвижны при боковых наклонах, необходимо выполнение XLIF на вершине дуги (2 диска если вершиной является позвонок, 3 диска если вершиной является диск) с деротацией и компрессией на вершине дуги с помощью заднего инструментария |
Тип IV: сагиттальный дисбаланс |
Нет или небольшая фронтальная деформация Сагиттальный дисбаланс или Сагиттальная компенсацией с выраженным болевым синдромом в спине или Сагиттальная компенсацией со стенозом |
Необходима задняя фиксация плюс остеотомия. Требуется рассмотреть возможность добавления XLIF (в тот же день или этапно) для увеличения жесткости вокруг PSO или в дестабилизированных сегментах после SPO В случае сочетания тяжелой сагиттальной и фронтальной деформаций необходимо выполнение XLIF на всех уровнях или на более ригидном участке и на уровнях с планируемой задней остеотомией плюс задняя фиксация В отдельных случаях, где требуется коррекция менее 30°, необходимо рассмотреть XLIF с использованием гиперлордотических кейджей плюс задняя фиксация |
1.5.5 Классификация спондилоартроза (табл. 4)
Стадия |
Субхондральный склероз |
Дегенерация хряща |
|---|---|---|
I |
Суставной отросток имеет тонкий слой кортикальной кости |
Равномерно толстый хрящ полностью покрывает суставную поверхность |
II |
Кортикальная кость суставных отростков локально утолщена |
Хрящ покрывает всю поверхность суставных поверхностей, но имеются очевидные элементы эрозии |
III |
Кортикальная кость утолщена, но меньше чем на половине поверхности суставных отростков |
Хрящ покрывает не всю поверхность суставных поверхностей, имеются оголенные регионы |
IV |
Плотная кортикальная кость покрывает больше половины поверхности суставных отростков |
Хрящ отсутствует, за исключением следов на суставной поверхности |
Таблица 4. Классификация стадий дегенерации суставного хряща и субхондрального склероза дугоотростчатых суставов по данным МРТ Grogan, 1997 [12].
Клинические симптомы и синдром дегенеративно-дистрофических изменений позвоночника могут делятся на рефлекторными и компрессионными.
А. Компрессионные синдромы дегенеративно-дистрофических изменений поясничного отдела позвоночника:
1) Корешковый компрессионный синдром.
компрессия верхне-поясничных корешков (L1–L3) встречается редко.
синдром корешка L4 (диск L3-L4) – иррадиация болей в передневнутренние отделы бедра, голени и внутреннюю лодыжку, гипестезия на передней поверхности бедра, слабость четырёхглавой мышцы, снижение или утрата коленного рефлекса;
синдром корешка L5 (диск L4-L5) – иррадиация болей из верхней ягодичной области в наружные отделы бедра и голени, иногда с распространением на тыл стопы, на I-III пальцы, гипестезия в этой же зоне; слабость перонеальной группы мышц, возможна гипотрофия, слабость разгибателя I пальца стопы;
синдром корешка S1 (диск L5-S1) – иррадиация болей из средней ягодичной области в задненаружные или задние отделы бедра, голени, в пятку с переходом на наружный край стопы и IV–V пальцы, гипестезия в задненаружных отделах голени и наружных отделах стопы; гипотрофия большой ягодичной и икроножной мышц, слабость икроножной мышцы, снижение или отсутствие ахиллова и подошвенного рефлексов.
2) Нейрогенная перемежающаяся хромота (Синдром Дежерина). Патогенетический механизм – механическое сдавление и ишемия невральных структур. Ишемия усиливается в вертикальном положении (в положении стоя во время ходьбы). При ходьбе сегментарная ротация приводит к ещё большему сужению позвоночного канала и ухудшению кровоснабжения спинного мозга и его элементов. Данный синдром имеет клиническую триаду: боль, нарушение чувствительной и двигательной сфер. Особенностью является то, что данные симптомы могут отсутствовать в покое в горизонтальном положении, но появляются при вертикализации и ходьбе.
3) Синдром полирадикулярной компрессии. Проявляется клинической картиной компрессии 2-х и более корешков каудальной группы.
4) Каудо-медуллярный синдром. Данный синдром возникает как при компрессии корешков каудальной группы, так и при сдавлении радикуло-медуллярной артерии (Депрож-Готтерона), что приводит к ишемии конуса и эпиконуса спинного мозга. Возникает клиническая картина нижнего вялого парапереза и нарушение функций тазовых органов по периферическому типу, сегментарными и корешковыми расстройствами чувствительности в аногенитальной области и ногах.
Б. Компрессионные синдромы шейного остеохондроза:
Корешковый синдром
o Синдром компрессии корешка С4 – проявляется болями в надплечье, может сопровождаться, амиотрофией трапециевидной, надостной и даже большой грудной мышцы.
o Синдром компрессии корешка С5 – проекционная боль и чувствительные расстройства локализуются в зоне дельтовидной мышцы, могут сопровождаться с ее слабостью и гипотрофией, снижением лопаточного рефлекса.
o Синдром компрессии корешка С6 – проекционная боль и чувствительные расстройства локализуются в виде полосы по наружному краю руки, до первого пальца кисти. Снижается сила мышц, сгибающих предплечье, нарушается рефлекс с двухглавой мышцы.
o Синдром компрессии корешка С7 – проекционная боль и чувствительные расстройства локализуются в виде полосы на тыльной поверхности руки, особенно в трех средних пальцах. Триципитальный рефлекс обычно снижен или отсутствует. Могут быть вегетативно-трофические нарушения в кисти.
o Синдром компрессии корешка C8 – проекция болей и чувствительных расстройств соответствует ульнарному краю руки, включая четвертый и пятый пальцы. Может быть снижен карпорадиальный рефлекс.
Синдром компрессии спинного мозга (миелопатия). Данный синдром проявляется двигательными и чувствительными сегментарными нарушениями на уровне компрессии и проводниковыми расстройствами ниже сдавления спинного мозга, нарушением функций тазовых органов по центральному типы, патологическими рефлексами.
В. Рефлекторные (некомпрессионные) синдромы остеохондроза поясничного отдела позвоночника:
1) местные болевые синдромы (люмбалгия, люмбаго);
2) рефлекторные отраженные синдромы (люмбоишиалгия, псевдоабдоминальные боли, псевдогенитальные боли и др.);
3) рефлекторные миодистонические, включая рефлекторно-компрессионные или туннельные синдромы:
а) синдром малой ягодичной мышцы;
б) синдром средней ягодичной мышцы;
в) синдром грушевидной мышцы;
г) «симфизо-стернальный синдром», «синдром симфиза», абдоминальгический синдром, пубальгия;
д) вертеброгенный подвздошно-поясничный синдром;
е) мышечно-тонические нарушения в абдукторах бедра, «ягодично-трактовый синдром»;
ж) аддукторный синдром;
з) тонические нарушения в ишиокруралъных мышцах бедра;
и) тонические нарушения в передней большеберцовой мышце;
к) крампи;
4) рефлекторные миосклеротомные (дистрофические) синдромы:
а) трохантериит;
б) коленный эпикондилит;
в) голеностопные и стопные периартрозы, метатарзальгия;
г) вторичные компрессионные синдромы нервов ноги в связи с дистрофией соединительнотканных структур (туннельные синдромы ущемления периферических нервов);
5) рефлекторные ангиопатические синдромы:
а) дистония сосудов ног с преобладанием вазоспазма или вазодилатации;
в) локальные экстравертебральные компрессионные и рефлекторные вазодистонии;
г) подгрушевидный синдром перемежающейся хромоты;
д) синдром беспокойных ног;
е) общие вертеброгенные и рефлекторные вазодистонии;
ж) синдром облитерирующего заболевания сосудов ног;
6) дискогенные патобиомеханические синдромы позвоночника или других суставов: функциональные блоки, регионарный постуральный дисбаланс мышц, неоптимальный двигательный стереотип [1].
Г) Рефлекторные (некомпрессионные) синдромы остеохондроза шейного отдела позвоночника:
1. Местные вертебральные синдромы;
2. Отраженные болевые синдромы;
3. Рефлекторные миодистонические синдромы;
Синдром нижней косой мышцы головы
Синдром передней лестничной мышцы
Синдром мышцы, поднимающей лопатку (лопаточно-реберный синдром);
Синдром малой грудной мышцы;
Туннельные синдромы нервов шеи и руки
4. Рефлекторные дистрофические синдромы;
Плечелопаточный периартроз;
Синдром плечо-кисть;
Эпикондилез;
Миофасциальные синдромы;
Синдром передней грудной стенки;
Синдром множественного нейроостеофиброза
5. Рефлекторные ангиопатические (нейроваскулярные) синдромы;
Дистонический синдром позвоночной артерии;
Ангиопатический кардиальгический синдром;
Ангиопатический спинальный синдром;
Ангиопатические брахиальные синдромы.
6. Дискогенные патобиомеханические нарушения
Боль при патологии крестцово-подвздошного сочленения может локализоваться в нижних отделах поясницы, крестца, таза ягодичной области. Обычно боль локализуется не выше уровня пояса, ниже уровня L5 позвонка. Возможно распространение болевого паттерна по задней поверхности ноги до уровня колена. Чаще болевой синдром при патологии КПС носит односторонний характер [22]. Важным признаком, указывающим на этиологическую роль КПС в болевом синдроме в пояснично-крестцовом отделе позвоночника, является положительный пальцевой признак Фортина.
Для оценки интенсивности болевого синдрома используют визуально-аналоговую (ВАШ) или цифровую рейтинговою шкалы (ЦРШ) (Приложение Г1) [23]. Оценка качества жизни пациентов с поясничным остеохондрозом проводится на основе индекса недееспособности Освестри (ODI – Oswestry disability index) (Приложение Г2) и европейского вопросника оценки качества жизни (EQ-5D – European Quality of Life Questionnaire – 5 dimension) (Приложение Г3) [23, 24]. Оценка качества жизни пациентов с шейным остеохондрозом проводится на основе Индекс ограничения жизнедеятельности из-за боли в шее (NDI - Neck Disability Index) (Приложение Г5) [25]. Оценка неврологического статуса пациентов с шейном миелопатией проводится по шкале оценки неврологического статуса Frankel (Приложение Г4) [26, 27]. Клинические шкалы и опросники очень широко применяются для оценки эффективности лечения. Однако статистически значимые различия не всегда означают улучшение результатов с точки зрения пациента. Для этого используется параметр минимальная клинически значимая разница (minimum clinically important difference MCID) [28]. MCID для каждой шкалы имеет отличающиеся значения на разных сроках наблюдения, характере патологии и видах хирургической помощи.
Критерии установления заболевания или состояния: диагноз устанавливается на основе жалоб, клинического осмотра, магнитно-резонансной томографии позвоночника. При необходимости диагноз может быть уточнен на основании данных лабораторных методов исследования, данных рентгенографии позвоночника и суставов, специальных исследований и проекций, рентгенографии позвоночника с функциональными пробами и рентгенографии позвоночника вертикальной, во весь рост, компьютерной томографии позвоночника.
Описаны в разделе «клиническая картина» (см раздел 1.6)
Рекомендовано обследовать пациента в положениях стоя, сидя и лежа [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии: Может обнаружиться патологическая поза с анталгическим (противоболевым) сколиозом, а также изменением физиологических грудного кифоза и поясничного лордоза. Необходимо выяснить возникли эти изменения осанки с момента болевого приступа или они существовали и раньше. Положив ладони обеих рук на крылья подвздошных костей с обеих сторон и расположив большие пальцы на уровне ладоней, проводят пальпацию паравертебральных мышц отмечая их болезненность. Фиксировав таз руками, а если возможно, усадив пациента на стул, следует предложить ему наклониться вперёд, назад, в стороны, насколько это возможно, проделать ротационные движения туловищем, наблюдая за характером движений позвоночного столба и осведомляясь о степени болезненности движений и о том, где именно ощущается болезненность. В норме все эти движения должны быть плавными и симметричными по амплитуде. Проводится проба с осевой нагрузкой на позвоночник (давление на голову, плечи), которая может быть болезненной. Активное сгибание поочерёдно одной и другой ноги в тазобедренном суставе самим больным в положении лёжа на спине, обычно вызывает боль в зоне основной патологии (ягодичной, крестцовой) вследствие неизбежного сокращения мышц этой области.
В положении лежа необходимо определение симптомов натяжения:
- симптом Ласега – пациент лежит на спине с разогнутыми ногами в тазобедренных и коленных суставах. Далее поочередно левая и правая нижняя конечность сгибается в тазобедренном суставе при разогнутом коленном суставе до появления или усиления болевого синдрома по ходу дерматома L5 или S1 корешка. Симптом считается положительным, если боль возникла или усилилась до достижения 45 градусов относительно горизонтали.
- симптом Вассермана - возникновение или усиление боли в зоне дерматомов L3, L4 корешков во время разгибания ноги в тазобедренном суставе у больного, лежащего на животе.
Рекомендовано считать патологию крестцово-подвздошного сустава (КПС) вероятной причиной боли в нижних отделах поясницы при наличии у пациента как минимум 3 положительных клинических тестов на дисфункцию данного сустава [11].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: С целью последующей диагностики патологии КПС могут быть использованы провокационные тесты, дополнительные методы диагностики (рентгенография таза, магнитно-резонансной томографии сустава, компьютерной томографии сустава, диагностические блоки местным анестетиком с рентген-контролем [29].
Провокационные нейроортопедические тесты:
тест компрессии (compression test);
дистракционный тест (distraction test);
тест давления на бедро (thigh thrust test);
тест ФАБЕР (Патрика) (FABER (Patrick`s) test);
тест крестцового сдвига (sacral thrust test);
Тест Йомана (Yeoman test);
Тест Генслена (Gaenslen test).
В 2 систематических обзорах (Hancock и др) [30], (Szadek и соавт.) [31], а также в 1 слепом проспективном исследовании (Laslett и др.) [32] была оценена диагностическая ценность тестов для выявления патологии крестцово-подвздошного сочленения в качестве причины боли в нижнем отделе спины. Авторам исследований удалось установить, что комбинация 3 провокационных тестов позволяет диагностировать патологию крестцово-подвздошного сустава, как основного источника симптомов у пациентов с болью ниже пятого поясничного позвонка. Если шесть тестов на провокацию КПС отрицательны, то патология КПС может быть исключена.
Рекомендуется сбор анамнеза и физикальное обследование с целью выявления факторов риска и заболеваний сердечно-сосудистой системы [33].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: К факторам риска развития сердечно-сосудистых заболеваний относят: артериальную гипертензию, курение, дислипидемию (повышение общего холестерина >4,9 ммоль/л и/или холестерина ЛПНП>3 ммоль/л и/или холестерина ЛПВП у мужчин <1,0 ммоль/л, у женщин - <1,2 ммоль/л и/или триглицеридов> 1,7 ммоль/л), сахарный диабет, семейный анамнез сердечно-сосудистых заболеваний в молодом возрасте (<55 лет для мужчин и <65 лет для женщин) [33]. Под установленным заболеванием сердечно-сосудистым заболеванием понимают: ишемическую болезнь сердца, цереброваскулярную болезнь, периферический атеросклероз, хроническую сердечную недостаточность, легочную гипертензию, клапанные пороки сердца, кардиомиопатии [34].
Рекомендуется оценка риска периоперационных сердечно-сосудистых осложнений с учетом вида планируемого оперативного лечения перелома ПОПК вне зависимости от наличия сопутствующей патологии [33].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5).
Комментарии: При проведении хирургического лечения по экстренным (менее 6 часов) и неотложным (6-24 часа) показаниям периоперационная оценка риска не проводится.
Малые ортопедические операции сопровождаются низким риском развития сердечно-сосудистых осложнений (30-дневный риск развития инфаркта миокарда или смерти от сердечно-сосудистой патологии после операции - менее 1%). Большие ортопедические операции сопровождаются промежуточным (умеренным) риском развития сердечно-сосудистых осложнений (30-дневный риск развития инфаркта миокарда или смерти от сердечно-сосудистой патологии после операции – 1-5%) [35].
Рекомендуется для оценки риска периоперационных сердечно-сосудистых осложнений использовать специальный алгоритм [Приложение Г6] [35].
Уровень убедительности рекомендации В (уровень достоверности доказательств – 5).
Рекомендуется проведение планового хирургического лечения без дополнительного обследования пациентам, у которых риск сердечно-сосудистых осложнений определен как низкий. У пациентов с промежуточным или высоким периоперационным риском развития сердечно-сосудистых осложнений рекомендуется оценка функционального статуса пациента [35].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Рекомендовано исследование уровня N-терминального фрагмента натрийуретического пропептида мозгового (NT-proBNP) в крови в случае промежуточного или высокого риска кардиоваскулярных осложнений и низком функциональном статусе пациента (см. Приложение Г6) [33-35].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Рекомендовано проведение МРТ позвоночника пациентам с жалобами на боль в области позвоночника и конечностях при отсутствии эффекта от приема нестероидных противовоспалительных и противоревматических препаратов для уточнения степени изменений морфологических структур позвоночника и сопоставления с клиническими симптомами для принятия решения о тактике лечения [37, 38].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 2).
Комментарии: Магнитно-резонансная томография (МРТ) позвоночника визуализирует сопутствующие изменения мягких тканей, дает возможность выявить мельчайшие изменения хрящей, костей, связок и сосудов, позволяет с большой точностью определить локализацию грыжевого выпячивания по длине и поперечнику позвоночного канала, степень дегенерации межпозвонковых дисков и нарушения циркуляции ликвора при компрессии дурального мешка и арахноидальных спаечных процессах, дифференцировать грыжевые выпячивания дисков от адгезивных процессов в эпидуральной клетчатке, воспалительных процессов, а также опухолевых и сосудистых новообразований. С некоторой погрешностью при МРТ можно установить размеры позвоночного канала и грыжи диска. МРТ (стандарт) с высокой напряженностью магнитного поля (1,5 – 3,0 Тесла) – основной метод диагностики и нейровизуализации дегенеративных поражений позвоночника. Данный вид исследования в последние десятилетия получил большое распространение и стал определяющим. Он полноценно дает возможность судить о изменениях позвонков, межпозвонковых дисков, связочного аппарата, нервных и других структур. Ввиду неинвазивности метода он может быть выполнен в амбулаторных условиях.
МРТ контроль послеоперационного состояния позвоночника рекомендовано проводить не ранее 3-х мес после оперативного лечения, так как наличие послеоперационных артефактов достигает 100 % на первый день после операции [39, 40].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Рекомендовано пациентам с дегенеративными заболеваниями позвоночника проведение компьютерной томографии позвоночника по показаниям, для детализации дегенеративно-дистрофических изменений и оценки размеров костных структур [38].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Компьютерная томография (КТ) позвоночника проводится в дополнение к МРТ. Она позволяет диагностировать костные и хрящевые изменения на начальных стадиях, определить минимальные аномалии. Так же КТ показана в случае невозможности проведения МРТ (имплантаты из магнитящихся металлов, водитель ритма сердца и т.д.). При введении контрастного средства интрадурально (КТ-миелография) данный метод становится более информативным. КТ-миелография является инвазивным методом исследования, что ограничивает его применение. При проведении КТ и КТ-миелографии есть возможность делать трехмерную реконструкцию позвоночных сегментов.
Рекомендовано пациентам с дегенеративными заболеваниями позвоночника в некоторых случаях, по показаниям, с целью уточнения диагноза проведение рентгенографии позвоночника, специальные исследования и проекции, рентгенографии позвоночника с функциональными пробами, рентгенографии позвоночника, вертикальная с целью оценки структурных и динамических изменений, а также для расчета параметров локального и глобального баланса позвоночника [41].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Обзорная рентгенография с функциональными пробами (прямая проекция в положении стоя прямо, боковая проекция в положении стоя и с наклоном вперед и назад в боковой проекции) позволяет наиболее полно получить общую характеристику костного строения пояснично-крестцового отдела позвоночника, выявить спондилолистез и гипермобильность (нестабильность) позвоночного сегмента, которая может не выявляться при магнитно-резонансной томографии позвоночника, выполняемой в горизонтальном положении, определить высоту межтеловых пространств, артроз межпозвонковых суставов, образование межтеловых остеофитов, выявить аномалию развития позвонков, люмбализацию, сакрализацию. Рентгенография позвоночника, вертикальная (степ-режим или постуральный) проводится следующим образом: боковая проекция - в положении стоя в обычной позе от свода черепа до средней трети бедренных костей, голова в свободном и удобном положении, положение кистей на противоположных ключицах; прямая - в положении стоя в обычной позе от свода черепа до средней трети бедренных костей, положение рук свободное вдоль туловища. Рентгенография позвоночника, вертикальная необходима для определения значений параметров сагиттального и фронтального баланса.
Для выполнения предоперационного планирования может быть применена система предоперационного планирования SmartPlan Ortho, SmartPlan Ortho 2D или иная аналогичная по функциям СПО ПП, обеспечивающая достижение описанного результата предоперационного планирования, внесённая в Единый реестр российских программ для электронных вычислительных машин и баз данных Минцифры России.
Рекомендовано на предоперационном этапе обследования пациента проводить комплексную визуализацию патологии позвоночника с целью предоперационного планирования корригирующих и стабилизирующих вмешательств (магнитно-резонансная томография позвоночника, рентгенография позвоночника вертикальная, при необходимости дополненная компьютерной томографией позвоночника, рентгенографией позвоночника (специальные исследования и проекции), рентгенография позвоночника с функциональными пробами. ) [42].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Комментарии: При наличии клинико-морфологического несоответствия возникает необходимость в наиболее полном и детальном обследовании пациента с использованием всех доступных методов. Отдельно взятый метод диагностики, даже из высокоинформативных, не всегда является достаточным для врачей-травматологов-ортопедов или врачей-нейрохирургов, что заставляет использовать их комбинацию.
Рекомендовано выполнять компьютерную томографию позвоночника пациентам, которым планируется проведение хирургического лечения, для определения плотности костной ткани в области предполагаемого хирургического вмешательства [43-45].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 3).
Комментарии. Компьютерная томография позвоночника является альтернативой рентгеноденситометрии поясничного отдела позвоночника в отношении определения минеральной плотности костной ткани, особенно у пациентов с дегенеративными поражениями позвоночника [46, 47]. Пороговым значением для выявления у пациентов нарушений минеральной плотности костной ткани является значения HU (Hounsfield unit)<135 [48]. HU является предиктором расшатывания винтов в ножке и теле позвонка при металлофиксации [49, 50]. При выявлении нарушений минеральной плотности костной ткани по данным компьтерной томографии необходимо определить потенциальную пользу от применения металлоконструкции, что связано с высоким риском ее расшатывания и последующим неудовлетворительным клиническим результатом
Рекомендовано проведение дополнительных методов визуализации крестцово-подвздошного сочленения только при подозрении на перелом, онкологический процесс в данной зоне, инфекцию, сакроилеит [51, 52].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2).
Комментарии: В ретроспективном исследовании Eno и др. [51] проанализировали данные компьютерной томографии 373 человек, у которых не было болей в пояснице или тазовом поясе, они обнаружили дегенерацию КПС у 65,1% исследуемых, отметив существенную дегенерацию у 30,5%. По данным систематического обзора Zelle и др. [52] МРТ крестцово-подвздошных сочленений показана для выявления раннего сакроилеита и опухолевых поражений. Однако, этот метод нельзя рекомендовать в качестве рутинной диагностики в связи с отсутствием сообщений об использовании МРТ при обследовании пациентов с дисфункцией КПС. Радионуклеидные исследования могут применяться для выявления сакроилеита, стрессового перелома или новообразования, вовлекающего КПС.
Дополнительные методы исследования имеют ограниченную роль в оценке боли при патологии КПС, при условии отсутствии опухоли данной локализации, инфекции или факта травмы в анамнезе у пациента. Компьютерная томография также имеет ограниченную диагностическую ценность при заболевании КПС из-за её низкой чувствительности и специфичности в выявлении источника боли. Рентгенография и МРТ, могут быть полезны при выявлении переломов крестца, опухолей, сакроилеита и анкилозирующего спондилоартрита. МРТ может использоваться при оценке сакроилеита у пациентов со спондилоартритом.
Рекомендовано пациентам с хронической болью в шее и неэффективной консервативной терапией выполнять инфильтрацияю раствором местного анестетика (лидокаин** АТХ: N01BB02, бупивакаин** АТХ: N01BB01, ропивакаин** N01BB09) в области проекции медиальных ветвей спинномозговых нервов с использованием рентгенографии шейного отдела позвоночника и введением рентгеноконтрастного средства (йопромид** ATХ: V08AB05, йогексол** ATХ: V08AB02) для диагностики патологии фасеточных суставов на уровне шейного отдела позвоночника [53].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 1).
Комментарии: В систематическом обзоре (Frank J.E. Falco и др) [53] было продемонстрировано, что диагностическая блокада с использованием местного анестетика (лидокаин** 1% 0,5 мл однократная инфильтрация (в данной дозировке нет ограничений по возрасту), бупивакаин** 0,25% 0,5 мл однократная инфильтрация (у взрослых и детей от 12 лет)) в области проекции медиальных ветвей спинномозговых нервов с внутрисуставной контрастной рентгенографией межпозвонкового хряща является безопасной и эффективной в рамках диагностики фасеточного синдрома на уровне шейного отдела позвоночника.
Рекомендовано пациентам с болью в нижней части спины и положительными провокационными нейроортопедическими тестами на патологию фасеточных суставов и неэффективной консервативной терапией выполнять диагностическую инфильтрацию раствором местного анестетика (лидокаин** АТХ: N01BB02, бупивакаин** АТХ: N01BB01, ропивакаин** N01BB09) в области проекции медиальных ветвей спинномозговых нервов или интраартикулярно с использованием рентгенографии пояснично-крестцового отдела позвоночника и введением рентгеноконтрастного средства (йопромид** ATХ: V08AB05, йогексол** ATХ: V08AB02) для диагностики клинически значимого патологически измененного фасеточного сустава в поясничном отделе позвоночника, а также для определения показаний к радиочастотной абляции фасеточных суставов [54].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 1).
Комментарии: В метаанализе (Lee CH и др.) [54] было продемонстрировано, что введение местного анестетика (лидокаин** 1% 0,75 мл однократная инфильтрация (в данной дозировке нет ограничений по возрасту), бупивакаин** 0,5% 0,5 мл однократная инфильтрация (у взрослых и детей от 12 лет)), в область проекции медиальных ветвей спинномозговых нервов или интраартикулярно с внутрисуставной контрастной рентгенографией межпозвонкового хряща являлось клинически значимым диагностическим методом перед проведением РЧA.
Рекомендовано пациентам с болью в нижней части спины и тремя и более положительными провокационными нейроортопедическими тестами на патологию КПС и неэффективной консервативной терапией инфильрация раствором местного анестетика (лидокаин** АТХ: N01BB02, бупивакаин** АТХ: N01BB01, ропивакаин** N01BB09) в крестцово-подвздошный сустав с использованием внутрисуставной контрастной рентгенографии крестцово-подвздошного сочленения для более точной диагностики патологии крестцово-подвздошного сочленения [55].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 1).
Комментарии: В систематическом обзоре (Simopolos и др.) [55] введение местного анестетика в крестцово-подвздошный сустав с флюроскопическим контролем является безопасными и обладает хорошей диагностической ценностью, когда оно используются для диагностики после отбора кандидатов на основе провокационных клинических тестов.
Рекомендовано проведение внутрисуставной контрастной рентгенографии межпозвонкового хряща (дискография) с контролем давления для диагностики причины хронического болевого синдрома в поясничном отделе позвоночника, устойчивого к консервативному лечению, если иные причины исключены [56, 57].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 1).
Комментарии: В систематических обзорах L.Manchikanti et al., 2009 и 2013 [56, 57] на основании анализа 9 работ достаточного методологического качества (критерии AHRQ) уровень достоверности доказательств (по критериям U.S. Preventive Services Task Force) для провокационной дискографии составил II-2 (хотя бы одно хорошо организованное проспективное контролируемое исследование с малой выборкой). Специфичность метода составила 0.94 (95% CI; 0.88 – 0.98), встречаемость дискогенной боли в структуре хронических болевых синдромов по данным дискографии - 26-39 %.
Рекомендовано проведение внутрисуставной контрастной рентгенографии межпозвонкового хряща (дискография) с инфильтрацией местным анестетиком (лидокаин** АТХ: N01BB02, бупивакаин** АТХ: N01BB01, ропивакаин** N01BB09) в межпозвонковый диск для диагностики причины хронического болевого синдрома в поясничном отделе позвоночника, устойчивого к консервативному лечению, если иные причины исключены [58, 59].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 3).
Комментарии: Во время написания клинических рекомендаций, системы для контролируемой по давлению дискографии не были доступны в РФ. Альтернативной является анальгетическая дискография - введение в диск местного анестетика (использовать лидокаин** 2% 0,5-1 мл (в данной дозировке нет ограничений по возрасту) или бупивакаин** 0,5% 0,5-1 мл (у взрослых и детей от 12 лет) или ропивакаин** 0,75% 0,5 мл (только у взрослых). В проспективных нерандомизированных исследованиях (R.Derbi et al., 2010 и 2012, W.Bartynski и W.Rothfus 2012) [58, 59] проводилось сравнение различных протоколов дискографии, использование местного анестетика (как в смеси с контрастным веществом при провокационной дискографии, так и при изолированном введении без контроля давления) не приводило к изменению результатов по сравнению с референтным методом, в том числе частоты встречаемости дискогенной боли. Пункция диска является инвазивной процедурой с потенциальным риском неврологических осложнений, дисцитов (примерно 1 на 1000 вмешательств) и ускорения дегенерации диска на фоне повреждения иглой и повышением внутридискового давления. Следует выполнять диагностические внутридисковые вмешательства в последнюю очередь, после менее инвазивных процедур.
3.1 Консервативное лечение
Рекомендовано проводить консервативное лечение пациентам с дегенеративными заболеваниями позвоночника, если в клинических проявлениях нет остро прогрессирующего неврологического дефицита [36, 60, 61].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Превалирующая часть пациентов получают результативную консервативную терапию (амбулаторную, стационарную, санаторно-курортную) со стойкой длительной ремиссией. У детей проводится консервативное лечение согласно аналогичному протоколу у взрослых, но с учетов соответсвующих доз лекарственных препаратов.
При обращении пациента с болями в шейном, грудном, поясничном и (или) в конечностях вследствие дегенеративно-дистрофических изменений за медицинской помощью в ряде случаев требуется проведение неотложной консервативной или хирургической помощи при гипералгической, паралитической формах корешкового синдрома, развитии каудомедуллярного синдрома или вертеброгенной остроразвивающейся компрессионной миелопатии. При наличии клинико-морфологического соответствия пациенту показано плановое хирургическое лечение с целью устранения компримирующего сосудисто-нервные образования субстрата.
3.1.1 Лекарственная терапия острой скелетно-мышечной (неспецифической) боли в нижней части спины
Рекомендовано проводить обучение пациентов в устном или письменном виде, содержащее информацию о доброкачественном течении заболевания, направленную на коррекцию поведения пациентов с острой неспецифической БНЧС [62].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2).
Комментарии: В систематическом обзоре и метаанализе (Traeger AC и др., 2015) [62] было продемонстрировано, что индивидуальное обучение пациентов хотя и не эффективно для снижения острой неспецифической БНЧС, но эффективно успокаивает пациентов и сокращает количество повторных обращений в пункты первичной медицинской помощи из-за БНЧС в течение года.
Рекомендовано применение нестероидных противовоспалительных и противоревматических препаратов (НПВП; АТХ код: М01А) у пациентов с острой неспецифической БНЧС [63, 64].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 1).
Комментарии: Рекомендация основана на данных 2 системных обзоров с метаанализом, в которых показано, что у пациентов с острой неспецифической БНЧС отмечается значительное уменьшение боли через 1 неделю приема НПВП, препараты назначались в эффективных дозах, на минимально необходимое количество дней для того, чтобы снизить риск возникновения побочных эффектов (Gianola S. и др, 2022) [63]. Нет достоверных данных, свидетельствующих о преимуществе какого-либо одного НПВП перед другими в отношении облегчения острой неспецифической БНЧС (Wewege MA и др, 2023) [64].
Не рекомендовано назначение парацетамола** при острой неспецифической БНЧС в качестве монотерапии и в сочетании в другими НПВП [65].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2).
Комментарии: Не доказано значимого преимущества парацетамола по сравнению с плацебо в отношении снижения боли и улучшения функционального состояния пациентов с острой неспецифической БНЧС [65].
Рекомендовано применение миорелаксантов центрального действия (толперизон (у взрослых)** АТХ код: M03BX04, тизанидин**; АТХ код: M03BX02) у пациентов с острой неспецифической БНЧС в комбинации с НПВП [63, 66, 67, 68].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 1).
Комментарии: Рекомендация основана на данных 3 системных обзоров с метаанализом и 1 рандомизированного мультицентрового контролируемого исследования, в которых получены данные в отношении эффективности противоболевого эффекта миорелаксантов в сочетании с НПВП [63, 66, 67, 68].
Рекомендовано назначение витаминов группы B (тиамин: АТХ код A11DA01 **, в дозе 50-100 мг в сутки, пиридоксин АТХ код: A11HA02 ** в дозе 50-150 мг в сутки и цианокобаламин**, АТХ код: B03BA01 в дозе 200-500 мкг) в дополнение к НПВП при острой неспецифической БНЧС [69].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 1).
Комментарии: В систематическом обзоре и метаанализе (Calderon-Ospina CA и др., 2020) [69] продемонстрировано, что комбинированная терапия НПВП (на примере диклофенака**) и витаминов группы В может иметь более эффективное обезболивающее действие по сравнению с монотерапией НПВП при острой неспецифической БНЧС. Однако нет достаточных доказательств, чтобы рекомендовать эту терапию при других типах боли из-за нехватки высококачественных исследований.
Не рекомендовано назначение глюкокортикоидов (ГКС; АТХ код: H02AB) пациентам с острой скелетно-мышечной болью в нижней части спины [70, 71].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2).
Комментарии: Отсутствуют убедительные данные о преимуществе применения глюкокортикоидов при острой неспецифической БНЧС по сравнению с другими группами препаратов, а также ввиду увеличения риска развития побочных явлений [70, 71].
Не рекомендовано применение опиоидов (трамадол АТХ N02AX02**, тапентадол**; ATX : N02AX06) у пациентов с острой скелетно-мышечной болью в нижней части спины [63, 64].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 1).
Комментарии: По данным 2 систематических обзоров с мета-анализом имеются данные о повышении риска побочных явлений при применении опиоидов по сравнению с другими группами препаратов, применяемых при острой неспецифической БНЧС [63,64].
3.1.2 Лекарственная терапия хронической скелетно-мышечной (неспецифической) боли в нижней части спины
Рекомендовано применение местных форм НПВП (диклофенак (с 12 лет)**, кетопрофен (с 15 лет)**, ибупрофен (с 14 лет)**; АТХ код: М01А) у пациентов с хронической неспецифической БС [72].
Уровень убедительности рекомендаций C (уровень достоверности доказательств –5).
Комментарии: Отсутствуют достоверные данные, свидетельствующие о преимуществе какого-либо одного НПВП перед другими в отношении облегчения неспецифической БС. Ввиду того, что парентеральное применение не имеет преимуществ в отношении эффективности, но существенно уступает в безопасности, целесообразно использование местных форм НПВП [72, 73].
Рекомендовано применение пероральных форм НПВП (диклофенак (с 6 лет)**, кетопрофен (с 12 лет)**, ибупрофен**, напроксен (с 15 лет), целекоксиб (с 16 лет); АТХ код: М01А) у пациентов с хронической неспецифической БС [72].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2).
Комментарии: Отмечается значительное уменьшение боли и нетрудоспособности через 1 неделю после начала приема пероральных форм НПВП [72,73]. Рекомендовано назначение НПВП в эффективных дозах, на минимально необходимое количество дней для того, чтобы снизить риск возникновения побочных эффектов [72-77].
Не рекомендовано применение парацетамола**; АТХ код: N02BE01) пациентам с хронической неспецифической БС в качестве монотерапии и в сочетании в другими НПВП [65, 78].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 1).
Комментарии: Результаты систематического обзора показывают, что парацетамол** не обеспечивает клинически значимого эффекта в краткосрочной перспективе, а долгосрочный эффект этого препарата при лечении боли в позвоночнике остается неизвестным. Более того, было обнаружено, что более высокий риск отклонения от нормы результатов функциональных тестов печени выявлен у пациентов, принимающих парацетамол**, хотя клинические последствия этого неясны [65, 78]. Сообщалось, что парацетамол**, не эффективен у пациентов с хронической болью в пояснице [74, 76, 78].
Рекомендовано применение миорелаксантов центрального действия (толперизона (у взрослых) АТХ код: M03BX04, тизанидина**; АТХ код: M03BX02) у пациентов с хронической неспецифической БС в комбинации с НПВП [80].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 1).
Комментарии: В клинических исследованиях эти препараты показывают хорошую эффективность, но, побочные реакции и лекарственные взаимодействия могут ограничивать их применение [79], снижая приверженность к лекарственной терапии [76, 77, 80].
Рекомендовано применение опиоидов (трамадол АТХ N02AX02 (с 14 лет)**, кодеин+ибупрофен АТХ N02AA59 (с 12 лет), кодеин +парацетамол АТХ N02AA59 (с 12 лет), морфин АТХ N02АА01 (с 3 лет)**, налоксон+оксикодон ATX N02AA55 (с 18 лет); при недостаточной эффективности НПВП в сочетании с другими группами препаратов у пациентов с хронической неспецифической БС [81].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 1).
Комментарии: У пациентов со слабой и умеренно выраженной болью пероральное назначение опиоидов II ступени (например, трамадола**, кодеина), может обеспечить эффективное обезболивание без неблагоприятных побочных эффектов. Лишь в качестве альтернативы и отсутствия эффективности лечения в длительный промежуток времени тяжело больным пациентам целесообразно назначить опиоиды III ступени (например, морфин, оксикодона) [81, 82]. Опиоиды не следует рассматривать как терапию первой линии при подострой или хронической боли. Ожидаемые преимущества терапии должны быть сопоставлены с рисками до начала терапии.
Рекомендовано применение селективных ингибиторов обратного захвата серотонина и норадреналина (дулоксетин, АТХ код N06AX21 (у взрослых, в дозе 30-60 мг в сутки) Другие антидепрессанты) у пациентов с хронической неспецифической БС [313].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1).
Комментарии: В соответствии c результатами системного обзора с метаанализом, имеются данные в отношении эффективности дулоксетина при лечении хронической неспецифической боли в нижней части спины [313].
Рекомендовано назначение трициклических антидепрессантов - неселективных ингибиторов обратного захвата моноаминов (амитриптилин**; АТХ код: N06AA09 в дозе 25-50 мг в сутки) пациентам с хронической неспецифической БС [314].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 2).
Комментарии: По данным исследования амитриптилина** у пациентов с хронической неспецифической БС было выявлено, что эффективность в отношении снижения боли минимальна, но наблюдается улучшения функционального состояния пациентов [87].
3.1.3 Лекарственная терапия острой корешковой (радикулярной) боли
Рекомендовано применение НПВП (АТХ код: М01А) при острой корешковой БНЧС, связанной с диско-радикулярным конфликтом [88-90].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 1).
Комментарии: Рекомендация основана на данных 2 системных обзоров с метаанализом и 1 рандомизированного контролируемого исследования, в которых получены доказательства низкой и умеренной степени о превосходстве НПВП по сравнению с плацебо в улучшении функционального исхода и уменьшении интенсивности боли пациентов с болью в нижней части спины и корешковой боли в ноге [88-90].
Рекомендовано применение глюкокортикоидов (#преднизолон** per os в дозировке 60 мг 3 дня с последующим снижением дозы на 20 мг каждые 3 дня, #метилпреднизолон** в дозе 500 мг в/в однократно болюсно или 160 мг в/м однократно; АТХ код H02AB) при острой корешковой БНЧС [91-93].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2).
Комментарии: Рекомендация основана на данных 3 РКИ [91-93], в которых было показано, что пероральное или парентеральное применение ГКС (преднизолон** в дозировке 60 мг 3 дня с последующим снижением дозы на 20 мг каждые 3 дня либо метилпреднизолон** в дозе 500 мг в/в однократно болюсно или 160 мг в/м однократно) позволило на короткий промежуток времени уменьшить интенсивность боли в ноге. Рекомендация также основана на данных системного обзора с метаанализом, в ходе которого было установлено, что применение ГКС способствовало снижению интенсивности боли в среднем на 12-29 баллов по 100-балльной шкале, в сравнении с плацебо (3,4 балла), (p<0,01).
Не рекомендовано назначение габапентиноидов (габапентин и прегабалин**, АТХ-N03AX другие противоэпилептические препараты). при острой корешковой БНЧС, связанной с диско-радикулярным конфликтом [95, 96].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
Комментарии: Рекомендация основана на данных 1 рандомизированного клинического исследования [94], а также, данных 2 системных обзоров с мета-анализом [95, 96]. В ходе исследований не было продемонстрировано значимого преимущества препаратов по сравнению с плацебо в отношении снижения интенсивности боли и улучшения функционального исхода у пациентов с острой радикулярной болью.
3.1.4 Лекарственная терапия хронической корешковой (радикулярной) боли
Рекомендовано применение селективных ингибиторов обратного захвата серотонина и норадреналина (дулоксетин, АТХ код N06AX21) у пациентов с хронической корешковой болью в дозе 60-120 мг в сутки [97].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2).
Комментарии: Рекомендация основана на проспективном двойном слепом рандомизированном контролируемом исследовании [97], в котором удалось установить эффективность дулоксетина у пациентов с хронической радикулярной болью.
Не рекомендовано назначение габапентиноидов (прегабалин**, габапентин, АТХ-N03AX другие противоэпилептические препараты) пациентам с хронической корешковой болью [95].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
Комментарии: По данным метаанализа было установлено, что габапентиноиды (габапентин, прегабалин) не уменьшают боль и не улучшают функциональный статус у пациентов с хронической радикулярной болью. Более того, было установлено, что назначение их сопровождается достоверно большим количеством побочных эффектов [95]. По данным двойного слепого рандомизированного плацебо-контролируемого исследования удалось установить, что прегабалин не эффективен в лечении хронической радикулярной боли, а назначение его сопровождалось большей частотой головокружения [94].
3.2. Пункционные вмешательства
Промежуточными методами лечения остеохондроза позвоночника являются пункционные вмешательства. В соответствии с зоной воздействия их можно разделить на вмешательства в области:
- дугоотростчатых (фасеточных) суставов шейного отдела позвоночника
- дугоотростчатых (фасеточных) суставов грудного отдела позвоночника
- дугоотростчатых (фасеточных) суставов поясничного отдела позвоночника
- крестцово-подвздошного сустава
- эпидурального пространства и спинномозговых нервов в шейном отделе позвоночника
- эпидурального пространства и спинномозговых нервов в грудном отделе позвоночника
- эпидурального пространства и спинномозговых нервов в поясничном и крестцовом отделе позвоночника
- на межпозвонковом диске
3.2.1. Пункционные интервенционные процедуры в области дугоотростчатых (фасеточных) суставов шейного отдела позвоночника
Рекомендовано периодически выполнять периартикулярные инфильтрации раствором местного анестетика (лидокаин** АТХ: N01BB02, бупивакаин** АТХ: N01BB01, ропивакаин** АТХ: N01BB09) с/без глюкокортикоида (дексаметазон** АТХ: H02AB02, триамцинолон АТХ: H02AB08, бетаметазон АТХ: H02AB01) медиальных ветвей спинномозговых нервов шейного отдела позвоночника с использованием рентгенографии шейного отдела позвоночника и введением рентгеноконтрастного средства (йопромид** ATХ: V08AB05, йогексол ATХ: V08AB02) для облегчения боли из дугоотростчатых (фасеточных) суставов и неэффективности различных методов неинвазивного лечения [98, 99].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2).
Комментарии: Результаты одного рандомизированного и одного проспективного обсервационного исследования указывают на эффективность периодической блокады медиальных ветвей спинномозговых нервов шейного отдела позвоночника для облегчения боли из дугоотростчатых суставов. Такая эффективность сохранялась на период исследования (2 года) с необходимостью выполнять блокады в среднем 3 раза в год и длительностью эффекта после однократной манипуляции продолжительностью 17-19 недель. При этом не получено данных о дополнительном эффекте глюкокортикостероида в качестве адъюванта к местному анестетику (лидокаин** 1% 0,5-2 мл (в данной дозировке нет ограничений по возрасту) или бупивакаин** 0,5% 0,5-2 мл (у взрослых и детей от 12 лет) [98, 99].
Рекомендовано периодически выполнять ультразвук-контролируемые периартикулярные инфильтрации раствором местного анестетика (лидокаин** АТХ: N01BB02, бупивакаин** АТХ: N01BB01, ропивакаин** АТХ: N01BB09) с/без глюкокортикоида (дексаметазон** АТХ: H02AB02, триамцинолон АТХ: H02AB08, бетаметазон АТХ: H02AB01) медиальных ветвей спинномозговых нервов шейного отдела позвоночника и третьего затылочного нерва для облегчения боли из дугоотростчатых (фасеточных) суставов и неэффективности различных методов неинвазивного лечения при ограниченной доступности или противопоказаниях к применению рентген-контроля [100-106].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии: Исследования показали сравнимую точность установки иглы для блокады при применении ультразвуковой навигации и меньшее (по сравнению с рентген-навигацией) количество времени для проведения процедуры и/или проходов иглы требуемое для этого. При этом доступные РКИ изучали воздействие лишь на третий затылочный и медиальную ветвь С7 спинномозгового нерва и снижение интенсивности боли не было первичной точкой оценки ни в одном из них. Исходы по облегчению боли для отдаленных периодов (1, 3, 6 месяцев) были оценены лишь в одном ретроспективном исследовании. [100-106].
Рекомендовано выполнять рентген-контролируемую высокочастотную денервацию фасеточных суставов шейного отдела позвоночника при диагностированном на основании блокад местным анестетиком источнике боли из дугоотростчатых суставов и неэффективности различных методов неинвазивного лечения [107-110].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 2).
Комментарии: В поддержку данной рекомендации выполнено, как минимум, одно РКИ и 3 обсервационных исследования. Отбор пациентов для радиочастотной денервации осуществляли на основании снижения интенсивности боли в шее на 80-100% после двух-трех рентген-контролируемых сравнительных блокад с инфильтрацией раствором местного анестетика (лидокаин** (АТХ: N01BB02) 1-2% 0,3-0,5 мл (в данной дозировке нет ограничений по возрасту) или бупивакаин** (АТХ: N01BB01) 0,25-0,5% 0,3-0,5 мл (у взрослых и детей от 12 лет) и 0,9% натрия хлорида 0,3-0,5 мл) и длительности облегчения боли не менее длительности действия использованного местного анестетика и отсутствия облегчения боли при применении 0,9% натрия хлорида. Радиочастотная денервация приводила к снижению интенсивности боли на 58-76% в течение 9-12 месяцев. [107-110].
Рекомендовано повторять высокочастотную денервацию фасеточных суставов шейного отдела позвоночника с использованием рентгенографии шейного отдела позвоночника частотой не более двух раз в год при эффективности предыдущей денервации, схожей клинической картине боли и неэффективности различных методов неинвазивного лечения [111].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4).
Комментарии: Как минимум, два ретроспективных исследования указывают на эффективность повторной РЧД дугоотростчатых суставов при условии успешности первой денервации и удовлетворенности пациента ее ходом и результатом. Диагностические блокады перед повторными денервациями авторы не выполняли. [111, 112].
Рекомендована инфильтрация дугоотросчатых (фасеточных суставов) шейного отдела позвоночника раствором местного анестетика (лидокаин** АТХ: N01BB02, бупивакаин** АТХ: N01BB01, ропивакаин** АТХ: N01BB09) с/без глюкокортикоида (дексаметазон** АТХ: H02AB02, триамцинолон АТХ: H02AB08, бетаметазон АТХ: H02AB01) под контролем внутрисуставной контрастной рентгенографии межпозвонкового хряща при боли нетравматической этиологии из дугоотростчатых (фасеточных) суставов шейного отдела позвоночника и неэффективности различных методов неинвазивного лечения пациентам, не рассматриваемым в качестве кандидатов для радиочастотной денервации или в случаях ее недоступности [113-118].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии: Существуют немногочисленные противоречивые данные о средне- и долгосрочной эффективности интраартикулярных инъекций местного анестетика с/без глюкокортикостероида при боли из дугоотростчатых суставов травматической и нетравматической этиологии. В проспективном обсервационном исследовании было показано, что у 24 (54,5%) из 44 пациентов, принимавших опиоиды с диагностированной на основании сравнительных блокад нетравматической болью из фасеточных суставовшейного отдела позвоночника, было получено снижение боли не менее, чем на 2 балла по вербальной цифровой рейтинговой шкале или 50% от исходной через 1 год. Проводилось интраартикулярное введение лидокаина** (1% 0,5 мл, в данной дозировке нет ограничений по возрасту) c/без глюкокортикоида. При этом у 11 из 24 пациентов интраартикулярные инъекции пришлось повторить с медианой интервала между первой и второй инъекцией 6 (размах 2-52) недель [115]. Все пациенты с положительным эффектом указали на прекращение приема опиоидов.
3.2.2 Пункционные интервенционные процедуры в области дугоотростчатых (фасеточных) суставов грудного отдела позвоночника
Рекомендовано периодически выполнять периартикулярные инфильтрации раствором местного анестетика (лидокаин** АТХ: N01BB02, бупивакаин** АТХ: N01BB01, ропивакаин** АТХ: N01BB09) с/без глюкокортикоида (дексаметазон** АТХ: H02AB02, триамцинолон АТХ: H02AB08, бетаметазон АТХ: H02AB01) медиальных ветвей спинномозговых нервов грудного отдела позвоночника под контролем рентгенографии грудного отдела позвоночника и с введением рентгеноконтрастного средства (йопромид** ATХ: V08AB05, йогексол** ATХ: V08AB02) для облегчения боли из дугоотростчатых (фасеточных) суставов и неэффективности различных методов неинвазивного лечения [119-121].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2).
Комментарии: Результаты двух рандомизированных и одного ретроспективного обсервационного исследования указывают на эффективность периодической блокады с/без глюкокортикостероидов медиальных ветвей спинномозговых нервов грудного отдела позвоночника для облегчения боли из дугоотростчатых суставов. Такая эффективность сохранялась на период исследования (2 года) с необходимостью выполнять блокады в среднем от 1 до 5 раза в год у 80-84% пациентов. В другом рандомизированном исследовании сравнивали снижение интенсивность боли не менее, чем на 50% в группе блокады медиальных ветвей у 40% пациентов [120, 121].
Рекомендована интраартикулярная инфильтрация раствором местного анестетика (лидокаин** АТХ: N01BB02, бупивакаин** АТХ: N01BB01, ропивакаин** АТХ: N01BB09) с/без глюкокортикоида (дексаметазон** АТХ: H02AB02, триамцинолон АТХ: H02AB08, бетаметазон АТХ: H02AB01 под контролем внутрисуставной контрастной рентгенографии при боли из дугоотростчатых (фасеточных) суставов грудного отдела позвоночника и неэффективности различных методов неинвазивного лечения [120].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 2).
Комментарии: В пользу данной рекомендации свидетельствую данные одного рандомизированного исследования (Lee D.G., 2018). Получены результаты о снижении интенсивности боли не менее, чем на 50%, в группе рентген-контролируемого с помощью контраста интраартикулярного введения местного анестетика (лидокаин** 2% 1 мл, в данной дозировке нет ограничений по возрасту) и глюкокортикоида у 65% пациентов.
Рекомендовано выполнять высокочастотную денервацию фасеточных суставов грудного отдела позвоночника при диагностированном на основании сравнительных блокад местным анестетиком источнике боли из дугоотростчатых суставов и неэффективности различных методов неинвазивного лечения [122, 123].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии: Рекомендация основана на результатах одного рандомизированного клинического и двух ретроспективных обсервационных исследований, использующих различные методы радиочастотного воздействия (биполярное, охлаждаемое). При этом первичная точка рандомизированного исследования была направлена на сравнение химионевролиза и РЧД нервов грудопоясничных фасеточных суставов у пациентов, нуждающихся в повторной денервации. Медиана снижения интенсивности боли не менее, чем на 50%, после первой денервации составила 10.7 месяцев (размах 6,3- 12,7 месяцев) и после повторной 10,7 (размах 5,4-24 месяцев). Большей части (71%) пациентов еще одного ретроспективного исследования выполнили биполярную денервацию дугоотростчатых суставов шейногрудного отдела позвоночника. 82% пациентов чувствовали облегчение боли не менее, чем на 50% через 12 месяцев после манипуляции. В еще одном ретроспективном исследовании показали, что среднее снижении боли не менее, чем на 50%, наблюдали в среднесрочной перспективе от 2 до 6 месяцев после охлаждаемой РЧД у отобранных на основании сравнительных блокад пациентов с болью из дугоотростчатых суставов грудного отдела позвоночника [122, 123].
3.2.3 Пункционные интервенционные процедуры в области дугоотростчатых (фасеточных) суставов поясничного отдела позвоночника
Рекомендовано выполнять периартикулярные инфильтрацию раствором местного анестетика (лидокаин** АТХ: N01BB02, бупивакаин** АТХ: N01BB01, ропивакаин** АТХ: N01BB09) с/без глюкокортикоида (дексаметазон** АТХ: H02AB02, триамцинолон АТХ: H02AB08, бетаметазон АТХ: H02AB01) медиальных ветвей спинномозговых нервов с рентгенографией поясничного и крестцового отдела позвоночника и с введением рентгеноконтрастного средства (йопромид** ATХ: V08AB05, йогексол** ATХ: V08AB02) при хронической боли, обусловленной патологией дугоотростчатых (фасеточных) суставов поясничного отдела позвоночника, диагностированной на основании клинического осмотра и данных исследований при отсутствии эффекта от консервативной терапии [124-127].
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 1).
Комментарии: Данная рекомендация основана на результатах 3 рандомизированных контролируемых исследований, 1 cистематического обзора с метаанализом, основанного на анализе рандомизированных клинических и обсервационных исследований эффективности применения различных инъекций местных анестетиков и ГКС при боли в поясничной области, обусловленной патологией дугоотростчатых суставов. Данная процедура приводит к уменьшению интенсивности боли на 50% и более и улучшению функционального состояния у 80% пациентов на срок от 6 до 24 месяцев. При эффективности процедуры и последующем рецидиве боли она может быть выполнена повторно [124-127].
Рекомендовано выполнять ультразвук-контролируемые инфильтрации медиальных ветвей спинномозговых нервов местным анестетиком (лидокаин** АТХ: N01BB02, бупивакаин АТХ: N01BB01, ропивакаин** АТХ: N01BB09) с/без глюкокортикоидов (дексаметазон** АТХ: H02AB02, триамцинолон АТХ: H02AB08, бетаметазон АТХ: H02AB01) при хронической боли, обусловленной патологией дугоотростчатых (фасеточных) суставов поясничного отдела позвоночника, диагностированной на основании клинического осмотра и данных исследований при отсутствии эффекта от консервативной терапии при ограниченной доступности или противопоказаниях к применению рентген-контроля [129].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 3).
Комментарии: Основанием для данной рекомендации служат результаты ретроспективного сравнительного исследования [128], наблюдательного исследования [129], систематического метаанализа [130]. После проведения манипуляций интенсивность боли значимо снижалась на срок 3-6 месяцев. При использовании ультразвуковой навигации возможно некорректное расположение игл, в особенности у пациентов с избыточным весом, поэтому ее применение у таких пациентов возможно при ограничении доступа или противопоказаниях к рентген-навигации [130].
Рекомендовано выполнять интраартикулярные инфильтрации в дугоотростчатые (фасеточные) суставы местным анестетиком (лидокаин** АТХ: N01BB02, бупивакаин** АТХ: N01BB01, ропивакаин** АТХ: N01BB09) с/без глюкокортикоида (дексаметазон** АТХ: H02AB02, триамцинолон АТХ: H02AB08, бетаметазон АТХ: H02AB01) с применением рентгеноконтрастного средства (йопромид** ATХ: V08AB05, йогексол** ATХ: V08AB02) при хронической боли, обусловленной патологией дугоотростчатых суставов поясничного отдела позвоночника, диагностированной на основании клинического осмотра и данных исследований при отсутствии эффекта от консервативной терапии [131].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 2).
Комментарии: Обоснованием рекомендации служит рандомизированное контролируемое исследование [131], нерандомизированное контролируемое сравнительное исследование [132], двойное слепое проспективное сравнительное исследование [133]. В ходе исследований изучалась эффективность интраартикулярных инъекций анестетика и стероида под контролем рентгеноскопии. Получены данные о значимом уменьшении интенсивности боли на срок 6-12 месяцев [131-132], в том числе, по сравнению с контрольной группой [131], а также об улучшении функционального статуса [131, 133].
Рекомендовано выполнять ультразвук-контролируемые интраартикулярные инфильтрации в дугоотростчатые (фасеточные) суставы местным анестетиком (лидокаин** АТХ: N01BB02, бупивакаин** АТХ: N01BB01, ропивакаин** АТХ: N01BB09 с глюкокортикоидом (дексаметазон** АТХ: H02AB02, триамцинолон АТХ: H02AB08, бетаметазон АТХ: H02AB01) при хронической боли, обусловленной патологией дугоотростчатых суставов поясничного отдела позвоночника, диагностированной на основании клинического осмотра и данных исследований при отсутствии эффекта от консервативной терапии при ограниченной доступности или противопоказаниях к применению рентген-контроля [133].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 2).
Комментарии: Обоснованием рекомендации служат данные сравнительного рандомизированного исследования [133], ретроспективного сравнительного исследования [134], в которых у большинства пациентов после проведения манипуляций эффект в виде снижения интенсивности боли и улучшения функционального статуса сохранялся на срок от 3 до 6 месяцев [133-136]. При использовании ультразвуковой навигации возможно некорректное расположение игл, в особенности у пациентов с избыточным весом, поэтому ее применение у таких пациентов возможно при ограничении доступа или противопоказаниях к рентген-навигации [130].
Рекомендовано выполнять рентген-контролируемую радиочастотную денервацию дугоотростчатых (фасеточных) суставов поясничного отдела позвоночника при хронической боли, обусловленной патологией дугоотростчатых суставов, диагностированной на основании клинического осмотра и данных исследований при отсутствии эффекта от консервативной терапии и после положительного ответа на диагностическую блокаду медиальных ветвей спинномозговых нервов с применением местного анестетика. При рецидиве боли после успешной первой РЧД возможно проведение повторной процедуры без снижения ее эффективности [127, 137-139].
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 1).
Комментарии: Обоснованием данной рекомендации служат минимум 2 рандомизированных контролируемых исследования и 1 мета-анализ, 1 систематический обзор с метаанализом [127, 137-139]. После проведения РЧА снижение интенсивности боли на 50% и улучшение функционального состояния сохранялись в течение 12 месяцев [127, 137-139].
Рекомендовано проведение повторной высокочастотной денервации фасеточных суставов суставов поясничного отдела позвоночника при рецидиве боли после успешной первой радиочастотной денервации [140, 141].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии: В ретроспективных исследованиях по изучению эффективности повторной РЧД при рецидиве боли было продемонстрировано, что при положительном ответе на первую РЧД все повторные РЧД были также эффективны со значимым снижением интенсивности боли в среднем 10,5 мес у 85% пациентов [140, 141].
3.2.4 Пункционные интервенционные процедуры в области крестцово-подвздошного сустава.
Рекомендовано пациентам с болью в нижней части спины и двумя и более положительными провокационными нейроортопедическими тестами на патологию крестцово-подвздошного сустава и неэффективной консервативной терапией интраартикулярное введение смеси глюкокортикоида (дексаметазон** АТХ: H02AB02, триамцинолон АТХ: H02AB08, бетаметазон АТХ: H02AB01) и инфильтрацию раствора местного анестетика (лидокаин** АТХ: N01BB02, бупивакаин** АТХ: N01BB01, ропивакаин** АТХ: N01BB09) под контролем внутрисуставной контрастной рентгенографии крестцово-подвздошного сочленения или под ультразвуковым контролем [143].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2).
Комментарий: В 1 систематическом обзоре (Kennedy и др.) [142] установлена средняя степень убедительности эффективности интраартикулярного введения глюкокортикостероида (ГКС) под рентген-контролем с введением ретгенконтрастного препарата. В двойном слепом исследовании (Maugars Y. и др.) [143] удалось установить значимое снижение боли в группе пациентов, которым вводился раствор ГКС под рентген-контролем. В проспективных рандомизированных контролируемых исследованиях (Jee и соавт.) [144], а также (Soneji и соавт.) [145] было установлено, что применение рентгеновской и УЗ навигация обеспечивают отдинаковую эффективность и безопасность интраартикулярных инъекций в КПС. Однако, при проведении диагностических блоков рекомендовано применение рентгеновской навигации, как более точной.
Рекомендовано пациентам с болью в нижней части спины и эффективной диагностической
Рекомендуется пациентам с дегенеративными заболеваниями позвоночника в период обострения болевого синдрома соблюдение ортопедического режима с целью снижения механической нагрузки на структуры позвоночника [1, 226, 227, 228, 229].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: При выраженном болевом синдроме в острый период рекомендован постельный режим на 1-2 дня, что способствует релаксации мышц и уменьшению внутридискового давления. Постельный режим продолжительностью более 4 дней не приносит пользы и в дальнейшем может привести к ухудшению состояния пациента [230-232] В клинических стандартах Австралийской комиссии по безопасности и качеству здравоохранения [228] в лечении боли в спине рекомендуется соблюдать двигательную активность и не рекомендуется постельный режим более 4 дней [223, 233- 235]. В 2 РКИ низкого качества показано преимущество двигательной активности перед постельным режимом [236, 237]. Результаты рандомизированных исследований с высокой степенью достоверности показывают, что физическую активность следует начинать спустя несколько суток после начала болевого синдрома, несмотря на то, что с началом возобновления двигательной активности боль может временно усилиться
Рекомендуется пациентам с дегенеративными заболеваниями позвоночника в период обострения болевого синдрома ношение ортопедического корсета на поясничный отдел позвоночника и ортопедических воротников на шейный отдел для уменьшения нагрузки на структуры позвоночника [226, 227, 238].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: В литературе мало освещается вопрос ортезирования при вертеброгенной боли, а представленные данные носят рекомендательный характер.
Американской ассациацией вертебрологов представлены клинические рекомендации лечения боли в спине, где на основании РКК среднего качества рекомендуется в острый период болевого синдрома ношение корсетов для уменьшения боли за счет стабилизации соотвтствующего позвоночниго двигательного сегмента и расслабления мышц [239-241].
После купирования острого болевого синдрома ношение корсетов и воротников рекомндуется только на период выполнения физических работ или длительного статического положения туловища или головы, что является профилактикой рецидива боли. Постоянное ношение корсетов приводит к снижению мышечного тонуса и в дальшейшем и силы мышц, а значит снижением их стабилизирующей функции [ 226].
Рекомендуется пациентам с хроническим вертеброгенным болевым синдромом (или в период ремиссии болевого синдрома) рациональная двигательная активность для уменьшения нагрузки на структуры позвоночника и профилактики обострений болевого синдрома [1, 226, 229].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии:
Наибольшее внимание практически во всех публикациях уделяется вопросам обучения пациентов и дациональной двигательной активности, как основным методическим подходам к лечению и профилактики вертеброгенных синдромов. Проведены многочисленные РКИ, показывающие эффективность образовательных программ в сравнении с программами физических упражнений, мануальной терапии, физиотерапии в отношении стабилизации как болевого синдрома, так и функции позвоночника [242-247]. Образовательные программам включены в стандарты оказания помощи при боли в спине [228]. Правильная механика движений уменьшает нагрузку на позвоночник при повседневной активности и, тем самым, уменьшает риск возникновения болевого синдрома. Созданы специальные обучающие программа, в ряде стран они носят название «Школа спины». Соблюдение представленных в них рекомендаций, основанных на РКК высокого качества, позволяют избежать перегрузку структур позвоночника, которая может провоцировать возникновение болевого синдрома и прогрессирование дегенеративно-дистрофического процесса [238, 248- 252]. Образовательные программы или школы спины обучают не только правильнму выполнению двигательных навыков в повседневной жизни, но и занятиям адекватными видами физкультуры и спорта. Рекоменбуется поддерживать ежедневную физическую активность настолько близкой к нормальной, насколько это возможно. В течение первой недели после уменьшения острой боли в спине, рекомендуется начинать разминку и ходьбу в воде, затем на свежем воздухе, езду на велосипеде, упражнения с участием больших мышечных групп с постепенным увеличением как самой нагрузки, так и длительности тренировок до 30 мин без отдыха [223, 233, 252- 255].
Рациональный режим включает следующие рекомендации:
1. Нельзя поднимать или носить тяжелые предметы, особенно на вытянутых вперед руках. Если необходимо поднять тяжелый предмет с пола следует присесть, а не наклоняться вперед. Поднимать тяжелые предметы можно только до уровня груди, а если нужно поднять их выше, следует встать на стул. Если предмет очень тяжелый, необходимо прибегать к посторонней помощи. Сумки с продуктами не должны превышать 5 кг, их лучше носить в обеих руках.
2. Избегать продолжительного пребывания в положении сидя. Каждые два часа работы в положении сидя следует делать 2-3 минутную паузу. В течение этой паузы можно встать, сделать несколько шагов по комнате. Стоя в удобном положении (ноги на ширине плеч) положив руки на поясницу, рекомендуется прогнуться назад и сохранить это положение 30-40 сек. Сидеть следует прямо на стуле такой высоты, чтобы ноги стояли на полу, а коленные суставы были на одном уровне с тазобедренными. Спина должна быть прижата к спинке стула. Под поясницу подкладывается специальный валик или свернутое рулоном полотенце. Такое же положение следует соблюдать и при вождении автомобиля. Не вставая со стула, можно дать отдых спине, если наклониться вперед, обхватив руками колени и положив голову на них. Такое положение удерживается от 2 до 5 минут.
Желательно избегать работы в наклонном положении (стирка белья в ванне, мытье пола, прополка и др.). Для выполнения подобных работ следует выбрать такое положение рабочего места, чтобы спина была в прямом положении. Например, при ручной стирке белья, следует поставить таз на высокую подставку; при мытье пола использовать швабру с длинной ручкой или положение на четвереньках.
При выполнении работы с длительным пребыванием в положении стоя (глажение белья) нужно попеременно ставить ногу на подставку типа детской скамейки, что помогает сохранить поясничный лордоз.
При длительной ходьбе рекомендуется носить удобную на среднем каблуке обувь.
3. Спать лучше на специальном матраце в положении на боку с согнутыми ногами, или на спине с подушкой под коленными суставами. В этих положениях мышцы спины во время ночного сна расслабляются и хорошо отдыхают.
4. Следует избегать сквозняков, переохлаждения. Нельзя сидеть на холодной земле и оставаться после плавания в мокром купальнике во время летнего отпуска.
Шейный отдел позвоночника имеет свои анатомо-физиологические особенности. Поэтому дополнительно даются следующие рекомендации:
- следует избегать положений и рабочих ситуаций с длительным сгибательным положением головы. Например, при работе на компьютере рекомендуется периодически облокачиваться на спинку стула и расслаблять руки, производя свободные качательные движения.
- нельзя переразгибать шейный отдел позвоночника (запрокидывать голову). Если необходимо что-то делать на плоскости выше вытянутых вперед рук, следует встать на стул или лестницу. Лучше избегать таких работ, как побелка потолка, крепление штор к карнизам и т.п.
- не следует спать на высокой подушке. Лучше подложить под шею валик.
Рекомендовано в раннем послеоперационном периоде для обезболивания, стимуляции заживления операционной раны, восстановления двигательной активности:
проводить медикаментозное (инъекционное, затем пероральное обезболивание, профилактическую противоязвенную и антитромботическую терапию) и физиотерапевтическое лечение;
исключать нагрузки на позвоночник (поднятие тяжестей, наклоны вперед, активные занятия ЛФК) [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: В раннем послеоперационном периоде (7-14 дней после радикальных вмешательств на позвоночнике) реабилитационные мероприятия проводятся с целью ранней двигательной активизации пациента, купирования болевого синдрома и стимуляции репаративных процессов в области раневого дефекта. Для оказания противоотечного и обезболивающего действия на область раны с первого дня после операции назначается локальная криотерапия (A24.01.005.003 Криотерапия локальная), со 2-го дня после полной остановки кровотечения возможно назначение низкоинтенсивного лазерного излучения, воздействие импульсным низкочастотным электромагнитным полем (A17.30.036). При выраженном болевом синдроме применяется чрескожная электронейростимуляция (A17.24.001 Чрескожная электронейростимуляция при заболеваниях периферической нервной системы), воздействие диадинамическими (A17.03.002 Воздействие диадинамическими токами (ДДТ-терапия) при костной патологии) и синусоидальными модулированными токами (A17.03.003 Воздействие синусоидальными модулированными токами (СМТтерапия) при костной патологии), электрофорез лекарственных препаратов при костной патологии (A17.03.001), рефлексотерапия (A21.03.003 Рефлексотерапия при заболеваниях костной системы).
Восстановление двигательной активности начинается с первого дня, проводятся мероприятия по вертикализации и восстановлению походки при необходимости используются вертикализаторы. Реабилитация немедикаментозными средствами проводится в комбинации с приемом нестероидных противовоспалительных и противоревматических препаратов, по показаниям назначаются глюкокортикоиды. При наличии дооперационных неврологических двигательных нарушений комплексное восстановительное лечение дополняется препаратами, улучшающими нервно-мышечную проводимость.
Рекомендовано проводить мануальную терапию при заболеваниях позвоночника (A21.03.006) при мышечно-скелетных болях, связанных с дегенеративно-дистрофическими изменениями позвоночника [256-259].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 1).
Комментарии: В пользу данной рекомендации указывают 9 РКИ (1176 пациентов), которые были признаны достаточно схожими, чтобы их можно было объединить для метаанализа. Имеются доказательства среднего качества, которые показывают статистически значимое влияние на уменьшение болевого при сравнительных исследованиях (по сравнению с как физическимими упражнения так и физиотерапией (SMD = -0,28, 95% ДИ от -0,47 до -0,09, p = 0,004; I 2 =57%). Среди пяти испытаний РКИ (695 пациентов) проведенная мобилизация по сравнению с препаратами сравнения показала статистически значимое уменьшение боли (SMD=-0,20, 95% ДИ от - 0,35 до -0,04; p=0,01; I 2 = 0%). Также отмечено, что эффект сохраняется через 3 и 6 месяцев наблюдения.
Рекомендовано проводить мануальную терапию при заболеваниях позвоночника (A21.03.006) пациентам с дискогенной пояснично-крестцовой радикулопатией [260, 261].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 1).
Комментарии: Данная рекомендация основана на систематическом обзоре и метаанализе 47 РКИ, включающих в общей сложности 9211 участников. Манипуляции дают эффект, приводящий улучшения функционирования позвоночника в краткосрочной перспективе, а также достоверное уменьшение болевого синдрома по сравнению с имитацией манипуляций. Так, у пациентов, получавшие манипуляционное лечение были более низкие средние баллы по ВАШ (р<0,0001).
Рекомендовано при постоянной боли в позвоночнике после операции на поясничном отделе использовать мануальную терапию при заболеваниях позвоночника (A21.03.006) ( [262, 263].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4).
Комментарии: Рекомендация включала 71 статью, описывающие 103 пациентов после оперативного лечения: ламинэктомия (40%), спондилодез (34%) и дискэктомия (29%). Манипуляции на поясничном уровне использовались у 85% пациентов, которая применялась через 1 год и больше после операции в 66% случаев. Ни в одном из случаев значимых результатов не получено. Данная рекомендация основана на систематическом обзоре с метаанализом, достоверность доказательств этого обзора остается низкой, учитывая, что он основан на отчетах о случаях и сериях исследований пациентов.
Не рекомендовано проведение манипуляционных техник с ротационными движениями шейного отдела позвоночника при минимальных проявлениях вертебробазилярной недостаточности, а также при нарастании неврологического дефицита [264, 265].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 4).
Комментарии: В немногочисленных противоречивых публикациях описываются возможные осложнения, которые связывают с проведением манипуляционных техник мануальной терапии.
Рекомендовано пациентам с дегенеративными заболеваниями позвоночника (М 51.1, М.54.5) применение массажа спины медицинского (А21.03.007) и массажа при заболеваниях позвоночника (A21.03.002).
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 1).
Комментарии: Данная рекомендация основана на результатах 25 РКИ с 3096 участниками Кокрановского обзора. Несмотря на то, что мало убедительный доказательств того, что массаж является эффективным средством лечения боли в нижней части спины (БНС) однако отмечено, что острая, подострая и хроническая БНС имеют улучшение исходов боли при массаже только в краткосрочном периоде наблюдения. Функциональное улучшение наблюдается у пациентов с подострой и хронической БНС по сравнению с неактивным контролем, но только при краткосрочном наблюдении [266, 267]. Однако синергетический эффект массажных манипуляций в сочетании с силовыми тренировками мышц кора при лечении пациентов с хронической неспецифической болью в пояснице может эффективно облегчить боль и дисфункцию в области поясницы, повысить динамическую и статическую мышечную выносливость и иметь значительные краткосрочные и долгосрочные эффекты [268, 269]. Такие виды массажа как миофасциальный релиз и шиатцу обладают в большей степени обезболивающим действием, чем лимфодренажный и соеденительнотканый виды массажа [270, 271].
Рекомендовано при хронической боли в шее (M50.1, M50.3, M50.8, M50.9, M54.2) применение массажа при заболеваниях позвоночника (A21.03.002). [272].
Рекомендовано: при дегенеративных заболеваниях позвоночника, с болью в спине и шее применять следующие типы упражнений: упражнения для укрепления мышц и повышения выносливости, упражнения для активизации/стабилизации специфических мышц туловища, упражнения для активизации/стабилизации глубоких мышц шеи, упражнения с моторным (двигательным) контролем (MCE), упражнения для улучшения подвижности и мобильности, упражнения на растяжку, упражнения на координацию, упражнения на централизацию и методы механической диагностики и терапии с предпочтительным направлением движений (МакКензи). Выбор того или иного типа упражнений или их совместное применение определяется особенностями болевого синдрома и функциональными нарушениями [273-277,282-286].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2).
Комментарии: для исключения неоднозначности в трактовке и понимании типов упражнений приводим их описания:
Упражнения для укрепления мышц и повышения выносливости – упражнения, предназначенные для восстановления и увеличения силы мышц, выносливости, улучшения функции отдельных мышц или групп мышц;
Упражнения для активизации/стабилизации специфических мышц туловища - упражнения, направленные на активизацию специфических глубоких мышц туловища (мышц «кора» - поперечных мышц живота, многораздельных мышц), и поверхностных («глобальных» мышц - прямых мышц живота, мышц, выпрямляющих позвоночник) для достижения активной стабилизации, контроля и улучшения координации в области поясницы и таза;
Упражнения для активизации/стабилизации глубоких мышц шеи упражнения, направленные на активизацию специфических глубоких мышц шеи для достижения активной стабилизации, контроля и улучшения координации в области головы и шеи;
Упражнения с моторным (двигательным) контролем (MCE) - упражнения с моторным контролем направлены восстановление координации и эффективного использования мышц, поддерживающих и контролирующих позвоночник через выполнение простых, а по мере увеличения навыков пациентов, более сложных функциональных заданий;
Общие упражнения - упражнения, направленные на восстановление или повышение силы и выносливости основных мышечных групп верхних/нижних конечностей и туловища, включая упражнения на гибкость/мобильность и аэробные упражнения;
Упражнения для улучшения подвижности и мобильности - упражнения, направленные на увеличение объема движений в позвоночнике и суставах или повторение определенных однотипных движений с целью уменьшения выраженности симптомов;
Упражнения на растяжку - комплекс упражнений, направленный на развитие гибкости и плавное растяжение мышц тела;
Упражнения на координацию – упражнения направленные на развитие способности совершать точные и контролируемые движения за счет синхронной работы разных групп мышц;
Упражнения на централизацию и методы механической диагностики и терапии с предпочтительным направлением движений (МакКензи) – упражнения, выбор которых основан на поиске повторяющегося или устойчивого движения в определенном направлении, которое вызывает уменьшение, централизацию или устранение симптомов;
Аэробные упражнения- это кардио- или кардио-респираторные упражнения, которые выполняются путем повторения последовательностей движений легкой и умеренной интенсивности в течение длительных периодов времени;
Мультимодальные (комплексные) упражнения - упражнения, которые соединяют в себе два или более указанных типов упражнений (методик).
Рекомендовано: для оценки выраженности функциональных нарушений при наличии болевого синдрома в спине, а также в связи с необходимостью динамического контроля уровня боли во время лечения, состояния и динамики функционального статуса пациента при оценке результатов физической терапии использовать домены международной классификации функционирования [311, 312].
Уровень убедительности рекомендаций – В (уровень достоверности доказательств 2)
Комментарии: могут быть использованы домены МКФ максимально соответсвующие функциональному статусу пациента, в качестве примера:
1. Боль в спине, в том числе с двигательным дефицитом:
Функции: b28013 боль в спине: b7101 подвижность нескольких суставов; b7108 функции подвижности сустава, другие уточненные;
Структуры: s76002 поясничный отдел позвоночника; s7601 мышцы туловища; s7602 связки и фасции туловища;
Активность и участие: d4108 изменение позы тела (сгибание, разгибание, ротация), d450 ходьба; d469 ходьба, передвижение и относящаяся к ним активность, другие уточненные и не уточненные.
2. Боль в спине с нарушением контроля движений:
Функции: b28013 боль в спине; b7601 контроль сложных произвольных движений;
Структуры: s76002 поясничный отдел позвоночника; s7601 мышцы туловища; s7602 связки и фасции туловища;
Активность и участие: d4158 поддержание положения тела, другое уточненное (поддержание позиции тела в нейтральном положении); d4106 перемещение центра тяжести тела (перемещение массы тела из одного положения в другое, стоя, сидя или лежа, например, перемещение тяжести с одной ноги на другую в вертикальном положении); d4154 нахождение в положении стоя (пребывание в положении стоя в течение требуемого времени, например, стоя в очереди); d4153 нахождение в положении сидя (пребывание в положении сидя, на сиденье или на полу, в течение требуемого времени, например, сидя за партой или столом; d450 ходьба; d469 ходьба, передвижение и относящаяся к ним активность, другие уточненные и не уточненные.
3. Боль в спине с радикулопатией:
Функции: b2804 иррадиирущая боль в сегменте или области;
Структуры: s1201 спинномозговые нервы;
Активность и участие: d4158 поддержание положения тела, другое уточненное (поддержание позиции тела в нейтральном положении); d4150 нахождение в положении лежа (пребывание в лежачем положении в течение требуемого времени, например, лежа в кровати).;d450 ходьба; d469 ходьба, передвижение и относящаяся к ним активность, другие уточненные и не уточненные.
В поддержку данной рекомендации приводится систематический обзор на основе в том числе 129 РКИ по хронической боли в нижней части спины [311]. Из которого следует, что МКФ предоставляет собой полезный инструмент и может быть применима для определения и количественной оценки использования различных методик в рамках показателей результатов. А также рекомендации экспертного конценсуса основывающегося на данных предварительных исследований, Дельфийском методе и эмпирических данных [312]
Рекомендовано выполнять упражнения на координацию, укрепление мышц туловища и повышение выносливости, упражнения с моторным контролем и упражнения на активацию и стабилизацию специфических мышц туловища для снижения болевого синдрома и улучшения функции у пациентов хронической болью в спине (в том числе с двигательным дефицитом) [273-275].
Уровень убедительности рекомендаций – В (уровень достоверности доказательств –1).
Комментарии: В поддержку данной рекомендации приводится 3 систематических обзора. Один обзор с использованием мета-анализа на основе 39 РКИ [273]. Мета-анализ показал снижение уровня боли в группе упражнений по сравнению с контрольной группой и группами, где применяли другое лечение. Анализ в подгруппах показал, что более эффективными являются упражнения на стабилизацию/координацию и укрепление мышц. Второй систематический обзор на основе 14 РКИ, в котором приводятся данные в пользу упражнений на укрепление мышц, увеличение гибкости и аэробных упражнений при хронической боли в спине [274]. Также учитывался систематический обзор на основе 28 РКИ, в котором выявлено, что методика активизации специфических мышц является более эффективной в сравнении с другими упражнениями, а также другими видами консервативной терапии и плацебо [275].
Рекомендовано выполнять упражнения с моторным контролем и упражнения на специфическую мышечную активацию у пациентов с хронической болью в спине и нарушением контроля движений [276, 277].
Уровень убедительности рекомендаций - В (уровень достоверности доказательств – 1).
Комментарии: Для диагностики нарушения контроля движений используются специфические тесты [278]. В поддержку данной рекомендации приводится 1 систематический обзор на основе 11 РКИ, в котором было продемонстрировано снижение уровня боли у пациентов после курса упражнений с моторным (двигательным) контролем непосрелдственно после курса упражнений, и улучшение функции в как непосредственно после упражнений, так и в среднесрочной перспективе [276]. В 4 из 11 РКИ также отмечалось улучшение функции. Также мы приняли во внимание 1 РКИ высокого качества с анализом результатов у 172 пациентов, где у пациентов с двигательными нарушениями отмечался лучший эффект от упражнений с моторным контролем чем других видов упражнений [277].
Рекомендовано выполнять мультимодальные упражнения, упражнения для активизации специфических мышц туловища, упражнения с моторным контролем, а также выполнять упражнения на централизацию и методы механической диагностики и терапии с предпочтительным направлением движений (МакКензи) пациентам с хронической болью в спине и радикулопатией [279-281].
Уровень убедительности рекомендации – С (уровень достоверности доказательств – 2).
Комментарии: В поддержку данной рекомендации приводится 1 систематический обзор на основе 6 РКИ с оценкой краткосрочных (5 РКИ) и среднесрочных результатов (3 РКИ) [279]. По данным исследований метод МакКензи показал более высокую эффективность в краткосрочной перспективе в сравнении с другими видами консервативной терапии, включая медикаментозное лечение, мануальную терапию и устные рекомендации. В 1 РКИ метод МакКензи в дополнении к устным рекомендациям показал более высокую эффективность в сравнении с методом мануальной терапии у пациентов длительной болью в спине [280]. В 1 РКИ с анализом данных 154 пациентов с хронической дискогенной радикулопатией выводы были сделаны в пользу мультимодальных упражнений [280]. Исследование продемонстрировало эффективность мультимодальных упражнений в сочетании с постуральной коррекцией в снижении боли в спине и ноге и улучшение функции как в краткосрочной, так и долгосрочной перспективе. В еще 1 РКИ на основе данных 54 пациентов в анализе подгрупп была продемонстрирована эффективность мультимодальных упражнений, включающих упражнения на специфическую мышечную активацию, в сравнении с устными рекомендациями, а именно уменьшение интенсивности боли в течение 10 недель и улучшение функции в течение года [281].
Рекомендовано: для оценки выраженности функциональных нарушений при наличии болевого синдрома в шее, а также в связи с необходимостью динамического контроля уровня боли во время лечения, состояния и динамики функционального статуса пациента при оценке результатов физической терапии использовать домены международной классификации функционирования [311, 312].
Комментарии: могут быть использованы домены МКФ максимально соответсвующие функциональному статусу пациента, в качестве примера:
1. Боль в шее с двигательными нарушеними:
Функции: B28010 боль в голове и шее, B7101 подвижность нескольких суставов;
Структуры: S76000 шейный отдел позвоночника;
Активность и участие: D4108 изменение позы тела (движение головы и шеи при взгляде вправо или влево).
2. Боль в шее с головной болью:
Функции: b28010 боль в голове и шее;
Структуры: s7103 суставы головы и шеи, s7104 мышцы головы и шеи;
Активность и участие: d4158 поддержание положения тела (поддержании положения головы и шеи в согнутом состоянии при чтении книги и разогнутом при работе с монитором).
3. Боль в шее с нарушением координации движений:
Функции: b7601 Контроль сложных произвольных движений;
Структуры: s7105 Связки и фасции головы и шеи; S 7104 мышцы головы и шеи;
Активность и участие: d4158 Поддержание положения тела, другое уточненное (поддержание позиции головы шеи и грудного отдела в нейтральном положении).
4. Боль в шее с радикулопатией;
Функции: b2804 Иррадиирущая боль в сегменте или области;
Структуры: s1201 Спинномозговые нервы;
Активность и участие: d4452 Вытягивание (Использование кистей и рук, чтобы достать, коснуться и схватить что-либо, например, чтобы дотянуться через стол или парту до книги).
Рекомендовано использование классификации боли в шее при выборе типов упражнений для ее лечения.
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 4).
Комментарии: Можно выделить 4 основных типа боли в шее:
Боль в шее с ограничением движения;
Боли в шее с нарушением координации движений (механизм возникновения часто связан с хлыстовой травмой шеи в анамнезе или боль имеет похожую симптоматику);
Боль в шее с сочетанной головной болью;
Боль в шее с радикулопатией.
Данная рекомендация основана как минимум на 2 РКИ [282, 283].
Рекомендовано при хронической боли в шее с ограничением движения выполнять комбинированные (мультимодальные) упражнения для шейного отдела, плечевого пояса и верхней конечности, упражнения на укрепление и повышение выносливости мышц, упражнения на растяжку упражнения для улучшения подвижности и мобильности, упражнения для статической/динамической стабилизации (в т.ч. укрепление глубоких мышц) [284-286].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 1).
Комментарии: В поддержку данной рекомендации выполнено как минимум 3 систематических обзора, включая 2 обзора с метанализом. в которых продемонстрирована эффективность применения этих упражнений, и в большей степени комбинации этих упражнений, для уменьшения боли и улучшения функции [284-286].
Рекомендовано при хронической боли в шее с нарушением координации (контроля) движений применять упражнения с субмаксимально прогрессивной нагрузкой, включая упражнения на растяжку, укрепление мышц шейного и грудного отделов, на повышение выносливости мышц, гибкости и координации под контролем специалиста, а также упражнения для вестибулярной реабилитации [287, 288].
Уровень убедительности рекомендаций – В (уровень достоверности доказательств – 2).
Комментарии: В поддержку данной рекомендации выполнено, как минимум, 2 систематических обзора. Первый включил 4761 статью и 21 РКИ в которых продемонстрированы лучшие результаты в виде уменьшения боли, улучшения функции и улучшения качества жизни в группах где применялись данные виды упражнений по сравнению с другими группами [287]. Второй обзор, на базе 12 РКИ, показал эффективность упражнений у пациентов с хроническим хлыстовым синдромом (хроническим болевым синдромом после хлыстовой травмы), а также улучшение по Шкале оценки головокружения - Dizziness Handicap Inventory scores при выполнении упражнений для вестибулярной реабилитации [288].
Рекомендовано при хронической боли в шее с сочетанной головной болью статические и динамические упражнения на укрепление, повышение выносливости мышц шеи и плечевого пояса, растяжение, упражнения на активацию и тренировку глубоких мышц шеи (сгибателей) с биологической обратной связью по давлению [284, 289, 290].
Уровень убедительности рекомендаций - В (уровень достоверности доказательств - 2).
Комментарии: В поддержку данной рекомендации выполнено, как минимум, 3 систематических обзора, в которых продемонстрирована эффективность применения этих упражнений, изменения выражались в виде уменьшения боли и улучшения функции [284, 289]. В одном из обзоров продемонстрирована наибольшая эффективность в комбинации с мануальной терапией [290].
Рекомендовано при хронической боли в шее с радикулопатией общие упражнения, в том числе на растяжение и укрепление мышц, упражнения с преимущественным направлением движения (централизационные) [284, 291, 292].
Уровень убедительности рекомендаций - С (уровень достоверности доказательств - 1).
Комментарии: В поддержку упражнений с преимущественным направлением движения приводим 1 РКИ в котором демонстрируется снижение боли и снижение индекса ограничения жизнедеятельности из-за боли в шее как в краткосрочной и так и в среднесрочной перспективе, тем не менее исследование не позволяет однозначно судить об эффективности упражнений McKenzie [291]. В пользу эффективности различных видов упражнений для пациентов с шейной радикулопатией мы учитываем также 2 систематических обзора с мета-анализом, в одном из них показано снижение уровня боли по ВАШ и улучшение по NDI (Индекс ограничения жизнедеятельности из-за боли в шее). Тем не менее с учетом разнородности данных исследований на которых базируются эти мета-анализы, уровень доказательности можно расценивать как низкий [284, 292].
Рекомендовано применение импульсного низкочастотного электромагнитного поля (A17.30.036). пациентам с дегенеративными заболеваниями позвоночника для купирования болевого синдрома, повышения функциональных возможностей (М 54.5, М 51.1) [293, 294].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 1).
Комментарии: Данная рекомендация основана на результатах 6 РКИ (391 пациент), 1 системного обзора (11 РКИ, 210 участников; 6,8 балла по шкале PEDRo, уровень доказательности 1b) и 1 Кокрановского обзора (636 больных). РКИ выявили значительное (на 30%) уменьшение болей, снижение показателя инвалидности (p<0,05) через 4 недели после лечения импульсными магнитными полями [293, 294]. Систематический обзор показал, что импульсное электромагнитное поле способно уменьшить интенсивность боли и улучшить функциональные возможности у людей с болями в пояснице (анкета боли и инвалидности показала среднее снижение на 42%) [293]
Рекомендовано воздействие низкоинтенсивным лазерным излучением (A17.30.036) пациентам с дегенеративными заболеваниями позвоночника для купирования болевого синдрома (М.54.5, М 51.1) [295-297].
Уровень убедительности рекомендаций - В (уровень достоверности доказательств - 1).
Комментарии: Данная рекомендация основана на результатах 4 РКИ (664 пациента с острой и хронической поясничной болью), 3 мета-анализов (22 РКИ, 1433 больных) и 1 Кокрановского обзора (4 РКИ, 224 больных) Метаанализы показали, что использование низкоинтенсивной лазеротерапии приводит к уменьшению боли на срок до 3-6 месяцев при отсутствии побочных эффектов при неспецифической боли в нижней части спины, снижении инвалидности со средним уровнем доказательности [295, 296, 298]. Снижение интенсивности боли (р<0,0001) и индекса инвалидности Освестри (p<0,05) наблюдалось как при краткосрочных (2 месяца), так и долгосрочных (12 месяцев) сроках наблюдения [297].
Рекомендовано воздействие интерференционными токами (A17.30.005) и чрескожной электронейростимуляции (A17.24.001) у пациентов с дегенеративными заболеваниями позвоночника (М54.5, М51.1), в том числе в послеоперационном периоде для купирования болевого синдрома, улучшения функциональных возможностей, предотвращения послеоперационных осложнений [299-302].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 1).
Комментарии: Данная рекомендация основана на результатах 6 РКИ (225 пациентов с хронической болью в пояснице и 48 добровольцев), 4 мета-анализов (44 РКИ, 2688 пациентов). Метанализы (6 баллов по шкале PEDro) выявили регресс хронической боли в пояснице на 9-14% как при использовании чрескожной электрической стимуляция нервов, так и при использовании интерференционного тока (0,36, ДИ от -0,56 до 1,27, I2= 91%) [299, 300]. Другой метанализ (16 РКИ, 655 участников) показал аналогичные результаты, при этом уменьшение болей в пояснице было как во время терапии (p=0,02), так и через 1-3 месяца после нее (p = 0,99) [303]. Из
Рекомендовано пациенту с дегенеративной патологией позвоночника для профилактики ее развития и прогрессирования:
соблюдать ортопедические рекомендации;
поддерживать оптимальные росто-весовые показатели;
систематически выполнять оптимальные физические нагрузки [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Большинство «позвоночных» болей могли быть предотвращены контролем осанки, походки и веса, достаточной ежедневной физической, в том числе спортивной активностью, соответствующей возрасту и здоровью. В массе своей люди с возрастом снижают двигательную активность, набирают вес и не уделяют внимания физическим упражнениям и тогда даже при несущественной физической нагрузке она становится избыточной и травмирующей.
В качестве мер профилактики развития и прогрессирования спондилоартроза рассматриваются:
снижение лишнего веса;
регулярные доступные и разнообразные физические нагрузки (лечебная физкультура, прогулки по свежему воздуху, фитнес, тренажеры, скандинавская ходьба и пр.);
рациональное и сбалансированное по составу и калорийности питание;
профилактика травматизма;
правильное распределение нагрузки на позвоночник;
индивидуальный подбор матраца и подушки;
ношение ортопедической обуви;
санация инфекционных очагов.
Рекомендовано диспансерное наблюдение пациента с дегенеративной патологией позвоночника у врача-невролога по месту жительства с целью оценки клинического состояния, а при необходимости проведения инструментального диагностического обследования [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Рекомендовано проинформировать пациента с дегенеративной патологией позвоночника для понимания им особенностей течения, вариантах лечения и исходов заболевания [304]:
о применяемых технологиях лечения;
о возможных исходах хирургического лечения;
о необходимости медицинской реабилитации в дальнейшем.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Рекомендовано для профилактики осложнений хирургического лечения пациента учитывать топографо-анатомические особенности пораженного сегмента, корректно подбирать инструментарий и имплантаты, соблюдать правила асептики и антисептики на всех этапах лечения [1, 304]:
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Показания для экстренной госпитализации в медицинскую организацию:
гипералгическая форма корешкового синдрома;
каудо-медуллярный синдром;
остроразвивающаяся миелопатия;
парализующий ишиаз.
Показания для плановой госпитализации в медицинскую организацию:
корешковый болевой синдром и (или) анталгический сколиоз, резистентный к консервативной терапии 4-6 нед.;
радикулопатия с нарастающим неврологическим дефицитом (парез 4 и менее баллов);
нейрогенная перемежающаяся хромота.
Показания для госпитализации в дневной стационар:
корешковый болевой синдром, местный болевой синдром (при ранее непроводимом консервативном лечении, либо отсутствие эффекта от терапии амбулаторно в течение 6-ти нед).
Показания к выписке пациента из медицинской организации:
завершенность хирургического лечения или его этапа(-ов) при многоэтапном вмешательстве.
Показания к выписке пациента из дневного стационара:
Законченный курс восстановительного лечения
В качестве возможных исходов хирургического лечения целесообразно использовать классификацию [305, 306]:
Осложнение (Complications) - любое отклонение от нормального послеоперационного течения, которое не вложено в саму эту процедуру и которое не является последствие лечения;
Неспособность вылечить (failure to cure) - заболевания и состояния, которые остаются неизменными после операции;
Последствия (sequelae) - это изменения, присущие вмешательству; неизбежны после операции.
Согласно данной классификации, объяснение пациенту возможных исходов может позволить пациенту подробно оценить необходимость и пользу от предлагаемого хирургического вмешательства, а врачу избежать двояких толкований в случае спорных моментов.
Осложнение необходимо классифицировать на три группы: специфические, технические и общие.
Рекомендовано классифицировать послеоперационные осложнения согласно классификации Clavien-Dindo [305]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии. Классификация Clavien-Dindo для послеоперационных осложнений включает 6 градиции [305]: Легкое - требуются только небольшие процедуры, которые можно проводить у постели больного, такие как установка внутривенных и мочевых катетеров (A11.12.001 Катетеризация подключичной и других центральных вен, А11.12.002 Катетеризация кубитальной и других периферических вен, A11.28.007 Катетеризация мочевого пузыря). Разрешены физиотерапия и следующие препараты: противорвотные препараты, анальгетики, диуретики, растворы, влияющие на водно-электролитный баланс; Умеренное - требуется фармакологическое лечение лекарствами, отличными от разрешенных при легких осложнениях, например, антибактеральными препаратами системного действия. Также сюда входит трансфузия крови (A18.05.012 Гемотрансфузия) и полное парентеральное питание; Тяжелое (вмешательство без общей анестезии*) - требуется проведение эндоскопической, инвазивной процедуры или повторной операции без общей анестезии; Тяжелое (операция под общим наркозом) - требуется проведение операции под общим наркозом; Тяжелое (системная недостаточность органов **); Смерть (послеоперационная смерть).
* Например: ревизия раны с применением снотворных и седативных средств и/или местной анестезии.
** С такими осложнениями обычно можно справиться в условиях отделения интенсивной терапии, но в некоторых случаях пациенты с осложнениями меньшей степени тяжести также могут быть госпитализированы в отделение интенсивной терапии. Для интраоперационных осложнений рекомендуется применять классификацию Stava. Выделено три класса осложнений: I класс — ошибки без последствий; II класс — ошибки с непосредственным распознаванием и коррекцией; III класс — нераспознанные ошибки, ведущие к значимым негативным последствиям [307].
Классификация Clavien-Dindo имеет отилчную внутри- (каппа>0.8) и межэкспертную воспроизводимость (каппа>0.8) в хирургии позвоночника возрослых [310].
Интра- и послеоперационно после декомпрессивных и декомпрессивно-стабилизирущих хирургических вмешательств возможно развитие следующих специфических осложенний: повреждение твёрдой мозговой оболочки, послеоперационная ликворея; появление или усугубление неврологического дефицита (двигательные нарушения, нарушения чувствительности, нарушение функций тазовых органов; эпидуральная гематома; мальпозиция винтов и миграция имлантатов; перелом частей позвонка; переломы элементов металлоконструкций; инфекции области хирургического вмешательства [316-318].
Хирургические осложнения, возникшие у оперированных пациентов, могут подразумевать проведение повторного оперативного вмешательства.
7.2 Особенности диагностики и хиругического лечения болевых и/или неврологических синдромов у беременных
Рекомендовано выполнение МРТ позвоночника для уточнения патологического субстарата дегенеративного заболевания позвоночника у беременных женщин при выраженном болевом синдроме и/или прогрессировании неврологического дефицита [319, 322].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2).
Комментарии. МРТ позвоночника представляет собой первый уровень и самый безопасный диагностический инструмент для беременных женщин, страдающих проблемами позвоночника, позволяющий провести неинвазивное и детальное обследование позвоночника.
Рекомендовано при возникновении выраженной корешковой боли, прогрессирующего неврологического дефицита, нарушениях функции тазовых органов, обусловленных грыжей межпозвонкового диска, не поддающихся медикаментозному лечению, рассмотреть возможность хирургического вмешательства [319].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2).
Комментарии. Декомпрессивное вмешательство (микродискэктомия) при грыже диска у беременных женщин является предпочтительным методом, высокоэффективным и безопасным, который не оказывает негативного влияния на течение беременности, роды или здоровье ребенка [320, 321]; декомпрессивно-стабилизирующие вмешательства не рекомендуются, так как могут привести к неблагоприятным последствиям для плода [320]. В качестве альтернативы традиционной микродискэктомии может быть рассмотрена эндоскопическая дискэктомия. Наиболее подходящие сроки и положение пациентки при хирургическом вмешательстве выбираются на основе гестационного срока и места патологии [319].














