Истинная аневризма грудной (АГА) и/или торакоабдоминальной аорты (ТААА) определяется как патологическое необратимое расширение аорты более чем на 50% от нормального диаметра (5,0-5,5 см и более). Диаметр аорты зависит от пола, возраста, веса, роста. Нормальным считается диаметр аорты менее 4,0 см. Расширение аорты свыше данного значения, но не достигшего критериев аневризмы, называют пограничным расширением аорты. При этом термин «эктазия» аорты, которым зачастую пользуются радиологи для описания умеренного расширения аорты, не является корректным в данном случае [1]. В отличие от «истинной» аневризмы, «ложная» (псевдоаневризма) представляет собой отграниченное окружающими артерию тканями скопление крови, сформировавшееся вне артериального сосуда в результате разрыва его стенки.
Основными этиологическими факторами АГА и ТААА являются наследственные заболевания, врожденные аортопатии, мультифакториальные дегенеративные заболевания, воспалительные заболевания и инфекционные заболевания. Кроме того, аневризматическое расширение нередко является исходом расслоения грудной или торакоабдоминальной аорты, в том числе в отсутствие значимого расширения аорты как до, так и сразу после развития расслоения. Аневризмы корня и восходящей аорты (ВА) нередко носят наследственный характер и формируются в более молодом возрасте, в то время как аневризмы нисходящего отдела грудной аорты чаще имеют дегенеративную этиологию и характерны для пациентов среднего и пожилого возраста [2,3]. Кроме того, аневризмы корня аорты и ВА также нередко развиваются у пациентов с двустворчатым аортальным клапаном (ДАК), хотя остаются не полностью ясными генетические основы развития ДАК и развитие сопутствующей аортопатии далеко не у всех пациентов [4,5]. Большинство же аневризм корня и ВА относятся к группе несиндромных несемейных (спорадических) аортопатий. Поскольку тактика ведения пациентов с аневризмами корня и ВА может отличаться в зависимости от причины и дополнительных факторов риска осложнений, ассоциированных с аортой, рекомендации по консервативному, транскатетерному, хирургическому и гибридному лечению могут отличаться (см. раздел 3 «Лечение»).
Примерно в 20% случаев АГА и ТААА связаны с генетически обусловленной или наследственной патологией. При этом их также называют наследственными заболеваниями грудной аорты (НЗГА), и некоторые из них сопровождаются мультисистемными симптомами (в этом случае они считаются синдромными НЗГА), а некоторые – изолированной патологией аорты с возможным вовлечением ее ветвей (несиндромные НЗГА) [6]. При НЗГА чаще всего поражаются корень, ВА или оба этих сегмента, но также они могут проявляться поражением дистальной аорты или расслоением аорты. Патогенные варианты множества генов могут приводить к формированию АГА, аневризм артерий головного мозга и АБА [6,7]. Примерно у 20% лиц с АГА или расслоением аорты имеются указания на заболевание грудной аорты в семейном анамнезе (по меньшей мере 1 заболевший родственник первой степени родства). Популяционные исследования продемонстрировали семейный характер АГА и расслоений – в случаях семейной патологии отмечается значимое увеличение риска развития АГА и расслоений аорты по сравнению со спорадическими случаями. В связи с этим среди пациентов с аневризмами корня и ВА, чрезвычайно важен скрининг родственников первой линии родства при помощи методов лучевой диагностики с целью определения нераспознанных, бессимптомных заболеваний грудной аорты.
Хотя существует определенное анатомическое разграничение между АГА и ТААА, это не подразумевает сопоставимость их всех по этиологии или естественному течению. Аневризмы корня и ВА в типичных случаях выявляются у пациентов более молодого возраста по сравнению с аневризмами нисходящего отдела грудной и ТААА (60 лет и 72 года, соответственно) [2]. Даже при учете лишь «спорадических» аневризм (т.е. аневризм при отсутствии признаков синдромной, семейной или подтвержденной генетической этиологии) значимая разница в возрасте пациентов двух групп (64 и 72 года, соответственно) сохраняется [2]. Кроме того, типичные факторы риска атеросклероза (т.е. артериальная гипертензия, сахарный диабет, курение) значительно реже встречаются у пациентов со спорадическими аневризмами корня и ВА по сравнению с больными с аневризмами нисходящего отдела грудной аорты [8]. Также распространенность кальцификации аорты или атером достаточно мала при спорадических аневризмах корня и ВА, но весьма высока при аневризмах нисходящего отдела грудной аорты (8–9% и 80–88% соответственно). В совокупности эти сведения свидетельствуют о том, что аневризмы корня и ВА чаще носят врожденный (и даже наследственный) характер, в то время как аневризмы нисходящего отдела аорты в основном имеют атеросклеротический генез. Хотя иногда их называют атеросклеротическими аневризмами, гораздо чаще аневризмы нисходящего отдела грудной аорты (не обусловленные заболеваниями соединительной ткани) характеризуются как «дегенеративные». Медикаментозные, хирургические и эндоваскулярные методы лечения спорадических и дегенеративных аневризм обсуждаются в разделе 3 «Лечение».
В семьях, члены которых страдают НЗГА, и причинный ген не идентифицирован, ведение в целом здоровых членов семей базируется на клинических характеристиках, применяемых в отношении больных членов семьи. К таким характеристикам относятся локализация аневризмы, диаметры грудной аорты в разных отделах у больных членов семьи, перенесших расслоение аорты типа А по Stanford, а также патология иных сосудов и другие симптомы, накапливающиеся на фоне АГА в семье.
Эти данные свидетельствуют о том, что гетерозиготные патогенные варианты одиночных генов становятся причиной НЗГА в большинстве семей. В семьях с НЗГА следует проводить соответствующие анализы (исследования) у лиц с подтвержденным диагнозом заболевания грудной аорты. При наличии патологии в семейном анамнезе она проявляется в более молодом возрасте (в среднем в 57 лет) [9]. В таких семьях с НЗГА отмечается вариабельная экспрессия генов, ответственных за заболевания грудной аорты, что находит отражение в разном возрасте, начале заболевания, разной частоте расслоения аорты на фоне ее диаметра <5,0 см, разном риске расслоения аорты типа В по Stanford и разной частоте развития дилатации корня аорты, тубулярной восходящей части грудной аорты либо обоих отделов. Кроме того, конкретные патологически измененные гены влияют на риск развития сопутствующих сосудистых заболеваний.
Факторы риска заболевания или состояния (группы заболеваний или состояний)
Большинство случаев АГА относятся к группе несемейных несиндромных (спорадических) аортопатий, ассоциированных с двустворчатым либо трехстворчатым аортальным клапаном. Основными факторами риска патологического расширения ВА являются артериальная гипертензия (АГ), моногенные заболевания соединительной ткани (синдромы Марфана, Элерса-Данло, Тернера, Лойеса-Дитца), гигантоклеточный артериит, атеросклероз; относительно нечастой причиной расширения и расслоения грудной аорты является инфекция (включая сифилитическое и микотическое поражение), а также аутоиммунные процессы.
Факторами риска аневризм корня, ВА, дуги и ТААА, а также расслоений аорты являются патогенные варианты генов, предрасполагающих к заболеваниям грудной аорты [10]. Хотя рекомендации сосредоточены на лицах из группы высокого риска одиночной генной мутации (Таблица 1), генетическое тестирование может оказаться полезным у многих пациентов с заболеваниями грудной аорты. Лишь патогенные или вероятно патогенные варианты могут провоцировать развитие заболеваний, и именно их следует использовать для каскадных генетических тестов, назначаемых всем родственникам из группы риска наследования патологических вариантов.
Таблица 1. Факторы риска семейных заболеваний грудной аорты
● Заболевание грудной аорты и симптомы синдрома Марфана, синдрома Лойеса-Дитца или сосудистого типа синдрома Элерса-Данло |
|---|
● Дебют заболевания грудной аорты в возрасте младше 60 лет |
● Заболевание грудной аорты или аневризмы периферических или внутричерепных артерий в семейном анамнезе у родственников первой или второй степени родства |
● Внезапная смерть неясной этиологии в относительно молодом возрасте среди родственников первой или второй степени родства |
«Традиционные» факторы риска атеросклероза (мужской пол, гиперхолестеринемия, курение, сахарный диабет) реже встречаются при аневризмах корня и ВА, нежели при аневризмах нисходящей грудной аорты.
В настоящее время пристальное внимание уделяется планиметрическим параметрам грудной аорты, рассматривающимся в качестве перспективных факторов риска формирования аневризм и расслоений. К таким признакам относят, кроме максимального диаметра аорты, ее кривизну, степень удлинения, определенные врожденные аномалии («бычья дуга» и т.п.). Установлено, что удлинение нерасширенной тубулярной части ВА (от уровня СТС до устья БЦС) более 90 мм может являться фактором риска расслоения аорты типа А по Stanford [11], а удлинение дуги аорты более 50 мм с высокой долей вероятности предрасполагает к расслоению аорты типа B по Stanford [12,13]. Отхождение БЦС и ЛОСА единым стволом (так называемая “бычья дуга”) и коарктация аорты также ассоциированы с формированием аневризм и расслоений грудной аорты.
Встречаемость АГА за последние 2 десятилетия значительно возросла и к настоящему времени достигает 5-10 случаев на 100 тыс. населения в год. Данный прирост обусловлен, в основном, совершенствованием диагностики патологии аорты. Заболевание наиболее характерно для пациентов старшей возрастной группы (50-70 лет). Эта патология аорты выявляется у мужчин в 2-4 раза чаще, чем у женщин [13,14]. Выживаемость при естественном течении АГА составляет 20% за 5-летний период от момента установления диагноза. Таким образом, пациенты с АГА находятся в группе высокого риска, что подтверждается данными литературы: только 41% пациентов с АГА доживают до этапа стационарного лечения [15]. Важное значение для прогнозирования выживаемости имеет максимальный диаметр грудной аорты. Известно, что в течение жизни человека диаметр аорты постепенно увеличивается. Так, ежегодное увеличение аневризмы ВА составляет, в среднем, 1 мм, а для аневризмы нисходящей аорты этот показатель соответствует 3 мм. Большие аневризмы аорты склонны к более быстрому росту - позже поправлю, это взаимоисключающие предложения. Согласно данным Chau и соавт., при диаметре аорты 8,0 см скорость ее роста увеличивается в 2 раза и составляет 1,9 мм в год [16]. Анамнез нарушения мозгового кровообращения, курение, атеросклероз периферических артерий достоверно увеличивают скорость роста аневризмы аорты [17]. Установлено, что диаметр ВА в среднем больше у страдающих артериальной гипертензией. Из результатов исследования Kuzmik G.A. и соавт. следует, что риск разрыва аневризмы аорты или развития расслоения растет пропорционально её диаметру. Так, ежегодный риск осложнений со стороны грудной аорты у пациентов с диаметром последней 40-49 мм может достигать 2%, тогда как при диаметре грудной аорты более 6 см частота подобных осложнений, в том числе фатальных, возрастает в 3-4 раза [16,18].
Аневризма и расслоение аорты (I71):
I71.1 Аневризма грудной части аорты разорванная;
I71.2 Аневризма грудной аорты без упоминания о разрыве;
I71.5 Аневризма грудной и брюшной аорты разорванная;
I71.6 Аневризма грудной и брюшной аорты без упоминания о разрыве;
I71.8 Аневризма аорты неуточненной локализации разорванная
I71.9 Аневризма аорты неуточненной локализации без упоминания о разрыве
Примеры оформления диагнозов:
Основной: Аневризма корня и восходящего отдела аорты. Тяжелая АН
Осложнения: ХСНсФВ, 1 стадии. III ФК (NYHA).
Классификация аневризм грудной аорты включает в себя следующие понятия:
● Аневризма корня аорты;
● Аневризма восходящей аорты;
● Аневризма дуги аорты;
● Аневризма нисходящей аорты;
● Торакоабдоминальная аневризма;
● Нередко встречаются комбинации зон расширения аорты, например аневризма корня, восходящей части и дуги аорты и т.п.
Среди истинных аневризм можно выделять веретеновидные и мешотчатые. Разными авторами предпринимались попытки классифицировать АГА по этиологическому признаку, однако, прежде всего, в связи с невозможностью выделения одного ведущего этиопатогенетического фактора, мы находим большинство подобных классификаций узконаправленными и имеющими ограниченное применение в научной и клинической практике. Одной из рациональных мы считаем систематизацию, предложенную исследователями Каролинского Института: предлагается аневризмы грудной аорты делить на моногенные (или синдромные, обусловленными генетическими нарушениями – синдромами Марфана, Элерса-Данло, Лойеса-Дитца и т.д.), ассоциированные с ДАК, и несиндромные несемейные, т.е. идиопатические [19]. На рисунке 1 представлен объединенный патогенетический подход, согласно которому аневризмы ВА предлагается делить на группы семейных и несемейных; в свою очередь, в каждой из данных групп выделяют подгруппы синдромных и несиндромных аневризм аорты, ассоциированных с мутациями различных генов, влияющих на структуру стенки аорты. ДАК может выступать в роли как (предположительно) самостоятельного этиологического фактора, так и являться «дополнительным состоянием». Таким образом, приблизительно около 75% пациентов с аневризмами ВА принадлежит к группе несиндромных несемейных, или спорадических аневризм, либо несиндромных несемейных аневризм ВА, ассоциированных с двустворчатым АК [20].
Аневризмы с вовлечением нисходящего отдела грудной и брюшной аорты обозначаются как ТААА. Классификация ТААА по Crawford, позже модифицированная Safi и соавторами [21] (Рисунок 2), не только описывает степень распространения аневризмы, но также позволяет прогнозировать заболеваемость и летальность при лечении аневризмы [22].
Кроме того, существует классификация воспалительных аневризм аорты Svensson L.G. и соавт., разработанная для пациентов с аортитами различной природы (болезнь Такаясу, гигантоклеточный аортит и др.) [23].
● Тип I – в зону расширения аорты полностью вовлечены грудной отдел, а также нисходящий или торакоабдоминальный отделы аорты;
● Тип II – в зону расширения аорты вовлечен восходящий отдел до уровня дуги аорты;
● Тип III – в зону расширения вовлечен торакоабдоминальный отдел аорты;
● Тип IV – аневризма субдиафрагмального отдела аорты.
Рисунок 1. Этиологическая классификация аневризм грудной аорты [20].
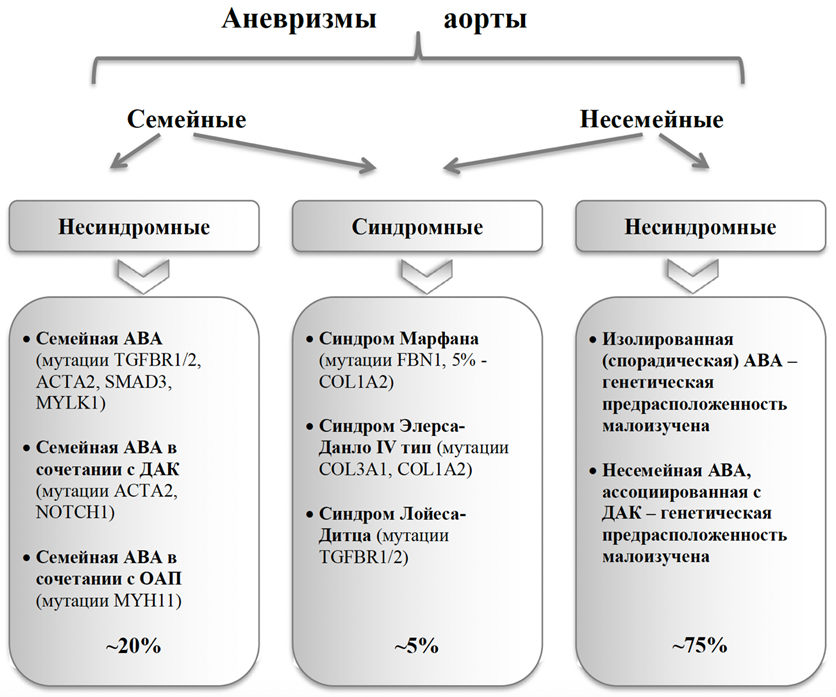
Примечания. АГА – аневризма грудной аорты; ДАК – двустворчатый аортальный клапан; ОАП – открытый артериальный проток; ACTA2 – ген-гладкомышечного актина; COL1A2 – ген коллагена типа 1-2; COL3A1 – ген коллагена типа 3-1; FBN1 – ген фибриллина-1; TGFBR1/2 – ген рецептора трансформирующего ростового фактора- 1/2 типа; MYH11 – ген белка тяжелых цепей миозина-11; MYLK1 – ген киназы легких цепей миозина; NOTCH1 – трансмембранный белок NOTCH1; SMAD3 – внутриклеточные белки семейства SMAD, передающие сигнал от лигандов (TGF) в ядро.
Рисунок 2. Классификация торакоабдоминальных аневризм аорты по Crawford
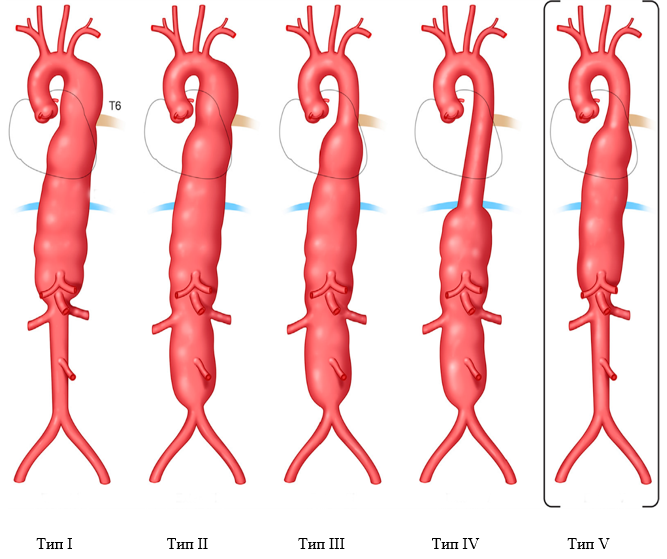
Классификация аневризм торакоабдоминального отдела аорты в соответствии со степенью поражения аорты, которая первоначально была предложена Crawford [24]: степень распространения I – от уровня ниже подключичной артерии до уровня выше чревного ствола или напротив верхней брыжеечной артерии, но выше почечных артерий; степень распространения II – от уровня ниже подключичной артерии, с поражением инфраренального отдела брюшной аорты, вплоть до уровня бифуркации аорты; степень распространения III – от уровня ниже межреберного промежутка Т6 до бифуркации аорты; степень распространения IV – от уровня ниже Т12, сужаясь к месту, аккурат выше бифуркации аорты. Safi и соавторы [21] предложили расширить классификацию добавлением степени распространения V – от уровня ниже Т6, сужаясь к месту, аккурат выше почечных артерий.
Аневризма аорты во многих случаях никак себя не проявляет. Симптоматика может возникать при формировании большого аневризматического мешка, сдавливающего окружающие структуры: кашель, одышка, осиплость голоса (вследствие сдавления возвратного нерва), отек верхних конечностей (в результате сдавления верхней полой или брахиоцефальной вены), болезненное или нарушенное глотание (по причине сдавления пищевода) при больших аневризмах грудной аорты, постоянные или периодические боли или дискомфорт в грудной клетке, ощущение «пульсации» в груди [25].
Рекомендуется выполнять сбор жалоб и анамнеза у всех пациентов с подозрением на АГА и ТААА для верификации диагноза [26].
ЕОК/РКО I C (УДД 4, УУР С)
Комментарии. Несмотря на то, что зачастую пациенты с аневризмой грудной аорты и незначительная часть больных с расслоением аорты не имеют клинических проявлений, с поражением аорты потенциально могут быть связаны следующие симптомы:
— острая резкая, ломящая или пульсирующая боль в груди или животе («ощущение разрыва»), с возможной миграцией в спину, шею, ягодицы, пах или ноги и наводить на мысль о расслоении аорты или другом ОАС;
— кашель, одышка или затрудненное / болезненное глотание, осиплость (из-за паралича левого гортанного нерва), дисфагия, гематемезис, отек верхних конечностей, кровохарканье при сдавлении аортой при ее аневризме или расслоении;
— инфаркт миокарда может быть одной из масок острого расслоения ВА;
— редкими проявлениями гигантских АВА являются сдавление различных отделов сердца, легочной артерии, а также правожелудочковая недостаточность
— инсульт, транзиторная ишемическая атака, параплегия или перемежающаяся хромота как результат ишемии головного или спинного мозга при расслоении аорты, или материальной эмболии при выраженном атеросклерозе аорты (например, при «shaggy aorta») [27].
жалобы, обусловленные аортальной регургитацией (при хронической аортальной регургитации в стадии компенсации клинические проявления могут отсутствовать в течение продолжительного периода времени. При приближении и наступлении декомпенсации наступает постепенное снижение толерантности к физическим нагрузкам, появление одышки при нагрузках (вначале при высокоинтенсивных нагрузках), ощущение «сердцебиений» в груди и «пульсаций» в голове. Нередкими проявлениями хронической аортальной регургитации являются неприятные ощущения, дискомфорт и боли в области сердца и в грудной клетке. Периферические отеки, ортопноэ и отек легких могут наблюдаться как при хронической, так и при острой аортальной регургитации. Острая аортальная регургитация, как правило, характеризуется внезапным появлением выраженной одышки и/или удушья. Ишемия миокарда, нередко развивающаяся при острой аортальной регургитации, может проявляться болевым синдромом в грудной клетке [28,29]. Сведения об имеющейся аневризме и/или расслоении ВА позволяют заподозрить вторичный характер аортальной регургитации[28,30] ).
Рекомендуется у пациентов с аневризмами корня и восходящего отдела грудной аорты или расслоением аорты собрать семейный анамнез (случаи заболеваний грудной аорты, двустворчатого аортального клапана, моногенных заболеваний соединительной ткани, внезапной смерти неясного генеза, аневризм периферических и внутричерепных артерий) на протяжении нескольких поколений [31].
ЕОК/РКО I C, АКК и ААC 1 В (УДД 4, УУР С)
Комментарии. Актуальные данные свидетельствуют о том, что у 13–20% пациентов с заболеванием грудной аорты без симптомов синдромов Марфана и Лойеса-Дитца обнаруживаются родственники первой степени родства со схожей патологией [31]. ЗГА в этих семьях обычно наследуются аутосомно-доминантным путем со снижением пенетрантности (особенно у женщин).
Рекомендуется выполнять физикальное обследование всех пациентов с подозрением на АГА и ТААА для установления диагноза [26].
ЕОК/РКО I C (УДД 4, УУР С)
Комментарии. Осмотр пациента с подозрением на аневризму аорты должен включать пальпацию и аускультацию грудной клетки и живота с целью выявления патологических артериальных пульсаций, шумов вследствие турбулентного кровотока, сравнение характеристик пульса и значений АД на руках.
Базовые лабораторные исследования включают выявление сердечно-сосудистых факторов риска и играют незначительную роль в диагностике заболеваний грудной аорты. Вместе с тем, существует ряд ситуаций, когда выполнение лабораторных исследований принципиально:
Рекомендуется всем пациентам с АГА и ТААА, госпитализирующимся в стационар для оперативного лечения, исследование кислотно-щелочного состояния крови (рН, ВЕ, рСО2, РО2, Lac - анализ капиллярной/артериальной/венозной проб) с целью оценки тяжести гипоксемии и степени выраженности метаболических нарушений, выполнение коагулограммы (ориентировочного исследования системы гемостаза) (активированное частичное тромбопластиновое время (АЧТВ), определение протромбинового (тромбопластинового) времени в крови (ПТИ), определение концентрации Д-димера в крови, исследование уровня фибриногена в крови, определение активности антитромбина III в крови), определение международного нормализованного отношения (МНО) для прогноза риска периоперационных кровотечений. Определение основных групп по системе AB0, определение антигена D системы резус (резус-фактор), определение фенотипа по антигенам C, c, E, e, Cw, K, k и определение антиэритроцитарных антител, определение антигена (HbsAg) вируса гепатита B (Hepatitis B virus) в крови, определение антител к вирусу гепатита C (Hepatitis C virus) в крови, определение антител к бледной трепонеме (Treponema pallidum) в крови, определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV 1) в крови, определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-2 (Human immunodeficiency virus HIV 2) в крови для исключения ассоциации с ВИЧ-инфекцией, гепатитом, а также в случае оперативного лечения при необходимости в пери- и/или послеоперационном периоде [32,33].
ЕОК/РКО I C (УУР C, УДД 5)
Рекомендуется проведение общего (клинического) анализа мочи, общего (клинического) анализа крови (с оценкой уровня гемоглобина и гематокрита, количества эритроцитов, лейкоцитов, тромбоцитов, скорости оседания эритроцитов) и анализа крови биохимического общетерапевтического (исследования уровня калия в крови, уровня натрия в крови, уровня глюкозы в крови, уровня креатинина в крови, исследование уровня общего белка в крови, уровня мочевины в крови, уровня общего билирубина в крови, определение активности аспартатаминотрансферазы и аланинаминотрансферазы в крови, исследование уровня общего трийодтиронина (Т3) в крови, уровня общего тироксина (Т4) сыворотки крови и уровня тиреотропного гормона (ТТГ) в крови, исследование уровня С-реактивного белка в сыворотке крови, уровня холестерина крови, уровня холестерина липопротеидов низкой плотности (ХсЛНП) и триглицеридов (ТГ),) для оценки почечной и печеночной функции, исключения воспаления и с целью выявления факторов риска сопутствующего атеросклероза и, при необходимости, коррекции терапии у всех пациентов с АГА и ТААА в рамках первичного обследования, при поступлении в стационар, а также в случае оперативного лечения при необходимости в пери- и/или послеоперационном периоде [32–34].
ЕОК/РКО I C (УДД 4, УУР С)
Рекомендуется рассмотреть возможность проведения генетического тестирования для выявления патогенных или вероятно патогенных мутаций у пациентов с аневризмами корня и восходящего отдела грудной аорты или хроническим расслоением грудной аорты и факторами риска НЗГА (таблица 1) [35].
ЕОК I С, АКК и ААC 1 В (УДД 4, УУР С)
Комментарии. Для диагностики требуется исследование 11 генов, которые, согласно подтвержденным сведениям, несут риски высокой пенетрантности заболеваний грудной аорты: FBN1, LOX, COL3A1, TGFBR1, TGFBR2, SMAD3, TGFB2, ACTA2, MYH11, MYLK, PRKG119. В этот список также входят гены, повышающие риск развития ЗГА и (или) обусловливающие системные симптомы, совпадающие с проявлениями синдромов Марфана, Лойеса-Дитца, сосудистого типа синдрома Элерса-Данло. [36]. Пациентам, соответствующим клинико-диагностическим критериям синдрома Марфана, но не страдающим эктопией (т.е. вывихом) хрусталика, желательно провести генетические анализы для исключения альтернативного диагноза (синдром Лойеса-Дитца). Генетические лаборатории классифицируют редкие варианты генов НЗГА следующим образом: патогенные, вероятно патогенные, варианты неизвестного значения, доброкачественные, вероятно доброкачественные. Варианты неизвестного значения не имеют подтвержденной связи с заболеваний грудной аорты и, таким образом, не должны применяться для выявления членов семей из группы риска, а также для принятия клинических решений.
Рекомендуется рассмотреть возможность проведения у пациентов с подтвержденным патогенным или вероятно патогенным вариантом гена, предрасполагающим к НЗГА, генетического консультирования, при этом клиническое ведение пациента необходимо скорректировать с учетом конкретного гена и варианта гена [37].
EOK I B, АКК и ААC I В (УДД 4, УУР С)
Комментарии. Мутации FBN1, TGFBR1, TGFBR2, SMAD3, TGFB2 выявляют в 6–8% семей с НЗГА, у членов которых отсутствуют симптомы синдромов Марфана и Лойеса-Дитца [35]. Подтверждено, что мутации ACTA2, MYH11, MYLK, LOX, PRKG1 могут вызывать НЗГА в отсутствие выраженных симптомов синдромов Марфана или Лойеса-Дитца [37]. В рамках клинического описания семей с НЗГА с патогенными вариантами недавно открытых генов установлено, что основной ген позволяет прогнозировать не только риск аневризмы и расслоения грудной аорты (АРГА), но и клиническую картину патологии аорты, риск развития расслоения аорты в определенном диапазоне диаметров аорты (см. ранее), а также риск развития и виды дополнительной сосудистой патологии. Например, мутации TGFBR2 предрасполагают к развитию не только АРГА, но и аневризм внутричерепных артерий, аневризм и расслоений иных артерий; мутации ACTA2 ведут к развитию АРГА и окклюзирующей патологии артерий (в том числе ранних инсультов, ишемической болезни сердца).
Рекомендуется рассмотреть возможность проведения генетического тестирования биологическим родственникам пациентов с известным заболеванием грудной аорты и выявленными у них патогенными или вероятно патогенным вариантам генов НЗГА [37,38].
ЕОК/РКО IC, АКК и ААC 1 В (УДД 4, УУР С)
Комментарии. Каскадный скрининг подразумевает применение расширенных визуализирующих методик для выявления бессимптомного расширения грудной аорты у лиц из группы риска в семьях с наследованием патогенного варианта НЗГА; данный процесс повторяют по мере выявления членов семей с расширением грудной аорты или носителей патогенного варианта [39]. Патогенные варианты в генах НЗГА обеспечивают повышенный риск развития заболевания грудной аорты, поэтому лица с подобными патогенными вариантами подлежат скринингу с проведением визуализации аорты на предмет выявления бессимптомных заболеваний грудной аорты [37,38].
Визуализирующие методы обследования имеют основополагающее значение для первичной диагностики и продленного наблюдения за пациентами с АГА и ТААА. Выбор адекватного метода обследования или их комбинации основывается на клинических проявлениях, объективном статусе, локализации патологического процесса, возраста пациента и сведений о дополнительных факторах риска ассоциированных с аортой осложнений. Кроме того, выбор метода определяться его наличием в медицинском, а также целесообразно учитывать опыт клиники в диагностике данных заболеваний и возможности выполнения различных визуализирующих исследований Диагностическая эффективность различных методов визуализации аорты представлена в Таблице 2. Выбор метода визуализации может зависеть от особенностей пациента, включая его гемодинамическую стабильность, наличие металлических имплантатов, сердечный ритм (тахикардия, частая экстрасистолия или фибрилляция предсердий), наличие аллергических реакций на йодсодержащие контрастные средства, функцию почек и переносимость процедуры (например, следует учитывать относительно более продолжительное время исследования и ограниченное пространство при проведении МРТ, что иногда требует седации) [40].
Таблица 2. Диагностическая эффективность различных методов визуализации аорты
Показатель |
КТА аорты |
МРА аорты |
ТТ-ЭхоКГ |
ЧП-ЭхоКГ |
УЗДГ и ДС |
|---|---|---|---|---|---|
Доступность |
+++ |
++ |
+++ |
++ |
+++ |
Транспортабельность |
- |
- |
+++ |
+++ |
+++ |
Скорость проведения исследования |
+++ |
+ |
++ |
++ |
++ |
Пространственное разрешение |
+++ |
++ |
++ |
+++ |
++ |
Временное разрешение |
+ |
++ |
+++ |
+++ |
+++ |
Трехмерный набор данных |
+++ |
++ |
+ |
+ |
+ |
Возможность оценки сосудов ветвей дуги |
+++ |
+++ |
++ |
+ |
НП |
Возможность оценки функции клапана и желудочка |
+ |
++ |
+++ |
+++ |
НП |
КТА – рентгеновская компьютерно-томографическая ангиография, МРА – магнитно-резонансная ангиография, НП – неприменимо, ЧП-ЭхоКГ – чреспищеводная эхокардиография, ТТ-ЭхоКГ – трансторакальная эхокардиография, УЗДГ и ДС – ультразвуковая допплерография и дуплексное сканирование. «+++» – отличные результаты, «++» – хорошие результаты, «+» – удовлетворительные результаты, «-» – недоступно. | |||||
Рекомендуется выполнение трансторакальной эхокардиографии (ТТ-Эхо КГ) всем пациентам с АГА и/или ТААА в качестве метода визуализации первой линии при оценке заболеваний грудной аорты [41].
ЕОК\РКО I В (УДД 4, УУР С)
Комментарии. ТТ Эхо-КГ предоставляет важную анатомическую информацию (наличие расширения, или расслоения) о восходящем отделе аорты (ВА). Вместе с тем, дистальная часть ВА и проксимальный отдел дуги аорты (слепое пятно) недоступны для визуализации из-за интерпозиции левого главного бронха. При ТТ ЭХО-КГ могут выявляться осложнения АГА (например, АН, гидроперикард), но ее диагностическая точность в случае ОАС ограничена (чувствительность: 78%–100% для расслоения типа A, 31%–55% – для типа B).
Рекомендуется у пациентов с впервые выявленным при ультразвуковом либо другом исследовании расширении любого отдела грудной аорты 40 мм и более и/или расслоением любого отдела грудной аорты выполнять КТА, либо МРА грудной и брюшной аорты [42].
ЕОК/РКО I B, АКК и ААC 1 В (УДД 4, УУР C)
Рекомендуется у пациентов с подтвержденным или предполагаемым заболеванием грудной аорты измерять ее диаметр в различных отделах по воспроизводимым анатомическим ориентирам. Каждое измерение должно выполняться на уровне воображаемой плоскости располагающейся перпендикулярно оси кровотока (аорты), а результаты измерения должны излагаться в четкой и последовательной форме. При асимметричном или овальном контуре поперечного сечения аорты следует отдельно указывать наибольший и наименьший диаметры аорты, а также протяженность расширения [42].
ЕОК/РКО I С, АКК и ААC 1 В (УДД 4, УУР C)
Комментарии. Измерения диаметра аорты следует проводить перпендикулярно оси аорты в определенных точках (Рисунок 3), а также выполнять дополнительные замеры в местах каких-либо аномалий (локальные расширения, изъязвления, гематомы). Крайними точками при измерении диаметра аорты должны быть внешние стороны ее стенки, то есть толщина стенки аорты при измерении ее диаметра должна учитываться. При выраженном утолщении аортальной стенки (5 мм и более), а также в случае наличия интрамуральной гематомы целесообразно отдельно измерять диаметр внутреннего просвета грудной аорты, толщину ее стенки, распространенность утолщения (гематомы), и отражать эти сведения в заключении [42].
Рекомендуется при проведении ТТ-ЭхоКГ пациентам с с АГА и/или ТААА измерять диаметр аорты от переднего края до переднего края, перпендикулярно оси кровотока, в конце диастолы [32,43,44].
ЕОК/РКО IIa С, АКК и ААC 2аС (УДД 5, УУР С)
Комментарии. Измерение от переднего края до переднего края при ТТ ЭХО-КГ показало хорошую корреляцию с измерениями от внутреннего края до внутреннего края на КТА и МРА. Метод измерения от внутреннего края до внутреннего края при ТТ ЭХО-КГ также показал отличное совпадение измерений, но только в исполнении опытных исследователей.
Рекомендуется, чтобы у пациентов с подтвержденным или предполагаемым поражением аорты эпизодическая и кумулятивная дозы ионизирующего облучения должны быть настолько низкими, насколько это возможно без потери качества визуализации [45].
ЕОК/РКО I С, АКК и ААC 1 С (УДД 4, УУР С)
Комментарии. Риск развития злокачественного новообразования, ассоциированный с проведением рентгеновской компьютерной томографии, остается спорным вопросом. В целом считается, что этот риск максимален в раннем возрасте, а затем значительно снижается. Внимательная оценка наличия показаний к проведению визуализирующего исследования аорты, оптимизация протокола КТА, использование альтернативных методик, например, МРА, являются действенными подходами для снижения лучевой нагрузки [45].
Рисунок 3. Особенности выполнения измерений аорты при эхокардиографии и рентгеновской компьютерно-томографической ангиографии
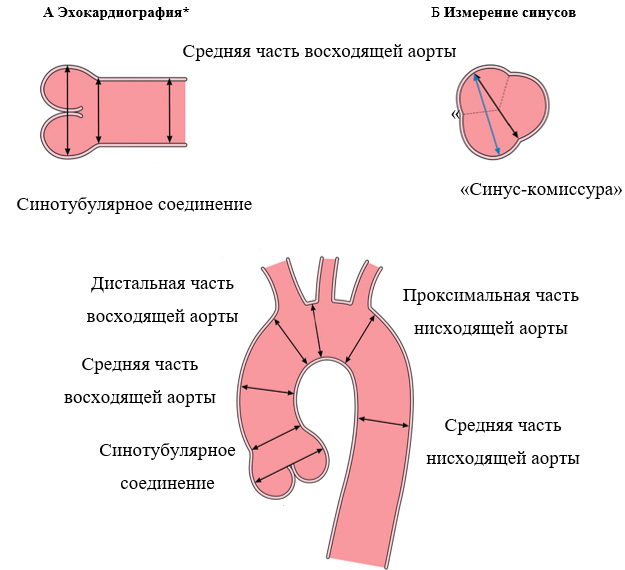
С МРА и КТА аорты†
(A) Методика измерений «между внешними краями», используемая при эхокардиографии, слева направо: измерение максимального диаметра на уровне корня аорты (синусов Вальсальвы), синотубулярного соединения и тубулярной части восходящей аорты. (Б) Измерения диаметров корня аорты «синус-комиссура» и «синус-синус» в ходе КТА или МРА. (С) Стандартные зоны измерений грудной аорты при анализе КТА или МРА. Источник: Боргер и соавторы [46], авторское право 2018 года; публикуется с согласия Elsevier, Inc. КТА –компьютерно-томографическая ангиография; МРА – магнитно-резонансная ангиография. *Между внешними краями. †Между внутренними стенками.
Рекомендуется у пациентов с подтвержденным или предполагаемым поражением грудной аорты при выполнении КТА или МРА аорты измерять диаметры на уровне синусов Вальсальвы, синотубулярного соединения и тубулярной части восходящего отдела аорты между ее внешними сторонами с использованием ЭКГ-синхронизированной методики (Таблица 3) [43].
ЕОК/РКО I С, АКК и ААC 1 С (УДД 4, УУР С)
Комментарии. Использование техники ЭКГ-синхронизации при проведении КТА уменьшает артефакты движения корня и восходящего отдела аорты [47], значительно повышая этим точность измерений и достоверность диагностики. При КТА и МРА грудной аорты диаметр корня аорты можно измерять от комиссуры до стенки противоположного синуса или от стенки одного синуса до стенки другого (Рисунок 4) [48]. Измерение от синуса до синуса и между внутренними краями на КТА грудной аорты и МРА грудной аорты продемонстрировало хорошую корреляцию с результатами эхокардиографии при измерении корня и восходящего сегмента аорты [43]. Измерение диаметра протеза аорты (например, имплантированного хирургическим путем синтетического сосудистого протеза либо стент-графта для транскатетерной изоляции патологии грудной аорты) может также включать проведение замеров между внутренними краями, что позволяет определить функциональный просвет и может быть использовано при планировании дополнительных лечебных мероприятий.
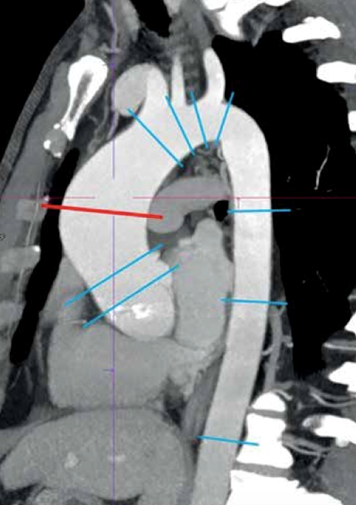
Рисунок 4. Стандартные зоны измерений диаметров грудной аорты (адаптировано из Скрипник А.Ю. и соавт., 2019 [49]).
Таблица 3. Основные составляющие заключений по результатам визуализации аорты методами КТА и МРА

КТА – рентгеновская компьютерно-томографическая ангиография; МРА– магнитно-резонансная ангиография |
|---|
Рекомендуется у пациентов с установленным или предполагаемым поражением аорты диаметр корня аорты указывать как максимальное расстояние между максимально взаимно удаленными точками синусов [50].
ЕОК/РКО I C, АКК и ААC I С (УДД 4, УУР С)
Рекомендуется для более эффективной оценки риска расслоения аорты и летального исхода у пациентов с подтвержденным или предполагаемым поражением аорты указывать не только абсолютные значения диаметров аорты, но и индексированные к росту и площади поверхности тела, а также абсолютные и индексированные значения площади поперечного сечения в зоне максимального расширения [41].
ЕОК/РКО Iia C, АКК и ААC 2А, С (УДД 4, УУР С)
Рекомендуется выполнение прицельной рентгенографии органов грудной клетки пациентам с подозрением на АГА и ТААА в рамках первичного обследования, при поступлении в стационар, а также в случае оперативного лечения при необходимости в пери- и/или послеоперационном периоде [51].
ЕОК\РКО I С (УДД 5, УУР С)
Рекомендуется выполнение КТА аорты при отсутствии противопоказаний пациентам с подозрением на АГА и/или ТААА в рамках первичного обследования, при поступлении в стационар, а также в случае оперативного лечения при необходимости в пери- и/или послеоперационном периоде для установления и подтверждения диагноза, а также для диагностики осложнений и сопутствующей патологии [51,52].
ЕОК\РКО I B (УДД 5, УУР С)
Комментарии. При необходимости КТА аорты может быть выполнена без использования рентгенконтрастных средств, содержащих йод позволит обеспечить вполне точную оценку диаметра аневризмы аорты, что может оказаться достаточным для наблюдения за состоянием тех пациентов, для которых проведение МРА аорты противопоказано или представляется невозможным по причине непереносимости. Тем не менее в некоторых случаях при КТА аорты может быть затруднена визуализация контура стенки аорты (например, на уровне корня). Использование внутривенных рентгенконтрастных йодсодержащих препаратов позволяет более четко определить границу между внутренним просветом аорты и ее стенкой, что, как правило, повышает точность диагностики пристеночных изменений. В некоторых случаях следует учитывать потенциальный риск развития аллергии на рентгенконтрастное йодсодержащее средство и его токсическое воздействие на почки. Тем не менее, согласно недавнему согласованному заявлению Американской коллегии радиологов и Американского Национального почечного фонда [53], риск развития острого почечного повреждения после внутривенного введения йодсодержащих рентгенконтрастных средств у пациентов с нарушением функции почек, вероятно, был переоценен.
Выполнение КТА всей аорты рекомендуется в качестве метода визуализации первой линии у пациентов с подозрением на острый аортальный синдром (разрыв аневризмы), поскольку он широко доступен, точен и позволяет получить информацию о разрыве, расширении и возможных осложнениях [54].
ЕОК\РКО I B (УДД 5, УУР С)
Рекомендуется выполнение МРА аорты и её ветвей «плановым» пациентам с подозрением на АГА и ТААА при отсутствии противопоказаний в рамках первичного обследования при невозможности выполнения КТА аорты, при поступлении в стационар, а также в случае оперативного лечения при необходимости в пери- и/или послеоперационном периоде для установления и подтверждения диагноза, а также диагностики осложнений и сопутствующей патологии [51,55].
ЕОК\РКО I С (УДД 5, УУР С)
Комментарии. МРА аорты обеспечивает визуализацию всей аорты и ее ветвей, позволяет охарактеризовать изменения стенок на предмет наличия воспаления и ОАС, а также предоставляет необходимую информацию для проведения физиологической оценки функции желудочков и клапанов сердца, количественной оценки скорости кровотока. При МРА не используются ионизирующее излучение и, зачастую, может не вводиться контрастный препарат. Поэтому часто именно МРА аорты является основным методом оценки врожденных аномалий аорты и хорошо подходит для проведения повторных визуализаций у молодых пациентов. Использование ЭКГ-синхронизации уменьшает выраженность артефактов движения корня аорты и наборов 3D-данных, что имеет решающее значение для получения точных и воспроизводимых результатов измерений. К ограничениям методики МРТ относятся ее пространственное разрешение (которое, хотя и является хорошим, но, как правило, все же несколько ниже, чем у КТ), а также появление артефактов на снимках пациентов, в теле которых имеется любой металлический имплант. Кроме того, доступность МРА аорты для визуализации аорты не так широка, как доступность КТА аорты. К другим недостаткам МРТ можно отнести более продолжительное время, требующееся для сбора данных, и ограниченную возможность мониторинга и лечения нестабильных пациентов в момент нахождения в томографе [56]. Поэтому МРА аорты реже используется при подозрении на острую аортальную патологию, особенно если состояние пациента оценивается как нестабильное. Для визуализации аорты доступны различные последовательности МРТ, в том числе МРА аорты, которая включает получение объемной анатомии аорты с такой толщиной среза, которая позволяет реконструировать изображения в нескольких плоскостях. При проведении МРА аорты часто используются внутривенные парамагнитные контрастные средства. В таких случаях у пациентов с сопутствующими заболеваниями почек существует некоторый риск развития контрастиндуцированного нефрогенного системного фиброза, однако этот риск может быть дополнительно снижен путем использования таких парамагнитных контрастных средств, которые относятся к группе II. Дополнительные возможности МРА аорты часто используются для визуализации анатомии аорты в тех ситуациях, когда внутривенное введение контрастного средства не требуется: например, кино-МРТ в последовательности градиентного эха (с артериальной кровью) и спин-эхо-последовательность (с венозной кровью).
Рекомендуется применять ЧП-ЭхоКГ во время всех «открытых» хирургических операций на восходящем отделе и дуге аорты у пациентов АГА и/или ТААА [57].
ЕОК\РКО I В, ЕАКТХ I, B (УДД 4, УУР C)
Комментарии. Относительная близость пищевода и дуги аорты позволяет получать изображения с высоким разрешением с помощью ЧП-ЭхоКГ. ЧП-ЭхоКГ интраоперационная превосходит ТТ-ЭхоКГ по уровню визуализации грудной аорты и играет важную роль в условиях, когда КТА аорты или МРА аорты может быть недоступна или невозможна, например, в отделении интенсивной терапии или операционной. ЧП-ЭхоКГ является полуинвазивным методом и требует седации, строгого контроля артериального давления, а также исключения заболеваний пищевода. Вследствие интерпозиции правого главного бронха и трахеи короткий сегмент дистального отдела восходящей аорты, как раз перед брахиоцефальным стволом, остается невидимым («слепое пятно»). Интраоперационная ЧП-ЭхоКГ также весьма эффективна для детализированной оценки строения и функции аортального клапана, а также для контроля нисходящего отдела грудной аорты при проведении гибридных вмешательств.
Рекомендуется использовать ЧП-ЭхоКГ у пациентов с АГА и/или ТААА в качестве альтернативы при нестабильной гемодинамике, невозможности транспортировки пациента, неясных результатах МРА аорты или КТА аорты [57].
ЕОК\РКО Iia B, ЕАКТХ Iia, B (УДД 4, УУР C)
Комментарии. Особенно часто ЧП-ЭхоКГ используется при интраоперационной оценке пациентов с ОАС для определения открытой хирургической и эндоваскулярной тактики, а также для оценки состояния истинного и ложного каналов аорты – как до, так и сразу после выполнения реконструкции [58].
Пациентам с подозрением на ОАС (разрыв аневризмы) рекомендуется проводить ЧП-ЭхоКГ для определения тактики ведения, оперативного вмешательства и выявления осложнений [54].
ЕОК\РКО I B (УДД 5, УУР С)
Рекомендуется в семье с диагностированными случаями аневризм корня и (или) ВА или расслоения аорты, если патологическая мутация не выявлена по данным генетических тестов, выполнение скринингового обследования биологических родственников из группы риска при помощи методик визуализации аорты [59].
ЕОК\РКО I B, АКК и ААC I В (УДД 4, УУР С)
Комментарии. Считается, что у пациентов, с характерными анамнезом (например, неоднократные случаи заболеваний грудной аорты в семейном анамнезе или спорадические заболевания грудной аорты с ранним началом в отсутствие факторов риска), несмотря на отсутствие патогенного варианта гена, нельзя исключить НЗГА так как возможно патологические генетические варианты у них присутствующие, еще не известны. В нескольких исследованиях была подтверждена польза скрининга (ТТ-ЭхоКГ) среди родственников (из группы риска) всех пациентов с заболеваниями грудной аорты с положительным семейным анамнезом [59]. При отрицательном результате рекомендуется выполнение повторной ТТ-ЭхоКГ спустя 5 лет у молодых членов семьи или через 10 лет у старших членов семьи.
Рекомендуется у пациентов с аневризмами корня и (или) ВА или расслоения аорты при отсутствии подтвержденного семейного анамнеза ЗГА или патогенных/вероятно патогенных мутаций выполнение скринингового обследования родственников первой степени родства при помощи визуализации аорты [59].
ЕОК\РКО I C, АКК и ААC I С (УДД 4, УУР С)
Комментарии. Исследования также свидетельствуют в пользу скрининга родственников первой степени родства среди пациентов с заболеваниями грудной аорты, у которых в семейном анамнезе нет указаний на подобные заболевания, хотя данные по этому вопросу более ограничены [59]. При отрицательных результатах скрининга визуализацию аорты можно повторить спустя несколько лет (в зависимости от возраста родственника и размеров аорты). Необходимо понимать, что не существует верхнего возрастного предела, при котором у пациентов могут развиваться заболевания грудной аорты и одновременно можно исключить генетическую этиологию заболевания.
Рекомендуется всем пациентам с ДАК выполнение визуализации корня и ВА на предмет наличия признаков ее расширения [60].
ЕОК\РКО I B, ЕАКТХ I, В (УДД 5, УРР C)
Комментарии. ДАК встречается в общей популяции в 1-2% случаев. До 50% пациентов с ДАК имеют ассоциированную аортопатию с вовлечением корня и тубулярной части ВА [60]. Рекомендуется скрининг родственников первой линии с помощью ТТ-ЭхоКГ для определения наличия ДАК и/или расширения восходящей аорты. КТ ангиография аорты или МРА аорты могут быть показаны для полной визуализации восходящей аорты и дуги. Может быть полезна ТТ-ЭхоКГ родственников в юном возрасте.
У пациентов с ДАК и расширением корня или ВА рекомендуется обследование всех родственников первой линии с помощью ТТ-ЭхоКГ для оценки наличия ДАК, расширения корня аорты и восходящей аорты или и того, и другого [61].
ЕОК\РКО I C, АКК и ААC I С (УДД 4, УУР С)
Комментарии. И ДАК, и расширение корня и восходящего отдела аорты могут быть семейными [61], и модели наследования семейных ДАК и аортопатии согласуются с аутосомно-доминантным паттерном с неполным проникновением. В семьях с ДАК и расширением корня и восходящего отдела аорты облигатные носители могут иметь и ДАК, и расширение аорты либо ни то, ни другое [61]. В семьях с ДАК и расширением корня и восходящего отдела аорты скрининг родственников первой степени (родителей, братьев и сестер и детей) с помощью ТТ-ЭхоКГ для оценки наличия ДАК и расширения аорты выявляет пораженных членов семьи. Если у члена семьи обнаруживается ДАК, расширение аорты или и то, и другое, показано каскадное обследование других родственных членов семьи. Поскольку в семьях с ДАК и расширением аорты могут быть члены семьи с расширением корня и восходящего отдела аорты при отсутствии ДАК, при недостаточной оценке восходящего отдела аорты с помощью ТТ-ЭхоКГ для полной оценки размера восходящей аорты следует выполнить КТА грудной аорты или МРА грудной аорты.
Рекомендуется пожизненное наблюдение за корнем и восходящим отделом аорты с помощью ТТ-ЭхоКГ, КТА грудной аорты или МРА грудной аорты с интервалом, зависящим от диаметра аорты и скорости ее роста у пациентов с ДАК и диаметром корня аорты и/или восходящего отдела аорты более 4,0 см [62].
ЕОК\РКО I C, АКК и ААC I С (УДД 4, УУР С)
Комментарии. В проспективном исследовании у 90 взрослых с ДАК среднее увеличение диаметра восходящей аорты составило 0,47 мм/г (диапазон 0,2–2,3 мм/г) за 4,8 года наблюдения [63]. ТТ-ЭхоКГ может документировать текущие диаметры аорты и позволяет рассчитать темпы ее роста. Среди когорты взрослых пациентов с ДАК (средний возраст – 55±17 лет) без АГА в исходе (т.е. исходный диаметр аорты составлял <4,5 см) у 13% через 14±6 лет после постановки диагноза развилась АГА, а 25-летний риск развития АГА составил 26% [64]. У многих взрослых корень аорты, восходящий отдел аорты или и то, и другое диаметром ≥4,0 см считаются расширенными, и поэтому с течением времени их следует контролировать с помощью обзорной визуализации для выявления прогрессирующего расширения.
Рекомендуется выполнять коронарографию (Ангиография коронарных артерий) всем пациентам с АГА и ТААА для выявления гемодинамически значимых стенозов коронарных артерий перед «открытым» хирургическим, эндоваскулярным или гибридным вмешательством в следующих ситуациях: возраст старше 40 лет, анамнез и/или симптомы ИБС, признаки ишемии миокарда, снижение ФВ ЛЖ <50%, один и более факторов риска ИБС и/или постлучевое поражения [28].
ЕОК\РКО I C (УДД 5, УРР С)
Комментарии. Инвазивное определение давлений в полостях сердца, измерение параметров центральной гемодинамики, оценка степени нарушений кровотока на клапанах и функции ЛЖ требуется в случаях недостаточно информативных неинвазивных исследований либо расхождения результатов последних с клиническими данными. Учитывая риск возможных осложнений, рутинное выполнение инвазивной манометрии одномоментно с коронарографией не рекомендуется. В связи с невысокой диагностической ценностью панаортографии в диагностике патологии грудной аорты не рекомендуется её выполнение при возможности выполнения КТА аорты или МРА аорты.
Рекомендуется рассмотреть возможность выполнения компьютерной томографической ангиографии коронарных артерий с ЭКГ синхронизацией в качестве альтернативы коронарографии у пациентов с планируемым лечением заболеваний на грудной аорте и невысокой вероятностью ИБС с целью выявления гемодинамически значимых стенозов, врожденных коронарных аномалий, а также уточнения анатомических особенностей коронарного русла [28].
ЕОК\РКО Iia C (УДД 5, УРР С)
Комментарии. У молодых пациентов с АГА, которым выполнялась КТА грудной аорты, целесообразна одномоментная оценка анатомии коронарных артерий, наличия кальциноза и признаков стенозирования. У пациентов моложе 40 лет без факторов риска ИБС с планируемым вмешательством на грудной аорте целесообразно визуализировать анатомию коронарного русла при коронарографии.
Рекомендуется использовать внутрисосудистое ультразвуковое исследование сосудистой стенки у пациентов с АГА и/или ТААА в качестве альтернативы при выполнении эндоваскулярного лечения для дополнительной диагностики, в качестве навигации, для уменьшения объема используемого контрастного средства, при неясных результатах МРА аорты или КТА аорты [57].
ЕОК\РКО I C (УДД 4, УУР C)
Комментарии. Внутрисосудистое ультразвуковое исследование сосудистой стенки при проведении эндоваскулярного лечения сложных патологий грудной и брюшной аорты, позволяет уточнить размер аорты, ее извитость, наличие бляшек, наличие кальцинатов, оценить устья ветвей аорты и дефекты внутрисосудистого наполнения (например, при тромбах и расслоении интимы), а также исследовать зону имплантации эндоваскулярного стент-графта для нисходящего отдела грудной аорты. Также помогает выявить пациентов, для которых эндоваскулярное лечение связано с высоким риском осложнений и/или противопоказано. Кроме того, может быть полезным при расслоении аорты, для оценки анатомии истинного и ложного каналов и тем самым позволяет сделать выбор между эндоваскулярным или открытым хирургическим лечением. Внутрисосудистое ультразвуковое исследование сосудистой стенки может использоваться для навигации во время раскрытия любых стент-графтов эндоваскулярных (для нисходящего отдела грудной аорты, абдоминальных и т.д.) и, во время окончательной оценки, для уменьшения объема, используемого рентгенконтрастного средства, содержащего йод [65].
Общие положения
Консервативное лечение аневризм грудного отдела аорты направлено на предотвращение увеличения диаметра аневризмы, развития осложнений, таких как разрыв или диссекция, отсрочки хирургического вмешательства, а также на контроль факторов риска, способствующих прогрессированию заболевания, снижение сердечно-сосудистой заболеваемости и смертности.
Немедикаментозная терапия включает модификацию образа жизни, отказ от курения и ограничение физической активности.
Медикаментозная терапия играет ключевую роль в снижении артериального давления и замедлении роста аневризмы при регулярном мониторинге размеров аневризмы с использованием современных методов визуализации, таких как МРА или КТА.
Хирургическое и эндоваскулярные методы лечения применяются в зависимости от размеров и локализации аневризмы, скорости её роста, симптоматики и наличия острых осложнений.
Важным аспектом лечения АГА является мультидисциплинарный подход, который учитывает генетические факторы, сопутствующие заболевания и индивидуальные риски пациента (Приложение А3).
3.1 Консервативное лечение
Рекомендуется пациентам с АГА и ТААА избегать интенсивных изометрических нагрузок (занятий тяжелой атлетикой или требующих маневра Вальсальвы), подъема тяжестей и занятий контактными видами спорта [32].
ЕОК\РКО I C, АКК и ААC I С (УДД 5, УУР C)
Комментарии. Маневр Вальсальвы может вызвать резкое повышение САД до >300 мм рт. Ст. Кроме того, показано, что высокоинтенсивные спортивные тренировки являются независимым предиктором роста корня аорты [66].
При целевом уровне АД пациентам с АГА и ТААА, рекомендуется выполнять 30–60 минут аэробной активности легкой или средней интенсивности не реже 3–4 дней в неделю [32].
ЕОК\РКО Iia C, АКК и ААC Iia С (УДД 5, УУР С)
Комментарии. Имеется консенсусное мнение экспертов, что легкая атлетика и аэробные упражнения низкой интенсивности безопасны и, вероятно, улучшают как физическое, так и психическое здоровье пациентов с АГА. Не существует единого консенсуса относительно безопасности статических и аэробных упражнений среднего уровня. Рекомендации по интенсивности упражнений лучше всего индивидуализировать, основываясь на нескольких факторах, которые включают в себя основную патологию аорты, диаметр аорты и, скорость роста аорты, возраст, семейный анамнез и любые другие признаки высокого риска (например, неконтролируемая гипертония) [32].
Рекомендуется пациентам с АГА и ТААА отказ от курения с целью снижения риска расслоения аорты, инфаркта миокарда и летального исхода [32,44].
ЕОК\РКО I C, АКК и ААC I С (УДД 5, УУР C)
Комментарии. Курение является фактором риска расширения АГА, а среди лиц с атеросклеротическим заболеванием аорты отказ от курения снижает показатели инфаркта миокарда и смерти [67,68]. Использование электронных сигарет, хотя и является эффективным средством отказа от курения, не было доказано как безопасное при использовании у пациентов с сосудистыми заболеваниями, включая АГА; кроме того, небольшие исследования показали, что ароматизирующие химические вещества в электронных сигаретах могут оказывать неблагоприятное воздействие на функцию эндотелия сосудов [69,70].
Пациентам с АГА и ТААА и средним систолическим АД (САД) ≥130 мм рт. Ст. или средним диастолическим АД (ДАД) ≥80 мм рт. Ст. рекомендуется назначать антигипертензивные препараты для снижения риска сердечно-сосудистых осложнений, согласно рекомендациям по артериальной гипертензии 2024 года [71,72].
ЕОК\РКО I В, АКК и ААC I В (УДД 5, УУР C)
Комментарии. Ни в одном рандомизированном клиническом исследовании не оценивался оптимальный порог, до которого следует снижать АД у пациентов с АГА для уменьшения риска осложнений со стороны аорты (рост аорты, расслоение аорты или разрыв аорты). Обновленные рекомендации AКК и AАС по артериальной гипертензии предполагают, что все пациенты с клиническими сердечно-сосудистыми заболеваниями должны иметь целевое САД <130 мм рт. Ст. или ДАД <80 мм рт. Ст., или и то, и другое [71]. Фактические данные подтверждают агрессивное снижение АД для уменьшения побочных эффектов, связанных с сосудами, и смертности от всех причин.
Рекомендуется назначение бета-адреноблокаторов у пациентов с АГА и ТААА для достижения целевых показателей АД при отсутствии противопоказаний и независимо от этиологии аневризмы [71].
ЕОК\РКО Iia C, АКК и ААC Iiа С (УДД 5, УУР C)
Комментарии. Проспективные данные о положительном эффекте бета-адреноблокаторов при АГА в зависимости от причины ограничены, при этом наиболее достоверные доказательные данные получены из когортных исследований пациентов с синдромом Марфана [65]. В небольшом открытом рандомизированном клиническом исследовании профилактического пропранолола** (средняя доза: 212±68 мг/сут) по сравнению с плацебо у подростков и взрослых с синдромом Марфана бета-адреноблокаторы замедляли рост корня аорты и уменьшали аортальные осложнения [73]. В исследовании 155 детей в возрасте <12 лет с синдромом Марфана при многофакторном анализе бета-адреноблокаторы снижали скорость роста корня аорты на 0,16 мм/год [74].
У пациентов с АГА и ТААА для достижения целевых показателей АД рекомендуется в качестве комбинированной терапии в дополнении к бета-адреноблокаторам назначать блокаторы ангиотензиновых рецепторов (БАР, АТХ: Антагонисты рецепторов ангиотензина II), при отсутствии противопоказаний и независимо от этиологии аневризмы [75].
ЕОК\РКО Iia C, АКК и ААC Iiа С (УДД 1, УУР A)
Комментарии. Метаанализ 1510 рандомизированных пациентов, оценивающий влияние БАР на заболевания грудной аорты, ассоциированное с синдромом Марфана, продемонстрировал более медленный рост корня аорты при использовании БАР (АТХ: Антагонисты рецепторов ангиотензина II) по сравнению с плацебо; при прямом сравнении с терапией бета-адреноблокаторами не было различий в росте аорты; и комбинация бета-адреноблокаторов + БАР (АТХ: Антагонисты рецепторов ангиотензина II) приводила к более медленному росту аорты, чем применение только бета-адреноблокаторов [75].
Рекомендуется назначение ингибиторов ГМГ-КоА-редуктазы пациентам с АГА и ТААА при наличии атеросклероза по данным визуализации или клинических признаков [76].
ЕОК\РКО Iia C, АКК и ААC Iiа С (УДД 5, УУР С)
Комментарии. Аневризмы аорты атеросклеротического генеза повышают риск инсульта и инфаркта миокарда, поэтому в соответствии с заключением третьей группы экспертов по лечению взрослых в США в рамках Национальной образовательной программы по холестерину (NCEP ATP III) они считаются эквивалентом ишемической болезни сердца с риском развития события >20% в течение 10 лет [77]. В «Руководстве AHA и ACC 2016 года по ведению пациентов с заболеваниями периферических артерий нижних конечностей» [78] дана рекомендация с уровнем доказательности 2a по применению ингибиторов ГМГ-КоА-редуктазы высокой интенсивности для достижения целевого уровня ЛПНП <70 мг/дл у пациентов с некоронарным атеросклеротическим заболеванием. По результатам совместной работы специалистов по лечению заболеваний, связанных с холестерином, при объединении данных 5 (рандомизированных клинических исследований (РКИ) с участием 39 612 пациентов на протяжении 5,1 лет, более интенсивное снижение уровня холестерина у пациентов с атеросклерозом привело к уменьшению основных сердечно-сосудистых событий еще на 15% по сравнению с тем, что было достигнуто при менее интенсивном снижении уровня холестерина[76]. Терапия ингибиторами ГМГ-КоА-редуктазы все еще является разумной при наличии сопутствующего атеросклеротического поражения у пациентов со спорадическими или генетически опосредованными аневризмами.
Рекомендуется рассмотреть возможность терапии ингибиторами ГМГ-КоА-редуктазы у пациентов с АГА и ТААА без признаков атеросклероза [79].
ЕОК\РКО Iib C, АКК и ААC Iib С (УДД 4, УУР С)
Комментарии. Долгое время выдвигалась гипотеза о том, что плейотропные эффекты ингибиторов ГМГ-КоА-редуктазы могут быть полезными для предотвращения неблагоприятного ремоделирования сосудистой стенки, связанного с АГА, тем самым замедляя рост, независимо от причины и наличия сопутствующего атеросклероза. Исследования на животных показали уменьшение роста аневризмы грудной клетки при терапии ингибиторами ГМГ-КоА-редуктазы, возможно, за счет регуляции активности матриксных металлопротеиназ. Исследование, в котором приняли участие 1348 пациентов с эктазией грудной аорты, в соответствии с анализом склонности продемонстрировало возможную пользу терапии ингибиторами ГМГ-КоА-редуктазы в снижении скорости роста аорты, а также аортальных осложнений [80]. В ретроспективном исследовании, включавшем 2267 пациентов, перенесших ЭВПГА по поводу аневризматической болезни, 1148 (64%) из которых получали ингибиторы ГМГ-КоА-редуктазы до операции, предоперационная терапия ингибиторами ГМГ-КоА-редуктазы была связана со значительно более низкими показателями периоперационных осложнений и 5-летней летальностью [81]. Возможная польза ингибиторов ГМГ-КоА-редуктазы в предотвращении неблагоприятных исходов, связанных с аортой, также была продемонстрирована в небольшом когортном исследовании, а в 2-х небольших исследованиях у пациентов с ДАК и аортопатией предполагается замедление роста аорты [79].
Рекомендуется пациентам с атеросклеротическим генезом АГА или ТААА и наличием атероматоза аорты или пенетрирующих атеросклеротических язв назначение низких доз ацетилсалициловой кислоты** при отсутствии противопоказаний [51].
ЕОК\РКО Iiа C, АКК и ААC Iia С (УДД 5, УУР С)
Комментарии. В исследовании SPARC (профилактика инсульта: оценка риска среди населения) атеросклероз аорты был взаимосвязан с ишемической болезнью сердца (ОШ – 2,99; 95%-й ДИ – 1,47–6,10; p=0,003)[82]. В свою очередь, при наличии ишемической болезни сердца ацетилсалициловая кислота** уже давно рекомендуется для снижения риска сердечно-сосудистых событий, включая инсульт, смерть, вызванную ишемической болезнью сердца, и инфаркт миокарда [51].
Пациентам с ОАС (разрывом аневризмы), для достижения целевых уровней АД имеющих противопоказания к назначению бета-адреноблокаторов, рекомендуется назначение недигидропиридиновых кальциевых блокаторов [83,84].
EОК\РКО Iia В (УДД 4, УУР С)
3.2 Хирургическое лечение аневризм восходящего отдела и корня аорты [85–87]
Желательно, чтобы плановое вмешательство при аневризмах корня и ВА выполнялось, когда риск нежелательных явлений – расслоения, разрыва или внезапной смерти перевешивает риски хирургического вмешательства. Ни в одном проспективном многоцентровом наблюдательном исследовании не оценивалось множество параметров (например, диаметр, длина или площадь аорты, изолированно или с индексацией к росту или площади поверхности тела, напряжению стенки, напряжению сдвига), предложенных для прогнозирования риска нежелательных аортальных событий. С чисто механической точки зрения расслоение или разрыв аорты можно рассматривать как событие, когда существует дисбаланс между нагрузками на стенку аневризмы и внутренней прочностью ее ткани. Вопрос о том, вызвано ли расслоение аорты повышенным напряжением стенки или снижением прочности стенки, или сочетанием того и другого, является областью активных исследований[88]. Максимальный диаметр аорты логично был основным критерием для планового лечения аневризмы, поскольку, согласно закону Лапласа, напряжение стенки увеличивается пропорционально радиусу аорты и обратно пропорционально толщине. Первоначальные исследования естественной динамики изучали риск разрыва или расслоения аорты в зависимости от ее диаметра, и точка отсчета для расслоения определила порог в 5,5 см, длительное время регулировавший клиническую практику. Хотя у значительной части пациентов с расслоением аорты типа А по Stanford диаметр составляет <5,5 см, этот хирургический порог по-прежнему эффективно снижает нежелательные явления [89].
Участниками рабочей группы было принято решение ввести понятия экспертных центров и экспертов по каждой проблеме, что возможно будет значимо влиять на результаты диагностики, открытого хирургического и рентгенхирургического лечения и периоперационного ведения пациентов с тяжелой патологией аорты.
Значение аортальной команды сложно переоценить, и в настоящее время во всех клинических рекомендациях активно обсуждается необходимость наличия таковой для качественного и оптимального способа оказания медицинской помощи пациентам [32,34]. Также, по нашему мнению, наличие специалистов открытого хирургического лечения вместе с эндоваскулярными методами лечения патологии аорты в одной клинике – это необходимое условие для экспертного центра.
Решением ведущих специалистов РФ по патологии аорты принято считать экспертными центрами клиники, имеющие опыт ежегодного открытого хирургического лечения каждой конкретной патологии, которая будет рассматриваться ниже. По открытому хирургическому лечению патологии ВА и дуги – не менее 50 вмешательств на ВА и 20 вмешательств на дуге аорты. По нисходящей грудной и торакоабдоминальной патологии – не менее 15 случаев открытых реконструкций АГА и ТААА в год по каждой группе. Что касается эндоваскулярной хирургии – ведущие специалисты не считают необходимым связывать опыт клиники с экспертностью её, ввиду активного участия приглашенных экспертов для развития эндоваскулярных методик повсеместно.
С учетом опыта и экспертностью центров, возможен более агрессивный подход к показаниям для открытого и эндоваскулярного методов лечения пациентов с аневризмой и расслоением аорты. Предлагаются следующие значения диаметров для вмешательства при бессимптомных аневризмах грудной аорты (Таблица 4):
Таблица 4. Рекомендуемые пороговые значения размера для вмешательства при бессимптомных аневризмах грудной аорты *
Этиология |
Корень аорты, см |
Восходящая аорта, см |
Дуга аорты, см |
Нисходящая и ТАА аорта, см |
|---|---|---|---|---|
Дегенеративные 1 |
5,5 (5) |
5,5 (5) |
5,5 |
НГА – 5,5 ТААА – 6 (5,5) |
Двустворчатый аортальный клапан 1 |
5,5 (5) |
5,5 (5) |
5,5 |
НГА – 5,5 ТААА – 6 (5,5) |
Генетические синдромы 1,2 |
5 (4,5) |
5 (4,5) |
5(4,5) |
5 (4,5) |
Семейная аортопатия1,3 |
4 – 4,5 |
4 – 4,5 |
5,5 |
НГА – 5,5 ТААА – 6 (5,5) |
Планирующиеся на кардиохирургическое вмешательство 1 |
5 (4,5) |
5 (4,5) |
5,5 |
НГА – 5,5 ТААА – 6 (5,5) |
Особенности выбора показаний к хирургическому вмешательству см. в соответствующих разделах рекомендаций
() – пороговые значения для экспертных центров
* Пороговые значения размера для вмешательства должны учитывать размер тела пациента эмпирически или с использованием предложенных формул; также имеет значение истончение стенки аорты, соотношение диаметров восходящей и нисходящей аорты, тип строения корня и восходящего отдела аорты, наличия аортальной недостаточности
1 – Для молодых пациентов, дисплазии соединительной ткани и в экспертных центрах – возможна более агрессивная тактика
2 – В зависимости от верифицированной генетической патологии
3 – Для женщин, ожидающих беременности, порог составляет 4,1-4,5 см.
Рекомендуется пациентам с аневризмами корня и ВА, у которых имеются симптомы, связанные с аневризмой, выполнять протезирование данного отдела аорты [90].
ЕОК\РКО I C, АКК и ААC I С (УДД 4, УУР С)
Комментарии. Крупные аневризмы по мере их роста могут сдавливать близлежащие структуры, что приводит к болевому синдрому в груди или спине. С другой стороны, боль иногда связана с быстрым ростом аорты. Следовательно, появление таких симптомов вызывает беспокойство по поводу повышенного риска разрыва аневризмы [90], и, следовательно, показано хирургическое вмешательство.
Рекомендуется выполнять протезирование аорты бессимптомным пациентам с аневризмами корня и/или ВА при максимальном диаметре аорты ≥5,5 см [91].
ЕОК\РКО I B, АКК и ААC I B (УДД 5, УУР С)
Комментарии. Максимальный диаметр аорты ≥5,5 см был главным критерием для планового хирургического лечения аневризм корня аорты или восходящего отдела грудной аорты [26,92] на основании исследований естественного течения аневризм грудной аорты, в которых изучались диаметр на момент неблагоприятного события и периоперационная смертность <5% [26,91]. Уровень смертности при плановом хирургическом вмешательстве на ВА низкий, в то время как риск осложнений, ассоциированных с аортой, является высоким, когда такая операция рекомендована, но не выполняется из-за нарушения пациентом предписанного режима терапии или сопутствующих заболеваний. В отсутствие дополнительных факторов риска применяется одно и то же пороговое значение диаметра аорты 5,5 см независимо от наличия трехстворчатого или двустворчатого АК [93].
Рекомендуется хирургическое вмешательство на корне и/или ВА в случае пациентов с аневризмой корня и/или ВА диаметром <5,5 см, скорость роста которой, подтвержденная данными КТА, составляет ≥0,3 см/год в течение двух последовательных лет или ≥0,5 см в течение 1 года [44].
ЕОК\РКО I C, АКК и ААC I С (УДД 5, УУР С)
Комментарии. Один метаанализ и ограниченные наблюдательные исследования показали, что рост аневризмы ВА происходит медленнее, чем сообщалось ранее, и эта скорость часто меньше 0,5 мм/год у пациентов с трехстворчатым АК и без генетически обусловленного заболевания аорты [94]. Также этот мета-анализ продемонстрировал, что быстрый рост аневризмы связан с повышенным риском разрыва [95]. Из-за присущей измерениям погрешности, а также вариабельности результатов у разных исследователей было бы трудно последовательно документировать рост от 1 мм до 2 мм в год по данным визуализации в динамике. Расхождения в измерениях могут возникать при сравнении различных методов визуализации или даже при использовании одного и того же метода при сравнении изображений, полученных с контрастным средством и без него. Как правило, темпы роста наиболее точны при оценке с помощью МРА аорты или КТА аорты с ЭКГ-синхронизацией с использованием методов измерения осевой линии [96]. Подтвержденный рост ≥0,5 см в год был и остается показанием к хирургическому вмешательству [26,97]. Более того, рост даже на 0,3 см в год все еще существенно превышает ожидаемые темпы роста аневризм корня и ВА, поэтому если такие темпы роста сохраняются в течение двух лет подряд, также рекомендуется протезирование аорты [44].
Рекомендуется хирургическое вмешательство на корне и/или ВА в случае асимптомных пациентов с аневризмами корня и/или ВА максимальным диаметром ≥5,0 см при выполнении опытными хирургами в экспертном аортальном центре (см. Таблицу 4) [98,99].
ЕОК\РКО I B, АКК и ААC I B (УДД 4, УУР С)
Комментарии. Риск расслоения или разрыва аорты коррелирует с увеличением диаметра аневризмы [89], как и скорость роста аорты [95]. Таким образом, можно ожидать, что аневризмы размером ≥5,0 см будут иметь больший риск осложнений или быстрого роста, чем аневризмы меньшего размера. Действительно, в отчете Паручури и соавт. [100] при диаметре аорты от 4,0 см до 4,4 см риск расслоения аорты повышался в 89 раз по сравнению с контрольным диаметром аорты ≤3,4 см, а при диаметре аорты ≥4,5 см риск ее разрыва возрастал в 6300 раз. Следовательно, многие опытные хирурги в экспертном аортальном центре предпочитают оперировать пациентов при диаметре ВА от 5,0 см до 5,4 см выборочно [101] при условии, что хирургический риск пациента низок [102], и при этом демонстрируются отличные результаты [103]. Однако в настоящее время проводится проспективное многоцентровое РКИ пациентов с аневризмами восходящего отдела грудной аорты 5,0–5,4 см, где сравниваются результаты ранней плановой операции и продленного наблюдения [104], результаты которого могут подкрепить последующие рекомендации.
Рекомендуется хирургическое вмешательство на корне и/или ВА пациентам с расширением корня и/или ВА максимальным диаметром ≥4,5 см, которым планируется выполнение пластики или протезирования трехстворчатого АК, при выполнении его опытными хирургами в экспертном аортальном центре (см. Таблицу 4) [99,105].
ЕОК\РКО Iia B, АКК и ААC Iia B (УДД 4, УУР C)
Рекомендуется хирургическое вмешательство на корне и/или ВА пациентам с аневризмой корня и/или ВА максимальным диаметром ≥5,0 см, которым планируется пластика или протезирование трехстворчатого АК [99,105].
ЕОК\РКО Iia B, АКК и ААC Iia B (УДД 4, УУР С)
Рекомендуется хирургическое вмешательство на корне и/или ВА пациентам с аневризмой корня и/или ВА максимальным диаметром ≥5,0 см, которым планируется выполнение кардиохирургического вмешательства по показаниям, отличным от пластики или протезирования АК [99,105].
ЕОК\РКО Iia B, АКК и ААC Iia B (УДД 4, УУР C)
Комментарии. Ранее в рекомендациях для пациентов с ДАК, перенесших протезирование или пластику АК в условиях искусственного кровообращения с сопутствующим расширением ВА максимальным диаметром ≥4,5 см, рекомендовалось одновременное протезирование ВА. С другой стороны, у пациентов, перенесших операцию на АК без одномоментного вмешательства на ВА (будь то для двустворчатого или трехстворчатого АК) было показано, что ассоциированные расширения ВА аневризмы прогрессируют медленно и характеризуются низкой частотой аортальных осложнений. Тем не менее, в ряде исследований также демонстрируется безопасность одновременного протезирования ВА при ее диаметре ≥4,5 см в случае выполнения опытными хирургами, работающими в экспертном аортальном центре [99,105]. Тем не менее, до тех пор, пока не появятся достоверные предикторы «аортальных» осложнений, в большинстве случаев пациентам, которым планируется выполнение пластики или протезирования АК при расширении ВА ≥5,0 см из-за более быстрой скорости роста и более высокого риска расслоения аорты, целесообразно рассматриваться одновременную операцию на ВА. Протезирование корня аорты должно планироваться индивидуально в зависимости от типа операции на АК (т.е. пластика АК с сохранением корня или без него в сравнении с протезированием клапана, реконструкция ВА с протезированием АК механическим или биологическим протезом), статуса пациента, его возраста и сопутствующих заболеваний. У пациентов, которым планируется кардиохирургическое вмешательство по показаниям, отличным вмешательства на АК, одновременное профилактическое протезирование ВА при ее диаметрее 5,0 см может быть целесообразным [26].
Рекомендуется пациентам с синдромом Марфана и расширением корня и/или ВА ≥5,0 см протезирование корня и/или ВА [26,44].
ЕОК\РКО I B, АКК и ААC I B (УДД 5, УУР С)
Комментарии. У пациентов с синдромом Марфана и дилатацией корня аорты плановое протезирование ВА улучшает выживаемость. В знаковом исследовании 1995 г. было отмечено существенное увеличение продолжительности жизни среди пациентов с синдромом Марфана, которым было выполнено плановое протезирование ВА, по сравнению с контрольной группой пациентов, находившихся под наблюдением в предыдущие эпохи [106]. Хотя риск расслоения аорты у пациентов с синдромом Марфана, получающих необходимую медицинскую помощь и соответствующим образом модифицирующих свой образ жизни, относительно невысок, он повышается при расширении ВА >5,0 см [106]. При профилактическом протезировании аорты коррекции подвергается как корень, так и тубулярный отдел. Некоторые клиники выступают за одномоментное проведение реконструкции дуги аорты по типу hemiarch во время планового протезирования корня или тубулярной части ВА, однако убедительные данные в поддержку этого подхода отсутствуют.
В отношении пациентов с синдромом Марфана, расширением корня и/или восходящего отдела аорты ≥4,5 см и признаками, ассоциированными с повышенным риском расслоения аорты (Таблица 5), резекция с протезированием корня и/или ВА аорты рекомендуется в том случае, если она выполняется опытными хирургами в экспертном центре [26,106,107].
ЕОК\РКО Iia B, АКК и ААC Iia B (УДД 4, УУР С)
Таблица 5. Факторы повышенного риска осложнений со стороны аорты у пациентов с синдромом Марфана
|
■ Семейный анамнез расслоения аорты ■ Быстрый рост диаметра аорты (≥0,3 см/год) ■ Диффузное расширение корня и восходящего отдела аорты [108] ■ Выраженная извитость позвоночных артерий [109] |
|---|
Комментарии. В одном исследовании, проводившемся на большой когорте пациентов с синдромом Марфана, около 20% перенесли плановую операцию при диаметре корня аорты <5,0 см [106,107,110]. Предикторы расслоения аорты и других неблагоприятных исходов со стороны аорты у пациентов с синдромом Марфана перечислены в таблице 7. Показаниями для более раннего вмешательства на ВА могут быть быстрый рост аорты (≥0,3 см/год), случаи расслоения аорты в семейном анамнезе, планирование беременности, тяжелая клапанная недостаточность, а также личные предпочтения пациента [44,107,111]. У большинства пациентов с синдромом Марфана темпы роста аорты относительно низки, однако скорость роста увеличивается вместе с размером аорты.
Для пациентов с синдромом Марфана, у которых отношение максимальной площади поперечного сечения корня и/или ВА (см2) к росту (м) ≥10, протезирование корня и/или ВА рекомендуется в том случае, если она выполняется опытными хирургами в экспертном аортальном центре [93,106].
ЕОК\РКО Iia C, АКК и ААC Iia C (УДД 5, УУР С)
Комментарии. Диаметр аорты может колебаться в зависимости от возраста, пола, роста и размера тела. Частота ассоциированных с аортой осложнений, включая ее расслоение, растет по мере увеличения диаметра аорты, индексированного по росту или площади поверхности тела. Когда максимальная площадь поперечного сечения корня или восходящей части аорты в квадрате (см2), разделенная на рост пациента (м), составляет ≥10 см2/м, целесообразно выполнение профилактического протезирования корня аорты. В исследовании, где этот параметр использовался для принятия решений о проведении профилактических оперативных вмешательств, были продемонстрированы хорошие результаты.
У пациентов с синдромом Марфана и подпороговым диаметром аорты, которые являются кандидатами для клапаносберегающего протезирования корня и ВА и имеют очень низкий хирургический риск, клапаносберегающее протезирование корня и ВА рекомендуется в том случае, если она выполняется опытными хирургами в экспертном аортальном центре [93,106].
ЕОК\РКО Iib B, АКК и ААC Iib B (УДД 4, УУР С)
Комментарии. Клапаносберегающее протезирование ВА ассоциировано с относительно невысоким хирургическим риском [106,107,110], если она выполняется опытными хирургами в составе специализированного аортального центра. Пациентам с аневризматическим расширением синусов Вальсальвы и тубулярного отдела ВА (в том числе ассоциированным с синдромами Марфана, Лойеса-Дитца, Элерса-Данло) рекомендуется выполнять протезирование корня и ВА с реимплантацией АК (операция David), а при невозможности – операцию Bentall – De Bono. Возможным вариантом является использование клапаносодержащего кондуита из ксеноперикарда. Главным критерием для выбора механического или биологического протеза клапана сердца является возраст пациента. Устойчивой тенденцией последнего времени является расширение использования биологических протезов клапанов сердца в когорте более молодых пациентов. Результаты операции Bentall – De Bono при АВА с сопутствующим трехстворчатым либо бикуспидальным АК значимо не различаются; госпитальная летальность сопоставима с операциями изолированного протезирования АК, а осложнения в отдаленном послеоперационном периоде нечасты. Одним из решений проблемы коррекции АН без использования искусственного клапана является операция Ross. В 1967 г. Donald Ross впервые выполнил аутотрансплантацию пульмонального клапана в аортальную позицию, что позволило по-новому взглянуть на возможности лечения пациентов с патологией корня аорты и АК. Аутографт легочной артерии демонстрирует прекрасные гемодинамические характеристики, функционирует в течение длительного времени, ассоциирован с низким риском тромбоэмболических и инфекционных осложнений. Недостатками операции Ross являются ее техническая сложность, узкие показания к выполнению, сложности с подбором оптимальных кандидатов для хирургического лечения данным методом. Кроме того, при аневризме корня аорты, распространяющейся дистальнее СТС, требуется протезирование измененного отдела аорты, что может быть выполнено с синтетическим либо ксеноперикардиальным протезом. При неизмененных (мягких, нефиброзированных и некальцинированных) створках трехстворчатого АК возможно выполнение клапаносберегающего вмешательства. Оптимальными кандидатами для подобного метода лечения являются больные с АН первого (расширение корня аорты в сочетании с морфологически нормальными створками) и второго (пролапс створок) типов. В 1992 г. T. David и соавт. опубликовали статью, описывающую протезирование корня аорты с сохранением АК методом его реимплантации в протез аорты. Отличительной чертой этого подхода является стабилизация корня аорты на всех уровнях (ФК АК, синусы Вальсальвы, СТС). Годом позже M. Sarsam и M. Yacoub описали клапаносохраняющее протезирование корня аорты с ремоделированием АК. От методики реимплантации T. David ремоделирование корня аорты принципиально отличается отсутствием стабилизации аорты на уровне ФК АК, что потенциально может приводить к рецидиву АН. Существует несколько модификаций протезирования корня аорты с сохранением АК: формирование псевдосинусов методом шовной пликации протеза аорты, использование протеза с синусами, сформированными фабричным способом, комбинация ремоделирования АК и стабилизации корня аорты путем имплантации полоски из тефлона либо опорного кольца. Одним из подвидов клапаносохраняющего протезирования корня аорты является методика Florida sleeve, предложенная P. Hess и соавт. в 2005 г. В отличие от операции David, при варианте Florida sleeve не производится иссечения синусов Вальсальвы – корень аорты имплантируется в протез целиком. Диаметр протеза подбирается таким образом, чтобы возможно было достичь восстановления нормальной запирательной функции АК. При необходимости в протез аорты реимплантируются одна либо обе коронарные артерии. Существует несколько модификаций способа Florida sleeve, и унифицированный и широко применяемый термин «реимплантация корня аорты» обозначает данный метод коррекции. Реимплантация корня аорты в протез демонстрирует стабильно хорошие клинические результаты в ближайшем послеоперационном периоде и может стать альтернативой классической операции David.
Пороговое значение диаметра корня и ВА для ее профилактического протезирования у пациентов с синдромом Лойеса-Дитца рекомендуется определять согласно конкретному генетическому варианту, диаметру аорты, скоростью роста ее диаметра, экстрааортальными особенностям, с учетом семейного анамнеза, возраста и пола пациента, а также предпочтениям врача и пациента (таблица 6) [39,112].
ЕОК\РКО I C, АКК и ААC I C (УДД 4, УУР С)
Комментарии. Патогенные варианты в TGFBR1, TGFBR2, SMAD3, TGFB2 и TGFB3 приводят к синдрому Лойеса-Дитца или могут вызывать аортопатию с незначительными внешними признаками. Основная часть информации описывает патогенные варианты TGFBR1 и TGFBR2 [113]. Пациенты с вариантами TGFBR1 и TGFBR2 подвержены риску расслоения аорты типа А в более молодом возрасте и при меньшем диаметре корня аорты, чем при синдроме Марфана [113]. В соответствии с более ранними рекомендациями, эта агрессивная аортопатия, особенно выраженная у пациентов с тяжелыми черепно-лицевыми нарушениями, требовала протезирования аорты уже при диаметре корня аорты >4,0 см [113]. Вместе с тем, согласно Рекомендациям ACC/AHA 2010 г. по лечению заболеваний грудной аорты, операция рекомендуется только в тех случаях, когда диаметр аорты составляет от 4,2 см до 4,6 см (в зависимости от метода визуализации) [26]. Варианты синдрома Лойеса-Дитца, связанные с патологией гена SMAD3, могут приводить к расслоению аорты различного диаметра [26,112]. Риск расслоения аорты выше у женщин с патологическими вариантами TGFBR2, у которых отмечаются определенные внеаортальные признаки. Ограниченные данные позволяют предполагать отсутствие более высокого риска расслоения аорты при ее меньшем размере у пациентов с вариантами TGFB2 [114] или TGFB3 [115] . Существует заметная внутрисемейная изменчивость поражения аорты при синдроме Лойеса-Дитца. Общее решение о сроках проведения профилактической операции для предотвращения расслоения аорты типа А при синдроме Лойеса-Дитца должно учитывать конкретный генетический вариант, диаметр и скорость роста аорты, а также возраст, пол, размер тела, семейный анамнез, личные предпочтения пациента и опыт хирурга.
Таблица 6. Пороговые значения диаметра восходящей аорты для профилактического протезирования корня и восходящей аорты при синдроме Лойеса-Дитца на основе генетического варианта
КР |
УД [ссылки] |
Аллель |
Наличие признаков высокого риска* |
Диаметр аорты (см) |
|
|---|---|---|---|---|---|
1 |
C [116] |
TGFBR1 |
Нет |
≥4,5 |
|
1 |
C [116] |
TGFBR2 |
Нет |
≥4,5 |
|
2b |
C [116] |
TGFBR1 |
Да |
≥4,0 |
|
2a |
C [113,116] |
TGFBR2 |
Да |
≥4,0 |
|
2a |
C [112,117] |
SMAD3 |
- |
≥4,5† |
|
2b |
C [114,115,118] |
TGFB2‡ |
- |
≥4,5† |
|
2b |
C [115,118] |
TGFB3 |
- |
≥ 5,0† |
|
|
* протезирование аорты может быть рекомендовано и при меньшем диаметре аорты в том случае, если синдром Лойеса-Дитца связан с патогенными вариантами генов TGFBR1 и TGFBR2, а также имеются признаки, ассоциированные с более высоким риском расслоения аорты, в том числе некоторые специфические патогенные варианты, женщины с TGFBR2 и небольшим размером тела, наличие тяжелых экстрааортальных симптомов (например, краниосиностоз, расщелина неба, гипертелоризм, расщепленный язычок, выраженная извитость артерий, расширение шрамов и полупрозрачная кожа), семейный анамнез расслоения аорты (особенно в молодом возрасте или при относительно небольшом диаметре аорты), скорость роста аорты >0,3 см/год. †Семейный анамнез, возраст и скорость роста аорты также определяют пороговые значения хирургического вмешательства. ‡Патогенные варианты в гене TGFB2 отличаются от вариантов в гене TGFBR2. КР – класс рекомендации; УД – уровень доказательности. |
|||||
У пациентов с синдромом Лойеса-Дитца, обусловленным патогенными вариантами TGFBR1, TGFBR2 или SMAD3, рекомендуется рассмотреть протезирование корн
Медицинская реабилитация для данного заболевания не разработана.
5.1 Наблюдение при расширении и аневризме грудной и торакоабдоминальной аорты
У пациентов с заболеваниями грудной аорты важна подробная исходная оценка всех сегментов грудной аорты, анатомии и функции АК. Для оценки состояния грудного отдела аорты обычно используются ТТ-ЭхоКГ, КТА грудной аорты и МРА грудной аорты.
Рекомендуется выполнение ТТ-ЭхоКГ пациентам с расширением грудной аорты в процессе обследования и установления диагноза, а также при последующем наблюдении, в том числе для оценки диаметров грудной аорты, анатомии и функции АК [44,244].
ЕОК\РКО I C, АКК и ААС I C (УДД 5, УУР С)
Комментарии. Проведение детального обследования с помощью ТТ-ЭхоКГ для оценки анатомии и функции АК является важным на начальном этапе наблюдения за пациентами с заболеваниями грудной аорты, которые не имеют показаний к хирургическому вмешательству. ТТ-ЭхоКГ, как правило, обеспечивает получение четких изображений корня и восходящего отдела аорты, является безопасной, воспроизводимой и может использоваться для многолетнего наблюдения. У отдельных пациентов со сложными окнами трансторакальной эхокардиографической визуализации ЧП-ЭхоКГ является альтернативой для оценки анатомии АК и размеров аорты [26,44,245].
Рекомендуется в процессе установления диагноза и для последующего наблюдения для оценки анатомии и диаметра грудной аорты пациентам с расширенной грудной аортой проведение КТА грудной аорты или МРА грудной аорты [26,55,58,246].
ЕОК\РКО IIa C, АКК и ААС IIa C (УДД 5, УУР С)
Комментарии. Для оценки всех сегментов грудной аорты, включая ветви дуги аорты, в качестве золотого стандарта предложена визуализация поперечного сечения тела человека с помощью КТА грудной аорты или МРА грудной аорты [55,247]. Спиральная КТ сердца с ЭКГ-синхронизацией сводит к минимуму артефакты движения и, таким образом, позволяет точно определить размеры корня, восходящего отдела аорты, морфологические особенности АК и других сердечных структур [55,247].
Рекомендуется для определения скорости расширения аорты у пациентов с расширенной грудной аортой выполнять визуализацию каждые 6–12 месяцев в динамике (в зависимости от индивидуальной анатомии с помощью ЭхоКГ, КТА грудной аорты или МРА грудной аорты); если размер аорты стабилен, контрольная визуализация рекомендуется каждые 6–24 месяца (в зависимости от диаметра аорты) [26,58,244].
ЕОК\РКО IIa C, АКК и ААС IIa C (УДД 5, УУР С)
Комментарии. Пациенты со стабильными размерами аорты могут длительно наблюдаться с помощью ТТ-ЭхоКГ, КТА грудной аорты или МРА грудной аорты. Частота визуализации в динамике должна быть индивидуальной и зависеть от этиологии аневризмы, диаметра аорты, скорости расширения аорты, близости диаметра аорты пороговому для принятия решения о хирургическом вмешательстве, возраста пациента [18,248]. В целом у пациентов с несиндромными пограничными расширениями грудной аорты скорость расширения аорты относительно низка, поэтому интервал для проведения визуализаций в динамике может быть увеличен.
Рекомендуется назначение монотерапии низкими дозами Ацетилсалициловой кислоты** (75-100 мг/сут) в течение первых 3 месяцев пациентам с аневризмой корня и/или ВА после клапаносохраняющей операции на корне и/или ВА при отсутствии других показаний к назначению оральных антикоагулянтов (B01A) Антитромботические средства) с целью профилактики тромботических осложнений [135,249].
ЕОК\РКО IIa С (УДД 5, УУР С)
Пациентам с сосудистым типом синдрома Элерса-Данло рекомендуется регулярное наблюдение за состоянием аорты и периферических артерий с помощью дуплексного сканирования сосудов, КТА или МРА [250,251].
ЕОК\РКО I С (УДД 4, УУР С)
У пациентов с синдромом Марфана рекомендуется выполнение ТТ- ЭхоКГ:
- ежегодно при диаметре корня аорты <45 мм и в отсутствие дополнительных факторов риска;
- не реже одного раза в 6 месяцев при диаметре корня аорты <45 мм при наличии дополнительных факторов риска;
- не реже одного раза в 6-12 месяцев при диаметре корня аорты ≥45 мм при отсутствии дополнительных факторов риска [32,58,252,253].
ЕОК\РКО I С (УДД 5, УУР С)
Пациентам с синдромом Марфана, которым ранее ранее не выполнялись хирургические вмешательства на аорте, рекомендуется полная визуализация торакоабдоминальной аорты и периферических артерий с помощью КТА либо МРА, а также УЗИ при первичном обследовании, затем каждые 3-5 лет при стабильном течении заболевания [32,252,254].
ЕОК\РКО I С (УДД 5, УУР С)
Пациентам с синдромом Лойеса-Дитца рекомендуется выполнение ТТ-ЭхоКГ при первичном осмотре, затем каждые 6-12 месяцев в зависимости от диаметра аорты и скорости ее расширения [32,113,255].
ЕОК\РКО I С (УДД 4, УУР С)
У пациентов с синдромом Лойеса-Дитца рекомендуется визуализация всей аорты и периферических артерий при первичном осмотре с помощью КТА или МРА и последующее наблюдение с контрольными визуализирующими исследованиями каждые 1-3 года [32,255].
ЕОК\РКО I С (УДД 5, УУР C)
5.2 Наблюдение за пациентами после транскатетерного (эндоваскулярного) вмешательства на аорте
Рекомендована КТА грудной аорты пациентам после транскатетерного (эндоваскулярного) вмешательства на аорте в течение первого месяца от момента выполнения процедуры (предпочтительно в рамках стационарного лечения), через 6 и 12 месяцев после транскатетерного вмешательства на аорте, а затем ежегодно в течение всей жизни с возможностью более частого проведения контрольных исследований, если будет выявлено эндоподтекание (эндолик) или другая вызывающая настороженность проблема [256,257].
ЕОК\РКО I В (УДД 4, УУР С)
Комментарии. В случаях, когда при КТА через 1 месяц выявлены морфологические проблемы с эндопротезом (например, «птичий клюв», загибание эндопротеза), эндоподтекание (эндолик) или признаки расширения аневризматического мешка, а также при неосложненном течении у пациентов высокого риска осложнений (например, после вмешательства по поводу ПАЯ или разрыва аорты), рекомендуется провести повторную КТА грудной аорты с визуализацией артерий и контрастированием в отсроченные фазы в течение 3-6 месяцев. В случаях низкого риска прогрессии расширения аорты, например, при уменьшении размера аневризмы аорты и стабильном состоянии более 3 лет, можно использовать КТ органов грудной полости для отслеживания размера аневризматического мешка и стабильности компонентов. Нельзя рекомендовать отмену наблюдения после транскатетерного вмешательства на аорте либо увеличение интервалов между исследованиями до менее одного раза в год, учитывая отсутствие доказательной базы по долгосрочной безопасности, а также наличие данных о росте аневризмы и появлении новых эндоликов, несмотря на ранее проведенную изоляцию аневризмы [256,257].
Рекомендуется продолжение долгосрочного наблюдения за пациентами после эндоваскулярного вмешательства на грудной аорте и визуализации аорты с помощью КТА каждые 5 лет, если по прошествии 5 лет после оперативного лечения не наблюдалось развития осложнений [22,32,258].
ЕОК\РКО IIa В (УДД 4, УУР С)
Рекомендуется проведение повторных КТА каждые 6–12 месяцев у пациентов с ростом аневризмы без признаков эндоподтеканий типа I или III [259].
ЕОК\РКО IIa С (УДД 5, УУР С)
У пациентов низкого риска начиная с 1 года после эндоваскулярного вмешательства на аорте рекомендуется проведение повторных ультразвуковых допплерографий и дуплексного сканирования с контрастным усилением каждые 2 года [44,260].
ЕОК\РКО IIa В (УДД 5, УУР С)
5.3. Наблюдение после хирургического лечения
После проведенного клапаносберегающего либо клапаноуносящего протезирования корня и/или восходящего отдела аорты у пациентов с АГА и\или ТААА, либо после протезирования АК и диаметре ВА в любой зоне >4,0 см рекомендуется пожизненное наблюдение и проведение визуализирующих исследований корня и восходящего отдела аорты методами ЭхоКГ, КТА или МРА с интервалами, зависящими от диаметра грудной аорты в разных отделах и темпа его роста, наличия ДАК, а также дополнительных факторов риска осложнений, ассоциированных с аортой [46].
ЕОК\РКО I С, АКК и ААC I С (УДД 4, УУР С)
Комментарии. Пациенты с ДАК, ранее перенесшие изолированное ПАК или пластику АК, остаются подверженными риску расширения и расслоения аорты в будущем. В серии из 1286 пациентов, перенесших изолированное ПАК по поводу ДАК с 1960 по 1995 гг., 15-летняя свобода от «аортальных» осложнений (расслоение аорты, аневризма аорты >5,0 см или операция по поводу аневризмы аорты) составила 89%, но она была ниже у пациентов с документально подтвержденным расширением аорты на исходном этапе по сравнению с пациентами с нормальными диаметрами аорты (85% против 93%; р=0,001) [261]. Пациенты с ДАК, перенесшие изолированное ПАК по поводу аортального стеноза и имеющие только легкую или умеренную дилатацию аорты, в ходе 15-летнего наблюдения характеризуются низким риском осложнений со стороны аорты [62], то время как те, кто перенес ПАК по поводу преобладающей АН, и лица с преобладающим расширением корня аорты («корневой» фенотип расширения ВА) имеют более высокий риск ассоциированных с аортой осложнений. Во время наблюдения за 56 пациентами с ДАК, перенесшими изолированное ПАК по поводу АН и имевших сопутствующее расширение корня аорты (4,0–5,0 см), осложнения со стороны аорты развились у 34% пациентов [62]. Пациенты с ДАК после изолированного ПАК по поводу АН подвержены более высокому риску позднего расслоения аорты по сравнению с больными, оперированными по поводу стеноза бикуспидального АК [262].
Пациентам, перенесшим «открытую» хирургическую реконструкцию грудной аорты, рекомендуется выполнение КТА грудной аорты в течение первого месяца от момента выполнения процедуры (предпочтительно в рамках стационарного лечения), через 6, 12 и 24 месяца после вмешательства, и далее при стабильном состоянии аорты каждые 5 лет [22,32,263].
ЕОК\РКО I В (УДД 4, УУР С)
6.1 Многопрофильные бригады, диспансерное наблюдение и логистика пациентов с заболеваниями грудной аорты
В стандартах оказания помощи при различных заболеваниях, основанных на доказательствах, отмечается, что результаты лечения пациентов критически взаимосвязаны как с количеством госпитализаций в целом, так и с объемом выполняемых в клинике операций на грудной аорте. Эффективность оказания медицинской помощи еще больше повышается при условии сотрудничества специалистов многопрофильных бригад, что способствует выбору наилучшей лечебной тактики для пациентов. Особенно это актуально в трудных случаях, когда имеется угроза развития мультиорганного поражения. Несмотря на отсутствие согласованного определения многопрофильной бригады по вмешательствам на аорте («аортальной» команды), за ее основу можно принять следующее: это специализированная бригада врачей, обладающих исключительно глубокими знаниями в области оценки и лечения заболеваний аорты, при этом помощь такой бригады носит комплексный и междисциплинарный характер [264]. Концепция таких комплексных центров, занимающихся патологией клапанов сердца, была официально закреплена в «Рекомендациях АСС/АНА 2020 г. по ведению пациентов с клапанными пороками сердца» [157]. В этом документе подчеркиваются многочисленные важные компоненты таких центров, начиная от знаний, опыта врачей, их технических навыков для сбора данных, а также научных достижений и уровня образования до оборудования и ресурсов, которыми должно располагать учреждение. Конкретные компоненты многопрофильных «аортальных» бригад могут отличаться от центра к центру, однако можно выделить наиболее общие черты, которые характерны для таких команд: наличие кардиохирургов, сосудистых хирургов и специалистов по эндоваскулярным методам лечения, обладающих большим опытом работы со сложными заболеваниями аорты в клинике, где ежегодно проводится большое количество оперативных вмешательств на аорте, наличие специалистов по визуализации, имеющих опыт работы с заболеваниями аорты, для выполнения и интерпретации КТА аорты, МРА аорты и ТТ-ЭхоКГ, наличие анестезиологов, имеющих опыт лечения острых заболеваний аорты и дренирования спинномозговой жидкости, и специалистов отделения реанимации и интенсивной терапии, также имеющих опыт ведения таких пациентов.
Заболевания грудной аорты, в особенности острые, являются опасными для жизни состояниями и требуют госпитализации пациента в стационар, где доступны все соответствующие диагностические и лечебные мероприятия. Минимальные требования для возможности адекватного ведения этих пациентов включают визуализацию с помощью КТА, ТТ-ЭхоКГ и ангиографии, наличие бригады сердечно-сосудистых хирургов, обладающих опытом применения искусственного кровообращения и циркуляторного ареста, а также возможности эндоваскулярных вмешательств. Кроме того, необходимо отделение интенсивной терапии, позволяющее осуществлять непрерывный мониторинг и коррекцию жизненно-важных функций, а также наличие специалистов, обладающих личным опытом и знаниями в ведении этой категории пациентов.
Перевод пациентов с заболеваниями грудной аорты, особенно с острыми состояниями, из одного медицинского учреждения в другое является опасным периодом для пациента и должен быть тщательно спланирован и эффективно осуществлен. Залогом успешного результата является полноценное врачебное взаимодействие на всех этапах транспортировки пациента.
Ретроспективная оценка пациентов с аневризмой грудной аорты и/или расслоением, особенно тех, у кого диагноз не был установлен своевременно, имеет решающее значение для изучения путей оптимизации диагностического и лечебного алгоритмов будущих пациентов.
Рекомендуется в целях улучшения результатов лечения и диспансерного наблюдения пациентов с бессимптомным течением распространенного поражения аорты, тех, кому может помочь комплексное любое открытое и эндоваскулярное лечение патологии аорты или имеющих множественные сопутствующие заболевания при рассмотрении возможности хирургического вмешательства направлять в экспертный центр, выполняющий большой объем вмешательств на грудной аорте (определение «экспертный центр» представлено в главе 3), имеющий в штате опытных хирургов в составе многопрофильной «аортальной» бригады [98].
ЕОК\РКО IIa C, АКК и ААC IIa C (УДД 4, УУР С)
Комментарии. В исследовании, в которое вошло 230 736 пациентов программы Medicare, перенесших операцию по поводу аневризмы брюшной аорты в период с 2001 по 2006 г., весь массив оперативных вмешательств (как «открыты», так эндоваскулярных) был разделен на квинтили. При этом скорректированная смертность снизилась по квинтилю вместе с ростом количества оказанных медицинских услуг, особенно в группе пациентов, перенесших открытые операции [265]. Преимущества большого объема операций в клинике для результатов хирургического лечения аналогичны таковым у пациентов с аневризмами грудной аорты. Хьюз и соавт. [98] проанализировали более 13 000 плановых операций на АК, корне и восходящем отделе аорте, выполненных в 741 больнице Северной Америки с 2004 по 2007 гг. Они обнаружили отрицательную связь между объемом оказанных медицинских услуг и скорректированным отношением шансов (ОШ) смертности пациентов (P <0,001), особенно при количестве вмешательств менее 30–40 в год. Обратная зависимость между годовым объемом вмешательств, проводимых в медучреждении, и смертностью была также продемонстрирована в более современной серии случаев, описанной Мори и соавт. [102]. На выборке из 53 000 операций на проксимальном отделе грудной аорты, проведенных в США с 2011 по 2016 гг., было показано, что риск периоперационной смертности значительно снижался, когда годовой объем оперативных вмешательств в медучреждении превышал 20–25 случаев (только 116 клиник в США выполнили более 20 случаев за год); в еще большей степени этот риск снижался, если годовой объем вмешательств составлял более 50 случаев (только 24 клиники в США выполнили более 50 случаев за год). Возможно, наиболее явная корреляция между количеством госпитализаций и уровнем смертности наблюдается среди пациентов с острым расслоением аорты. В ретроспективном анализе историй болезни 232 пациентов с острым расслоением аорты типа А, перенесших срочную операцию в одном из медицинских центров Великобритании, 30-дневная смертность была значительно ниже у тех пациентов, кого оперировал хирург, уже имеющий опыт работы операций на аорте (по сравнению с хирургом, не являющимся специалистом по аорте), и составила 10% против 26%, соответственно (P=0,02). Кроме того, хирурги, специализирующиеся на заболеваниях аорты, значительно чаще выполняли вмешательства на ее корне (43,0% против 17,3%; P=0,001), а продолжительность пережатия аорты во время операции у них была значительно ниже [266]. Наконец, по данным Умана-Пизано и соавт. [267], смертность после вмешательства по поводу расслоения аорты составила 14% против 24% у хирургов с большим и малым объемом выполняемых операций, соответственно. Очевидно, что не всем пациентам с заболеваниями грудной аорты доступна помощь многопрофильных бригад, особенно в условиях развития ОАС. Тем не менее, при плановом протезировании аорты (особенно при пороговых значениях ее диаметра) более низкий уровень периоперационной смертности у опытных «аортальных» хирургов в экспертных центрах с большим объемом ежегодно выполняемых вмешательств может дополнительно обосновать раннее проведение операции. Сходным образом, если протезирование аорты является относительно новыми или технически сложными, то наилучшие результаты, скорее всего, будут получены в центрах с активно оперирующими хирургами, имеющими опыт работы с новыми методиками. Следовательно, в настоящем руководстве присутствует ряд рекомендаций, в которых указано, что некоторые виды «открытых» хирургических или эндоваскулярных методов лечения заболеваний аорты должны выполняться опытными хирургами в экспертных центрах, где организованы многопрофильные «аортальные» бригады.
Рекомендуется пациентов с ОАС (разрывом аорты), требующих любого срочного вмешательства при возможности направлять в экспертный центр, где выбор тактики лечения будет осуществляться многопрофильной командой специалистов [66,266].
ЕОК\РКО I C, АКК и ААC I C (УДД 4, УУР С)
Комментарии. Андерсен и соавт. [66] сравнили результаты протезирования ВА по поводу острого расслоения аорты типа А. Были сравнены результаты лечения до и после внедрения программы многопрофильной хирургии грудной аорты, и было установлено, что после внедрения многопрофильной бригады периоперационная смертность резко снизилась, и это значительное снижение смертности сохранялось в течение 5 лет наблюдения (P=0,002). Аналогичным образом, в исследовании из Англии [266] сообщалось, что в клиниках, где были внедрены программы по созданию многопрофильных бригад, специализирующихся на лечении заболеваний грудной аорты, было достигнуто значительное снижение смертности по сравнению с больницами без таких программ.
Особенностью хронических заболеваний грудной аорты является необходимость регулярных скрининговых визуализирующих исследований. Диагностические скрининги, в том числе с применением методов лучевой диагностики, возможно проводить в амбулаторных условиях с дальнейшей интерпретацией полученных данных профильными врачами-хирургами.
Скорая специализированная медицинская помощь оказывается пациентам с подозрением на острые заболевания грудной аорты (разрыв и острое расслоение). В остальных случаях пациенты с хроническими заболеваниями грудной аорты сохраняют мобильность и обращаются за плановой медицинской помощью самостоятельно.
Высокотехнологичная медицинская помощь оказывается в условиях стационара врачами сердечно-сосудистыми хирургами, в ряде случаев врачами по рентгенэндоваскулярной диагностике и лечению. Для проведения диагностических исследований привлекаются врачи ультразвуковой диагностики, врачи-рентгенологи, врачи функциональной диагностики.
Показаниями для плановой госпитализации пациентов с заболеваниями грудной аорты в стационар являются:
хирургическое или эндоваскулярное лечение заболеваний грудной аорты;
хирургическое или эндоваскулярное лечение состояний и осложнений после открытых и эндоваскулярных вмешательств на грудной аорте.
Не являются показаниями для госпитализации:
периодические диагностические скрининги заболеваний грудной аорты при технической возможности их выполнения в амбулаторном порядке.
Показаниями для экстренной госпитализации пациентов с заболеванием грудной аорты в стационар являются:
разрыв, расслоение, ИМГ, ПАЯ грудной аорты или подозрение на эти состояния;
появление/усиление клинических симптомов ранее диагностированного заболевания грудной аорты.
Критерии выписки из стационара:
завершенное хирургическое или эндоваскулярное лечение заболевания грудной аорты, состояний или осложнений после открытых и эндоваскулярных вмешательств.
7.1 Стандартизация диаметров корня аорты и восходящего отдела грудной аорты в зависимости от размеров тела
В соответствии с пороговыми значениями диаметра аорты, представленными в настоящих рекомендациях в отношении планирования хирургических вмешательств, пороговые значения диаметра 4,0–4,5 см предусмотрены для пациентов, чьи рост, площадь поверхности тела (ППТ) или оба этих показателя находятся в пределах 1–2 стандартных отклонений от средних значений. Для мужчин и женщин, рост которых значительно меньше или больше средних значений, эти диаметры должны быть скорректированы в меньшую или бóльшую сторону соответственно. Некоторые методики стандартизации диаметра аорты в настоящее время используются в клинической практике и клинических исследованиях [67].
Z-оценка. Z-оценка довольно часто применяется при анализе расширения аорты у детей, поскольку возрастные изменения размеров тела ребенка делают определение нормальных размеров аорты особенно проблематичным, как и отличие нормального роста аорты от патологического. Для расчета z-индекса подготовлены нормограммы, где показатели ППТ сопоставлены с диаметром корня аорты. Одним из недостатков ППТ является наличие нескольких формул для ее расчета, согласно которым для одного пациента можно получить разные результаты. Также существует несколько калькуляторов Z-оценки, и все они также работают по-разному. Наконец, большинство литературных источников, касающихся естественного течения ОАС, базируются на диаметрах аорты, в то время как сообщения об исходах на основе Z-оценок не представлены широко, в связи с чем Z-оценка обычно не применяется для регистрации степени расширения аорты у взрослых.
Размерный индекс аорты и ростовой индекс аорты. Чаще всего в рамках клинической работы со взрослыми пациентами проводят стандартизацию диаметров аорты, используя отношения диаметра аорты к ППТ или росту пациента. В 2006 году Davies и соавт. [268] показали, что размерный индекс аорты (РазмИА), который определяют по формуле «диаметр аорты (см)/ППТ (м2)», является лучшим предиктором нежелательных аортальных явлений по сравнению исключительно с диаметром, а для стратификации пациентов с аневризмами аорты по группам низкого, среднего и высокого рисков достаточно воспользоваться простой номограммой. Однако неясно, влияет ли значимым образом масса тела взрослого на ожидаемый нормальный диаметр аорты, при этом выраженные колебания массы тела не должны влиять на увеличение или уменьшение размеров аорты. В связи с этим Zafar и соавторы [41] проанализировали возможное превосходство ростового индекса аорты (РостИА, который определяют по формуле «диаметр аорты (см)/рост пациента (м)») над РазмИА; установлено, что РостИА по меньшей мере не уступает РазмИА [41], при этом обладает преимуществом более простых расчетов.
Отношение площади поперечного сечения к росту. Еще один подход к стандартизации диаметра аорты по росту был предложен Svensson и соавторами в 2002 г. [69] – они проводили расчет отношения площади поперечного сечения аорты (см) к росту пациента (м). В первичных исследованиях в качестве порога для проведения вмешательств применялось отношение площади поперечного сечения к росту >10 см2/м из-за значительного увеличения риска нежелательных явлений; при этом в более актуальных сообщениях данная группа пользовалась более простым отношением площади поперечного сечения к росту ≥10 см2/м (а не >10 см2/2) в качестве прогностического порога повышенного риска [70,103].
7.2 Стратификация риска хирургического лечения
Рекомендуется для пациентов с аневризмой грудной аорты и ТААА проводить стратификацию риска при планировании хирургического лечения [269,270].
ЕОК\РКО I C (УДД 4, УУР С)
Комментарии. Для выбора хирургической тактики и оптимизации лечения важнейшей задачей является выявление факторов риска и прогнозирование исхода операции. С этой целью рекомендуется использовать формулы для оценки риска летального исхода, представленные на сайтах Society of Thoracic Surgeons (www.riskcalc.sts.org) и European System for Cardiac Operative Risk Evaluation (www.euroscore.org). К категории высокого риска относятся пациенты, имеющие уровни логистического EuroSCORE ≥10%, EuroSCORE II ≥4 [269,270]. Выбор дополнительных методов обследования для верификации сопутствующих заболеваний определяется клинической ситуацией. При планировании лечения пациента важно учитывать ряд факторов, не включенных в шкалы EuroSCORE II и STS, но влияющих на риск осложнений вмешательства на грудной аорте. С высоким риском осложнений и плохим прогнозом после хирургических или транскатетерных вмешательств на восходящем отделе аорты и/или АК ассоциированы состояние недостаточного питания, кахексия, когнитивные нарушения, ряд индивидуальных анатомических особенностей, влияющих на технику хирургической коррекции ("фарфоровая" аорта, тяжелый кальциноз фиброзного кольца АК и прилегающих структур выходного отдела ЛЖ). Патология других органов и систем включает заболевания почек, печени, легких. Печеночная недостаточность до операции ассоциирована с повышенным риском осложнений. Имеющаяся у пациента хроническая болезнь почек 4 и 5 стадии (скорость клубочковой фильтрации <30 мл/мин) обусловливает высокий риск развития в ближайшем послеоперационном периоде острой почечной недостаточности, необходимости диализа, тяжелых осложнений и неблагоприятного исхода. Патология легких в сочетании с болевым синдромом в раннем послеоперационном периоде после вмешательства на АК с использованием полной срединной стернотомии в случае продленной искусственной вентиляции легких является фактором риска осложнений со стороны дыхательной системы. Так как с возрастом пациента растет встречаемость и тяжесть сопутствующих заболеваний, верная оценка соотношения риска и пользы того или иного метода лечения усложняется. При планировании лечения пациента с заболеванием аорты большую роль играет мультидисциплинарная команда специалистов («аортальная» команда), всесторонне оценивающая исходные данные и вырабатывающая оптимальную тактику ведения. Главной целью деятельности специализированных центров (клиник) является обеспечение высокого качества диагностики и лечения заболеваний аорты. Это достигается непрерывным медицинским образованием персонала, сочетанием клинической и научной деятельности, а также путем увеличения объемов оказываемой помощи. В условиях большого объема выполняемых операций и хороших результатов последних возможно эффективное внедрение в практику технических приемов и методик, характеризующихся крутой кривой обучения [271].
7.3 Нерешенные проблемы
Большая часть рекомендаций в настоящем документе основана на ограниченных сериях хирургических вмешательств, ретроспективном характере анализа данных, одноцентровых исследованиях пациентов с заболеваниями грудной аорты. Вследствие недостаточной доказательной базы рекомендаций рабочая группа подчеркивает необходимость продолжения исследовательской работы с целью ликвидации пробелов при ведении пациентов с заболеваниями грудной аорты. Так, на сегодняшний день:
- недостаточно эпидемиологических данных о распространенности ОАС;
- необходимы современные данные о рисках аортальных осложнений.
- требуется подтверждение наиболее точного, воспроизводимого и предиктивного способа измерения аорты с использованием различных диагностических методов;
- не выявлены предикторы аортальных осложнений (помимо размера) у пациентов с дилатацией грудной аорты.
- требуется изучение эффекта воздействия на факторы риска в отношении предотвращения или снижения скорости прогрессирования заболеваний грудной аорты.
- необходим поиск генетических, эпигенетических, анатомических детерминант развития и прогрессирования различных форм заболеваний грудной аорты и предикторов острого аортального синдрома.
- отсутствуют доказательства об эффективности существующей медикаментозной терапии при хронических заболеваниях грудной аорты, а также данные о новых группах препаратов;
- в отношении аневризм грудной аорты необходимо проведение РКИ для определения оптимального срока профилактических вмешательств в зависимости от распространенности поражения и других характеристик, а также индивидуальных особенностей пациента;
- отсутствуют высоко доказательные работы по оценке гендерных различий по течению заболевания и результатах хирургического лечения как у пациентов с аневризмами аорты, так и с ее расслоением.
- требуется увеличение доказательной базы при выборе наилучшего варианта лечения у пациентов с острыми и хроническими заболеваниями дуги аорты.
- необходима стандартизация терминологии.













