Диагностика, лечение и профилактика венозных тромбоэмболических осложнений в травматологии и ортопедииКод: 940 • Редакция: 1
Ключевые слова
тромбоз глубоких вен
венозные тромбоэмболические осложнения
тромбоэмболия легочных артерий
риск венозных тромбоэмболических осложнений
профилактика венозных тромбоэмболических осложнении
осложнения эндопротезирования суставов
осложнения после ортопедических операций
Венозные тромбоэмболические осложнения (ВТЭО) – собирательное понятие, объединяющее тромбоз подкожных, глубоких вен, а также легочную тромбоэмболию.
Профилактика ВТЭО – система мер, направленная на предупреждение развития опасных для жизни пациента и функции конечности осложнений (ТЭЛА и ТГВ).
Венозные тромбоэмболические осложнения представляют собой сложное (многофакторное) заболевание, включающее взаимодействие между приобретенной или наследственной предрасположенностью к тромбозу и воздействием окружающей среды. В этиопатогенезе ВТЭО при хирургических вмешательствах можно выделить два основных звена – это непосредственно хирургическая травма и эндотелиальная дисфункция.
В настоящее время под травматичностью операции понимают не просто повреждение тканей в зоне хирургического вмешательства, но и большое количество патологических процессов. Хирургический стресс проявляется многофункциональными изменениями, происходящими в организме пациента под влиянием агрессивных факторов хирургического вмешательства: психоэмоционального возбуждения, боли, повреждения мягких тканей и кровеносных сосудов, патологических рефлексов и массивной кровопотери.
Изменения в организме, происходящие на фоне хирургического вмешательства, представляют собой программируемый стресс, следствием которого являются существенные изменения реологических свойств крови. Совокупность нарушений регуляции в системе гемостаза, приводящих к повышению свёртывающей способности, замедление кровотока в конечности и повреждение сосудистой стенки составляют триаду Вирхова, лежащую в основе патогенеза тромбоэмболических осложнений. В патогенезе развития тромбоэмболических осложнений после эндопротезирования крупных суставов пусковым механизмом является массивная травма тканей, повреждение кровеносных сосудов и обнажение сосудистого коллагена [1].
Выброс катехоламинов в ответ на хирургическую агрессию также увеличивает агрегационные свойства тромбоцитов. При этом активизируется как сосудисто-тромбоцитарное (за счет выброса в кровоток тромбопластических факторов из тромбоцитов), так и коагуляционное (за счет высвобождения тромбопластических веществ из стенки сосудов) звенья гемостаза [2, 3]. Внешний путь коагуляционного гемостаза приводит к образованию первичного сгустка и при массивном повреждении тканей происходит в течение 15 секунд [4]. Повреждение эндотелия сосудов запускает свертывание крови по внутреннему пути. В норме эндотелий секретирует антикоагулянтные факторы, препятствующие адгезии форменных элементов к стенке сосуда. При травме сосуда эта способность теряется и на месте повреждения формируется сначала тромбоцитарный тромб, а затем фибриновый тромб. Другими причинами повышенного риска тромбообразования являются вынужденное положение конечности, к примеру, при эндопротезировании коленного сустава, когда выраженное сгибание в оперированном суставе приводит к компрессии сосудов в подколенной ямке, а также применение турникета гибкого, что вызывает стаз крови, перерастяжение и микроразрывы сосудистой стенки. Кроме того, манипуляции в костномозговом канале во время установки эндопротеза, применение костного цемента, активируют внешний путь свертывания крови за счет образования большого количества тромбина, что также увеличивает риск тромбообразования.
Таким образом, патогенез тромбообразования при хирургическом вмешательстве представлен в виде сменяющих друг друга процессов: хирургическая агрессия запускает классическую триаду Вирхова: интраоперационная травма сосудов, замедление кровотока из-за вынужденного положения конечности и наложения турникета гибкого при эндопротезировании коленного сустава и активация коагуляционного гемостаза. Далее каскад цитокинов и гуморальных медиаторов провоцирует нарушение сосудистого тонуса и миграцию лейкоцитов к месту повреждения сосуда. Вследствие этого на протяжении сосудов образуются конгломераты, состоящие из нитей фибрина и форменных элементов крови. Отрываясь от сосудистой стенки данные конгломераты могут вызывать тромбоэмболию. Действие факторов продолжается в послеоперационном периоде, причем важную роль играют такие факторы, как послеоперационная боль и вынужденная иммобилизация пациентов.
Отдельную группу составляют больные с переломами костей нижних конечностей, костей таза, а также пострадавшие с политравмой. Их особенностью является то, что активация свёртывающей системы крови происходит в несколько этапов. Первичная травма сопровождается значительным повреждением тканей, включая эндотелий сосудов, и выделением большого количества тканевого фактора, способствующего активации свёртывающей системы крови. Затем в течение короткого промежутка времени этим пациентам выполняется операция остеосинтеза перелома, что является дополнительной травмой и повторно активирует свёртывающую систему. Кроме того, пострадавшие с политравмой нередко нуждаются в этапных операциях, которые производятся два-три и более раз с интервалами в одну – две недели. При этом каждое хирургическое вмешательство приводит к активации гемостатического каскада. В результате риск развития посттравматических венозных тромбозов в этой группе больных значительно превышает риск подобных осложнений у больных ортопедического профиля, которым обычно выполняется одна операция. Кроме того, если ортопедического пациента можно подготовить к плановому оперативному вмешательству, компенсировав заболевания сердечно-сосудистой системы, явления венозной недостаточности нижних конечностей и другую сопутствующую патологию, способную увеличить риски венозных тромбозов, то пациент с травмой поступает в стационар и оперируется в экстренном или срочном порядке. Соответственно, возможность адекватного воздействия на сопутствующую соматическую патологию у врачей-хирургов обычно отсутствует в силу дефицита времени.
Большие ортопедические операции сопряжены с высоким риском развития ВТЭО – симптоматического и бессимптомного тромбоза глубоких вен и тромбоэмболии легочной артерии, которые являются потенциально опасными для жизни пациентов [5]. К основным ортопедическим операциям, вызывающим наибольшую озабоченность, относятся операции тотального эндопротезирования коленного сустава, тотального эндопротезирования тазобедренного сустава и переломы бедра.
Частота различных тробоэмболических осложнений варьирует. Бессимптомные тромбозы глубоких вен (диагностируемые только при скрининговом УЗАС) встречаются в 12,6–31,1% случаев после первичного эндопротезирования [6, 7]. Клинически значимые ТГВ развиваются гораздо реже - в 0,75–2,1% случаев [8, 9]. Наиболее тяжелое осложнение — тромбоэмболия легочной артерии (ТЭЛА) регистрируется в 0,41-1,93% случаев. При этом обструкция легочной артерии или ее ветвей не только потенциально опасна для жизни, но и может привести к хроническим осложнениям с плохим прогнозом, таким как тромбоэмболическая легочная гипертензия [10, 11]. Тромбозы глубоких вен являются основным промежуточным процессом, необходимым для развития ТЭЛА, связанной с хирургическим вмешательством, и повышают риск ее развития. Кроме того, приблизительно у 5-10% пациентов с симптоматическими ТГВ в течение последующих 10 и более лет развивается тяжелый посттромботический синдром, проявляющийся формированием венозных язв, периферических отеков и хронической боли [12].
В настоящее время общепринятой практикой при оценке эффективности тромбопрофилактики является учет только симптоматических тромбоэмболий, что обусловлено отсутствием различий через 2 года после хирургического вмешательства в клинических исходах (смертность от сердечно-сосудистых причин) между пациентами, у которых регистрировались бессимптомные ВТЭО, и при отсутствии данных осложнений [13].
I80.1 Флебит и тромбофлебит бедренной вены
I80.2 Флебит и тромбофлебит других глубоких сосудов нижних конечностей. Тромбоз глубоких вен БДУ
I80.3 Флебит и тромбофлебит нижних конечностей неуточненный. Эмболия или тромбоз нижних конечностей БДУ
Венозные тромбозы можно классифицировать по локализации, направлению тромботического процесса, степени фиксации тромба, степени гемодинамических расстройств и наличию осложнений [14, 15].
По локализации венозные тромбозы можно разделить в зависимости от:
- сосудистого бассейна: верхней или нижней (наиболее опасны в отношении развития ТЭЛА) полой вены;
- венозной системы: поверхностной, глубокой;
- вен, пораженных тромботическим процессом: проксимальный и дистальный уровни поражения.
По распространенности тромботического поражения: сегментарное или распространённое, двустороннее, мультифокальное.
По направлению распространения выделяют восходящий или нисходящий тромботическй процесс.
По степени фиксации тромба к венозной стенке:
- окклюзионный;
- неокклюзионный: пристеночный, флотирующий (эмболоопасный).
Выделяют три степени гемодинамических расстройств:
- легкая;
- средней тяжести;
- тяжѐлая.
По наличию осложнений венозный тромбоз подразделяют на:
- неосложненный;
- восходящий поверхностный тромбофлебит (верхняя граница тромба на уровне верхней трети бедра) – эмболоопасная форма;
- осложненный: ТЭЛА, венозная гангрена, посттромботическая болезнь (хроническая венозная недостаточность), тромбоз вен нижних конечностей с переходом на нижнюю полую вену.
Клинические проявления зависят от локализации тромбоза, распространенности и характера поражения венозного русла, а также длительности заболевания. В начальный период при неокклюзивных формах клиническая симптоматика слабо выражена либо вообще отсутствует. Иногда первым признаком ТГВ могут быть симптомы ТЭЛА. Типичный спектр симптоматики включает отек всей конечности либо ее части; цианоз кожных покровов и усиление рисунка подкожных вен; распирающую боль в конечности; боль по ходу сосудисто-нервного пучка [16].
Критерием диагноза служит сочетание симптомов тромботической окклюзии глубоких вен (отек голени, отек голени и бедра с болью или без нее в нижней конечности, ощущением тяжести в ней), возникших внезапно, и инструментальных (ультразвуковых, рентгеновских) данных о наличии тромботических масс в просвете глубоких вен. При бессимптомном ТГВ критерием диагноза служит инструментально подтвержденное наличие тромботических масс в просвете глубоких вен у пациента из группы риска ВТЭО, направленного на исследование с целью скрининга [345]. Основными целями диагностики острого венозного тромбоза при подтверждении диагноза являются определение его локализации, распространённости и эмболоопасности. К эмболоопасным ТГВ относят флотирующие тромбы, имеющие единственную точку фиксации в дистальном отделе. Тромбоз поверхностных вен представляет угрозу развития ТЭЛА при переходе на глубокую венозную систему.
Целесообразно провести все диагностические исследования при подозрении на ВТЭО в течение 24 часов, чтобы обеспечить быстрое лечение, если диагноз подтвержден, и избежать ненужных повторных доз антикоагулянтов, если диагноз исключен.
При обследовании пациентов с подозрением на острый венозный тромбоз и/или ТЭЛА рекомендуется активное уточнение жалоб, которые могут свидетельствовать о наличии тромботического поражения вен и лёгочной тромбоэмболии, и тщательный сбор анамнеза для выявления, в том числе, малосимптомных форм венозного тромбоза и тромбоэмболии дистальных ветвей лёгочных артерий [17–20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии. При сборе анамнеза необходимо уточнить дату получения травмы или выполненной ортопедической операции, проводилась ли пациенту профилактика ВТЭО, если да, какими методами, наличие в анамнезе эпизодов ТГВ и ТЭЛА, семейный анамнез (вероятность врождённой тромбофилии).
При неокклюзивных формах венозного тромбоза у больных с повреждениями ОДА жалобы, свидетельствующие о тромботическом поражении вен, часто минимальны или отсутствуют, поскольку венозный кровоток по сосуду частично сохранён. Для окклюзирующего варианта тромбоза характерно развитие острых (в течение несколько часов) распирающих ногу болей, отека, цианоза соответствующего сегмента. Развитие у пациента коллаптоидного состояния, болей за грудиной и кровохарканья требует экстренного обследования для исключения ТЭЛА.
Клинические признаки тромбоза поверхностных (подкожных) и глубоких вен конечностей существенно различаются. Тромбоз поверхностных вен (ТПВ) в клинической практике традиционно обозначают термином «тромбофлебит» в связи с наличием легко выявляемых признаков воспаления (как правило, асептического) стенки вены и паравазальной клетчатки.
Клинические признаки тромбоза поверхностных вен:
боль по ходу тромбированных подкожных вен;
полоса гиперемии в проекции поражённой вены;
при пальпации ‒ шнуровидный, плотный, резко болезненный тяж;
местное повышение температуры, гиперестезия кожных покровов.
Клинические проявления ТГВ менее специфичны, зависят от локализации тромбоза, распространённости и характера поражения венозного русла, длительности заболевания. На фоне посттравматического (послеоперационного) отёка клиническое выявление ТГВ представляет сложную задачу. В начальный период при неокклюзивных формах тромбоза клиническая симптоматика не выражена либо вообще отсутствует. Нередко первыми признаками, свидетельствующими о ТГВ, у госпитального пациента могут быть симптомы ТЭЛА.
Типичный спектр симптоматики ТГВ включает:
• отёк всей конечности либо голени;
• цианоз кожных покровов и усиление рисунка подкожных вен;
• распирающую боль в конечности;
• боль по ходу сосудисто-нервного пучка.
Всем пациентам с подозрением на ВТЭО рекомендуется выполнить физикальное обследование для исключения других причин клинической симптоматики [21–24].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
Комментарии. Обследуя больного с подозрением на венозный тромбоз, следует обязательно осмотреть обе нижние конечности. Нередко тромбоз развивается в травмированной и контралатеральной конечностях одновременно. Возможно двустороннее поражение как поверхностных, так и глубоких вен. На фоне травмы (операции), посттравматического (послеоперационного) отёка и болевого синдрома ТГВ не имеет выраженных клинических проявлений и его ранняя диагностика только по клиническим признакам существенно затруднена. Необходимо целенаправленно выявлять наличие симптомов, указывающих на ТЭЛА. Развитие лёгочной эмболии однозначно свидетельствует о тромбозе глубоких вен.
Эмболоопасность тромба не коррелирует с выраженностью клинической симптоматики. Флотирующий тромб, угрожающий фатальной ТЭЛА, может иметь минимальные клинические проявления, поскольку он не перекрывает полностью просвет магистральной вены.
Ценность физикального исследования для точного установления протяженности ТПВ невелика в связи с тем, что истинная распространённость тромбоза подкожных вен значительно превышает клинически определяемые признаки тромбофлебита.
У значительной части пациентов переход тромботического процесса с поверхностных на глубокие венозные магистрали протекает бессимптомно.
Для клинической оценки вероятности ТГВ при обследовании пациента рекомендуется использование шкалы Wells (Приложение Г1). По сумме набранных баллов больных разделяют на группы с низкой, средней и высокой вероятностью венозного тромбоза [25–29].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
Комментарии. Объём и тактика дальнейшего обследования и лечения определяется после консультации врача-сердечно-сосудистого хирурга. Поскольку клинические данные не позволяют с уверенностью исключить наличие ТГВ, диагностический поиск должен включать последующее лабораторное и инструментальное обследование.
Для клинической оценки вероятности ТЭЛА при обследовании пациента рекомендуется использование шкалы Wells или модифицированной шкалы Geneva (Приложение Г2 и Г3) [26, 28, 30–32].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 1)
Комментарий. Клинические признаки ТЭЛА разнообразны и мало специфичны. Наличие и выраженность симптомов определяется размерами, локализацией тромбоэмболов и исходным кардиореспираторным статусом пациента. По клиническим данным нельзя категорично ни подтвердить, ни отвергнуть наличие ТЭЛА. Однако такая предварительная оценка необходима, чтобы в последующем надлежащим образом интерпретировать результаты инструментальной и лабораторной диагностики. ТЭЛА может быть условно подразделена на три группы: массивную (эмболическое поражение лёгочного ствола и/или главных лёгочных артерий), субмассивную (окклюзия от 30 до 50% артериального русла лёгких) и тромбоэмболию мелких ветвей лёгочных артерий (суммарное поражение менее 30% артериального русла лёгких). Объём и тактика дальнейшего обследования определяется после консультации врача-сердечно-сосудистого хирурга. Выбор дальнейшей лечебной тактики у больного с ТЭЛА в специализированном отделении определяют на основе определения риска смерти в ближайшие 30 суток (высокий, промежуточный, низкий).
Пациентам без клинических признаков, позволяющих предположить ТГВ и/или ТЭЛА, не рекомендуется проводить определение концентрации Д-димера в крови с целью скрининга [33–36].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии. Повышенный уровень Д-димера в плазме крови свидетельствует об активных процессах образования и распада фибрина. Наряду с высокой чувствительностью тест имеет низкую специфичность. Повышенный уровень Д-димера выявляют при многих состояниях, в том числе после травм, перенесённых оперативных вмешательств, при воспалении, инфекционном процессе, опухолях, а также у пожилых людей и пациентов, длительно находящихся в стационаре.
У больных с повреждениями опорно-двигательного аппарата изолированное повышение уровня Д-димера не может рассматриваться как патогномоничный признак ВТЭО.
Пациентам с клинической симптоматикой и анамнезом, не оставляющими сомнений в наличии ТГВ и/или ТЭЛА, не рекомендуется для первичной диагностики проводить определение концентрации Д-димера в крови [11, 37].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Пациентам с клиническими признаками, позволяющими заподозрить ТГВ и/или ТЭЛА, при отсутствии возможности выполнить в ближайшие часы (A04.12.006) Дуплексное сканирование сосудов (артерий и вен) нижних конечностей или (A04.12.002.001) Ультразвуковую допплерографию сосудов (артерий и вен) нижних конечностей, рекомендуется определение концентрации Д-димера в крови [38, 39, 154-160].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
Комментарии. Повышение уровня Д-димера в крови у пациентов после травм или ортопедических операций не является достоверным признаком венозного тромбоза, поскольку его увеличение является компенсаторной реакцией системы гемостаза на повреждение опорно-двигательного аппарата. Однако нормальный уровень Д-димера позволяет с высокой вероятностью исключить наличие ВТЭО.
Всем пациентам с подозрением на тромбоз поверхностных, глубоких вен нижних конечностей и/или ТЭЛА рекомендуется выполнение (A04.12.006) Дуплексного сканирования сосудов (артерий и вен) нижних конечностей, (A04.12.002.001) или Ультразвуковой допплерографии сосудов (артерий и вен) нижних конечностей и (A04.12.022 ) Дуплексного сканирования сосудов малого таза с целью уточнения диагноза и определения дальнейшей тактики лечения [34, 40–45].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии. В стандартный объём (A04.12.006) Дуплексного сканирования сосудов (артерий и вен) нижних конечностей, (A04.12.002.001) Ультразвуковой допплерографии сосудов (артерий и вен) нижних конечностей, (A04.12.022) Дуплексного сканирования сосудов малого таза обязательно должно входить исследование поверхностных и глубоких вен не только повреждённой, но и контралатеральной конечности для исключения их симультанного поражения, часто протекающего бессимптомно. Глубокое венозное русло обеих нижних конечностей осматривают на всём протяжении, начиная от дистальных отделов голени до уровня паховой связки, а если не препятствует кишечный газ, то и сосуды илиокавального сегмента. Выполняя (A04.12.006) Дуплексное сканирование сосудов (артерий и вен) нижних конечностей, (A04.12.002.001) Ультразвуковую допплерографию сосудов (артерий и вен) нижних конечностей, (A04.12.022) Дуплексное сканирование сосудов малого таза, (A04.12.015.001) Триплексное сканирование нижней полой вены, подвздошных вен и вен нижних конечностей (комплексное) пациентам с тромбозом поверхностных вен, следует визуализировать сафено-феморальное и сафено-поплитеальное соустья и типичные группы перфорантных вен для исключения перехода тромбоза на глубокое венозное русло. При наличии возможности (A04.12.006) Дуплексное сканирование сосудов (артерий и вен) нижних конечностей, (A04.12.002.001) Ультразвуковая допплерография сосудов (артерий и вен) нижних конечностей, (A04.12.022) Дуплексное сканирование сосудов малого таза следует выполнить в течение ближайших 4 часов.
При распространении тромбоза на илиокавальный сегмент, в случае невозможности определения его проксимальной границы и эмболоопасности по данным УЗАС рекомендуется выполнение (A06.12.021) Флебография нижней полой вены или компьютерно-томографическая ангиография, с целью определения проксимальной границы тромба и его эмболоопасности [46–49].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
Комментарии. В случае выявления эмболоопасного тромба вторым этапом исследования возможно выполнение лечебных манипуляций: имплантации кава-фильтра***, (A16.12.003.001) Эндоваскулярная тромбэктомия аспирационная, (A16.23.034.012) локальный эндоваскулярный трансартериальный тромболизис.
Пациентам, которым оперативное лечение планируется в отсроченном порядке через несколько дней после травмы, рекомендуется выполнение УЗАС обеих нижних конечностей с максимальным приближением исследования к дате операции для выявления бессимптомных венозных тромбозов, особенно, если адекватная медикаментозная профилактика не проводилось [50–54].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
Комментарии. В случае выявления эмболоопасного тромба вторым этапом исследования возможно выполнение лечебных манипуляций: имплантации кава-фильтра***, A16.12.003.001 Эндоваскулярная тромбэктомия аспирационная, (A16.23.034.012) локальный эндоваскулярный трансартериальный тромболизис.
Пациентам, которым профилактические мероприятия не выполнялись в полном объеме или у которых имеется особенно высокий риск развития ВТЭО, рекомендуется выполнение УЗАС перед началом активизации для выявления бессимптомных тромбозов глубоких вен [52, 55–57].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
Пациенту, находящемуся в травматологическом или ортопедическом отделении, при подозрении на лёгочную тромбоэмболию в экстренном порядке необходимо выполнить регистрацию электрокардиограммы и рентгенографию легких для исключения иной патологии сердечно-сосудистой и дыхательной систем [16, 58–60].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии. Регистрация электрокардиограммы и рентгенография легких позволяют исключить иную кардиальную и лёгочную патологию, имеющую сходную с ТЭЛА клиническую картину. При переводе пациента в специализированное отделение сосудистой хирургии при подозрении на ТЭЛА дополнительно выполняют спиральную компьютерную томографию легких с контрастированием лёгочных артерий, позволяющую выявить нарушения перфузии лёгочного артериального русла, эхокардиографию, радионуклидное перфузионное сканирование (сцинтиграфию) лёгких (A07.09.003 Сцинтиграфия легких перфузионная), зондирование правых камер сердца, ангиографию легочной артерии и ее ветвей.
Задачи лечения ТГВ, независимо от его локализации, следующие:
- остановить распространение тромботического процесса;
- предотвратить ТЭЛА;
- не допустить прогрессирование отёка и возможную венозную гангрену;
- восстановить (полностью или частично) проходимость глубоких вен;
- предупредить рецидив тромбоза.
Хирургические и терапевтические методы в лечении ТГВ используют комплексно, в зависимости от приоритета задач, решаемых при лечении больного. Сфера приложения хирургических вмешательств в связи с появлением новых поколений эффективных антикоагулянтов и высокоинформативных неинвазивных методов диагностики, которые возможно использовать для динамического наблюдения за эффективностью лечения, в настоящее время имеет отчётливую тенденцию к сужению. В доминирующей доле наблюдений их задача – предотвращение массивной лёгочной эмболии. В послеоперационном периоде обязательно (при отсутствии противопоказаний к антикоагулянтам) проведение длительной антикоагулянтной терапии.
Выявление признаков острого тромбоза поверхностных, глубоких вен и/или ТЭЛА, а также обоснованное подозрение на них является основанием для консультации врача-сердечно-сосудистого хирурга. Дальнейшее лечение больных с ВТЭО проводят совместно врач-сердечно-сосудистый хирург и врач-травматолог-ортопед.
Операции на ОДА должны быть отложены до устранения опасности возможной лёгочной тромбоэмболии. При наличии гипсовой повязки следует её рассечь и развести края. До инструментального обследования больным с ТГВ и/или ТЭЛА должен быть предписан строгий постельный режим для снижения риска ТЭЛА. После обследования пациенты с неэмболоопасными формами венозного тромбоза могут быть активизированы.
3.1 Консервативное лечение
Вопросы консервативного лечения ТПВ рассмотрены в клинических рекомендациях «Флебит и тромбофлебит поверхностных сосудов» 2024 г, утвержденных научным комитетом Минздрава России.
Всем больным с ТГВ и/или ТЭЛА рекомендуется проведение антикоагулянтной терапии (при отсутствии противопоказаний) терапевтическими дозами (табл. 3.1):
нефракционированного гепарина (НФГ; син.: гепарин натрия**) [61-63, 161, 165, 167],
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
НМГ [61-63, 161, 165, 167],
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
фондапаринукса натрия [61-63, 162, 164, 166],
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 1)
апиксабана** [61-64, 161],
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
дабигатрана этексилата** [61-63, 161],
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
ривароксабана** [61-63, 161, 163, 164],
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 1)
непрямым антикоагулянтом (антагонистом витамина К) [61-63, 161, 163].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
Комментарий. Основой лечения больных с ВТЭО (в том числе бессимптомными) является антикоагулянтная терапия, поскольку только она способна остановить прогрессирование тромбоза. Введение лечебных доз антикоагулянтов при обоснованном подозрении на ТГВ и/или ТЭЛА и отсутствии противопоказаний должно быть начато ещё до инструментальной верификации диагноза. В условиях, когда дальнейшая тактика ведения больного ещё не определена, целесообразно использовать внутривенную инфузию НФГ (гепарин натрия**).
Таблица 3.1. Режимы использования и дозировка антикоагулянтов для лечения ТГВ
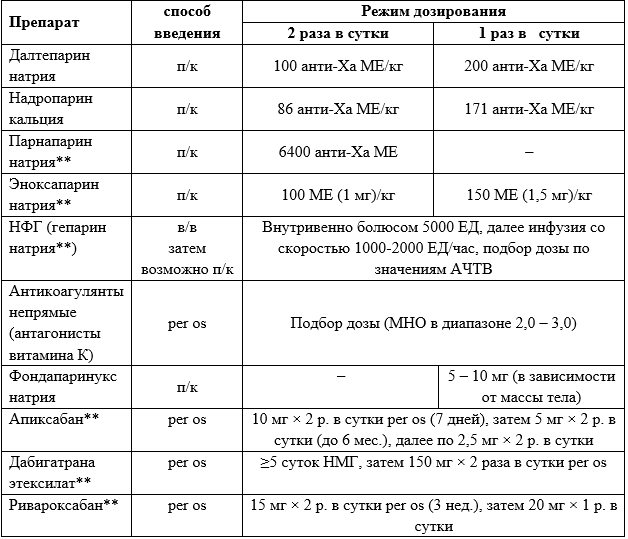
При обоснованном подозрении на ВТЭО рекомендуется начинать антикоагулянтную терапию до инструментальной верификации диагноза [61].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии. Экстренная инструментальная диагностика венозного тромбоза возможна, как правило, только в условиях специализированного сосудистого отделения. В связи с этим период времени от постановки клинического диагноза до выполнения УЗАС пациенту отделения травматологии и ортопедии может быть существенным. Известно, что раннее начало антикоагулянтной терапии позволяет в 3-4 раза уменьшить частоту ТЭЛА. В случае исключения ТГВ антикоагулянты отменяют.
У больных с неэмболоопасными формами ТГВ антикоагулянтная терапия рекомендуется в качестве основного метода лечения. В случаях выполнения по показаниям хирургического или эндоваскулярного вмешательства, системного или регионарного тромболизиса рекомендуется последующее проведение антикоагулянтной терапии [61, 62, 169, 170].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Рекомендуется использовать одинаковые подходы к применению антикоагулянтов при ТГВ (нижних и верхних конечностей) и ТЭЛА [61, 68–70, 168, 171, 172].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2)
Всем больным с ТГВ нижних конечностей рекомендуется (при отсутствии противопоказаний) эластическая компрессия обеих нижних конечностей с использованием компрессионного трикотажа 2-3-го класса [71, 72].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
Комментарии. Эластическая компрессия не должна прерываться при операциях на нижних конечностях: чулок (либо бинт, что менее эффективно) должен находиться на неоперируемой конечности во время оперативного вмешательства, на оперированную конечность чулок (бинт) надевают на операционном столе непосредственно после завершения операции. Проводить эластическую компрессию нижних конечностей следует до восстановления обычного двигательного режима больного, продолжая её в амбулаторных условиях.
Лечение больных с ТГВ, которым предполагается хирургическое, эндоваскулярное вмешательство или тромболизис, а также которые находятся на ИВЛ, рекомендуется начинать с парентерального введения антикоагулянтов НФГ (гепарина натрия**), далтепарина натрия, надропарина кальция, парнапарина натрия**, эноксапарина натрия** или фондапаринукса натрия [61, 73].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии. В случае развития ТГВ у больного с высоким риском кровотечения или если ему предполагается срочное хирургическое или эндоваскулярное вмешательство, целесообразно антикоагулянтную терапию начать с применения препаратов, для которых существует антидот. Для НФГ (гепарина натрия**) и НМГ таким антидотом служит протамина сульфат**, для дабигатрана этексилата** – идаруцизумаб. В случае использования других ПОАК интервал между последним приёмом препарата и оперативным вмешательством должен составлять, в зависимости от клиренса креатинина, от 24 до 48 часов. В большинстве случаев следует предпочесть НМГ или фондапаринукс натрия. Для НМГ возможно как двукратное, так и однократное введение препаратов (табл.3.1).
Антикоагулянтную терапию у больных, находящимся в стабильном состоянии и которым не планируют выполнение оперативного вмешательства или тромболизиса, рекомендуется проводить с использованием апиксабана**, дабигатрана этексилата** или ривароксабана** [61, 62, 73, 168, 173, 174].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии. У стабильного больного терапию апиксабаном** или ривароксабаном** следует начинать сразу после подтверждения диагноза ТГВ или переходить на эти лекарственные средства в первые 2 суток после начатого введения парентеральных антикоагулянтов. Перевод на дабигатрана этексилат** возможен с 5 суток от начала терапии парентеральными антикоагулянтами.
Большинству пациентов с ТГВ рекомендуется проведение антикоагулянтной терапии в течение не менее 3-х месяцев [61, 62, 175, 176].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
Больным с проксимальной локализацией ТГВ, перенёсшим ТЭЛА, при наличии тромбофилий, сопряжённых с высоким риском рецидива ВТЭО (антифосфолипидный синдром, дефицит антикоагулянтных протеинов C или S, мутации фактора V Лейдена или протромбина G20210A), при низком риске кровотечения и возможности поддерживать стабильный уровень антикоагуляции рекомендуется продолжение антикоагулянтной терапии до 6 мес. и более [61, 62, 177-183].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
У больных с ТГВ на фоне злокачественных новообразований с высоким риском кровотечения, а также у беременных, которым противопоказаны оральные антикоагулянты, рекомендуется предпочесть продлённое использование НМГ (подкожное введение лечебной дозы в первый месяц с возможностью последующего снижения до 75% от лечебной) [74–76].
Уровень убедительности рекомендаций С (уровень достоверности доказательств –5)
При выявлении в стационаре неэмболоопасной формы ТГВ у больного с повреждениями или заболеваниями ОДА и не нуждающегося по этому поводу в экстренном или срочном оперативном вмешательстве, рекомендуется проведение антикоагулянтной терапии парентеральными препаратами (лечебные дозы НМГ предпочтительны) и динамический ультразвуковой контроль за состоянием тромба и венозного русла. После стабилизации тромботического процесса, подтверждённого данными УЗАС, и стихания острых клинических проявлений тромбоза (через 3-5 суток) возможно выполнение оперативного вмешательства на ОДА [77].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии. За 12 ч до операции лечебную дозировку антикоагулянтов заменяют на профилактическую дозу НМГ. После операции (через 24 ч после предшествующей инъекции) при условии стабильного гемостаза повторно вводят НМГ в профилактической дозе. Со 2-х суток послеоперационного периода используют лечебные дозы антикоагулянтов. В послеоперационном периоде проводят динамический ультразвуковой контроль за состоянием тромба и венозного русла (каждые 3-5 сут.).
У пациентов с ТЭЛА давностью до 14 суток, приводящей к шоку или стойкой артериальной гипотензии, рекомендуется тромболитическая терапия (A11.12.003.002 Внутривенное введение лекарственных препаратов для тромболитической терапии) при отсутствии противопоказаний к её проведению [73, 78, 313-339].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 1)
Комментарии. ТЭЛА с выраженными нарушениями гемодинамики (шок, стойкая артериальная гипотензия) является абсолютным показанием для проведения тромболитической терапии (A11.12.003.002 Внутривенное введение лекарственных препаратов для тромболитической терапии). Чем раньше начата тромболитическая терапия, тем лучше ее результаты. Наилучшие результаты достигаются при длительности заболевания до 48 ч от момента эмболизации. В то же время можно рассчитывать на эффект при продолжительности заболевания до 14 сут. [73, 78, 313-318].
Массивная ТЭЛА является жизнеугрожающим состоянием. Одним из абсолютных противопоказаний является операция в предшествующие 10—14 дней, так как проведение тромболизиса при массивной ТЭЛА у больных в раннем послеоперационном периоде всегда связано с риском развития фатального кровотечения. При сохраняющейся нестабильной гемодинамике и выраженных дыхательных расстройствах на 10—12-е сутки послеоперационного периода необходимо провести тромболитическую терапию (A11.12.003.002 Внутривенное введение лекарственных препаратов для тромболитической терапии) в стандартном режиме. У пациентов с крайней тяжестью состояния и верифицированной массивной ТЭЛА проведение тромболитической терапии возможно болюсным введением («жизнеспасающий режим») [319-326]. Многоцентровое открытое рандомизированное сравнительное клиническое исследование ФОРПЕ (n=310) показало не меньшую эффективность рекомбинантного белка, содержащего аминокислотную последовательность стафилокиназы** (B01AD) по сравнению с алтеплазой** (B01AD02), в лечении пациентов с массивной тромбоэмболией легочной артерии с гемодинамической нестабильностью, и имеет более высокий профиль безопасности. Неиммуногенный рекомбинантный белок, содержащий аминокислотную последовательность стафилокиназы** (B01AD) используется в виде однократного болюса независимо от массы тела у всех пациентов с массивной ТЭЛА, что упрощает их лечение [327]. Проведение тромболитической терапии (A11.12.003.002 Внутривенное введение лекарственных препаратов для тромболитической терапии) при массивной ТЭЛА у беременных позволяет нормализовать центральную гемодинамику, уменьшить проявления правожелудочковой недостаточности, устранить гипоксемию у матери и плода и провести роды в срок, а используемый тромболитический препарат алтеплаза** (B01AD02) не обладает тератогенным эффектом на поздних сроках беременности. В доклинических исследованиях показано, что неиммуногенный рекомбинантный белок, содержащий аминокислотную последовательность стафилокиназы** (B01AD) не обладает эмбриотоксическими, тератогенными и репротоксичными свойствами. Подробнее о ведении пациентов с ТЭЛА у беременных рассматривается в соответствующих рекомендациях [328-339].
3.2. Оперативное лечение
Вопросы оперативного лечения ТПВ рассмотрены в клинических рекомендациях «Флебит и тромбофлебит поверхностных сосудов» 2024 г, утвержденных научным комитетом Минздрава России.
Выполнение эндоваскулярных (имплантация кава-фильтра***, катетерная тромбэктомия) и открытых хирургических вмешательств (тромбэктомия, перевязка глубокой вены проксимальнее тромба, пликация НПВ) в качестве метода предотвращения массивной ТЭЛА рекомендуется больным с ТГВ по следующим показаниям [82, 83, 184-190]:
- невозможность проведения надлежащей антикоагулянтной терапии;
- неэффективность адекватной антикоагулянтной терапии, на фоне которой происходит нарастание тромбоза с формированием эмболоопасного тромба (флотирующего тромба значительного диаметра длиной более 5-7 см);
- наличие эмболоопасного тромба илиокавального сегмента в момент первичной диагностики тромбоза;
- рецидивирующая ТЭЛА с высокой (систолическое давление в лёгочном стволе >50 мм рт. ст.) лёгочной гипертензией;
- некорректная позиция установленной ранее постоянной модели кава-фильтра*** (например, миграция его в почечную вену), исключающая возможность повторной имплантации (пликацию производят после флеботомии и удаления кава-фильтра***).
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
Комментарии. Приоритетным является имплантация кава-фильтров съёмных моделей (Кава-фильтр, временный/постоянный***), которые должны быть удалены после устранения опасности ТЭЛА, а именно перехода флотирующего тромба в неэмболоопасную форму за счёт фиксации подвижной его части к венозной стенке. Для большинства съёмных моделей кава-фильтров (Кава-фильтр, временный/постоянный***), оптимальный период их удаления составляет 3-4 недели.
При выявлении в стационаре эмболоопасного (флотирующего) тромба у больного с повреждениями или заболеваниями ОДА, и не нуждающегося по этому поводу в экстренном или срочном оперативном вмешательстве, рекомендуется имплантация съёмной модели кава-фильтра (Кава-фильтр, временный/постоянный***), после чего возможно оперативное вмешательство на ОДА в сроки, определяемые врачом-травматологом-ортопедом. Тактику антикоагулянтной терапии рекомендуется использовать аналогичную применяемой при неэмболоопасной форме ТГВ [84, 85].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
При выявлении в стационаре тромбоза илиокавального сегмента у больного с повреждениями или заболеваниями ОДА и нуждающегося по этому поводу в экстренном или срочном оперативном вмешательстве любой формы, из-за высокой вероятности прогрессирования тромботического процесса рекомендуется имплантация съёмной модели кава-фильтра (Кава-фильтр, временный/постоянный***) с последующим выполнением предполагаемого оперативного вмешательства на ОДА [84, 85].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии. После операции (через 6-12 ч) при условии стабильного гемостаза вводят антикоагулянты в профилактической дозе. Со 2-х суток послеоперационного периода используют лечебные дозы антикоагулянтов. В послеоперационном периоде проводят динамический ультразвуковой контроль за состоянием тромба и венозного русла.
При выявлении в стационаре эмболоопасного тромба бедренно-подколенного сегмента у больного с повреждениями или заболеваниями ОДА и нуждающегося по этому поводу в экстренном или срочном оперативном вмешательстве, рекомендуется имплантация съёмной модели кава-фильтра (Кава-фильтр, временный/постоянный***) либо, в качестве альтернативы, перевязка (или пликация) поверхностной бедренной вены нитью хирургической рассасывающейся (прим. нить хирургическая из поли (L-лактид кокапролактона***), с последующим выполнением предполагаемого оперативного вмешательства на ОДА [84, 85].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии. Больным с флотирующим тромбом общей бедренной вены первоначально выполняют тромбэктомию из общей бедренной вены. Затем перевязывают (плицируют) поверхностную бедренную вену тотчас дистальнее впадения глубокой вены бедра, проходимость которой является обязательным условием выполнения данной операции. Выполнение вмешательства на глубокой венозной системе возможно первым этапом в одну операционную сессию с вмешательством на ОДА.
При выявлении в стационаре изолированного тромбоза вен голени у пациента, нуждающегося в выполнении экстренного или срочного оперативного вмешательства на опорно-двигательном аппарате, рекомендуется проведение необходимого вмешательства и назначение антикоагулянтной терапии в послеоперационном периоде на фоне динамического контроля состояния тромба и венозного русла с помощью УЗАС [84, 85].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Программа реабилитационных мероприятий определяется основным заболевание или его осложнением и (или) характером операции, в частности, использованием высокотехнологичных или миниинвазивных вмешательств.
В настоящее время оптимальным следует признать подход, согласно которому профилактику ВТЭО проводят абсолютно всем пациентам, поступающим в стационар. Характер профилактических мер определяется степенью риска.
5.1 Оценка степени риска развития ВТЭО в травматологии и ортопедии
Несмотря на невозможность точного прогнозирования развития венозных тромбоэмболических осложнений, необходимо оценить степень вероятности их развития. Наличие у пациента факторов, предрасполагающих к ВТЭО (табл. 5.1), служит основанием для отнесения его к той или иной группе риска. Одним из наиболее удобных инструментов определения риска ВТЭО в хирургии служит шкала Caprini (Приложение Г5). В зависимости от наличия факторов риска и планируемой операции пациенту присваивают степень риска развития ВТЭО (Приложение Г6) [86]. При отсутствии профилактики у больного с очень низким (0 баллов), низким (1-2 балла), умеренном (3-4 балла) и высоком (≥5 баллов) риске вероятность развития ВТЭО составляет соответственно менее 0,5, 1,5, 3 и 6%. В связи с отсутствием принципиальных различий в частоте ВТЭО и тактике ведения и профилактики пациентов низкого и очень низкого рисков в клинической практике целесообразно объединить в одну группу низкой вероятности ВТЭО.
Таблица 5.1. Вероятность ВТЭО при различных предрасполагающих факторах
Факторы, повышающие вероятность ВТЭО более чем в 10 раз |
|---|
|
Факторы, повышающие вероятность ВТЭО в 2-9 раз |
|
Факторы, повышающие вероятность ВТЭО менее чем в 2 раза |
|
5.2 Средства профилактики ВТЭО
Для предупреждения ВТЭО у пациента с травмой или операцией на ОДА, прежде всего, следует минимизировать или устранить действие факторов, способствующих тромбообразованию: восстановить объем циркулирующей крови, нормализовать гемодинамику, применить адекватное обезболивание, предупредить развитие инфекционных осложнений. Необходимо стремиться к возможно более ранней мобилизации больного, восстановлению объёма движений в суставах конечностей. При возможности следует стабильно зафиксировать отломки в ранние сроки после перелома. Применение стабильного функционального остеосинтеза, уменьшение травматичности оперативных вмешательств за счёт использования современных технологий закрытого остеосинтеза позволяют сократить время ограничения подвижности пациента с повреждениями и заболеваниями опорно-двигательного аппарата.
Профилактика ВТЭО включает в себя следующие методы:
немедикаментозные – применяют у всех пациентов с ограниченной двигательной активностью (мобильностью):
— максимальную и возможно более раннюю активизацию больных после операции, включая методы пассивной нагрузки: вертикализация, механотерапия, кинезотерапия и др.;
— обеспечение максимально возможной активности мышц нижних конечностей пациентов, находящихся на длительном постельном режиме, местные процедуры, увеличивающие объемный поток крови через глубокие вены нижних конечностей (эластическая компрессия нижних конечностей, прерывистая пневмокомпрессия нижних конечностей, миостимуляция мышц голени и т.д.);
— активные и пассивные нагрузки на верхние конечности, улучшающие циркуляцию крови в целом, стимулирующие антитромботическую активность эндотелия;
медикаментозные — проведение фармакологической тромбопрофилактики у пациентов с умеренным и высоким риском развития ВТЭО.
5.2.1 Немедикаментозные средства профилактики ВТЭО
К немедикаментозным средствам относят механические способы профилактки, а именно – статическую эластическую компрессию нижних конечностей, последовательную перемежающуюся пневматическую компрессию (ППК), венозную помпу для стопы, миостимуляцию мышц голени и лечебную физкультуру. Основной целью применения немедикаментозных методов является ускорение венозного кровотока, при этом их использование не увеличивает опасность геморрагических осложнений. Механическую профилактику следует начать до операции, продолжать во время и после нее вплоть до восстановления двигательной активности.
Последовательная перемежающаяся пневматическая компрессия (ПППК) нижних конечностей величиной 40–50 мм рт. ст. с помощью специальных манжет и аппарата является наиболее эффективным из механических способов профилактики. Её следует применять в соответствии с инструкцией к аппарату у пациентов, находящихся на постельном режиме.
Статическую эластическую компрессию нижних конечностей с помощью медицинского компрессионного трикотажа (чулки, обеспечивающие оптимальное распределение давления на нижние конечности) или бинтов эластичных медицинских следует начинать при поступлении больного, поскольку пребывание в стационаре всегда связано с ограничением двигательной активности и замедлением скорости венозного кровотока. Накладывать бинт эластичный медицинский должен обученный персонал (правила наложения эластичных бинтов изложены в Приложении Г7). Ежедневно утром и вечером следует проверять и при необходимости корректировать состояние бинта. Специальный профилактический медицинский компрессионный трикотаж (чулки дозированной компрессии) эффективнее и проще в использовании, самостоятельно поддерживает необходимый градиент давления. Однако он требует предварительного подбора и из-за развивающегося отека не всегда обеспечивает адекватную степень компрессии в ближайшем послеоперационном периоде. Применение компрессионного трикотажа целесообразно при плановых оперативных вмешательствах. Эластическую компрессию продолжают во время операций на нижних конечностях: чулок (бинт) должен находиться на неоперируемой конечности во время оперативного вмешательства, на оперированную конечность его одевают (накладывают) на операционном столе непосредственно после завершения операции [55].
A17.02.001 Электростимуляция мышц голени (ЭНСМГ) – процедура рекомендована всем пациентам, находящимся на постельном режиме, как в стационаре, так и на амбулаторном этапе лечения. Проводится с помощью различного рода электронейростимуляторов (стационарных приборов или индивидуальных переносных) согласно прилагаемой инструкции. Необходимым элементом является наличие электродов, накладываемых на икроножные мышцы пациента. Возможно сочетание метода со статической эластической компрессией и ЛФК. Может рассматриваться как альтернатива методу ПППК [88].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
Лечебную физическую культуру применяют у всех больных. Особое значение имеют движения в голеностопном суставе и пальцах стопы. Лечебная физкультура не может быть заменой медикаментозным и механическим способам профилактики ВТЭО.
5.2.2. Медикаментозные средства, их дозы и режимы применения
5.2.2.1. Антикоагулянты
Группа антикоагулянтов включает в себя препараты НФГ (гепарин натрия**), НМГ, ПОАК (табл. 5.3) и антагонистов витамина К (АВК). Однако в настоящее время препараты из группы АВК (варфарин**) самостоятельно для профилактики ВТЭО в травматологии и ортопедии практически не используются. Единственной группой пациентов, которые нуждаются в их приеме, остаются пациенты, получающие АВК в связи с соматической патологией или имеющие непереносимость всех остальных антикоагулянтов.
Особое внимание во время медикаментозной профилактики ВТЭО следует уделять снижению периоперационной кровопотери. Необходимо добиваться тщательного интраоперационного гемостаза, применять современные гемостатические средства, использовать технологии кровесбережения и антифибринолитические средства (транексамовую кислоту** и др.).
Таблица 5.3. Рекомендуемые дозы и режим введения антикоагулянтовдля профилактики ВТЭО при оперативном лечении пациентов1
Рекомендуемые дозы и режим введения |
||
|---|---|---|
Препарат |
при средней степени риска развития ВТЭО |
при высокой степени риска развития ВТЭО |
НФГ (гепарин натрия**) |
Подкожно 2500 МЕ за 2–4 часа до операции, затем 2500 МЕ через 6–8 часов после операции, далее по 5000 МЕ 2–3 раза/сут.4 |
Подкожно 5000 МЕ за 4–6 часов3 до операции, затем 5000 МЕ через 6–8 часов после операции, далее по 5000 МЕ 3 раза/сут. |
Бемипарин натрия2 |
Подкожно 2500 анти-Ха МЕ за 2 ч до операции или через 6 ч после операции, затем ежедневно по 2500 анти-Ха МЕ 1 раз/сут. 4 |
Подкожно 3500 анти-Ха МЕ за 2 часа до операции или через 6 часов после операции, затем ежедневно по 3500 анти-Ха МЕ 1 раз/сут. |
Далтепарин натрия2 |
Подкожно 2500 анти-Ха МЕ за 2 часа до операции, затем 2500 анти-Ха МЕ 1 раз/сут. 4 |
(1) подкожно 5000 анти-Ха МЕ вечером накануне операции, затем 5000 анти-Ха МЕ каждый вечер. (2) подкожно 2500 анти-Ха МЕ за 2 часа до операции, затем 2500 анти-Ха МЕ через 8–12 часов (но не ранее чем через 4 часа после окончания операции), затем со следующего дня 5000 анти-Ха МЕ каждое утро. (3) подкожно 2500 анти-Ха МЕ через 4–8 часов после операции, затем со следующего дня 5000 анти-Ха МЕ 1 раз/сут. |
Надропарин кальция2 |
Подкожно 2850 анти-Ха МЕ (0,3 мл) за 2–4 часа до операции, затем 0,3 мл 1 раз/сут. 4 |
Подкожно 38 анти-Ха МЕ/кг за 12 часов до операции, 38 анти-Ха МЕ/кг через 12 ч после окончания операции, затем 38 анти-Ха МЕ/кг 1 раз/сут. на 2-е и 3-и сутки после операции, с 4-х суток после операции доза может быть увеличена до 57 анти-Ха МЕ/кг 1 раз/сут. |
Парнапарин натрия** |
Подкожно 3200 анти-Ха МЕ (0,3) за 2 часа до операции, затем по 0,3 1 раз/сут. 4 |
Подкожно 0,4 мл (4250 анти-Ха МЕ) через 12 часов после окончания операции, затем 1 раз\сутки |
Эноксапарин натрия2** |
Подкожно 20 мг за 2 часа до операции, затем 20-40 мг 1 раз/сут. 4 |
Подкожно 40 мг за 12 ч до операции или через 12– 24 час. После операции, затем 40 мг 1 раз/сут. |
Фондапаринукс натрия |
Подкожно 2,5 мг через 6-24 часа после операции, затем 1 раз/сут. |
|
Апиксабан** |
Перорально по 2,5 мг 2 раза в сутки; первая доза не ранее чем через 12–24 ч после завершения операции по достижении гемостаза |
|
Дабигатрана этексилат** |
Перорально по 220 мг или по 150 мг (пациентам: старше 75 лет, при умеренном нарушении функции почек – клиренс креатинина 30–50 мл/мин, принимающим амиодарон**, верапамил**, 1 раз в сутки; первый приём – в половинной суточной дозе не ранее чем через 1–4 часа после завершения операции по достижении гемостаза |
|
Ривароксабан** |
Перорально по 10 мг 1 раз в сутки; первая доза не ранее чем через 6–10 ч после завершения операции по достижении гемостаза |
|
1 – препараты сгруппированы в соответствии с фармакологическими свойствами, НМГ и пероральные антикоагулянты перечислены по алфавиту;
2 – у больных с низкой массой тела (менее 50 кг) разумно уменьшить профилактическую дозу НМГ в 2 раза, а у больных с выраженным ожирением (масса тела более 120 кг, индекс массы тела более 50 кг/м2) – увеличить ее на 25%; у таких пациентов оправдана коррекция дозы НМГ по уровню анти-Ха активности в крови;
3 – время введения НФГ (гепарин натрия**) до операции соответствует мнению экспертов с учетом обширности ортопедических операций, связанных с повышенным риском кровопотери;
4 – данные рекомендации отражают мнение экспертов и основаны на дозах и режиме применения препаратов группы гепарина в общей хирургии.
При использовании любых антикоагулянтов необходимо активно мониторировать признаки возможных геморрагических осложнений, исходно определить и регулярно контролировать уровень гемоглобина, гематокрит и клиренс креатинина (см. п. 5.4). При введении препаратов группы гепарина необходимо дополнительно регулярно контролировать количество тромбоцитов в крови.
Согласно инструкциям по применению препаратов при назначении и выборе дозы антикоагулянтов прямого действия (ПОАК) необходимо учитывать функцию почек. Для этого следует определять уровень креатинина в крови (A09.05.020 Исследование уровня креатинина в крови) и рассчитать клиренс креатинина с помощью формулы Кокрофта – Голта:

Если показатель сывороточного креатинина выражен в мкмоль/л, то результат надо умножить на 88. В соответствии с рассчитанным клиренсом креатинина устанавливают степень нарушения функции почек:
Легкая – клиренс креатинина 51–80 мл/мин
Средняя – клиренс креатинина 30–50 мл/мин
Тяжелая – клиренс креатинина менее 30.
В зависимости от степени почечной недостаточности производят назначение и коррекцию дозы ПОАК и НМГ (табл. 5.4).
Таблица 5.4. Дозирование ПОАК и НМГ при проведении профилактики ВТЭО у пациентов со сниженной функцией почек
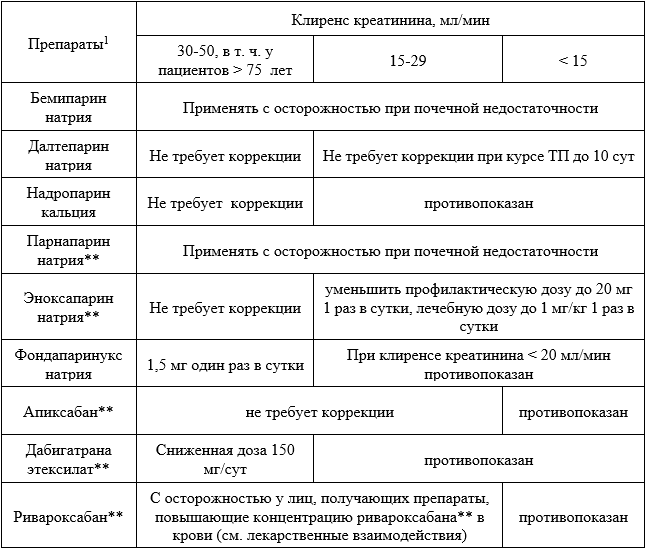
1 – препараты сгруппированы в соответствии с фармакологическими свойствами, НМГ и пероральные антикоагулянты перечислены по алфавиту
5.2.2.2. Антиагреганты, кроме гепарина
Группой лекарственных средств, с принципиально другим механизмом действия препятствующих тромбообразованию, являются антиагреганты, кроме гепарина. В отличие от антикоагулянтов они действуют на первом этапе свертывания крови, во время которого происходит агрегация тромбоцитов, блокируя адгезию тромбоцитов к эндотелию сосудов.
Единственным препаратом, который в настоящее время включен в целый ряд национальных рекомендаций по профилактике ВТЭО после планового эндопротезирования тазобедренного или коленного сустава (см. п. 5.4.1.) у пациентов без дополнительных факторов риска развития тромбозов является АСК** [89–92]. Рандомизированные клинические исследования и опубликованные мета-анализы показывают, что АСК** демонстрирует схожую с антикоагулянтами эффективность в профилактике ВТЭО после эндопротезирования коленного или тазобедренного сустава как при ступенчатой фармакологической профилактике, когда ее назначают после нескольких дней НМГ вне зависимости от дополнительных факторов риска ВТЭО у пациентов [93], так и при приеме с первых суток после операции у пациентов без дополнительных факторов риска [94].
Другие препараты данной группы (клопидогрел**, прасугрел, тикагрелор**) применяют при лечении кардиологической патологии. Пациенты, постоянно принимающие антиагреганты, кроме гепарина или антикоагулянты по терапевтическим показаниям, характеризуется высоким риском развития геморрагических осложнений. Рекомендации по ведению данной категории пациентов изложены в разделе 5.4.10.
5.2.2.3. Препараты для экстренного прерывания эффектов антитромботической терапии при неотложных операциях
В таблице 5.5 представлены препараты позволяющие в той или иной степени нейтрализовать эффект антикоагулянтов или антиагрегантов, кроме гепарина в случаях развития тяжелых кровотечений, необходимости выполнения неотложного хирургического вмешательства у пациента, получающего антитромботическую терапию или профилактику [95, 96].
Таблица 5.5. Препараты для купирования действия антитромботических средств
Препарат, действие которого необходимо прервать |
Препараты, ингибирующие антитромботическое действие |
|---|---|
НФГ (гепарин натрия**) [95] |
протамина сульфат** - медленный в/в болюс (1-3 мин) в дозе 1 мг / 100 МЕ НФГ, введенного за последние 2-3 ч. При неэффективности (продолжающееся кровотечение) – инфузия протамина сульфата** под контролем АЧТВ. |
НМГ [95, 348] |
эффективного антидота нет, протамина сульфат** ингибирует не более 50% активности НМГ. Возможно в/в введение протамина сульфата** 1 мг на 100 анти-Хa НМГ; повторно – 0,5 мг/100 анти-Хa НМГ. При продолжающемся жизнеугрожающем кровотечении после применения протамина сульфата** и при подозрении, что сохраняется резидуальный эффект низкомолекулярных гепаринов АТХ Группа гепарина), который вносит вклад в кровотечение, возможно применение #активированного рекомбинантного VII фактора свертывания (rFVIIa) внутривенно в дозе 20 – 106 мкг/кг [348] |
Варфарин** [95] |
перед экстренной операцией – свежезамороженная плазма или факторы свертывания крови II,VII,IX и Х в комбинации [Протромбиновый комплекс]** (25 МЕ/кг) фитоменадион от 10 до 20 мг внутривенно |
Дабигатрана этексилат** [96] |
специфический ингибитор – идаруцизумаб (2 флакона по 2,5 г/50 мл) в виде двух внутривенных последовательных болюсных введений или инфузий длительностью не более 5-10 минут каждая |
|
Фондапаринукс натрия, апиксабан**, ривароксабан**, дабигатрана этексилат** (при недоступности идаруцизумаба) [96] |
факторы свертывания крови II,VII,IX и Х в комбинации [Протромбиновый комплекс]** - начальная доза 50 МЕ/кг, возможно последующее введение дозы 25 МЕ/кг или антиингибиторный коагулянтный комплекс** - 50 ЕД/кг (максимальная доза – 200 ЕД/кг), или рекомбинантный активированный #фактор свертывания крови VII** - 90 мкг/кг |
Клопидогрел**, тикагрелор** [95] |
тромбоконцентрат – 2 дозы/7 кг массы больного (может быть неэффективен в течение 12 ч после введения тикагрелора**) |
5.3 Общие подходы к профилактике ВТЭО
Каждому пациенту с травмой или перед плановой ортопедической операцией рекомендуется оценить и задокументировать степень риска развития ВТЭО [16, 86].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Для оценки риска развития ВЭТО у пациента перед операцией целесообразно использовать шкалы бальной оценки степени риска развития ВЭТО по Caprini (табл. 5.2), но можно использовать и другие шкалы или калькуляторы.
Всем пациентам с ограниченной двигательной активностью (мобильностью) вне зависимости от определенной степени риска развития ВТЭО рекомендуется проводить профилактику ВТЭО механическими методами [92].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Всем пациентам с повреждением и/или травмой ОДА при умеренном или высоком риске развития ВТЭО рекомендуется проводить профилактику ВТЭО медикаментозными (фармакологическими) методами, как правило, до восстановления обычной или ожидаемой двигательной активности больного (табл. 5.6) [89, 90, 92].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Таблица 5.6. Лекарственные средства, рекомендуемые для профилактики ВТЭО
Планируемое лечение |
Рекомендуемые препараты1 |
Длительность профилактики |
|
|---|---|---|---|
Консервативное лечение повреждений и заболеваний ОДА, сопровождающееся длительным ограничением подвижности пациента |
|
До восстановления обычной или ожидаемой двигательной активности |
|
Отсроченное оперативное лечение повреждений позвоночника, таза, нижних конечностей (предоперационный период) |
|
До дня операции, далее в зависимости от оперативного вмешательства |
|
Остеосинтез бедра |
|
Не менее 5–6 недель |
|
|
Эндопротезирование |
|
Не менее 5 недель |
|
- тазобедренного сустава |
|||
- коленного сустава |
Не менее 2 недель |
||
Другие большие ортопедические операции на нижних конечностях |
|
До восстановления обычной или ожидаемой двигательной активности или 6 недель, в зависимости от того, что наступит раньше |
|
Другие операции на опорно-двигательном аппарате4 |
|
До восстановления обычной или ожидаемой двигательной активности или 6 недель, в зависимости от того, что наступит раньше |
|
1 – препараты пронумерованы в порядке приоритетности назначения (в соответствии с накопленной доказательной базой и суждением экспертов);
2 – эти лекарственные средства изучены при эндопротезировании тазобедренного и коленного сустава, однако, согласно регистрации в Российской Федерации, могут использоваться и при указанных ортопедических операциях;
3 – только в виде таблеток, покрытых кишечнорастворимой пленочной оболочкой;
4 – за исключением острой травмы спинного мозга и тяжелой черепно-мозговой травмы (см. п. 5.4.8).
Комментарии. При выборе антикоагулянта необходимо учитывать противопоказания к применению препарата, изложенные в инструкции производителя. Рекомендуется отдавать предпочтение препаратам, имеющим собственные клинические исследования по оценке их эффективности и безопасности, выполненные у данного контингента больных. Препараты аналоги низкомолекулярных гепаринов (биологические аналоги) (АТХ B01AB Группа гепарина) можно использовать только в случаях, когда в надлежащих проспективных сравнительных клинических испытаниях по профилактике и лечению ВТЭО доказано, что эффективность и безопасность данного лекарственного средства существенно не отличается от оригинального препарата.
Пациентам с умеренным/высоким риском развития ВТЭО, нуждающимся в фармакологической профилактике после травмы или операции на ОДА, при противопоказаниях или отказе от назначения антикоагулянтов, развитии нежелательных явлений на фоне их приема рекомендуется рассмотреть назначение АСК** в сочетании с механическими видами профилактики [93, 94, 104, 152, 153].
Уровень убедительности рекомендаций A (уровень достоверности доказательств –1)
Комментарий: Было показано, что АСК** в дозах от 30 мг до 150 мг является достаточным для ингибирования функции тромбоцитов ЦОГ-1 [5]. Недавнее перекрестное исследование показало, что низкие дозы ацетилсалициловой кислоты** связаны с меньшей частотой желудочнокишечных осложнений при сохранении антитромботического эффекта [343]. Наиболее часто используемой дозировкой в России является 100 мг [94, 344].
Пациентам с умеренным или высоким риском развития ВТЭО, которым противопоказана любая фармакологическая профилактика или которые отказываются от назначения лекарственных препаратов, рекомендуется назначение механических видов профилактики [16, 55, 90, 92, 97].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Рекомендуется продолжение профилактики до восстановления обычной или ожидаемой двигательной активности больного [55, 90, 92].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
5.4 Особенности антикоагулянтной профилактики в различных клинических ситуациях
5.4.1. Плановое эндопротезирование тазобедренного или коленного сустава
Всем пациентам после планового ЭП ТБС или КС рекомендуется фармакологическая профилактика ВТЭО [16, 167, 191-198].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 1)
Комментарии. Большие ортопедические операции, к которым относят эндопротезирование коленного и тазобедренного сустава, сопровождаются высоким риском развития ВТЭО [5, 89, 195, 196].
Пациентам перед ЭП ТБС или КС, нуждающимся в фармакологической профилактике ВТЭО в дооперационном периоде, рекомендуется применять НМГ, при невозможности их назначения – НФГ (гепарин натрия**) [16, 55, 167, 191, 193, 199-201].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 1)
Пациентам с риском развития геморрагических осложнений после ЭП ТБС или КС рекомендуется отсрочить первое введение НМГ, дабигатрана этексилата** или ривароксабана** до достижения гемостаза (не менее чем на 8-12 часов после окончания операции) [13, 98, 202].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
Комментарии. Для предупреждения послеоперационных геморрагических осложнений целесообразно начать введение НМГ не позднее 12-и часов до или не ранее 12 часов после эндопротезирования, НФГ (гепарин натрия**) – не позднее 4-6 часов до или не ранее 12 часов после операции [13, 202]. При этом известно, что нет принципиальных различий в эффективности и безопасности фармакологической профилактики при ее начале до или после эндопротезирования [98]. Согласно инструкциям по применению минимальное время после операции, когда можно начать прием препаратов, составляет для половинной дозы дабигатрана этексилата** 1-4 часа, для ривароксабана** – 6-10 чаосов, для апиксабана** – 12-24 часа, однако, в случае недостигнутого гемостаза прием антикоагулянтов следует отложить. Эффективность дабигатрана этексилата** сопоставима, а ривароксабана** и апиксабана** – превосходит энаксапарин натрия** [99, 170, 171, 203-205], при этом для всех препаратов характерно быстрое достижение Сmax в кровотоке. Таким образом, по аналогии с отсрочкой первого введения НМГ для снижения риска развития геморрагических осложнений целесообразно отсрочить первый прием ПОАК минимум на 8 часов.
Пациентам после планового ЭП ТБС или КС при условии ранней активизации и отсутствии у них других факторов риска развития ВТЭО помимо операции рекомендуется наряду с антикоагулянтами рассматривать АСК** как средство профилактики ВТЭО [89–92, 191, 206-210].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 1)
Пациентам после ЭП ТБС, выполненного в экстренном или срочном порядке по поводу перелома проксимального отдела или шейки бедренной кости, при отсутствии противопоказаний к назначению антикоагулянтов, не рекомендуется применение АСК** в качестве единственного средства профилактики ВТЭО [191, 194, 207, 208, 210].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 1)
Комментарии. В последние годы в связи со снижением травматичности планового эндопротезирования коленного или тазобедренного сустава и возможности ранней активизации пациентов возрос интерес к применению АСК** для профилактики ТГВ и ТЭЛА у данной категории пациентов. Опубликованные результаты Датского и Испанского национальных регистров эндопротезирования продемонстрировали на когортах, включающих соответственно 37223 и 58037 пациентов, принимающих АСК**, частоту ТГВ менее 1% и ТЭЛА 0,3% и менее [100, 101]. В 2012 г. препарат был внесен в рекомендации American College of Chest Physicians (США) для применения при ЭП ТБС или КС при невозможности назначения ПОАК и НМГ [5]. Дальнейшие сравнительные исследования и мета-анализы показали сопоставимую частоту тромбозов при приеме АСК** и варфарина** с целевыми значениями МНО 1,5-1,8 [102], при продленной тромбопрофилактике после 10 дней НМГ с последующим приемом АСК** или НМГ [93]. Кроме того, сочетание АСК** с механической профилактикой не показало преимущества в сравнении с только фармакологической профилактикой АСК** [103]. Рандомизированное исследование тромбопрофилактики у пациентов без дополнительных фактров риска ВТЭО после ЭН КС также не выявило различий между группами сравнения в зависимости от приема АСК**, дабигатрана этексилата** или ривароксабана** [94]. В 2018 г. АСК** включили как один из препаратов выбора, наряду с ПОАК и НМГ при плановом эндопротезировании ТБС или КС в Британские (NICE), Австралийские и Европейские национальные рекомендации [90–92]. Несмотря на имеющийся в публикациях разброс дозировок АСК**, в РФ дозами, зарегистрированными для профилактики ТГВ и ТЭЛА при длительной иммобилизации в результате обширного хирургического вмешательства, являются 100-200 мг один раз в сутки. В отечественных РКИ исследовали дозу АСК** 100 мг 1 раз в сутки [104], аналогичный режим примема указанного антиагреганта, кроме гепарина, рекомендует ASA (Arthroplasty Society of Australia) [92]. Таким образом, на сегодняшний день накоплена большая доказательная база для включения АСК** в рекомендации по профилактике ВТЭО при плановых вмешательствах у пациентов без выраженной кардиологической или иной соматической патологии, ведущей к высокому риску развития ТГВ и ТЭЛА. Необходимо помнить, что совместное применение антиагрегантов, кроме гепарина, с антикоагулянтами сопровождается повышенным риском развития кровотечения, применение высоких доз АСК** повышает риск развития язв желудка, что может привести к кровотечению из ЖКТ.
Пациентам после эндопротезирования тазобедренного сустава рекомендуется продолжение профилактики ВТЭО до 5 недель, после эндопротезирования коленного сустава – минимум 2 недели или до восстановления ожидаемой двигательной активности больного, в зависимости от того, что наступит раньше [16, 90, 92, 167].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии. Современные национальные руководства определяют продолжительность тромбопрофилактики после эндопротезирования коленного и тазобедренного суставов – минимум 10-14 дней, с продлением до 35-и дней при наличии у пациента дополнительных факторов риска [5, 16, 55, 90, 92, 97, 203, 204, 212-226]. Указанные сроки назначения антикоагулянтов обусловлены изменениями в системе коагуляции, сохраняющимися в течение нескольких недель после хирургического вмешательства. К ним относят угнетение фибринолитической активности крови, активацию коагуляции и снижение уровня естественных антикоагулянтов, таких как АТ-III. Из-за сохраняющейся тенденции к сокращению койко-дня возможные ВТЭО чаще развиваются на амбулаторном этапе после выписки из стационара.
5.4.1.1. Эндопротезирование тазобедренного или коленного сустава у пациентов с терминальной болезнью почек (ХБП) 5Д стадии, находящихся на гемодиализе
Пациентам, находящимся на программном или перитонеальном гемодиализе, с отсутствием спонтанных кровотечений из паренхиматозных органов в анамнезе, рекомендуется проведение медикаментозной и механической профилактики ВТЭО после ЭП ТБС или КС [92, 105, 106].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии. Хроническая почечная недостаточность сопровождается повышением количества провоспалительных и протромботических агентов. Чаcтота глубоких тромбозов у пациентов с ХБП 3-4 стадией – 43,8% [106]. Частота тромбоэмболии легочной артерии у больных с терминальной стадией почечной недостаточности составляет 2,1% [105]. Пациенты, находящиеся на хроническом гемодиализе, должны быть стратифицированы по высокому риску тромбоэмоблических осложнений и введение антикоагулянта должно проводится ежедневно, включая дозу антикоагулянта во время процедуры гемодиализа [92]. Механическая профилактика (эластическая компрессия нижних конечностей) ВТЭО в послеоперационном периоде оказывает более значимый клинический эффект по сравнению с больными обычной популяции [92]. Известно, что пациентам с терминальной ХБП 5Д стадии после ЭП ТБС или КС профилактика ВТЭО только во время процедуры гемодиализа недостаточна [107, 108]. Эндопротезирование тазобедренного и коленного сустава является ортопедическим оперативным вмешательством с высоким риском развития ВТЭО у больных, находящихся на хроническом гемодиализе. Вероятность глубокого тромбоза при эндопротезированиие крупных суставов у больных на гемодиализе в 1,65 (95% ДИ: 1,13–2,40; p = 0,01) раз выше по сравнению с больными без ХБП [106]. Однократное введение НМГ в стандартной дозировке в конце процедуры гемодиализа после эндопротезирования тазобедренного и коленного сустава не снижает риск развития ВТЭО, повышая риск смерти в 1,32 раза (95% ДИ: 1,01 – 1,71 p<0,05) [107].
Пациентам, находящимся на программном или перитонеальном гемодиализе, при наличии в анамнезе спонтанных кровотечений из паренхиматозных органов, не рекомендуется проведение медикаментозной профилактики ВТЭО в междиализный день после ЭП ТБС или КС [109, 227-229].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2)
Комментарии. Дополнительное введение НМГ пациентам с терминальной стадией ХБП в междиализные дни после больших хирургических операций повышает риск кровотечений и общесоматических осложнений [109].
Пациентам с терминальной ХБП 5Д стадией после «больших» ортопедических операций для проведения фармакологической профилактики ВТЭО рекомендуется назначать в междиализный день НМГ (далтепарин натрия 2500 анти-Ха МЕ п/к в сутки или эноксапарин натрия** в дозе 20 мг п/к в сутки), при их недоступности НФГ (гепарин натрия**) [63, 109–112, 227, 230-232].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4) – для эноксапарина натрия**
Комментарии. Наиболее частой причиной являются сердечно-сосудистые осложнения, вызванные гиперкалиемией и дислипедемией, усугубляемые НФГ (гепарин натрия**) [111, 112]. Частота ВТЭО при ежедневном и
Несмотря на планирование проведения диагностических и лечебных мероприятий пациентам при развитии ТГВ, помощь носит неотложный характер. Отсрочка начала лечения приводит к снижению показателей эффективности лечения у данной категории пациентов и утяжеляет прогноз на реконвалесценцию тромба у конкретного больного, а в ряде случаев при развитии ТЭЛА может привести к летальному исходу.
Проведение диагностических мероприятий на этапе постановки диагноза и в период между этапами лечения может осуществляться в амбулаторных условиях. Проведение этапов хирургического лечения, включающего анестезиологическое пособие и другую сопроводительную терапию, требует пребывания в стационаре.
После первого эпизода ТГВ просттромботический синдром развивается в течение 2 лет у 60% пациентов. У каждого четвертого пациента с ТЭЛА развивается рецидив тромбоэмболии в течение последующих 5 лет, особенно при наличии онкологических заболеваний или патологии гемостаза. Около 20% нелеченных проксимальных ТГВ приводят к развитию ТЭЛА, летальность при которой составляет 10-20%. Назначение рациональной антикоагулянтной терапии снижает смертность в 5-10 раз.
С учетом большого количества лекарственных взаимодействий АВК (варфарина**) с лекарственными препаратами и пищей, пациентов, получающих данный АК, следует информировать о необходимости соблюдении диеты и регулярного мониторинга МНО для поддержания его терапевтических значений. У женщин, принимающих гормональные контрацептивы системного действия, риск ТГВ возрастает в 3-5 раз, при этом риск максимален в первые 4 месяца от начала приема данной категории препаратов и снижается до популяционного через 3 месяца после их отмены.













