Болезнь, стирающая личность
Этот безумный мир
За последний век медицина позволила человеку практически удвоить среднюю продолжительность жизни. Сегодня для жителей развитых стран 80+ — возраст долгожителя, а в США, скорее всего, в ближайшее время к старшей возрастной группе отнесут уже перешагнувших 90-летний жизненный рубеж. Эти успехи заставили врачей столкнуться с проблемами, которые в начале XX века даже не предполагались. На смену инфекционным эпидемиям, выкашивающим население целых городов, пришли неинфекционные, мало уступающие по числу жертв, — диабет, сердечно-сосудистые заболевания (ССЗ), деменция.
Самой распространенной причиной деменции (около 60—80% всех случаев) стала болезнь Альцгеймера (БА) — заболевание нейродегенеративное, прогрессирующее и неизлечимое. С ростом числа пожилых людей на планете, основных ее жертв, актуальность БА приобретает глобальный характер. Всемирная организация здравоохранения и Международная федерация ассоциаций по борьбе с болезнью Альцгеймера (Alzheimer's Disease International) объединяют усилия мирового медицинского сообщества для сохранения когнитивного здоровья человечества, требующего привлечения дополнительных ресурсов и выработки системных решений для борьбы с деменцией, повышения осведомленности о БА и важности этой проблемы, особенно среди врачей.
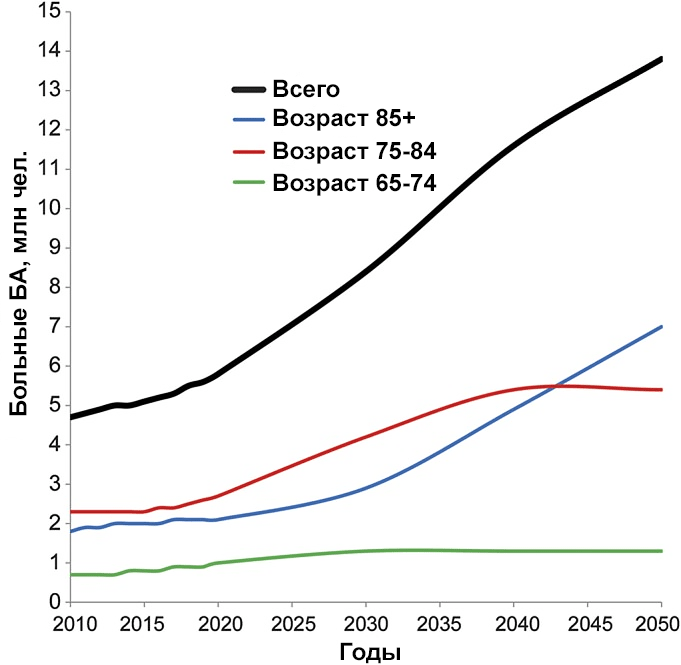
Рисунок. Ожидаемый рост числа пациентов с болезнью Альцгеймера в США1
Сегодня в мире более 55 млн человек живут с деменцией. Ежегодно их число прирастает 10 млн новых больных.2,3 К середине столетия их может стать уже 139 млн.4,5 Наибольший прирост случаев деменции ожидается в странах с низким и средним уровнем доходов населения — с 60 до 71%, а также в странах с быстрым приростом пожилого населения. 4,5
В научном сообществе есть и альтернативная позиция: катастрофического роста заболеваемости БА не будет — спасет возрастающий уровень образования населения (регулярные тренировки мозга спасают от Альцгеймера).6
Экономические потери, связанные с деменцией, по объему превышают и ССЗ, и онкопатологии. Специалисты ВОЗ говорят о 1,4% от ВВП в развитых странах в год.3 Причем медикаментозное лечение обходится относительно недорого, а вот стоимость ухода за такими пациентами вырастает в 17 раз. Если материальную нагрузку на семьи этих больных можно подсчитать по специальным формулам и схемам, то оценить глубокое эмоциональное воздействие БА на близких пациента практически невозможно.
Жизнь за пределами памяти
Характерная для БА триада «афазия-апраксия-агнозия» — прогрессирующее снижение когнитивных функций человека. Есть и другие неврологические и психические симптомы болезни, но они в меньшей степени влияют на состояние пациента.
От других видов деменции БА отличается прежде всего тем, что даже на ее ранних этапах поражается так называемая биографическая память человека. У больного искажаются и вовсе исчезают личные воспоминания — он забывает имена родственников, смерти близких; катастрофически утрачивается весь прошлый опыт. Еще одна типичная черта этой болезни — эмоционально-аффективные нарушения у больного.
Личностные изменения болезнь часто вносит уже на ранних стадиях. Пациент становится подозрительным и конфликтным. Нередко у него появляются бредовые идеи ущерба, направленного против него и его близких, – ему кажется, что у него крадут вещи, собираются от него избавиться, «сдать в дом престарелых» и т.д. Обращает внимание и бесцельная двигательная активность пациента — ходит из угла в угол, перекладывает вещи с одного места на другое, сбегает из дома. На более поздних стадиях БА поведенческие нарушения усугубляются: больной может стать более агрессивным, наносить себе различные повреждения, перестает следить за своей внешностью, у некоторых пациентов возможны галлюцинации (чаще зрительные).
Разрушение личности сопровождается:
- потерей навыков (праксиса);
- способностью совершать самые простые действия (апраксия);
- распознавать предметы и узнавать людей (агнозия);
- специфическими речевыми нарушениями (слова и слоги заменяются близкими по звучанию), а затем и полным исчезновением речи (афазия).
Итог развития БА: пациент не способен себя обслуживать (самостоятельно есть, передвигаться, контролировать тазовые функции, пр.).
В группе риска по БА люди старше 60 лет: среди 65-летних приблизительно каждый деcятый страдает этой болезнью (у женщин вероятность заболеть вдвое выше); в группе 85+ заболевших — каждый третий. В среднем пациенты с БА живут около 8—10 лет с момента появления первых клинических проявлений.
Загадки Альцгеймера
Болезнь Альцгеймера — это неврологическое заболевание, особенностью которого считается поражение височно-теменных полушарий головного мозга и холинергических нейронов базального ядра Мейнерта. В первую очередь при БА поражаются медиальные отделы височной доли. Атрофия гиппокампа — ранний, хотя не абсолютно специфичный маркер заболевания. Наличие единичных мелких сосудистых очагов или ограниченного перивентрикулярного лейкоареоза не исключает диагноз болезни Альцгеймера.7
Начинается заболевание не в то время, когда человек стал путаться в датах или именах, а значительно раньше – за 10—15 лет. Первым отклонениям в поведении пациентов предшествуют физиологические изменения в их организме: в головном мозге (ГМ) формируются и откладываются в межклеточном пространстве β-амилоидные бляшки. В формировании этих характерных скоплений принимает участие β-амилоид (Aβ) — пептид, образующийся особым ферментативным расщеплением его белка-предшественника (APP).8
Другое важное звено патогенеза БА — гиперфосфорилирование тау-белка (τ-белка), ведущее к дестабилизации микротрубочек и образованию нейрофибриллярных клубочков в телах нейронов. Помимо этого последние изыскания указывают на участие экзосом в прионовидном транспорте модифицированных белков и нейрофибриллярных клубочков по всему объему ГМ. Еще один потенциальный механизм развития БА — накопление железа в структурах мозга, его взаимодействие с Аβ, избыточная продукция активных форм кислорода и окислительное повреждение клеток.9
Накопленные данные о Аβ позволили ученым выдвинуть амилоидную гипотезу БА. Но новые знания расширяют представления научного сообщества о патогенезе этого заболевания. Ряд ученых, например, высказываются о том, что Aβ хотя и необходим для запуска механизма развития БА, но недостаточен.10 Приводятся сведения, демонстрирующие, что распространенность внеклеточных отложений Аβ в коре ГМ менее коррелирует с когнитивным снижением, нежели количество скоплений τ-белка внутри клеток. Более того, последовательность появления последних в различных отделах ГМ ассоциируется с появлением определенных симптомов болезни.11
Но представления, сложившиеся в рамках амилоидной и тау-гипотез, не объясняют всех накопленных научных данных. К ранее выдвинутым версиям исследователи предлагают генетическую теорию (аллель Е 4 гена APOE),12 нейроиммуномодуляционную.13,14 Со времен Алоиза Альцгеймера в изучении БА сделано немало. Но заболевание, описанное им в начале прошлого века и на изучение которого в наше время тратятся триллионы долларов, не спешит раскрывать всех своих медико-биологических секретов, и к полному пониманию его молекулярных основ ученые еще не пришли.
Бруно Веллас (Bruno Vellas), MD, PhD., заведующий кафедрой геронтологии и отделения гериатрической внутренней медицины, госпиталь Тулузского университета, член Международного института медицинских исследований (INSERM) 1295: «Мы наблюдаем все больше «молодых» пациентов в возрасте 50—60 лет с диагнозом болезнь Альцгеймера. Возможно, это связано с тем, что улучшается диагностика, поэтому врачи стали выявлять заболевание раньше и нам кажется, что болезнь молодеет».
Кто виновть и что делать
Не имея ответа на вопрос о виновниках болезни Альцгеймера, трудно добиться серьезных успехов в борьбе с ней. Поэтому даже при нынешних высоких технологиях остаются сложности в диагностировании заболевания. Впрочем, это не единственная причина. Есть еще и отсутствие самокритичности в оценке собственного состояния у пациента, и нередко недостаточная настороженность врача в отношении БА. Так или иначе, а заболевание часто остается незамеченным до поздних этапов развития.15
Диагностические критерии болезни Альцгеймера, характеристики стадий заболевания, положения по физикальному и неврологическому обследованию, алгоритм диагностических мероприятий подробно описаны в клинических рекомендациях, подготовленных экспертами.16 Они обращают внимание врачей на необходимость комплексного подхода к обследованию пациентов с этим сложным гетерогенным заболеванием, этиология которого продолжает оставаться предметом активного изучения.
Отмечается специалистами важность опроса пациента и близко знакомых с ним/ухаживающих за ним лиц (информантов) для уточнения жалоб и анамнестических сведений (включая уточнение по сопутствующей медикаментозной терапии и препаратам, потенциально негативно влияющих на выраженность когнитивных нарушений); общего осмотра с обязательной оценкой неврологических симптомов; нейропсихологического тестирования с оценкой характера когнитивных нарушений.16
Для исключения сопутствующих состояний, усугубляющих тяжесть когнитивных нарушений проводятся лабораторные исследования. Рекомендовано выполнение общих анализов мочи и крови, общетерапевтического биохимического анализа крови — с оценкой концентрации глюкозы, общего белка, общего билирубина, АЛТ, АСТ, креатинина, мочевины, уровней натрия, калия, кальция.
Ведущее место в диагностике БА занимают инструментальные методы, очень информативны методы нейровизуализации.
Диагноз БА сегодня может быть поставлен даже до того, как сформировался синдром деменции. На основе амнестического синдрома гиппокампального типа и биомаркеров, отражающих локализацию и природу альцгеймеровского нейродегенеративного процесса устанавливается: накопление β-амилоида — концентрация амилоида β42 в спинномозговой жидкости (СМЖ); накопление амилоидного трейсера по данным позитронно-эмиссионной томографии (ПЭТ); повышение общего и фосфорилированного τ-белка в СМЖ, снижение метаболизма глюкозы (ФДГ/ПЭТ); корковая атрофия (структурная МРТ) в височно-теменных областях.
А ранняя диагностика БА — это своевременно назначенная терапия, позволяющая сохранить имеющиеся когнитивные функции, отодвинуть и замедлить прогрессирование болезни.5
FDA одобрены лекарственные препараты и комбинация лекарственных средств для лечения БА:9
- ингибиторы ацетилхолинэстеразы (АХЭ): донепезил, галантамин и ривастигмин – для лечения легкой и умеренной БА;
- антагонист NMDA рецепторов — мемантин — для лечения умеренной и тяжелой форм БА;
- моноклональное антитело к β-амилоиду — адуканумаб — для лечения додементных когнитивных мягких когнитивных расстройств и ранних стадий БА;
- комбинация донепезила и мемантина.
Да, пока речь не идет об излечении пациентов с БА. Но есть надежды на фундаментальные исследования в области изучения ГМ и ЦНС, в том числе в рамках различных программ (BRAIN Initiative — Brain Research through Advancing Innovative Neurotechnologies17), и на успехи фарминдустрии, чьи специалисты исследуют несколько десятков новых препаратов от БА. Среди них средства как болезнь-модифицирующей терапии, направленной на предотвращение аккумуляции Aβ и гиперфосфорилирования τ-белка, так и симптоматической терапии, улучшающей когнитивное функционирование пациентов и купирование нейропсихиатрических и поведенческих симптомов.
Основные рекомендации по оптимизации терапии болезни Альцгеймера:9
- снижение когнитивных функций не норма в любом возрасте, поэтому все пациенты с когнитивными нарушениями должны пройти диагностическое обследование;
- необходимо следовать рекомендованным стандартам терапии;16
- лечение должно быть длительным с использованием оптимальных терапевтических доз и соблюдением предписанного режима лечения;
- для снижения нежелательных эффектов терапии целесообразно использование новых форм препаратов или модифицированных схем приема ЛП;
- индивидуализация терапии в рамках стандартов и мониторинг терапевтического эффекта;
- эффективность терапии на стадии умеренной деменции может быть повышена за счет использования комбинированной (ингибиторы АХЭ + мемантин) и мультимодальной терапии (+ церебролизин);
- для повышения комплаентности необходимо просвещать семью больного о критериях эффективности лечения БА и целях долговременной терапии.













