Представлен новый подход к лечению дефицита декарбоксилазы ароматических L‑аминокислот
Дефицит декарбоксилазы ароматических L-аминокислот (дефицит AADC) (OMIM: 608643) — редкое аутосомно-рецессивное заболевание, обусловленное патогенными вариантами гена декарбоксилазы ароматических L-аминокислот (ген DDC). Возникающий вследствие патогенных мутаций дефицит моноаминов (дофамина, серотонина) приводит к раннему развитию заболевания, характеризующегося мышечной гипотонией, нарушениями двигательных и вегетативных функций, расстройствами поведения. Эффективность существующих лекарственных подходов в лечении данного заболевания не оправдывает ожиданий, вследствие чего 80% пациентов испытывают серьезные двигательные и когнитивные нарушения, а также имеют повышенный риск преждевременной смерти.
Наибольшую результативность в терапии дефицита AADC продемонстрировал новый препарат эладокаген эксупарвовек — рекомбинантный аденоассоциированный вирусный агент 2-го типа, содержащий комплементарную ДНК человека, кодирующую декарбоксилазу ароматических L‑аминокислот (AADC). Введение препарата осуществляется посредством нейрохирургической стереотаксической операции в область путамена головного мозга. В результате переноса гена DDC, кодирующего фермент AADC, происходит повышение выработки дофамина и серотонина, что оказывает выраженный лечебный эффект в отношении наиболее тяжелых проявлений дефицита AADC.
Подчеркивается важность лечения таких пациентов в раннем возрасте, однако наука также накапливает опыт применения эладокагена эксупарвовека среди пациентов старше десяти лет. Авторы анализируемой работы подчеркивают, что это первое исследование в Европе, в котором рассматривается эффективность препарата, введенного двум пациентам в возрасте старше десяти лет с тяжелой формой дефицита AADC.
Материалы и методы исследования
Пациенты с симптомами заболевания и отсутствием признаков улучшения состояния на фоне проводимого стандартного лечения были отобраны мультидисциплинарной группой экспертов для получения терапии эладокагеном эксупарвовеком. Введение препарата проводилось в больнице при Университете Монпелье во Франции. Основной и послеоперационный протоколы обследования пациентов, нейрохирургический метод введения, согласно рекомендациям производителя, были утверждены Национальным агентством по безопасности лекарственных средств и медицинских изделий Франции.
Каждый пациент получил 1,8 × 1011 вектор-геномов, доставленных посредством четырех инъекций по 80 мкл в путамен головного мозга, вводимых со скоростью 3 мкл/мин.
Клинико-параклиническая оценка
Клинические данные регистрировались в медицинской карте пациентов в ходе каждого контрольного обследования. Проводился сбор информации о состоянии двигательной и когнитивной функций, нарушениях сна, перепадах настроения, степени раздражительности, уровне ощущения психологического комфорта, общем самочувствии, сложности ухода за пациентами в соответствии с результатами опросника «Индекс здоровья детей с ограниченными возможностями» (CPCHILD), состоянии желудочно-кишечного тракта и способности самостоятельно принимать пищу, их весе, возникновении респираторных инфекций, изменениях медикаментозного лечения, дискинезии и наличия окулогирных кризов. Магнитно-резонансная томография головного мозга, L-6-[18F] фтор-3, 4-дигидроксифенилаланин (18F-ДОФА) позитронно-эмиссионная томография (ПЭТ) были выполнены до введения генной терапии, через один месяц после введения, а затем еще раз год спустя. Анализ ликвора был проведен до лечения и 18 месяцев спустя. Кроме того, замерялся исходный уровень титров антиаденоассоциированного вируса 2-го типа, а также его изменение через три, шесть, 12 и 18 месяцев после проведенного лечения.
Результаты
До применения генной терапии оба пациента не удерживали голову и имели ограниченную спонтанную двигательную активность, несмотря на проводимую стандартную терапию.
Благодаря применению эладокагена эксупарвовека продемонстрирован устойчивый положительный эффект лечения у обоих пациентов старше десяти лет. Анамнез заболевания пациентов представлен в Таблице 1. Данные продолжительного наблюдения приведены в Таблице 2.
Результаты клинического обследования
Двигательные функции
Благодаря препарату эладокаген эксупарвовек у обоих пациентов наблюдалось улучшение двигательных функций, в особенности повышение тонуса аксиальной мускулатуры и увеличение объема произвольных движений в конечностях. Пациент 1 начал дотягиваться до объектов через шесть месяцев после введения генной терапии, а через десять месяцев — держать голову. У пациента 2 восстановился тонус мышц шеи через шесть месяцев, а через 12 месяцев он смог хватать объекты. У обоих участников исследования отмечалось уменьшение признаков дистонии и окулогирных кризов (их продолжительности, частоты и тяжести проявления) через три месяца после инъекции эладокагена эксупарвовека.
Поведенческие и когнитивные функции
Изначально оба пациента страдали от перепадов настроения, повышенной плаксивости и нарушений сна, могли общаться только посредством зрительного контакта и грубого горлового звука. Начиная с четвертой недели после применения генной терапии, ухаживавшие за пациентами сообщали об улучшении сна у испытуемых, снижении раздражительности и улучшениях в период бодрствования.
У обоих участников исследования также отмечалось жизнерадостное поведение (через полгода после генной терапии у пациента 1 развился новый навык — способность смеяться), повышение концентрации внимания и улучшение навыков общения. Через шесть месяцев после инъекции препарата оба пациента начали издавать различные звуки и произносить слоги, чтобы позвать людей, осуществлявших уход за ними. Через 18 месяцев пациент 1 мог говорить двусложные слова. Улучшение когнитивных способностей обоих участников исследования было подтверждено оценкой их адаптивного поведения на основе шкалы Вайнленда.
Другие функции
Улучшение способности испытуемых самостоятельно принимать пищу, а также отказ от кормления через зонд привели к увеличению их веса и улучшению общего качества жизни. У пациента 2 значительно снизилось число случаев заражения респираторными инфекциями.
Нежелательные явления
В ходе и после хирургической операции по введению эладокагена эксупарвовека не отмечалось каких-либо серьезных нежелательных явлений. Через 36 часов после инъекции препарата у пациента 2 наблюдалась серия кратковременных фокальных эпилептических приступов на фоне повышения температуры, не вызванного инфекционным заболеванием. Однако подобные приступы отмечались у испытуемого и до введения генной терапии.
В течение четырех недель после инъекции эладокагена эксупарвовека оба пациента испытывали умеренную и транзиторную дискинезию, вследствие чего пациенту 1 была назначена небольшая доза тетрабеназина, а пациенту 2 уменьшили дозировку дофаминергических препаратов. Кроме того, исследователи отмечают возникновение менингоцеле в месте инъекции у пациента 1 вследствие кратковременного истечения спинно-мозговой жидкости (СМЖ), разрешившегося самостоятельно.
Результаты параклинического обследования
Послеоперационная магнитно-резонансная томография не выявила никаких признаков внутримозгового кровоизлияния и наличия какой-либо инфекции. У обоих пациентов наблюдалось серьезное нарушение захвата 18F-ДОФА в начале исследования и улучшение процесса через месяц после инъекции эладокагена эксупарвовека. Более высокий уровень захвата 18F-ДОФА сохранялся и через год, хотя и имел гетерогенный характер у пациента 2.
Известно, что 18F-ДОФА быстро «вымывается» из нейронов путамена, если не метаболизируется в дофамин. В связи с этим свидетельством восстановления уровня активности фермента декарбоксилазы ароматических L-аминокислот является улучшение усвоения 18F-ДОФЫ у пациентов через один год после инъекции препарата.
О восстановлении активности фермента может также свидетельствовать повышенное содержание гомованилиновой кислоты в СМЖ. При последнем контрольном визите у пациента 2 наблюдалось повышение содержания метаболита дофамина гомованилиновой кислоты в ликворе, но не уровня метаболита серотонина 5-гидроксииндолуксусной кислоты. У пациента 1 уровень дофамина в течение года после инъекции препарата не изменился. Однако исследователи добавили, что на сегодня нет научных данных, которые могут подтвердить, что повышение уровня содержания гомованилиновой кислоты в спинномозговой жидкости в результате доставки эладокагена эксупарвовека в головной мозг можно считать биомаркером восстановления активности AADC. Требуются дополнительные исследования в этой области.
Ранее проведенные исследования эладокагена эксупарвовека
По результатам ранее проведенных исследований, в которых приняли участие 39 пациентов с дефицитом AADC (средний возраст ≤ 6 лет), введение эладокагена эксупарвовека в путамен способствовало значительному улучшению их двигательных и когнитивных способностей. Такой же эффект наблюдался у семи пациентов, которым вводили препарат в средний мозг. Авторы утверждают, что генная терапия подействовала быстрее и имела более заметный эффект среди пациентов, средний возраст которых составлял шесть лет, чем у двух испытуемых, рассматриваемых в текущем исследовании. Особенно это касается общих двигательных функций и навыков мелкой моторики (способности есть самостоятельно, дотягиваться до предметов/хватать их). У детей с дефицитом AADC младше трех лет показатели функционального восстановления были еще выше после инъекции препарата.
Кроме того, сообщается, что ранее проводилось исследование препарата, в котором приняли участие четыре человека в возрасте старше десяти лет, страдающих дефицитом AADC. Через восемь месяцев после инъекции эладокагена эксупарвовека в путамен трое испытуемых начали ходить с опорой, один пациент — при поддержке ухаживающего за ним лица. У всех участников исследования развилась способность хватать предметы, исчезли симптомы окулогирных кризов и дистонии. У пациентов возникали побочные эффекты в виде дискинезии после применения генной терапии, которая наблюдалась также в ходе ранее проведенных исследований, длилась менее шести месяцев и поддавалась медикаментозному контролю.
Выводы
По мнению авторов, представленное исследование служит обоснованием для применения препарата генной терапии среди более взрослых пациентов. Соответствие полученных результатов с данными ранее проведенных исследований свидетельствует о безопасности доставки гена DDC в головной мозг и возможности использования эладокагена эксупарвовека не только среди детей, но и у пациентов более старшей возрастной группы, страдающих тяжелой формой дефицита декарбоксилазы ароматических L-аминокислот. Контроль и наблюдение за состоянием пациентов после введения препарата поможет лучше оценить биологическую и клиническую эффективность данной инновационной терапии.
Препарат эладокаген эксупарвовек (Upstaza) одобрен Европейским агентством по контролю лекарственных средств (EMA) для лечения взрослых и детей с тяжелым дефицитом декарбоксилазы ароматических L-аминокислот у пациентов с генетически подтвержденным диагнозом. Также, в апреле 2023 года был опубликован финальный проект рекомендаций NICE, в котором Национальный институт здравоохранения и совершенствования медицинской помощи Великобритании рекомендует терапию элодакагеном эксупарвовеком для детей с ультраредким заболеванием — дефицитом AADC.
Таблица 1. Исходные характеристики пациентов
|
Пациент 1 |
Пациент 2 |
|
|
Родители |
Не состоят в кровном родстве |
Являются кровными родственниками |
|
Течение родов |
Без осложнений |
Без осложнений |
|
Вес и рост ребенка при рождении |
2,85 кг; 49,5 см |
3,26 кг; 51 см |
|
Возраст начала проявления симптомов дефицита AADC |
3,8 месяца после рождения |
6 месяцев после рождения |
|
Нуклеотидный вариант гена DDC |
Гомозиготный патогенный c.1040G>A (p.Arg347Gln) |
Гомозиготный патогенный c.1040G>A (p.Arg347Gln) |
|
Симптомы при постановке диагноза |
|
|
|
Общий анамнез |
||
|
Моторные функции |
|
|
|
Окулогирные кризы (возраст начала проявления/последние сведения о проявлении симптома у пациента) |
|
|
|
Перепады настроения/нарушения сна |
|
|
|
Пищеварительная система |
|
|
|
Дыхательная система |
|
|
|
Дополнительные сведения |
|
|
|
Предшествующая терапия |
|
|
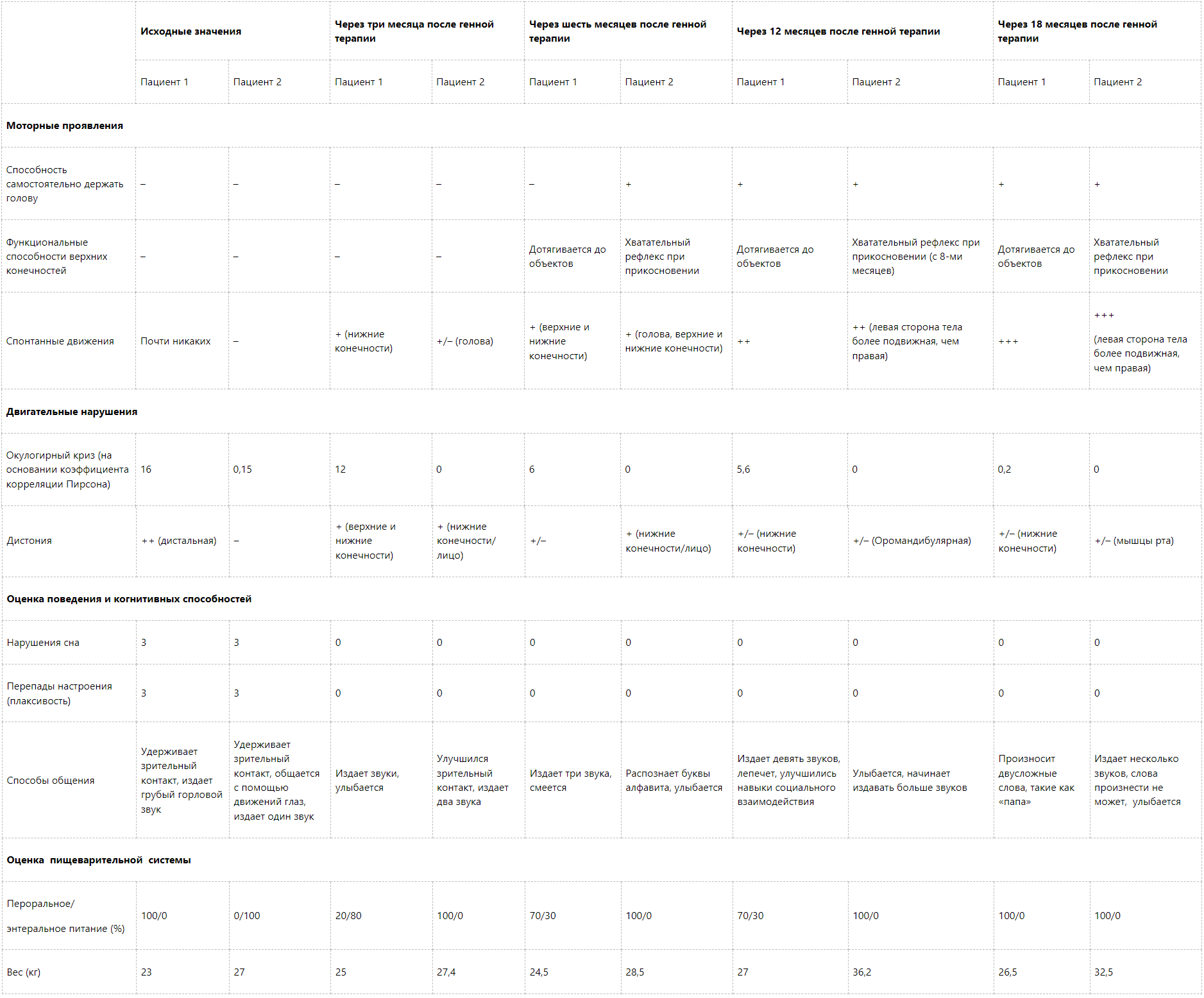
Таблица 2. Динамика показателей основных функций